- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 7611:2007 Túi nhựa mềm để chứa máu và chế phẩm máu người
| Số hiệu: | TCVN 7611:2007 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Y tế-Sức khỏe |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
14/08/2007 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 7611:2007
Nội dung tóm tắt đang được cập nhật, Quý khách vui lòng quay lại sau!
Tải tiêu chuẩn Việt Nam TCVN 7611:2007
TIÊU CHUẨN QUỐC GIA
TCVN 7611 : 2007
ISO 3826 : 1993
TÚI NHỰA MỀM ĐỂ CHỨA MÁU VÀ CHẾ PHẨM MÁU NGƯỜI
Plastics collapsible containers for human blood and blood components
Lời nói đầu
TCVN 7611 : 2007 hoàn toàn tương đương với ISO 3826 : 1993.
TCVN 7611 : 2007 do Tiểu Ban Kỹ thuật Tiêu chuẩn TCVN/TC210/SC2 Trang thiết bị y tế biên soạn, trên cơ sở dự thảo đề nghị của Viện Trang thiết bị và Công trình y tế - Bộ Y tế, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
TÚI NHỰA MỀM ĐỂ CHỨA MÁU VÀ CHẾ PHẨM MÁU NGƯỜI
Plastics collapsible containers for human blood and blood components
1. Phạm vi áp dụng
1.1. Tiêu chuẩn này qui định các yêu cầu, bao gồm các yêu cầu về tính năng của chất dẻo poly (vinyl clorua) (PVC) có sử dụng chất làm dẻo di – (2-etylhexyl) phtalat (DEHP) để làm túi nhựa mềm, kín, vô trùng, có kèm dây lấy máu, van của túi, kim lấy máu trọn bộ và có thể kèm dây chuyển, để lấy máu, bảo quản, điều chế, vận chuyển, chiết tách, quản lý máu và các chế phẩm máu. Túi chứa có thể chứa chất chống đông và/hoặc dung dịch bảo quản, tùy thuộc vào dự định sử dụng. Các yêu cầu này cũng được đề cập để
a) đảm bảo chất lượng của máy và thành phần máu được duy trì tốt nhất;
b) tạo khả năng cho việc lấy máu, nhận dạng, bảo quản, chiết tách, truyền máu một cách có hiệu quả và an toàn, với chú ý đặc biệt để giảm đến tối thiểu những rủi ro nguy hiểm từ
- nhiễm khuẩn, đặc biệt là nhiễm vi khuẩn,
- tắc mạch do khí,
- nhầm lẫn trong việc nhận dạng túi và mẫu thí điểm của chất chứa trong túi,
- tương tác giữa túi và chất chứa trong túi;
c) đảm bảo tương thích chắc năng khi sử dụng kết hợp với bộ truyền như quy định trong ISO 1135-4;
d) có độ bền tối đa đối với nứt vỡ và hư hỏng trong bao gói có khối lượng và thể tích tối thiểu.
1.2. Các yêu cầu quy định trong tiêu chuẩn này cũng áp dụng cho túi nhựa kép, ví dụ bộ túi đôi, túi ba hoặc túi bốn.
1.3. Thuật ngữ “túi nhựa” được sử dụng trong toàn bộ tiêu chuẩn này mang ý nghĩa là túi chứa kết hợp với dây và kim lấy máu, van túi, chất chống đông và/hoặc dung dịch bảo quản, dây chuyển và túi phụ.
1.4. Ngoại trừ các quy định khác, tất cả các phép thử quy định trong tiêu chuẩn này đều áp dụng cho túi nhựa được chuẩn bị để sử dụng ngay.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau là rất cần thiết cho việc áp dụng tiêu chuẩn. Đối với các tài liệu viện dẫn ghi năm ban hành thì áp dụng bản được nêu. Đối với các tài liệu viện dẫn không ghi năm ban hành thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi (nếu có).
TCVN 6087 : 2004 (ISO 247 : 1990) Cao su – xác định độ trọ.
TCVN 7610-3 : 2007 (ISO 1135-3 : 1986) Thiết bị truyền dùng trong y tế - Phần 3: Bộ dây lấy máu.
ISO 1135-4 Transfution equipment for medical use – Part 4: Transfution sets for single use (Thiết bị truyền dùng trong y tế - Phần 4: Bộ dây truyền dùng một lần).
3. Kích thước và ký hiệu qui ước
3.1. Kích thước
Xem Hình 1 và Bảng 1. Chỉ những giá trị kích thước nêu trên Hình 1 là bắt buộc; các kích thước ghi trong Bảng 1 có mục đích hướng dẫn.
CHÚ THÍCH
1) Hình vẽ minh họa các thành phần của túi nhựa và một số kích thước đã nêu không phải là yêu cầu kỹ thuật của tiêu chuẩn này.
2) Để hướng dẫn, các kích thước bổ sung được nêu trong Bảng 1, Các kích thước này là tùy chọn và không phải là yêu cầu của tiêu chuẩn này.
Bảng 1 – Kích thước của túi nhựa, vùng ghi nhãn và dung tích danh nghĩa
(chỉ có mục đích hướng dẫn)
Kích thước tính bằng milimét
| Dung tích | Chiều rộng | Chiều cao | Kích thước vùng ghi nhãn | |
| b2 ± 5 | h2 ± 5 | |||
| 100 | 75 | 120 | 60 | 85 |
| 250 | 120 | 130 | 90 | 85 |
| 400 | 120 | 170 | 100 | 100 |
| 500 | 120 | 185 | 100 | 100 |
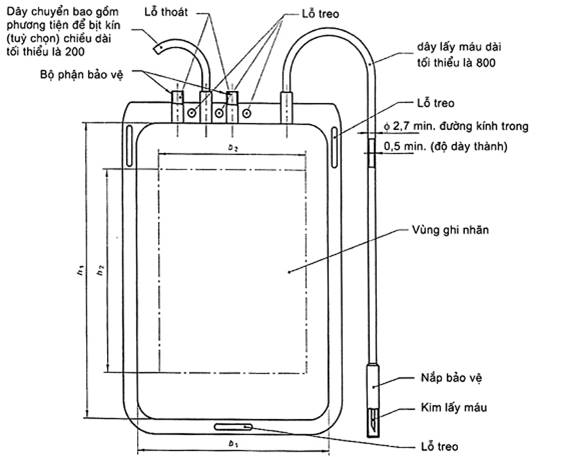
Hình 1 – Sơ đồ thể hiện túi nhựa
3.2. Ví dụ ký hiệu qui ước
Ví dụ ký hiệu qui ước của túi nhựa mềm có dung tích danh nghĩa 250 ml phù hợp với yêu cầu đã quy định trong tiêu chuẩn này như sau:
Túi lấy máu TCVN 7611 (ISO 3826) – 250
4. Thiết kế
4.1. Yêu cầu chung
Thiết kế túi nhựa phải đảm bảo an toàn và thuận lợi cho lấy máu, bảo quản, điều chế, vận chuyển, chiết tách và quản lý máu toàn phần và các chế phẩm máu. Thiết kế và sản xuất phải không gây ra ảnh hưởng bất lợi tới việc bảo quản máu và các chế phẩm máu. Túi phải cho phép điều chế huyết tương hoặc ly tâm hoặc hòa loãng các thành phần của tế bào máu trong điều kiện nguy cơ nhiễm khuẩn tối thiểu. Túi phải phù hợp với bộ dây truyền máu quy định trong ISO 1135-4. Thiết kế túi cũng phải đảm bảo có thể đặt túi vào trong cốc của máy ly tâm.
4.2. Hàm lượng khí
4.2.1. Tổng thể tích của không khí chứa trong đường thu gom máu và trong túi dùng để thu gom máu và đối với từng túi chuyển cùng các ống dẫn phụ của túi phải không vượt quá 10 ml. Thể tích của không khí chứa trong mỗi túi chuyển bổ sung và ống dẫn phụ phải không vượt quá 10 ml.
4.2.2. Khi sử dụng theo hướng dẫn của nhà sản xuất, túi nhựa phải có khả năng đựng đầy máu mà không cần không khí.
4.3. Ép dưới áp lực
Túi nhựa được rót nước ở nhiệt ở 23 0C ± 2 0C với một lượng bằng dung tích danh nghĩa của túi, rồi nối với bộ dây truyền như quy định trong ISO 1135-4 với một lỗ thông (xem 4.8) phải rỗng không bị rò rỉ trong 2 phút khi ép túi từ từ giữa hai tấm mỏng đến một áp lực bên trong là 40 kPa trên áp suất khí quyển.
4.4. Mẫu thí điểm
Túi nhựa phải được thiết kế sao cho các mẫu thí điểm không gây nhầm lẫn, sau khi sử dụng rộng rãi có thể thu gom lại để tiến hành các phép thử phòng thí nghiệm phù hợp.
4.5. Tốc độ lấy máu
4.5.1. Túi nhựa phải đủ mềm dẻo để có độ bền tối thiểu khi rót đầy trong điều kiện sử dụng bình thường.
4.5.2. Túi nhựa phải được thiết kế sao cho có khả năng được rót đầy đến dung tích danh nghĩa trong thời gian ít hơn 8 phút khi thử phù hợp ví B.2.
4.6. Dây lấy máu và dây chuyển
4.6.1. Túi nhựa có thể có một hoặc nhiều dây lấy máu hoặc dây chuyển để lấy và chiết tách máu và các chế phẩm máu.
Dây chuyển phải được lắp với một thiết bị có tác dụng ngăn cản và khi bị bẻ thì các thành phần của máu chảy tự do theo hướng đã định.
4.6.2. Các ống phải sao cho có thể hàn kín được và không bị xẹp khi sử dụng thông thường.
4.6.3. Túi nhựa được đổ đầy nước (xem Chú thích 4 ở 5.2.8) đến dung tích danh nghĩa và được hàn kín và các ống nối với túi nhựa sẽ được hàn kín và một mối nối chống rò rỉ, bền vững, chịu được lực căng 20 N tác động vào mép mối nối trong 15 giây mà không có rò rỉ. Lực căng phải được tác động vào các góc tới mép mối nối và dọc theo trục của mặt phẳng túi tại nhiệt độ 23 0C ± 2 0C.
Mối nối không được có rò rỉ và túi phải phù hợp với yêu cầu đã quy định trong 5.2.8.
4.6.4. Khi kiểm tra bằng mắt thường, dây truyền phải không được có bất kỳ vết rạn nứt, phồng giộp, vặn xoắn và các khuyết tật khác.
4.7. Kim lấy máu
Kim lấy máu phải đồng bộ với dây lấy máu và được che chắn bằng nắp bảo vệ. Nắp bảo vệ sẽ ngăn chặn sự rò rỉ của chất chống đông và/hoặc dung dịch bảo quản từ túi nhựa trong quá trình bảo quản, duy trì độ vô trùng của đường dẫn chất lỏng và có thể tháo ra được một cách dễ dàng. Nắp bảo vệ phải có tem niêm phong và được chế tạo sao cho không có khả năng thay thế hoặc mọi tác động đến nắp đều phát hiện được.
Kim lấy máu, như quy định trong TCVN 7610-3 : 2007 (ISO 1135-3), không bị lỏng khi đã lắp ráp, phải chịu được tác động của lực căng 20 N dọc trục ống trong 15 giây.
4.8. Lỗ thông
4.8.1. Túi nhựa phải có một hoặc một số cửa lỗ thông để máu và các chế phẩm của máu ra bộ dây truyền. Các lỗ thông phải có nắp kín có thể đâm thủng và không thể hàn kín lại được. Các lỗ thông đó phải nối được với bộ dây truyền mà không bị rò rỉ khi nối ghép hoặc khi sử dụng, ngay cả khi ép dưới áp lực (xem 4.3). Để đảm bảo chức năng có thể hoán đổi cho nhau, các lỗ thông phải có kích thước và thiết kế sao cho nối ghép được với dụng cụ xuyên kín (đầu kim côn) của bộ dây truyền phù hợp với ISO 1135-4. Tước khi nắp kín bị xuyên thủng bởi đầu nhọn của dụng cụ xuyên kín, các lỗ thông đã được bịt kín bởi dụng cụ xuyên kín.
4.8.2. Mỗi lỗ thông phải được lắp khít với một bộ phận niêm phong bảo đảm duy trì vô trùng bên trong.
4.9. Hệ thống treo
Túi nhựa phải có phương tiện thích hợp để treo hoặc định vị mà không gây trở ngại cho việc sử dụng túi trong quá trình lấy máu, bảo quản, điều chế, vận chuyển và quản lý máu. Lỗ treo hoặc định vị phải có khả năng chịu được lực căng 20 N tác động dọc theo trục của lỗ thông trong 60 phút tại nhiệt độ 23 0C ± 2 0C mà không bị đứt.
5. Yêu cầu
5.1. Yêu cầu chung
Túi nhựa phải trong suốt, hầu như không màu (xem 5.3.2), mềm dẻo, vô trùng, không gây sốt, không có độc tính (xem 5.4) và không vỡ trong điều kiện sử dụng (xem 5.2.5). Túi nhựa phải tương thích với vật chứa trong điều kiện bảo quản thông thường. Túi phải được tiệt trùng trong giai đoạn sản xuất cuối, và túi phải không bị dính hoặc trở nên dính trong quá trình tiệt trùng hoặc, trong quá trình bảo quản suốt thời hạn sử dụng ở nhiệt độ không vượt quá 40 0C.
Túi nhựa phải có tính sinh học, hóa học và vật lý ổn định đối với vật chứa của nó trong suốt thời hạn sử dụng và không cho phép vi khuẩn thâm nhập. Bất kỳ chất nào đó chiết lọc từ túi nhờ chất chống đông và/hoặc dung dịch bảo quản, máu và các thành phần máu, do sự tương tác hóa học hoặc sự phân hủy vật lý, phải nằm trong giới hạn quy định.
Ở nhiều nước, trong dược điển quốc gia, qui chuẩn quốc gia hoặc tiêu chuẩn có trình bày chi tiết các phép thử phù hợp để đánh giá các tương tác hóa học và vật lý như vậy. Tuy nhiên, phải sử dụng các phương pháp thử chỉ dẫn ở Bảng 2, nếu không có các qui chuẩn này.
5.2. Yêu cầu vật lý
5.2.1. Điều kiện sản xuất
Mọi quá trình liên quan trong sản xuất, lắp ráp và bảo quản của túi nhựa phải được thực hiện trong điều kiện sạch và hợp vệ sinh phù hợp với qui định hiện hành của nhà nước và các thỏa thuận quốc tế. Mọi cảnh báo phải được thực thi ở tất cả các giai đoạn để giảm nguy cơ lây nhiễm ngẫu nhiên của vi khuẩn hoặc chất lạ từ ngoài vào.
5.2.2. Tiệt trùng
5.2.2.1. Túi nhựa phải được tiệt trùng bằng nồi hấp hoặc bằng phương pháp khác đã được cơ quan nhà nước có thẩm quyền chấp thuận.
5.2.2.2. Phương pháp tiệt trùng đã sử dụng không được tác động bất lợi đến vật liệu hoặc chất chứa đựng và cũng không làm lỏng các mối ghép và làm hỏng các mối hàn trong vật liệu nhựa, cũng không làm thay đổi nghiêm trọng về hình dạng của túi nhựa.
5.2.2.3. Nhà sản xuất phải đưa ra được bằng chứng công nhận của cơ quan kiểm định nhà nước về hiệu lực của quá trình tiệt trùng đã sử dụng thực tế. Nếu cơ quan nhà nước có thẩm quyền yêu cầu phải kiểm tra thêm hiệu lực của quá trình tiệt trùng, thì phải tiến hành với từng lô tiệt trùng.
5.2.3. Độ trong suốt
Khi thử với dung dịch theo như quy định trong B.1, màu trắng sữa của dung dịch treo phải cảm nhận được khi quan sát qua túi nhựa có so sánh với một túi tương tự đã rót đầy nước.
5.2.4. Màu sắc
Vật liệu của túi nhựa phải không có màu để không ảnh hưởng đến đánh giá màu của máu.
5.2.5. Độ ổn định nhiệt
Túi nhựa đã rót nước tinh khiết đến một nửa dung tích danh nghĩa, phải chịu được thời gian lưu giữ là 24 giờ ở - 80 0C, sau đó nhúng vào nước ở 50 0C ± 2 0C trong 20 phút, rồi trở lại nhiệt độ phòng. Túi nhựa phải đáp ứng với các yêu cầu của 4.6.3, 4.9, 5.2.7 và 5.2.8.
CHÚ THÍCH 3 Nếu sử dụng dung dịch đông lạnh, túi nhựa có thể được bọc trong bao bảo vệ để tránh tiếp xúc trực tiếp giữa dung dịch đông lạnh và túi nhựa.
5.2.6. Sự bay hơi nước
Túi nhựa không có bao gói ngoài, phải được rót chất chống đông và/hoặc dung dịch bảo quản đến thể tích đã ghi nhãn, nếu có thể, với một thể tích dung dịch natri clorua [p(NaCl) = 9 g/l] bằng dung tích danh nghĩa, nút kín và ghi nhãn sẵn sàng để sử dụng. Sau đó túi nhựa được bảo quản trong điều kiện có điều hòa không khí ổn định khoảng sáu tuần tại nhiệt độ 5 0C ± 1 0C và độ ẩm tương đối tối đa là 55 % mà không hao hụt lớn hơn 2 % (khối lượng) nước từ dung dịch.
5.2.7. Tính chống vặn xoắn
Khi quay ly tâm, túi nhựa đã rót nước đến dung tích danh nghĩa phải chịu được một gia tốc 5000 g trong 30 phút tại nhiệt độ 4 0C và 37 0C mà không bị vặn xoắn lâu dài.
5.2.8. Tính chống rò rỉ1)
Khi rót nước đến dung tích danh nghĩa rồi nút kín, túi nhựa phải không bị rò rỉ trong các điều kiện ly tâm 5000 g trong 30 phút ở 4 0C, sau đó trong 30 phút ở 37 0C. Ngoài ra, túi được rót tương tự đến dung tích danh nghĩa (ngang với vạch giấy chỉ thị đã dán) rồi nút kín, phải không xuất hiện rò rỉ khi bị ép từ từ giữa hai tấm, đến áp lực bên trong tương đương 100 kPa trên áp suất khí quyển ở 23 0C ± 2 0C đạt được trong vòng 1 phút rồi duy trì trong 10 phút.
CHÚ THÍCH Khi túi nhựa được rót dung dịch chống đông, ví dụ dung dịch ACD hoặc các dung dịch khác có pH tương tự, có thể phát hiện được rò rỉ bằng cách ép túi áp vào các tấm giấy quì màu xanh rồi quan sát diễn biến của các đốm màu hồng trên giấy. Đối với dung dịch có pH khác, có thể sử dụng cùng phương pháp này với chỉ thị phù hợp. Có thể sử dụng các phương pháp thay thế có cùng cấp độ nhạy.
5.2.9. Dộ bền đánh dấu và ghi nhãn
Nhãn bị phá hủy khi cố gắng bóc nhãn.
Khi thử phù hợp với B.3, nhãn phải không bị bong khỏi túi sau khi nhấc khỏi nước. Chữ in trên nhãn hoặc trên túi phải còn rõ ràng.
5.3. Yêu cầu hóa học
5.3.1. Yêu cầu đối với chất chiết
Khi tiến hành các phép thử thích hợp trên chất chiết thu được theo A.2 và A.3.9, các giới hạn không được vượt quá quy định trong Bảng 2.
5.3.2. Yêu cầu đối với vật liệu nhựa
Khi vật liệu nhựa được thử theo phương pháp nêu trong cột 3 Bảng 3, các giới hạn chỉ ra ở cột 2 của Bảng 3 không được vượt quá.
Bảng 2 – Các giới hạn trong chất chiết
| Đặc tính | Giới hạn | Phương pháp thử |
| Chất ôxy hóa | ≤ 2 ml c(0,5 Na2S2O3) = 0,01 mol/l | A.3.1 |
| Amoniăc (NH3) | ≤ 2 mg/l | A.3.2 |
| Ion clo (Cl-) | ≤ 4 mg/l | A.3.3 |
| Độ axit hoặc kiềm | ≤ 0,4 ml c(NaOH) = 0,01 mol/l hoặc | A.3.4 |
| Cặn sau bốc hơi | ≤ 3 mg/100 ml | A.3.5 |
| Màu trắng đục | Trắng đục nhẹ nhưng không rõ hơn so với trắng đục của huyền phù đối chứng 2 | A.3.6 |
| Màu sắc | Không màu | A.3.7 |
| Hấp thụ tia cực tím (UV) | Tiêu hủy ≤ 0,2 trong dải từ 230 nm đến 360 nm | A.3.8 |
| Di(2-ethylhexyl)phthalate (DEHP) có thể chiết | ≤ 10 mg/100 ml | A.3.9 |
Bảng 3 – Các giới hạn hóa học trong vật liệu nhựa
| Đặc tính | Giới hạn | Phương pháp thử | |
| Độ tro | ≤ 1 mg/kg | A.4.1 | |
| Nguyên tố | Ba, Pb | ≤ 1 mg/kg | A.4.2.1 |
| Cd, Sn | ≤ 0,6 mg/kg | A.4.2.2 | |
| Mono vinyl clorua | ≤ 1 | A.4.3 | |
5.4. Yêu cầu sinh học
Túi nhựa không được tiết ra bất kỳ chất nào có thể ảnh hưởng bất lợi đến hiệu quả điều trị của máu và các thành phần máu, bao gồm các chất có thể bộc lộ độc tính, độc tế bào, kìm hãm vi khuẩn, diệt khuẩn, gây sốt hoặc phản ứng tan máu.
Ở nhiều nước trong dược điển quốc gia, qui chuẩn quốc gia hoặc tiêu chuẩn có trình bày chi tiết các phép thử phù hợp để đánh giá an toàn sinh học và độ vô khuẩn. Tuy nhiên, phải sử dụng phương pháp thử đã quy định ở Bảng C.1, nếu không có các qui chuẩn này.
5.4.1. Yêu cầu đối với phép thử công nhận kiểu
Phép thử công nhận kiểu phải được thiết lập và đánh giá bởi các chuyên gia trong lĩnh vực truyền và độc tính của vật liệu nhựa. Lĩnh vực này phải bao gồm các yếu tố trong 5.4.1.1 đến 5.4.1.4.
5.4.1.1. An toàn sinh học chung của túi nhựa
Vật liệu phải được đánh giá tương thích sinh học bằng cách tiến hành các phép thử phù hợp đối với các đặc tính nêu chi tiết trong Bảng C.1 và các kết quả thử phải chỉ rõ là không có độ độc.
5.4.1.2. Tương thích của túi nhựa với quá trình sản xuất và tiệt trùng
Quá trình sản xuất, tiệt trùng và sự tiếp xúc lâu dài với dung dịch chống đông, máu và các thành phần máu không được thay đổi đặc tính của vật liệu nhựa và bản thân túi nhựa.
5.4.1.3. Tương thích của vật liệu túi nhựa với chất chống đông và/hoặc dung dịch bảo quản, với máu và các thành phần máu
Sự di chuyển sau khi tiệt trùng và tiếp xúc lâu dài của các thành phần hoặc phụ gia của vật liệu nhựa phải không làm thay đổi đặc tính của chất chống đông và/hoặc dung dịch bảo quản, của máu và các thành phần máu hoặc gây ra bất kỳ nguy cơ độc hại nào cho bệnh nhân.
5.4.1.4. An toàn sinh học của túi nhựa với các yếu tố tế bào của máu và thành phần máu
Phép thử công nhận kiểu phải bao gồm vấn đề an toàn sinh học.
5.4.2. Yêu cầu đối với phép thử lô
5.4.2.1. Sự vô khuẩn
Túi nhựa và các chất trong túi phải vô trùng; hướng dẫn về thử nghiệm vô trùng nêu trong C.3.1.
5.4.2.2. Chất gây sốt
Túi nhựa phải được đánh giá về sự không có chất gây sốt bằng cách sử dụng một phép thử phù hợp (hướng dẫn về thử nghiệm chất gây sốt nêu trong C.3.2) và các kết quả phải chỉ ra bằng túi nhựa là không có khả năng gây sốt.
6. Bao gói
Túi nhựa phải được đặt bên trong một bao bì kín, phù hợp với các yêu cầu quy định dưới đây.
6.1. Túi nhựa phải không bị hao hụt nhiều hơn 2,5 % (khối lượng) nước từ chất chống đông và/hoặc dung dịch bảo quản trong quá trình lưu giữ 1 năm ở độ ẩm 55 %, tại 23 0C ± 2 0C và áp suất khí quyển.
6.2. Nhà sản xuất phải xác minh thời gian sử dụng của túi nhựa trên cơ sở dữ liệu ổn định. Khi chứa chất chống đông và/hoặc dung dịch bảo quản, thời hạn sử dụng không được lớn hơn so với thời gian chứa nước có hao hụt 5 % (khối lượng), nhưng trong mọi trường hợp không được nhỏ hơn 2 năm.
CHÚ THÍCH 5 Trong tiêu chuẩn này thuật ngữ “thời hạn sử dụng” nhằm chỉ khoảng thời gian giữa ngày tháng tiệt trùng và ngày mà túi nhựa không được phép sử dụng để thu gom máu.
6.3. Bề mặt bên trong của bao gói ngoài phải không tương tác với bất kỳ chất nào chứa trong bao gói và phải được xử lý để ngăn ngừa sự sinh trưởng của mốc hoặc nấm ở bên trong túi. Nếu sử dụng thuốc diệt nấm, phải có bằng chứng để chỉ rõ là không có sự thâm nhập hoặc tác động độc hại nào lên túi nhựa và các chất trong bao gói.
6.4. Bao gói ngoài phải được làm kín có niêm phong và để ngăn ngừa việc mở ra hoặc đóng lại mà không phá hủy dấu niêm phong.
6.5. Bao gói ngoài phải đủ bền để chống lại hư hỏng trong các điều kiện va chạm và sử dụng thông thường.
6.6. Bao gói ngoài phải không ngấm độc tương xứng có thể gây ra nguy hiểm khi sử dụng.
6.7. Túi nhựa và các thành phần phải được sắp xếp trong bao gói ngoài sao cho dây lấy máu và dây nối (dây chuyển) không bị thắt nút, vặn xoắn và dính bết.
7. Ghi nhãn
Đánh dấu và ghi nhãn của túi nhựa phải phù hợp với các qui định hiện hành của Nhà nước và phải bao gồm các yêu cầu quy định trong 7.1 đến 7.4.
7.1. Ghi nhãn trên túi nhựa
Nhãn phải bao gồm các thông tin sau:
a) mô tả nội dung;
b) bản chất và thể tích, tính bằng mililit, hoặc khối lượng tính bằng gam của chất chống đông và/ hoặc dung dịch bảo quản và mọi vật liệu khác được giới thiệu; thể tích tính bằng mililit hoặc khối lượng tính bằng gam của máu và các thành phần máu lấy được;
c) công bố: “VÔ TRÙNG VÀ KHÔNG CÓ CHẤT GÂY SỐT”;
d) chỉ dẫn: “KHÔNG SỬ DỤNG NẾU THẤY BẤT KỲ DẤU HIỆU HƯ HỎNG”, hoặc lời thay thế tương tự;
e) chỉ dẫn: “TÚI KHÔNG ĐƯỢC DÙNG LẠI”, hoặc lời thay thế tương tự;
f) chỉ dẫn: “KHÔNG ĐƯỢC GÂY THỦNG”;
g) hướng dẫn sử dụng túi nhựa, bao gồm các điều kiện bảo quản túi nhựa khi rót đầy máu và các thành phần máu.
h) tên và địa chỉ nhà sản xuất và/ hoặc tên và địa chỉ nhà chịu trách nhiệm cung cấp;
i) ký hiệu lô;
j) ngày tháng hết hạn sử dụng đối với túi nhựa chưa sử dụng được biểu thị bằng lời chỉ dẫn: “KHÔNG CHỨA MÁU SAU NGÀY….”.
7.2. Ghi nhãn trên bao gói ngoài
Nhãn phải bao gồm các thông tin sau:
a) tên và địa chỉ nhà sản xuất và/hoặc tên và địa chỉ của nhà chịu trách nhiệm cung cấp;
b) mô tả nội dung;
c) ngày tháng hết hạn sử dụng;
d) hướng dẫn: “KHÔNG ĐƯỢC SỬ DỤNG NHIỀU HƠN n2) NGÀY SAU KHI MỞ BAO GÓI NGOÀI”;
e) ký hiệu lô.
7.3. Ghi nhãn trên thùng vận chuyển
Nhãn phải bao gồm các thông tin sau:
a) tên và địa chỉ nhà sản xuất và/hoặc tên và địa chỉ của người chịu trách nhiệm cung cấp;
b) mô tả nội dung;
c) điều kiện lưu giữ.
7.4. Yêu cầu ghi nhãn
Nhãn phải đảm bảo:
a) định nhóm máu, ví dụ ABO và nhóm Rh, và số tham chiếu có thể được ghi trên túi nhựa, và một số tham chiếu thích hợp ghi trên mẫu thí điểm; cũng phải có khoảng trống tương xứng cho các nội dung theo qui định hiện hành của Nhà nước;
b) để trống một phần túi nhựa và không ghi nhãn để có thể kiểm tra vật chứa bằng cách nhìn bên ngoài;
c) không có sự khuếch tán của mực từ nhãn vào vật liệu nhựa của túi gây tác hại cho vật chứa;
d) chữ in trên nhãn giữ nguyên rõ ràng trong thời hạn sử dụng;
e) có thể sử dụng bút mực hoặc bút chì để viết lên nhãn;
f) mọi chất dính sử dụng trên nhãn không được phép tạo điều kiện cho vi khuẩn phát triển và không có tác động có hại trên túi nhựa hoặc vật chứa trong túi.
Nhãn do nhà sản xuất gắn lên túi nhựa, trước khi lấy máu, không được ghi bất kỳ thông tin đặc biệt liên quan đến máu hoặc thành phần máu hoặc loại máu hoặc thành phần máu sẽ lấy.
8. Áp dụng các phép thử
CHÚ THÍCH 6 Phép thử công nhận kiểu và phép thử lô nêu trong 8.1 và 8.2 chỉ với mục đích hướng dẫn.
8.1. Phép thử công nhận kiểu
Trên công thức nhựa mới, trên công thức đã thỏa thuận trong đó mọi thay đổi đã thực hiện hoặc trên sự thay đổi chất chống đông và/hoặc dung dịch bảo quản, có thể phải lặp lại một loạt phép thử hóa quy định trong A.3 và A.4, một loạt các phép thử an toàn sinh học (hướng dẫn thử nghiệm sinh học được nêu trong Phụ lục C) và các phép thử trong Phụ lục B.
8.2. Phép thử lô
Trên mỗi lô sản xuất túi nhựa thành phẩm, phải tiến hành các phép thử quy định trong 4.2, 4.3, 4.6.3, 4.7 đến 4.9, 5.2.4, 5.2.7 đến 5.2.9 và trong điều 7 và 9. Ngoài ra, cần tiến hành các phép thử vô trùng và chất gây sốt (xem 5.4.2.1 và 5.4.2.2) trên mỗi lô đã tiệt trùng.
CHÚ THÍCH
7) Đối với túi nhựa chứa chất chống đông và/hoặc dung dịch bảo quản, thuật ngữ “lô” có nghĩa là số lượng của túi nhựa đã chuẩn bị, đã rót đầy dung dịch chống đông từ một lô đơn và đã tiệt trùng trong vòng một chu kỳ làm việc liên tục.
8) Đối với túi nhựa không chứa chất chống đông và/hoặc dung dịch bảo quản, thuật ngữ “lô” có nghĩa là số lượng túi nhựa đã chuẩn bị trong vòng một ngày làm việc và đã tiệt trùng trong một chu trình.
9. Dung dịch chống đông và/hoặc dung dịch bảo quản
Chất lượng của dung dịch chống đông và/hoặc dung dịch bảo quản, nếu có, phải đáp ứng yêu cầu của dược điển quốc gia và qui chuẩn quốc gia.
PHỤ LỤC A
(Quy định)
CÁC PHÉP THỬ HÓA HỌC
A.1. Quy định chung
Lấy các vật liệu để thử nghiệm từ máu và các dẫn xuất của máu tiếp xúc vật liệu của túi nhựa thành phẩm, rỗng và đã tiệt trùng, tức là ở trạng thái chúng có thể được sử dụng để truyền, lấy máu, chiết tách và các quy trình quản lý, bao gồm các tấm nhựa dùng làm túi lấy máu và ống nhựa dùng làm dây lấy máu, dây chuyển và bất cứ bộ phận nào sẽ được đưa vào tiếp xúc với máu và chế phẩm máu.
A.2. Chuẩn bị dung dịch chiết và dung dịch trắng
A.2.1. Chuẩn bị mẫu
Các phép thử quy định trong A.3 yêu cầu diện tích bề mặt là 1250 cm2 đối với mỗi mẫu nhựa ở dạng tấm hoặc ống.
A.2.1.1. Mẫu dạng tấm
Sử dụng một mẫu không có chữ in hoặc nhãn, có diện tích bề mặt là 625 cm2 (diện tích bề mặt tổng cộng của cả hai mặt là 1250 cm2). Cắt mẫu thành các miếng diện tích xấp xỉ 10 cm2 (một mặt).
A.2.1.2. Mẫu dạng ống
Tính chiều dài yêu cầu l, biểu thị bằng centimét như sau:
Trong đó:
d1 là đường kính trọng, tính bằng xentimét;
d2 là đường kính ngoài, tính bằng xentimét.
Cắt ống thành các đoạn dài xấp xỉ 5 cm.
A.2.2. Chuẩn bị dung dịch chiết
Để gạt bỏ mọi chất nhiễm bẩn bề mặt, chất hạt, xơ vải, chất chống đông và/hoặc dung dịch bảo quản, v.v…, đặt mẫu cắt trong bình thủy tinh có nút đậy, đổ 100 ml nước cất để nguội, lắc vài lần rồi gạn cạn nước. Lặp lại động tác này một lần nữa.
Đặt mẫu cắt trong một bình thủy tinh borosilicat với 250 ml nước cất và đậy nắp bình. Đun nóng bình trong hơi nước bão hòa ở 121 0C ± 1 0C trong 20 phút, làm nguội nhanh đến nhiệt độ phòng (23 0C) rồi điều chỉnh thể tích đến 250 ml bằng nước cất. Các mẫu nhựa không được có khuynh hướng trương dính với nhau.
A.2.3. Chuẩn bị dung dịch trắng
Để kiểm tra, chuẩn bị một mẫu trắng theo cách tương ứng, bỏ qua mẫu nhựa.
A.3. Phép thử trên dung dịch chiết
A.3.1. Chất ôxy hóa
Thêm 20 ml dung dịch kali permanganat [c(KMnO4) = 0,002 mol/l] và 1 ml dung dịch axit sunfuric [c(H2SO4 = 1 mol/l] vào 20 ml dung dịch chiết (xem A.2.2) trong một bình nón thủy tinh borosilicat. Giữ hỗn hợp ở nhiệt độ phòng (23 0C ± 5 0C) trong 15 phút. Thêm 0,1 g kali iodua và 5 giọt dung dịch tinh bột. Chuẩn độ bằng dung dịch natri thiosunfat [c(0,5Na2S2O3) = 0,01 mol/l].
Tại cùng thời điểm tiến hành chuẩn độ mẫu trắng.
Xác định hiệu số thể tích của dung dịch natri thiosunfat dùng trong hai lần chuẩn độ.
A.3.2. Amoniac
Dung dịch chiết phải phù hợp với phép thử giới hạn về amoniăc.
A.3.3. Ion clorua
Thêm 0,3 ml dung dịch bạc nitrat [c(AgNO3) = 0,1 mol/l] vào 0,15ml axit nitric loãng. Thêm dung dịch có được vào 15 ml dung dịch chiết.
Chuẩn bị dung dịch đối chứng theo cùng biện pháp, bằng cách sử dụng 12 ml dung dịch clorua tiêu chuẩn (5 ppm Cl-) và 3 ml nước.
Lắc hỗn hợp. Sau 2 phút, dung dịch chiết không được đục hơn so với dung dịch đối chứng. Phải tránh ánh nắng ban ngày.
A.3.4. Độ axit hoặc độ kiềm
Khi thêm 2 giọt dung dịch phenolphtalein vào 10 ml dung dịch chiết, dung dịch phải không nhuộm màu đỏ. Khi thêm 0,4 ml dung dịch natri hydroxit [c(NaOH) = 0,01 mol/l], dung dịch phải nhuộm màu đỏ.
Khi thêm 0,8 ml axit clohydric [c(HCl) = 0,01 mol/l], màu đỏ sẽ biến mất. Thêm 5 giọt metyl đỏ dung dịch sẽ tạo thành màu da cam.
A.3.5. Cặn sau bốc hơi
Bốc hơi 100 ml dung dịch chiết đến khô cạn trong một chậu nước rồi sấy tại 105 0C đến khối lượng không đổi.
Xác định khối lượng của cặn.
A.3.6. Độ trong và mức độ trắng đục
Sử dụng ống thử đồng màu, trong suốt, thủy tinh trung tính có một đáy phẳng và đường kính trong từ 15 mm đến 25 mm, so sánh chất lỏng được kiểm tra với huyền phù đối chứng mới được chuẩn bị như mô tả dưới đây, chiều sâu của lớp là 40 mm. So sánh các dung dịch trong ánh sáng khuếch tán ban ngày sau khi chuẩn bị huyền phù đối chứng 5 phút, quan sát chúng ở tư thế thẳng đứng dựa vào một nền màu đen. Sự khuếch tán ánh sáng phải sao cho huyền phù đối chứng 1 có thể dễ dàng phân biệt được với nước và sao cho huyền phù đối chứng 2 có thể dễ dàng phân biệt được với huyền phù đối chứng 1.
A.3.6.1. Thuốc thử
A.3.6.1.1. Dung dịch hydrazin sunfat
Hòa tan 1 g hydrazin sunfat trong nước rồi pha loãng đến 100 ml. Để yên trong 4 giờ đến 6 giờ.
A.3.6.1.2. Dung dịch hexametylentetramin
Hòa tan 2,5 g hexametylentetramin trong 25 ml nước trong bình thủy tinh có nút.
A.3.6.1.3. Huyền phù trắng đục ban đầu
Thêm 25 ml dung dịch hydrazin sunfat (A.3.6.1.1) vào dung dịch hexametylentetramin (A.3.6.1.2). Trộn đều rồi để yên trong 24 giờ.
Huyền phù này phải ổn định trong 2 tháng, với điều kiện là nó được bảo quản trong bình thủy tinh không có khuyết tật bề mặt. Huyền phù không được bám dính vào thủy tinh và phải được trộn đều trước khi sử dụng.
A.3.6.1.4. Chuẩn trắng đục
Pha loãng 15 ml huyền phù trắng đục ban đầu (A.3.6.1.3) đến 1000 ml bằng nước.
Huyền phù này phải mới được chuẩn bị và có thể được lưu giữ tối đa là 24 giờ.
A.3.6.1.5. Huyền phù đối chứng
Chuẩn bị huyền phù đối chứng phù hợp với Bảng A.1. Trộn đều và lắc trước khi sử dụng.
Bảng A.1 – Huyền phù đối chứng
Thể tích tính bằng mililít
| Huyền phù đối chứng | 1 | 2 | 3 | 4 |
| Chuẩn trắng đục | 5 | 10 | 30 | 50 |
| Nước | 95 | 90 | 70 | 50 |
A.3.6.2. Biểu thị kết quả
A.3.6.2.1. Chất lỏng được đánh giá là trong nếu độ trong của nó giống như độ trong của nước hoặc của dung môi đã sử dụng, khi kiểm tra trong điều kiện đã mô tả trên, hoặc nếu độ trắng đục của nó không dễ thấy hơn độ trắng đục của huyền phù đối chứng 1.
A.3.6.2.2. Chất lỏng được đánh giá là trắng đục nhẹ nếu độ trắng đục của nó dễ thấy hơn A.3.6.2.1, nhưng không dễ thấy hơn độ trắng đục của huyền phù đối chứng 2.
A.3.6.2.3. Chất lỏng được đánh giá là trắng đục nếu độ trắng đục của nó dễ thấy hơn A.3.6.2.2, nhưng không dễ thấy hơn độ trắng đục của huyền phù đối chứng 3.
A.3.6.2.4. Chất lỏng là trắng đục cao nếu độ trắng đục của nó dễ thấy hơn A.3.6.2.3, nhưng không dễ thấy hơn độ trắng đục của huyền phù đối chứng 4.
A.3.7. Mức độ nhuộm màu
Kiểm tra mức độ nhuộm màu của chất lỏng trong dải đỏ - vàng – nâu được tiến hành bởi một trong hai phương pháp quy định trong A.3.7.1 và A.3.7.2.
A.3.7.1. Phương pháp 1
Sử dụng các ống không màu, trong suốt, thủy tinh trung tính có đường kính trong 12 mm, so sánh 2 ml chất lỏng được kiểm tra với 2 ml nước. So sánh màu trong ánh sáng khuếch tán ban ngày, quan sát chúng ở tư thế nằm ngang dựa vào một nền màu trắng.
A.3.7.2. Phương pháp 2
Sử dụng các ống không màu, trong suốt, thủy tinh trung tính có đường kính trong 16 mm, so sánh 10 ml chất lỏng được kiểm tra với 10 ml nước. Kiểm tra cột chất lỏng xuôi theo trục thẳng đứng của ống trong ánh sáng khuếch tán ban ngày dựa vào một nền màu trắng.
A.3.7.3. Biểu thị kết quả
Chất lỏng được đánh giá là không màu nếu nó có sự xuất hiện của nước trong điều kiện như quy định đối với phương pháp 1 và phương pháp 2.
A.3.8. Hấp thụ tia cực tím (UV)
Xác định sự hấp thụ tia UV của dung dịch chiết trong cuvét 1 cum để trống. Sự hấp thụ được xác định trong dải từ 230 nm đến 360 nm.
A.3.9. Xác định di-(2-ethylhexyl)phthalat (DEHP) có thể chiết
A.3.9.1. Thuốc thử
A.3.9.1.1. Etanol: từ 95,1 % (V/V) đến 96,6 % (V/V), p từ 0,8050 g/ml đến 0,8123 g/ml.
A.3.9.1.2. Dung môi chiết: hỗn hợp nước ethanol có tỷ trọng từ 0,9373 g/ml đến 0,9378 g/ml, xác định được bằng tỷ trọng kế.
A.3.9.1.3. Di-(2-ethylhexyl)phthalat (C24H38O4): không màu, chất lỏng có dầu không hòa tan được trong nước, hòa tan trong dung môi hữu cơ: p từ 0,982 g/ml, chỉ số khúc xạ tại 20 0C là ![]() từ 1,486 đến 1,487.
từ 1,486 đến 1,487.
A.3.9.2. Chuẩn bị dung dịch chuẩn
A.3.9.2.1. Dung dịch 1
Hòa tan 1 g DEHP (A.3.9.1.3) trong etanol (A.3.9.1.1) rồi pha loãng đến 100 ml bằng etanol.
A.3.9.2.2. Dung dịch 2
Pha loãng dung dịch (A.3.9.2.1) đến 100 ml bằng etanol.
A.3.9.2.3. Dung dịch chuẩn từ A đến E
A: Pha loãng 20 ml dung dịch 2 (A.3.9.2.2) đến 100 ml bằng dung môi chiết (A.3.9.1.2) (DEHP hàm lượng 20 mg/100ml).
B: Pha loãng 10 ml dung dịch 2 đến 100 ml bằng dung môi chiết (DEHP hàm lượng: 10 mg/100 ml).
C: Pha loãng 5 ml dung dịch 2 đến 100 ml bằng dung môi chiết (DEHP hàm lượng: 5 mg/100 ml).
D: Pha loãng 2 ml dung dịch 2 đến 100 ml bằng dung môi chiết (DEHP hàm lượng: 2 mg/100 ml).
E: Pha loãng 1 ml dung dịch 2 đến 100 ml bằng dung môi chiết (DEHP hàm lượng: 1 mg/100 ml).
A.3.9.3. Đường cong hiệu chuẩn
Đo độ hấp thụ cực đại của các dung dịch chuẩn (A.3.9.2.3) tại 272 nm, sử dụng dung môi chiết như dung dịch đối chứng và đồ thị đường cong của chất hấp thụ dựa vào nồng độ DEHP.
A.3.9.4. Quy trình chiết
Rót một thể tích dung môi chiết đã đun nóng đến 37 0C vào túi nhựa rỗng đến một nửa dung tích danh nghĩa qua dây lấy máu. Đuổi hết không khí khỏi túi rồi nút kín dây lấy máu. Nhúng túi đã rót ở vị trí nằm ngang trong một chậu nước duy trì ở 37 0C ± 1 0C trong (60 ± 1) phút không rung lắc. Lấy túi khỏi chậu nước, xoay ngược túi mười lần rồi đổ chất chứa trong túi vào một bình thủy tinh.
Đô độ hấp thụ cực đại tại 272 nm sử dụng dung môi chiết như là dung dịch đối chứng.
A.3.9.5. Biểu thị kết quả
Xác định số lượng DEHP có thể chiết bằng cách so sánh kết quả thu được đối với túi nhựa (xem A.3.9.4) với đường cong hiệu chuẩn độ hấp thụ đối với dung dịch chuẩn (xem A.3.9.3).
A.4. Phép thử với vật liệu nhựa
A.4.1. Xác định tro
Sử dụng mẫu ở dạng tấm hoặc dạng ống không có chữ in hoặc nhãn.
Cặn tro phải được xác định theo TCVN 6087:2004 (ISO 247:1990), phương pháp B.
A.4.2. Xác định các nguyên tố
A.4.2.1. Xác định hàm lượng bari và chì
Đốt 10 g vật liệu nhựa trong lò silic dioxit. Hòa tan cặn tro trong 5 ml axit clohydric (p = 1,18 g/ml) rồi bay hơi đến khô trong chậu nước. Hòa tan cặn tro trong 10 ml dung dịch axit clohydric [c(HCl)=1 mol/l].
Xác định hàm lượng bari và chì bằng quang phổ hấp thụ nguyên tử (AAS).
A.4.2.2. Xác định hàm lượng thiếc và cadimi
Đặt 5 g vật liệu nhựa trong bình đốt. Thêm 30 ml axit sunfuric (p = 1,83 g/ml) rồi đun nóng cho đến khi thu được khối xiro màu đen. Thêm dung dịch hydro peoxit 30 % (V/V) cho đến khi thu được chất lỏng không màu. Làm nguội và pha loãng đến 50 ml bằng nước.
Xác định hàm lượng thiếc bằng quang phổ hấp thụ nguyên tử không có ngọn lửa và hàm lượng cadimi bằng quang phổ hấp thụ nguyên tử ngọn lửa (AAS).
A.4.3. Xác định monomer vinyl clorua
A.4.3.1. Thuốc thử
Trong quá trình phân tích, ngoại trừ các công bố khác, chỉ sử dụng các thuốc thử đã được ghi nhận có phẩm cấp phân tích.
CẢNH BÁO – Vinyl clorua là chất khí nguy hiểm ở nhiệt độ bình thường.
Vinyl clorua là một chất gây ung thư.
Vinyl clorua phải được tiếp xúc trong tủ hút thông gió tốt và nhân viên phải đeo găng làm bằng vật liệu ví dụ như neopren không dễ hấp thụ vinyl clorua. Phải cẩn thận trong việc loại bỏ một cách an toàn mọi dung dịch có chứa vinyl clorua.
A.4.3.1.1. Chất phản ứng dietyl ete tinh chế: Dietyl ete [(C2H5)2O] tinh chế để sử dụng như chất chuẩn nội.
A.4.3.1.2. Dimetylaxetamid: N,N-Dimetylaxetamid (C4H9NO), Mr = 87,12; chất lỏng không màu, có thể trộn lẫn với nước và với nhiều dung môi hữu cơ, p = 0,94 g/ml, điểm sôi ![]() 165 0C.
165 0C.
A.4.3.1.3. Vinyl clorua, độ tinh khiết cao hơn 99,5 %.
A.4.3.1.4. Dimetylstearylamid3): N, N – Dimetylstearylamid (C20H41NO2), Mr = 327,5; một khối màu trắng hoặc trắng nhạt, có thể hòa tan được trong nhiều dung môi hữu cơ, điểm nóng chảy ≈ 51 oC.
A.4.3.1.5. Polyetylenglycol 4003): Mr ![]() 400; chất lỏng không màu hoặc gần như không màu, sền sệt, có thể trộn lẫn với nước, có thể hòa tan tốt trong axeton, rượu cồn và clorofom.
400; chất lỏng không màu hoặc gần như không màu, sền sệt, có thể trộn lẫn với nước, có thể hòa tan tốt trong axeton, rượu cồn và clorofom.
A.4.3.2. Chuẩn bị dung dịch chuẩn nội
Sử dụng ống tiêm cực nhỏ, tiêm 10 ![]() dietyl ete (A.4.3.1.1), như là dung dịch chuẩn nội, vào 20 ml dimetylaxetamid (A.4.3.1.2), nhúng đầu kim vào trong dung môi. Ngay trước khi sử dụng pha loãng dung dịch đến 1000 lần thể tích của nó bằng dimetylaxetamid (A.4.3.12).
dietyl ete (A.4.3.1.1), như là dung dịch chuẩn nội, vào 20 ml dimetylaxetamid (A.4.3.1.2), nhúng đầu kim vào trong dung môi. Ngay trước khi sử dụng pha loãng dung dịch đến 1000 lần thể tích của nó bằng dimetylaxetamid (A.4.3.12).
A.4.3.3. Chuẩn bị dung dịch thử
Đặt 1 g vật liệu cần kiểm tra trong lọ 50 ml rồi thêm 10 ml dung dịch chuẩn nội (A.4.3.2). Đậy lọ và vặn chặt nút. Lắc đều. Đặt lọ trong chậu nước ở 60 0C ± 1 0C trong 2 giờ.
A.4.3.4. Chuẩn bị dung dịch vinyl clorua ban đầu
Đặt 50 ml dimetylaxetamid (A.4.3.1.2) trong lọ 50 ml; đậy lọ và vặn chặt nút. Cân lọ và chất chứa trong lọ chính xác đến 0,1 mg. Hút vinyl clorua thể khí (A.4.3.1.3) vào ống tiêm khí 50 ml. Lắp kim tiêm dưới da vào ống tiêm rồi bơm từ từ thể tích vinyl clorua vào lọ đang lắc nhẹ và tránh tiếp xúc giữa chất lỏng và kim tiêm. Cân lại lọ. Sự tăng khối lượng khoảng 60 mg.
1 dung dịch thu được như vậy chứa khoảng 1,2
vinyl clorua.
A.4.3.5. Chuẩn bị dung dịch chuẩn vinyl clorua
Pha loãng 5 ml dung dịch vinyl clorua ban đầu đến 20 ml bằng dimetylaxetamid (A.4.3.1.2).
A.4.3.6. Chuẩn bị dung dịch đối chứng
Đặt 10 ml dung dịch chuẩn nội (A.4.3.2) vào từng lọ trong số sáu lọ 50 ml. Đậy lọ và vặn chặt nút. Tiêm 1 , 2
, 3
, 5
và 10
dung dịch chuẩn vinyl clorua (A.4.3.5), lần lượt, vào năm lọ. Sáu dung dịch thu được chứa 0
và
vinyl clorua. Lắc đều đặt các lọ trong chậu nước ở 60 0C ± 1 0C trong 2 giờ.
A.4.3.7. Quy trình ghi sắc ký
Thực hiện quy trình ghi sắc ký bằng cách sử dụng
a) cột thép không rỉ, dài 3 m có đường kính trong 3 mm, nhồi cột bằng điatomit để ghi sắc ký khí đã thấm đẫm bằng dimetyl stearylamid (A.4.3.1.4) 5 % (khối lượng) và polyetylenglycol 400 (A.4.3.1.5) 5 % (khối lượng).
b) nitơ để ghi sắc ký như một khí mang có lưu lượng là 30 ml/phút.
c) detector ion hóa ngọn lửa
Duy trì nhiệt độ của cột tại 45 0C, của mũi tiêm tại 100 0C và của detector tại 150 0C.
Tiêm 1 ml pha khí đã hút từ khoảng chứa thêm trên dung dịch thử (A.4.3.3) và từ khoảng chứa thêm trên dung dịch đối chứng (A.4.3.6) vào cột.
Xác định lượng vinyl clorua trong dung dịch thử.
A.4.3.8. Biểu thị kết quả
Tính số lượng vinyl clorua, biểu thị bằng microgam trên gam vật liệu thử.
PHỤ LỤC B
(Quy định)
CÁC PHÉP THỬ VẬT LÝ
B.1. Thử độ trong suốt
Rót vào túi nhựa rỗng đến thể tích danh nghĩa của túi một thể tích huyền phù trắng đục ban đầu (A.3.6.1.3) đã pha loãng đến độ hấp thụ là 0,37 đến 0,43 tại 640 nm (hệ số pha loãng khoảng 1 : 16) trong cuvét 1 cm.
B.2. Thử tốc độ lấy máu
Từ một nguồn chứa 500 ml chất lỏng ở nhiệt độ 37 0C ± 2 0C có độ nhớt 3,4 x 10-6 m2/s tại 37 0C và dưới áp suất là 9,3 kPa, tiêm vào túi tại nhiệt độ 23 0C ± 2 0C qua kim lấy máu có đường kính trong là 1,4 mm trong cùng mức độ thủy tĩnh như ở đỉnh túi. Kim lấy máu phải phù hợp với TCVN 7610-3 : 2007 (ISO 1135-3).
CHÚ THÍCH 9 Chất lỏng phù hợp để sử dụng trong phép thử này là dung dịch gluco trong nước (400 g/l).
B.3. Thử độ bền của nhãn
Túi nhựa đã đổ đầy đến thể tích danh nghĩa và nút kín, được lưu giữ trong 5 ngày ở nhiệt độ 5 0C ± 1 0C. Lúc đầu phải đặt thời gian là 24 giờ ở nhiệt độ tối đa là – 40 0C, sau đó là 24 giờ ở 5 0C ±1 0C. Túi nhựa đã có nhãn và/hoặc đã in chữ phải được chìm ngập trong nước chảy qua vòi duy trì ở nhiệt độ 20 0C ± 1 0C trong 24 giờ.
PHỤ LỤC C
(tham khảo)
CÁC PHÉP THỬ SINH HỌC
C.1. Quy định chung
An toàn sinh học của vật liệu sử dụng làm túi nhựa phụ thuộc mức độ lớn vào bản chất cụ thể của giới hạn sử dụng. Không thể quy định một bộ các phương pháp thử tính tương thích cần thiết và đầy đủ để xác minh an toàn sinh học cho mọi vật liệu và ứng dụng. Phạm vi thử nghiệm an toàn sinh học của vật liệu là một lĩnh vực mới liên quan với các phương pháp hoàn thiện đang tiến triển nhanh chóng; bởi vậy, phụ lục này chỉ đưa ra những nguyên tắc hướng dẫn.
C.2. Phép thử công nhận kiểu
Các phương pháp thử sinh học đã liệt kê trong Bảng C.1 phải được coi là những yêu cầu tối thiểu. Có thể thực hiện các phép thử bổ sung nếu tình trạng hiện hành yêu cầu các phép thử như vậy.
Các phương pháp thử phải tiến hành phù hợp với các yêu cầu như quy định trong dược điển quốc gia, đạo luật chính phủ hoặc tiêu chuẩn nhà nước.
Khi không có các đạo luật nhà nước, các phép thử này có thể được thực hiện phù hợp với các đạo luật đã giới thiệu như liệt kê trong Bảng C.1 và phải được đánh giá bởi chuyên gia trong lĩnh vực độc tính của vật liệu nhựa.
C.3. Phép thử lô
C.3.1. Độ vô trùng
Phải tiến hành theo các yêu cầu của dược điển quốc gia hoặc tiêu chuẩn nhà nước nêu chi tiết các phép thử vô trùng phù hợp. Tuy nhiên, khi không có các đạo luật như vậy, phải sử dụng phương pháp thử đã giới thiệu trong C.2.7 ở Bảng C.1.
C.3.2. Chất gây sốt
Phải tiến hành theo các yêu cầu của dược điển quốc gia hoặc tiêu chuẩn nhà nước nêu chi tiết các phép thử vô trùng phù hợp. Tuy nhiên, khi không có các đạo luật như vậy, phải sử dụng phương pháp thử đã giới thiệu trong C.2.6 ở Bảng C.1.
C.4. Tan máu
Mong muốn quy định một phép thử về tiêu máu có thể so sánh được trong tiêu chuẩn này bởi vì trong hầu hết dược điển và/hoặc tiêu chuẩn không có phép thử về hiệu ứng tiêu máu.
C.4.1. Chuẩn bị dung dịch treo hồng cầu
Pha loãng một thể tích máu người mới chuẩn bị, đã chống đông theo dược điển quốc gia, với năm thể tích dung dịch natri clorua [p(NaCl) = 9 g/l] đã tiệt trùng. Ly tâm trong 5 phút tại 1500 g đến 2000 g ở máy ly tâm văng. Gạt bỏ lớp nước trong trên mặt rồi lặp lại cách xử lý huyền phù erythrocyt trong cùng điều kiện với cùng thể tích của dung dịch natri clorua.
Pha loãng dung dịch thu được bằng dung dịch natri clorua [p(NaCl) = 9 g/l] đã tiệt trùng theo tỷ lệ 1 : 9. Phải sử dụng dung dịch này trong vòng 6 giờ sau khi làm và để ở nhiệt độ phòng.
C.4.2. Quy trình
Cho bay hơi 125 ml dung dịch chiết (A.2.2) ở nhiệt độ 100 0C. Hòa tan cặn trong 5 ml dung dịch natri clorua [p(NaCl) = 9 g/l] đã tiệt trùng. Thêm 1 ml huyền phù erythrocyt (C.4.1) và để yên hỗn dịch trong 20 phút ở nhiệt độ 37 0C ± 1 0C. Ly tâm trong 5 phút tại 1500 g đến 2000 g ở máy ly tâm văng.
Đồng thời chuẩn bị huyền phù trắng trong cùng điều kiện, không thêm cặn khô vào lượng bay hơi của dung dịch chiết.
CHÚ THÍCH 10 Phép thử đã mô tả có thể không phát hiện ra thành phần chất bốc của dung dịch chiết; tuy nhiên có thể bằng cách cô đặc dung dịch chiết thì thu được dung dịch có độ nhạy cao hơn.
Đo độ hấp thụ của lớp trong trên bề mặt tại 540 nm trong cuvét 1 cm có sử dụng huyền phù trắng như một đối chứng. Độ hấp thụ của dung dịch thử so với mẫu trắng không được chênh lệch lớn hơn 10 %.
Bảng C.1 – Giới thiệu các phương pháp thử sinh học
| Khoản | Phép thử | Giới thiệu phương pháp thử được sử dụng |
| C.2.1 | Độc tính nuôi cấy tế bào | ASTM F 813, Thực hành đánh giá nuôi cấy tế bào tiếp xúc trực tiếp của vật liệu dùng cho trang thiết bị y tế. Dược điển Pháp BS 5736, Phần 10: Phương pháp thử độ độc tế bào trong nuôi cấy của dung dịch chiết từ trang thiết bị y tế |
| C.2.2 | Sự tan máu | Dược điển châu Âu hoặc C.4 của tiêu chuẩn này |
| C.2.3 | Tiêm hệ thống (độc tính cấp) | BS 5736, phần 3: Phương pháp thử độc tính hệ thống; đánh giá độc tính cấp của dung dịch chiết từ trang thiết bị y tế Dược điển châu Âu Dược điển Hợp chủng quốc Hoa Kỳ |
| C.2.4 | Độ nhạy | ASTM F 748, Thực hành lựa chọn phương pháp thử sinh học di truyền đối với vật liệu và trang thiết bị BS 5736, Phần 6: Phương pháp thử sự nhạy cảm. Đánh giá tiềm năng của trang thiết bị y tế tạo ra chứng viêm da tiếp xúc trễ |
| C.2.5 | Tiêm dưới da (kích thích) | BS 5736, Phần 4: Phương pháp thử phản ứng dưới da của chất chiết từ trang thiết bị y tế. Dược điển Hợp chủng quốc Hoa kỳ |
| C.2.6 | Phép thử gây sốt trên thỏ | BS 5736, Phần 5: Phương pháp thử độc hệ thống: Đánh giá hiện tượng gây sốt trong thỏ của chất chiết từ trang thiết bị y tế Dược điển châu Âu Dược điển Hợp chủng quốc Hoa Kỳ |
| C.2.7 | Phép thử vô trùng | Dược điển Hợp chủng quốc Hoa Kỳ Dược điển châu Âu |
1) Phép thử quay ly tâm quy định trong 5.8.2 có thể được tiến hành trong một thao tác đơn với phép thử quy định trong 5.2.7.
2) n: do nhà sản xuất xác định.
3) Hallcomind M18 (dimetylstearinamit) và Cacbovac 400 (polyetylenglycol 400) là những ví dụ về những sản phẩm phù hợp có giá trị thương mại. Thông tin này được cung cấp để thuận tiện cho người sử dụng tiêu chuẩn này và không là xác nhận của ISO về sản phẩm này.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 7611:2007 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 7611:2007 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 7611:2007 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 7611:2007 DOC (Bản Word)