- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 13405:2021 ISO 7199:2016 WITH AMD 1:2020 Vật cấy ghép tim mạch và các cơ quan nhân tạo - Thiết bị trao đổi khí – máu (thiết bị cung cấp oxy máu)
| Số hiệu: | TCVN 13405:2021 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Y tế-Sức khỏe |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
31/12/2021 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 13405:2021
Tiêu chuẩn Quốc gia TCVN 13405:2021 về Thiết bị Cung cấp Oxy Máu: Nội dung cần chú ý đối với nhà sản xuất và người sử dụng
Tiêu chuẩn Quốc gia TCVN 13405:2021 ISO 7199:2016 WITH AMD 1:2020, được ban hành với mục đích quy định các yêu cầu cho thiết bị trao đổi khí - máu (thiết bị cung cấp oxy máu) nhằm đảm bảo tính an toàn và chức năng của thiết bị trong việc hỗ trợ hoặc thay thế chức năng hô hấp của phổi. Tiêu chuẩn này đã được Viện Trang thiết bị và Công trình y tế biên soạn, Bộ Y tế đề nghị, và Tổng cục Tiêu chuẩn Đo lường Chất lượng công bố.
Tiêu chuẩn này thể hiện quy trình đánh giá hiệu năng của thiết bị cung cấp oxy máu. Cụ thể, nhà sản xuất cần chú ý tới các yêu cầu về mức độ an toàn và hiệu suất thiết bị, đảm bảo đáp ứng được yêu cầu sử dụng trong y tế. Đặc biệt, tiêu chuẩn này xác định rõ rằng thiết bị phải được thử nghiệm để đảm bảo khả năng vận chuyển oxy và carbonic, tổn hại tế bào máu, và tính năng lọc… Qua đó, người sử dụng cũng có thể so sánh các thiết bị hiện có một cách hiệu quả hơn.
Một điểm quan trọng là tiêu chuẩn không áp dụng cho thiết bị cấy ghép trong cơ thể, mà chỉ quy định cho thiết bị sử dụng bên ngoài, phục vụ cho mục đích cung cấp oxy cho máu. Các thông tin liên quan đến thiết bị cung cấp oxy máu cần phải được công khai rõ ràng, bao gồm thông tin về nhà sản xuất, hướng dẫn sử dụng và các điều kiện đặc biệt về tiệt trùng. Điều này giúp người sử dụng nắm được cách sử dụng an toàn và hiệu quả.
Ngoài ra, tiêu chuẩn cũng yêu cầu các thử nghiệm và đo lường để xác định sự phù hợp với các đặc điểm sinh học như tính tiệt khuẩn, tương thích sinh học của vật liệu với máu, và tính toàn vẹn của đường dẫn máu. Những yêu cầu này đảm bảo việc sản xuất và sử dụng thiết bị cung cấp oxy máu đạt được tiêu chuẩn về chất lượng.
Tiêu chuẩn TCVN 13405:2021 được ban hành vào năm 2021, không có thông tin cụ thể về văn bản hết hiệu lực hoặc bị thay thế. Việc tham chiếu nguồn tài liệu và các tiêu chuẩn khác liên quan đến thiết bị y tế cũng được nhấn mạnh, giúp nhà sản xuất nắm bắt rõ hơn về các yêu cầu khác trong quy trình sản xuất và thử nghiệm.
Tóm lại, tiêu chuẩn TCVN 13405:2021 quy định các yêu cầu cơ bản đối với thiết bị cung cấp oxy máu, đảm bảo rằng cả nhà sản xuất và người sử dụng phải nắm rõ các yêu cầu về tính năng, hiệu suất cũng như quy trình thử nghiệm, từ đó nâng cao tính hiệu quả và an toàn cho thiết bị trong hoạt động y tế.
Tải tiêu chuẩn Việt Nam TCVN 13405:2021
TIÊU CHUẨN QUỐC GIA
TCVN 13405:2021
ISO 7199:2016 WITH AMD 1:2020
VẬT CẤY GHÉP TIM MẠCH VÀ CÁC CƠ QUAN NHÂN TẠO - THIẾT BỊ TRAO ĐỔI KHÍ - MÁU (THIẾT BỊ CUNG CẤP OXY MÁU)
Cardiovascular implants and artificial organs - Blood-gas exchangers (oxygenators)
Lời nói đầu
TCVN 13405:2021 hoàn toàn tương đương với ISO 7199:2016 và Sửa đổi 1:2020;
TCVN 13405:2021 do Viện Trang thiết bị và Công trình y tế biên soạn, Bộ Y tế đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
Lời giới thiệu
Tiêu chuẩn này đảm bảo rằng các thiết bị được thiết kế để hỗ trợ sự trao đổi khí hoặc thay thế chức năng hô hấp bình thường của phổi được thử nghiệm một cách thỏa đáng cả về độ an toàn và chức năng, và đảm bảo rằng các đặc điểm của thiết bị ngoài cơ thể được bộc lộ một cách thỏa đáng khi ghi nhãn thiết bị.
Do vậy tiêu chuẩn này chứa các quy trình sử dụng để đánh giá các thiết bị trao đổi giữa máu và khí ngoài cơ thể (thiết bị cung cấp oxy máu). Các quy trình thử nghiệm để xác định sự vận chuyển khí, tổn hại tế bào máu và tính năng trao đổi nhiệt được mô tả, mặc dù không nêu rõ những giới hạn đối với các đặc điểm này. Tuy nhiên, việc dễ dàng xác định các đặc điểm tính năng có thể giúp người sử dụng lựa chọn một thiết bị cung cấp oxy máu phù hợp với nhu cầu của bệnh nhân.
Tiêu chuẩn này cũng bao gồm những yêu cầu báo cáo tối thiểu, cho phép người sử dụng so sánh các đặc điểm tính năng của các thiết bị cung cấp oxy máu có thiết kế khác nhau theo một cách chuẩn mực.
Tiêu chuẩn này tham khảo các tiêu chuẩn khác trong đó có thể tìm thấy các phương pháp xác định các đặc điểm chung cho các thiết bị y tế.
Không có quy định nào được đưa ra để định lượng sự hình thành bọt khí nhỏ hay các thành phần hữu hình của máu bò do hiện nay chưa có sự đồng thuận về các phương pháp thử nghiệm có thể lặp lại kết quả một cách thỏa đáng.
Những yêu cầu đối với các nghiên cứu động vật và nghiên cứu lâm sàng không được đưa vào trong tiêu chuẩn này. Những nghiên cứu như vậy có thể là những phần của hệ thống đánh giá chất lượng của nhà sản xuất.
Tiêu chuẩn này chỉ chứa những yêu cầu dành riêng cho thiết bị cung cấp oxy máu. Những yêu cầu không đặc trưng riêng có thể tham khảo các tiêu chuẩn khác liệt kê trong thư mục tài liệu tham khảo. Do không độc tính là chủ đề của một tiêu chuẩn ngang bằng/cấp độ 1 trong tương lai, nên tiêu chuẩn này không đề cập đến không độc tính.
VẬT CẤY GHÉP TIM MẠCH VÀ CÁC CƠ QUAN NHÂN TẠO - THIẾT BỊ TRAO ĐỔI KHÍ - MÁU (THIẾT BỊ CUNG CẤP OXY MÁU)
Cardiovascular implants and artificial organs - Blood-gas exchangers (oxygenators)
1 Phạm vi áp dụng
Tiêu chuẩn này quy định các yêu cầu cho thiết bị trao đổi khí-máu ngoài cơ thể vô khuẩn dùng một lần (BGE) (thiết bị cung cấp oxy máu) để cung cấp oxy và loại bỏ khí cacbonic khỏi máu người.
Tiêu chuẩn này cũng áp dụng cho các thiết bị trao đổi nhiệt và các bộ lọc máu đường động mạch, là bộ phận tích hợp của thiết bị cung cấp oxy máu.
Tiêu chuẩn này cũng áp dụng cho thiết bị bên ngoài chỉ sử dụng cho thiết bị cung cấp oxy máu.
Tiêu chuẩn này không áp dụng cho:
- Thiết bị cung cấp oxy máu cấy ghép trong cơ thể;
- Thiết bị cung cấp oxy máu chất lỏng;
- Các mạch ống dẫn tuần hoàn ngoài cơ thể (các ống dẫn máu);
- Thiết bị trao đổi nhiệt riêng biệt;
- Các thiết bị phụ trợ riêng biệt, và
- Bộ lọc máu đường động mạch riêng biệt.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 7391-1 (ISO 10993-1), Đánh giá sinh học trang thiết bị y tế - Phần 1: Đánh giá và thử nghiệm
TCVN 7391-4 (ISO 10993-4), Đánh giá sinh học trang thiết bị y tế - Phần 4: Chọn phép thử tương tác với máu
TCVN 7391 -7 (ISO 10993-7), Đánh giá sinh học trang thiết bị y tế - Phần 7: Dư lượng sau tiệt trùng bằng etylen oxit
TCVN 7391-11 (ISO 10993-11), Đánh giá sinh học trang thiết bị y tế - Phần 11: Phép thử độc tính toàn thân
TCVN 7392: 2004 (ISO 11135: 1994), Trang thiết bị y tế - Xác nhận và kiểm soát thường qui tiệt trùng bằng etylen oxit
TCVN 7393-1 (ISO 11137-1), Tiệt khuẩn sản phẩm chăm sóc sức khỏe - Bức xạ - Phần 1: Yêu cầu triển khai, đánh giá xác nhận và kiểm soát thường quy quá trình tiệt khuẩn thiết bị y tế
TCVN 7394-1 (ISO 11607-1), Bao gói trang thiết bị y tế đã tiệt khuẩn - Phần 1: Yêu cầu đối với vật liệu, hệ thống bảo vệ tiệt khuẩn và hệ thống bao gói
TCVN 7394-2 (ISO 11607-2), Bao gói trang thiết bị y tế đã tiệt khuẩn - Phần 2: Yêu cầu đánh giá xác nhận đối với quá trình tạo hình, niêm kín và lắp ráp
TCVN 13389 (ISO 15675), Vật cấy ghép tim mạch và các cơ quan nhân tạo - Hệ thống tim phổi nhân tạo - Bộ lọc đường máu động mạch
ISO 17665-1, Sterilization of health care products - Moist heat - Part 1: Requirements for the development, validation and routine control of a sterilization process for medical devices (Tiệt khuẩn sản phẩm chăm sóc sức khoẻ - Nhiệt ẩm - Phần 1: Yêu cầu triển khai, đánh giá xác nhận và kiểm soát thường quy quá trình tiệt khuẩn thiết bị y tế)
ISO 80369-7, Small-bore connectors for liquids and gases in healthcare applications - Part 7: Connectors for intravascular or hypodermic applications (Đầu nối có lỗ nhỏ cho chất lỏng và khí trong các ứng dụng chăm sóc sức khỏe - Phần 7: Đầu nối cho các ứng dụng nội mạch hoặc dưới da)
3 Thuật ngữ và định nghĩa
Trong tiêu chuẩn này, áp dụng các định nghĩa sau:
3.1
Thiết bị trao đổi khí-máu (thiết bị cung cấp oxy máu) (blood-gas exchanger /oxygenator)
Thiết bị ngoài cơ thể được thiết kế để bổ sung, hoặc để thay thế cho chức năng hô hấp của phổi
3.2
Đường dẫn máu (blood pathway)
Các đường của thiết bị cung cấp oxy máu chứa máu trong sử dụng lâm sàng
3.3
Đường dẫn khí (gas pathway)
Các phần của thiết bị cung cấp oxy máu chứa khí lưu thông trong quá trình sử dụng lâm sàng
3.4
Thiết bị trao đổi nhiệt (heat exchanger)
Thành phần dùng để kiểm soát nhiệt độ máu lưu thông hoặc dung dịch mồi
3.5
Hệ số tính năng của thiết bị trao đổi nhiệt, R (heat exchanger performance factor R)
Tỷ lệ chênh lệch giữa nhiệt độ của máu tại đầu ra của thiết bị cung cấp oxy máu và nhiệt độ máu tại đầu vào của thiết bị cung cấp oxy máu với hiệu giữa nhiệt độ của nước tại đầu vào của thiết bị trao đổi nhiệt và nhiệt độ của máu tại đầu vào của thiết bị cung cấp oxy máu
3.6
Bộ lọc động mạch tích hợp (integral arterial part)
Thành phần sử dụng để lọc các tiểu thể như cục máu đông, các mảnh tế bào, và cục nghẽn khí ra khỏi máu
3.7
Hiệu suất lọc (filtration efficiency)
Khả năng của bộ lọc loại bỏ các tiểu thể khỏi dịch thử mô phỏng máu, thể hiện theo tỷ lệ phần trăm
3.8
Phần tích hợp (integral part)
Phần nối với thiết bị cung cấp oxy máu và thường không thể tách được bởi người sử dụng
3.9
Biến số hoạt động (operating variables)
Các cài đặt của các bộ kiểm soát tác động đến chức năng của thiết bị
3.10
Giảm tiểu cầu (platelet reduction)
Giảm phần trăm tiểu cầu chứa trong một mạch ống nối với một thiết bị cung cấp oxy máu, là hàm số của thời gian
3.11
Nồng độ haemoglobin tự do trong huyết tương (plasma-free haemoglobin level)
Nồng độ hemoglobin tự do trong huyết tương trong một mạch ống nối với thiết bị cung cấp oxy máu, là hàm số của thời gian.
3.11.1
Chỉ số phân hủy máu chuẩn hóa (normalized index of hemolysis - NIH).
Số gam hemoglobin tự do trong huyết tương giải phóng ra sau khi bơm 100 lít máu
| NIH (g/1001) = ∆fHb . V. | 100 - Hct | . | 100 | (1) |
| 100 | Q.t |
Trong đó
∆fHb là tăng nồng độ (g/l) Hemoglobin tự do trong huyết tương trong khoảng thời gian lấy mẫu
V là thể tích tuần hoàn, tính bằng lít (L)
Q là lưu lượng, tính bằng lít/phút (L/min)
Hct là hematocrit (%)
t là khoảng thời gian lấy mẫu (min)
3.12
Giảm bạch cầu (white blood cell reduction)
Giảm phần trăm tế bào bạch cầu chứa trong một mạch ống gắn với thiết bị cung cấp oxy máu, là hàm số của thời gian
3.13
Thể tích máu tồn dư (residual blood volume)
Hiệu giữa thể tích mồi của đơn vị và thể tích máu có thể rút ra
3.14
Chất đồng đẳng máu (blood analogue)
Dung dịch thử nghiệm mô phỏng độ nhớt của máu trong khoảng 2,0 x 10-3 Pa.s (2,0 cP), đến 3,5 x 10-3Pa.s (3,5 cP).
3.15
Thiết bị thuộc tính cung cấp oxy máu (predicate oxygenator)
Thiết bị cung cấp oxy máu tương tự với thiết bị cung cấp oxy máu thử nghiệm, trước đây đã được chấp thuận và sử dụng cho mục đích lâm sàng tương tự
4 Các yêu cầu
4.1 Các đặc điểm sinh học
4.1.1 Tính tiệt khuẩn và tính không gây sốt
Đường máu phải tiệt khuẩn và không gây sốt. Kiểm tra sự phù hợp theo 5.2.1.
4.1.2 Sự tương thích sinh học
Tất cả các thành phần của đường máu phải tương thích sinh học với mục đích sử dụng của chúng. Kiểm tra sự phù hợp theo 5.2.2.
4.2 Các đặc điểm vật lý
4.2.1 Tính toàn vẹn của đường dẫn máu
Khi kiểm tra theo 5.3.1, đường dẫn máu phải không bị rò rỉ.
4.2.2 Tính toàn vẹn đường dẫn dịch của thiết bị trao đổi nhiệt
Khi kiểm tra theo 5.3.2, đường dẫn dịch của thiết bị trao đổi nhiệt phải không bị rò rỉ
4.2.3 Thể tích máu
Khi kiểm tra theo 5.3.3, thể tích đường dẫn máu phải nằm trong khoảng dung sai xác định bởi nhà sản xuất (xem 6.3)
4.2.4 Các đầu nối
Đầu nối để kết nối với đường dẫn máu khi kiểm tra theo 5.3.4 phải đạt được sự kết nối chắc chắn.
Khi kiểm tra theo 5.3.4, kết nối khí với đường dẫn khí phải không bị tách rời.
CHÚ THÍCH 1: Các đầu nối loại cho phép kết nối các ống có đường kính trong 4,8 mm; 6,3 mm; 9,5 mm hay 12,7 mm, hoặc loại phù hợp với ISO 8637-1:2017, Hình 1, hoặc loại phù hợp với ISO 80369-7, đã chứng tỏ thỏa mãn.
CHÚ THÍCH 2: Các đầu nối có kích thước như cho trong Phụ lục A và phù hợp với đồng hồ đo chức năng và phụ kiện thép tham chiếu là một cách để đáp ứng với yêu cầu này.
Thử nghiệm tính năng của các đầu nối phải được thực hiện theo Điều 6, ISO 80369-7:2016. Các phụ kiện tham chiếu nêu trong Phụ lục A có thể được sử dụng trong thử nghiệm tính năng của các đầu nối.
Các đầu nối đối với đường dẫn dịch của thiết bị trao đổi nhiệt phải có khả năng kết nối với các bộ nối cái nhanh.
CHÚ THÍCH 3: Các đầu nối phù hợp với ISO 8637-1:2017, Hình 2 được coi là một cách để đáp ứng với yêu cầu này.
4.3 Các đặc điểm tính năng
4.3.1 Tỷ lệ vận chuyển oxy và cacbonic
Khi xác định theo 5.4.1, tỷ lệ vận chuyển oxy và cacbonic phải nằm trong phạm vi giá trị xác định bởi nhà sản xuất (xem 6.3).
4.3.2 Hệ số tính năng của thiết bị trao đổi nhiệt
Khi xác định theo 5.4.2, các hệ số tính năng của thiết bị trao đổi nhiệt phải nằm trong phạm vi giá trị xác định bởi nhà sản xuất (xem 6.3).
4.3.3 Hiệu suất lọc động mạch tích hợp
Khi thử nghiệm theo 5.4.5, hiệu suất lọc của mọi thiết bị riêng phải đạt ít nhất 80 % khi thử với các tiểu thể lớn hơn 20 % so với kích cỡ lỗ danh nghĩa của màng lọc.
4.3.4 Dung tích lưu lượng qua bộ lọc động mạch tích hợp
Khi thử nghiệm theo 5.4.6, kết quả thử nghiệm sẽ chứng tỏ các giới hạn lưu lượng và áp suất đảm bảo hoạt động hiệu quả và an toàn như xác định bởi nhà sản xuất.
4.3.5 Khả năng xử lý khí của bộ lọc động mạch tích hợp
Khi thử nghiệm theo 5.4.7, kết quả thử nghiệm phải chứng tỏ khả năng xử lý khí như xác định bởi nhà sản xuất.
4.3.6 Tổn hại tế bào máu
4.3.6.1 Hemoglobin tự do trong huyết tương
Khi xác định theo 5.4.3, tăng nồng độ hemoglobin tự do trong huyết tương phải nằm trong phạm vi giá trị xác định bởi nhà sản xuất.
Kết quả tan huyết phải được công bố theo mg/dl và NIH.
4.3.6.2 Giảm tiểu cầu và giảm bạch cầu
Khi xác định theo 5.4.3, giảm phần trăm tiểu cầu và giảm phần trăm bạch cầu phải nằm trong phạm vi giá trị xác định bởi nhà sản xuất.
4.3.7 Những thay đổi tính năng theo thời gian
Khi xác định theo 5.4.1, tỷ lệ vận chuyển oxy và cacbonic trong suốt quá trình thử nghiệm phải duy trì ổn định trong phạm vi giá trị xác định bởi nhà sản xuất.
4.3.8 Tuổi thọ
Khi xác định theo 5.4.4, kết quả thử nghiệm nên chứng tỏ tuổi thọ được định mức giống như quy định bởi nhà sản xuất.
5 Các thử nghiệm và đo lường để xác định sự phù hợp với tiêu chuẩn này
5.1 Yêu cầu chung
5.1.1 Thử nghiệm và đo lường phải được thực hiện với thiết bị thử nghiệm được chuẩn bị theo các chỉ dẫn sử dụng lâm sàng của nhà sản xuất.
5.1.2 Các biến số hoạt động phải phù hợp với biến số xác định bởi nhà sản xuất để sử dụng lâm sàng, trừ khi có quy định khác.
5.1.3 Trừ khi có công bố khác, nhiệt độ của các dung dịch thử nghiệm phải là (37 ± 1) °C.
5.1.4 Nếu sự liên quan giữa các biến số không theo tuyến tính, phải thực hiện đủ thử nghiệm xác định để cho phép nội suy hợp lý giữa các điểm dữ liệu.
5.1.5 Quy trình thử nghiệm hay đo lường phải được coi là quy trình tham khảo. Có thể chấp nhận các phương pháp khác miễn là các thao tác đó đã chứng tỏ chính xác và có tính lặp lại tương tự.
5.2 Đặc điểm sinh học
5.2.1 Tính tiệt khuẩn và tính không gây sốt
Kiểm tra sự phù hợp bằng cách xem xét tài liệu tiệt khuẩn và thử nghiệm chất gây sốt của nhà sản xuất, theo ISO 17665-1, TCVN 7392 (ISO 11135), TCVN 7393-1 (ISO 11137-1) và TCVN 7391-11 (ISO 10993-11) nếu có thể.
5.2.2 Sự tương thích sinh học
Kiểm tra sự phù hợp bằng cách thử nghiệm hoặc bằng cách xem xét tài liệu của nhà sản xuất về tính tương thích sinh học đối với thiết bị hoàn thiện, theo TCVN 7391-1 (ISO 10993-1) và TCVN 7391-7 (ISO 10993-7) nếu có thể.
5.3 Đặc điểm vật lý
5.3.1 Tính toàn vẹn của đường dẫn máu
5.3.1.1 Dịch thử nghiệm
Dịch thử nghiệm phải là nước.
5.3.1.2 Cách tiến hành
Đặt thiết bị cần thử nghiệm vào trong một vòng tuần hoàn thử nghiệm thích hợp. Đặt đường dẫn máu của thiết bị đến áp suất gấp 1,5 lần áp suất tối đa quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng. Nếu không có quy định áp suất tối đa, thử nghiệm phải thực hiện ở áp suất 152 kPa trong vòng 6 h hoặc theo thời gian quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng. Kiểm tra bằng mắt xem thiết bị có bị rò rỉ nước hay không.
5.3.2 Tính toàn vẹn đường dẫn nước của thiết bị trao đổi nhiệt
5.3.2.1 Dịch thử nghiệm
Dịch thử nghiệm phải là nước.
5.3.2.2 Cách tiến hành
Đặt thiết bị cần thử nghiệm vào trong một vòng tuần hoàn thử nghiệm thích hợp. Đặt đường dịch của thiết bị trao đổi nhiệt đến áp suất gấp 1,5 lần áp suất quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng. Nếu không có quy định áp suất tối đa, thử nghiệm phải thực hiện ở áp suất 350 kPa trong vòng 6 h hoặc theo thời gian quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng. Kiểm tra bằng mắt xem thiết bị có bị rò rỉ nước hay không.
5.3.3 Thể tích máu
5.3.3.1 Dịch thử nghiệm
Dịch thử nghiệm phải là máu toàn phần kháng đông hoặc nước.
5.3.3.2 Cách tiến hành
Thể tích của đường dẫn máu phải được xác định trong phạm vi của các biến số hoạt động quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng (xem 6.3).
5.3.3.3 Thể tích máu tồn dư
Xác định thể tích máu tồn dư bằng cách giữ thiết bị ở vị trí thoát dịch thuận lợi nhất trong vòng 20 s sau thời gian không khí lần đầu xuất hiện tại cửa thoát dịch cho đến khi thấy không còn dịch trong thiết bị.
5.3.4 Đầu nối
Thực hiện kết nối theo các hướng dẫn sử dụng của nhà sản xuất.
Sự kết nối chịu được lực kéo 15 N trong vòng 15 s mà không bị tách rời.
5.4 Các đặc điểm tính năng
5.4.1 Tỷ lệ vận chuyển oxy và cacbonic
5.4.1.1 Môi trường thử nghiệm
Dịch thử nghiệm cho đường dẫn máu phải là máu kháng đông. Môi trường thử nghiệm cho đường khí phải là khí có nồng độ oxy, ni tơ và cacbonic đã biết.
5.4.1.2 Cách tiến hành
5.4.1.2.1 Quy định chung
Đặt thiết bị cần thử nghiệm trong một vòng tuần hoàn thích hợp. Thực hiện thử nghiệm bằng cách sử dụng các điều kiện ở cửa vào của máu như sau trong khi xác định tỷ lệ vận chuyển oxy và cacbonic:
- Phần trăm oxyhaemogloblin (65 ± 5).
- Haemoglobin: (12 ± 1) g/dl.
- Ba zơ: (0 ± 5) mmol/l.
- Áp lực riêng phần CO2 trong máu: PCO2: (6,0 ± 0,7) kPa.
Tỷ lệ vận chuyển oxy và cacbonic phải được xác định trên phạm vi các biến số hoạt động quy định bởi nhà sản xuất (xem 6.3).
Giữa mỗi bộ số đo, phải giữ lưu lượng máu ở mức tối đa quy định bởi nhà sản xuất cho mục đích sử dụng lâm sàng (xem 6.3).
Việc xác định tỷ lệ vận chuyển oxy và cacbonic phải thực hiện khi bắt đầu thử nghiệm. Đối với các phép đo phụ thuộc, thực hiện đo khi bắt đầu thử nghiệm và sau đó đo lại sau 1 h, 3 h và 6 h. Nếu có thể, tiếp tục đo với quãng cách 6 h.
Có thể áp dụng các thử nghiệm in vitro cũng như thử nghiệm sử dụng mẫu động vật.
Có thể dùng máu tươi thay cho máu nếu cần thiết trong khi đo chuyển oxy và cacbonic.
Không cần thu thập dữ liệu ở các điều kiện xác định chính xác. Có thể chấp nhận các kết quả tương đối thu được bằng phép nội suy hợp lý.
5.4.1.2.2 Điều kiện lâm sàng
Để có thông tin bổ sung, nên xem xét các điều kiện thử nghiệm sau.
Đặt thiết bị thử nghiệm trong một vòng tuần hoàn thử nghiệm thích hợp. Thực hiện thử nghiệm xác định tỷ lệ chuyển oxy và cacbonic bằng cách sử dụng điều kiện đầu vào của máu như sau:
- thay đổi nhiệt độ đến phạm vi 28 °C và 18 °C ± 1 °C.
- tỷ lệ phần trăm oxyhaemogloblin: (65 ± 5).
- haemoglobin: (8 ± 2) g/dl.
- bazơ: (0 ± 5) mmol/l.
- áp lực riêng phần CO2 trong máu, PCO2: (6,0 ± 0,7) kPa.
5.4.2 Hệ số tính năng của thiết bị trao đổi nhiệt
5.4.2.1 Dịch thử nghiệm
Dịch thử nghiệm cho đường máu phải là máu kháng đông hoặc nước.
5.4.2.2 Cách tiến hành
Đặt thiết bị cần thử nghiệm trong một vòng tuần hoàn thử nghiệm thích hợp. Thực nghiệm thử nghiệm in vitro trong các điều kiện sau:
- nhiệt độ đầu vào của máu, Tin.blood: (30 ± 1) °C
- nhiệt độ đầu vào của nước, Tin.water: (40 ± 1) °C
Xác định hệ số tính năng của thiết bị trao đổi nhiệt phải thực hiện trên phạm vi biến số hoạt động xác định bởi nhà sản xuất (xem 6.3).
5.4.2.3 Phương trình
Hệ số tính năng thiết bị trao đổi nhiệt được tính theo phương trình sau:
| R = | Tout.blood - Tin.blood |
|
| Tin.water - Tin.blood |
|
Trong đó:
Tout.blood là nhiệt độ của máu tại đầu ra của thiết bị cung cấp oxy máu , theo °C
Tin.blood là nhiệt độ của máu tại đầu vào của thiết bị cung cấp oxy máu, theo °C
Tin.water là nhiệt độ của nước tại đầu vào của thiết bị trao đổi nhiệt, theo °C
5.4.3 Tổn hại tế bào máu
5.4.3.1 Môi trường thử nghiệm
Dịch thử nghiệm cho đường máu phải là máu kháng đông. Môi trường thử nghiệm cho đường dẫn khí phải là chất khí có nồng độ xác định oxy, nitơ và cacbonic.
5.4.3.2 Cách tiến hành
Phải lắp đặt hai bộ mạch dẫn gồm các thành phần thích hợp, giống nhau, bao gồm 1 bơm, hệ thống ống nối một bình chứa (như quy định bởi nhà sản xuất và có kích thước thích hợp với thiết bị thử nghiệm) và một thiết bị trao đổi nhiệt. Đặt thiết bị thử nghiệm trong một bộ mạch dẫn. Đặt thiết bị thuộc tính oxy hóa huyết trong vòng tuần hoàn thứ hai. Mồi và khử bọt khí bằng cách cho tuần hoàn một dung dịch thích hợp trước khi cho máu vào. Các thể tích dịch thử nghiệm của đường dẫn máu khi bắt đầu thử nghiệm phải trong khoảng 1 % của nhau, Thực hiện thử nghiệm in vitro bằng cách sử dụng các điều kiện trong Bảng 1. Nên thực hiện một số lượng đủ các cặp thử nghiệm để hỗ trợ phân tích thống kê. Thiết bị cung cấp oxy máu nên được thử nghiệm trong cùng điều kiện.
Lịch trình lấy mẫu phải phù hợp với Bảng 2. Thời gian lấy mẫu thường xuyên hơn có thể tùy ý.
5.4.4 Tuổi thọ
Bằng cách sử dụng phương pháp đã xác thực, nên thực hiện làm lão hóa trên các thiết bị cuối, hoàn thiện, đã tiệt khuẩn trong bao bì đầu để xác định tuổi thọ danh nghĩa.
5.4.5 Hiệu suất lọc
5.4.5.1 Dịch thử nghiệm
Dịch thử nghiệm phải là dung dịch glycerin hay nước. Dịch thử nghiệm phải chứa 350 đến 5000 tiểu thể/ml, trong đó 15 % -25 % lớn hơn kích thước lỗ danh nghĩa của màng lọc.
5.4.5.2 Cách tiến hành
Cho 500 ml dung dịch thử nghiệm ở nhiệt độ phòng (20 °C đến 22 °C) đi qua thiết bị ở lưu lượng không dưới 100 ml/min và áp suất không quá 152 kPa (22 psi). Xác định số lượng trung bình tiểu thể trước lọc và sau lọc. Thử nghiệm phải được thực hiện tại lưu lượng khuyến nghị bởi nhà sản xuất. Tính toán hiệu suất lọc, sử dụng các số đọc từ phạm vi kích thước của các tiểu thể thử nghiệm sử dụng cho mỗi mẫu thử nghiệm, bằng cách lấy số lượng tiểu thể trung bình trước lọc trừ đi số lượng tiểu thể trung bình sau lọc, chia cho số tiểu thể trung bình trước lọc rồi nhân với 100 để thu được phần trăm.
5.4.6 Lưu lượng qua bộ lọc động mạch tích hợp
5.4.6.1 Dung dịch thử nghiệm
Dung dịch thử nghiệm phải là máu toàn phần kháng đông hoặc dung dịch đồng đẳng máu.
5.4.6.2 Cách tiến hành
Đặt thiết bị thử nghiệm trong một vòng tuần hoàn thử nghiệm thích hợp. Đặt lưu lượng ở lưu lượng tối đa và theo dõi áp suất đầu vào và đầu ra qua thiết bị trong vòng 6 h. Đo lưu lượng bằng cách sử dụng một lưu lượng kế. Ghi mọi sự thay đổi áp suất trong quá trình thử nghiệm.
Nếu sử dụng máu toàn phần kháng đông, thử nghiệm này không tính đến ảnh hưởng của các thành phần máu hữu hình hoặc các kết tập protein.
5.4.7 Khả năng xử lý không khí của bộ lọc động mạch tích hợp
5.4.7.1 Dung dịch thử nghiệm
Dung dịch thử nghiệm phải là máu toàn phần kháng đông với hàm lượng haemoglobin là (12 ± 1) g/dl.
5.4.7.2 Cách tiến hành
Sử dụng ống thông hơi của bộ lọc như xác định trong hướng dẫn sử dụng của nhà sản xuất. Chiều dài và đường kính trong của ống thông hơi phải như quy định. Đối áp suất tại lưu lượng tối đa là 26,6 kPa (3,9 psi) ± 5 %. Sử dụng bộ khử bọt khí để đo bọt khí sau màng lọc tích hợp tích tụ trong vòng 5 min từ mỗi lần tiêm, ở lưu lượng 33 %, 67 % và 100 % lưu lượng tối đa xác định, phải tiêm làm một lượng 30 ml không khí trong phòng đối với thiết bị cung cấp oxy máu người lớn (đối với thiết bị cung cấp oxy máu trẻ em hay trẻ sơ sinh với lưu lượng tối đa cao hơn 500 ml/min, lượng bơm phải tăng tới 2,5 ml cho mỗi lưu lượng tối đa 500 ml/min; lượng bơm khí tối đa là 10 ml). Phải cung cấp chỉ dẫn điểm bơm khí trong hệ tuần hoàn thử nghiệm, mức tiêm và loại bơm sử dụng để tuần hoàn dịch thử nghiệm trong biên bản thử nghiệm.
5.4.7.3 Kết quả
Kết quả báo cáo phải thể hiện theo hiệu suất phần trăm toàn bộ lượng khí được loại bỏ.
Bảng 1 - Điều kiện cho thử nghiệm in vitro sự tổn hại tế bào máu
| Hạng mục | Mức độ | Biến thiên tối đa |
| Lưu lượng máu | Tối đa xác định bởi nhà sản xuất cho mục đích sử dụng lâm sàng (xem 6.3) | ± 5% |
| Lưu lượng khí | Tối đa xác định bởi nhà sản xuất cho mục đích sử dụng lâm sàng (xem 6.3) | ± 5% |
| PCO2 (áp suất CO2 trong máu) | 5,3 kPa | ± 0,7 kPa |
| Ba zơ | 0a | ± 5 mmol/l |
| Máu glucose | 10 mmol/ | ± 5 mmol/l |
| Haemoglobin | 12 g/dl | ± 1 g/dl |
| a Chú ý rằng 0 (zero) là 24 mmol/l bicarbonate (HCO3-). | ||
Bảng 2 - Thời gian biểu lấy mẫu
| Thông số | Trước thử | Thời gian, sau khi bắt đầu thử nghiệm (min) | |||
| 10 | 30 | 180 | 360 | ||
| Haemoglobin tự do trong huyết tương | X |
| X | X | X |
| Tế bào bạch cầu | X |
| X | X | X |
| Tiểu cầu | X |
| X | X | X |
| Giá trị khí trong máu PCO2 PO2 pH Ba zơ | X | X | X | X | X |
| Haemoglobin | X | X | X | X | X |
| Glucose | X |
|
|
|
|
| Thời gian đông máu hoạt hóa | X |
|
|
|
|
| Nhiệt độ | X | X | X | X | X |
| Lưu lượng | X | X | X | X | X |
6 Thông tin cung cấp bởi nhà sản xuất
6.1 Thông tin về thiết bị cung cấp oxy máu
Phải cung cấp thông tin sau về thiết bị cung cấp oxy máu:
a) nhận biết nhà sản xuất;
b) mẻ, lô hoặc số sê ri;
c) định mẫu mã;
d) hướng dòng máu và/hay dòng khí và/hay dòng nước nếu cần thiết.
6.2 Thông tin về bao gói
6.2.1 Hộp chứa đơn vị sản phẩm
Thông tin sau phải nhìn thấy qua hoặc có sẵn trên hộp chứa đơn vị sản phẩm:
a) tên và địa chỉ nhà sản xuất;
b) mô tả các thành phần chứa bên trong;
c) định mẫu mã;
d) công bố về tính tiệt khuẩn và tính không gây sốt;
e) hạn sử dụng;
f) mẻ, lô hoặc số sê ri;
g) chữ “Đọc hướng dẫn trước khi sử dụng”. Có thể bổ sung ký hiệu ∆! trước dòng chữ “đọc hướng dẫn trước khi sử dụng”;
h) mọi điều kiện xử lý hoặc bảo quản đặc biệt;
i) công bố về sử dụng một lần. Có thể sử dụng ký hiệu ![]() .
.
6.2.2 Bao gói vận chuyển
Phải có thông tin sau trên bao gói vận chuyển:
a) tên và địa chỉ nhà sản xuất;
b) mô tả các thành phần chứa bên trong, kể cả số lượng thành phần;
c) định mẫu mã;
d) công bố về tính tiệt khuẩn và tính không gây sốt;
e) thời hạn sử dụng;
f) mọi chỉ dẫn về xử lý, bảo quản đặc biệt hoặc chỉ dẫn mở bao bì.
6.3 Thông tin trong các tài liệu kèm theo
Mỗi bao gói vận chuyển phải chứa một tờ rơi “Hướng dẫn sử dụng” với các thông tin sau:
a) địa chỉ và số điện thoại, số telefax của nhà sản xuất;
b) định mẫu mã;
c) thiết bị phụ trợ cần thiết;
d) hướng dẫn về các thao tác cần thiết, đặc biệt hoặc đặc trưng riêng, nếu thích hợp;
e) hướng đặt thiết bị cung cấp oxy máu trong bộ đỡ hoặc cơ cấu hoạt động;
f) cách lắp, loại và cách đảm bảo các bộ nối ống;
g) vị trí và mục đích của các cửa vào và cửa ra bổ sung;
h) mồi và vận hành thiết bị trao đổi nhiệt;
i) thao tác mồi;
j) hướng dòng máu, khí và nước;
k) các quy trình vận hành chung để sử dụng bình thường;
l) thao tác khuyến nghị để thay thế thiết bị cung cấp oxy máu khi đang làm việc;
m) lưu lượng máu tối đa và tối thiểu khuyến nghị;
n) thể tích vận hành tối đa và tối thiểu của đường máu. Kể cả mọi bình chứa tích hợp;
o) lưu lượng khí tối đa và tối thiểu xác định;
p) hệ số tính năng của thiết bị trao đổi nhiệt;
q.) khả năng xử lý khí;
r) thể tích máu dư;
s) tỷ lệ chuyển oxy và cacbonic;
t) giới hạn áp suất cho các đường dẫn máu, đường dẫn nước và đường dẫn khí;
u) công bố rằng các chi tiết sau có được theo yêu cầu:
1) phương pháp tiệt khuẩn;
2) danh sách vật liệu của đường máu;
3) dữ liệu rò rỉ huyết tương qua mọi màng bán thấm, nếu có thể;
4) độ giảm áp suất đường máu tại phạm vi lưu lượng máu xác định bởi nhà sản xuất cho mục đích sử dụng lâm sàng;
5) độ giảm áp suất đường khí tại lưu lượng tối đa của máu và khí, xác định bởi nhà sản xuất cho mục đích sử dụng lâm sàng;
6) dữ liệu liên quan đến tổn hại tế bào máu;
7) dữ liệu về sự giải phóng tiểu thể từ thiết bị cung cấp oxy máu theo hệ thống quản lý, kiểm soát chất lượng của nhà sản xuất;
8) dung sai liên quan đối với các dữ liệu trình bày.
6.4 Thông tin ghi nổi bật trong các tài liệu kèm theo
Thông tin sau phải ghi nổi bật trong tài liệu kèm theo:
a) các giới hạn áp suất;
b) các giới hạn lưu lượng;
c) các giới hạn mức độ máu;
d) các giới hạn khác của thiết bị.
7 Bao gói
Bao gói phải tuân thủ các yêu cầu thích hợp của TCVN 7394-1 (ISO 11607-1) và TCVN 7394-2 (ISO 11607-2).
Phụ lục A
(tham khảo)
Ví dụ về các đầu nối
A.1 Khớp nối trượt Luer
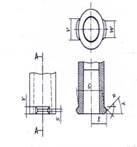
A.1.1 Hình A.1 và A.2 mô tả các khớp nối trượt Luer. Đối với các kích thước tương ứng, xem Bảng A.1.
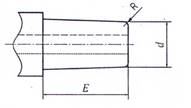
a) Khớp nối hình nón đực 6 % (Luer) (“khớp nối đực”)
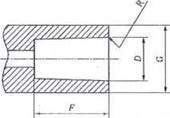
b) Khớp nối hình nón cái 6 % (Luer) (“khớp nối cái”)
CHÚ THÍCH: Xem Chú dẫn và kích thước đưa ra trong Bảng A.1.
Hình A.1 - Khớp nối hình nón 6 % (Luer) điển hình
Bảng A.1 - Kích thước của khớp nối hình nón 6 % (Luer)
| Tham chiếu | Quy định | Kích thước (mm) | |||
| Vật liệu cứng | Vật liệu bán cứng | ||||
| A | Khớp nối đực | N/A | N/A | ||
| B | Khớp nối cái | N/A | N/A | ||
| Kích thước cơ bản | d | min. | Đường kính tối thiểu của phần cuối của khớp nối hình nón đực (đường kính tham chiếu) | 3,925 | 3,925 |
| max. | Đường kính tối đa ở phần cuối của khớp nối hình nón đực | 3,990 | 4,027 | ||
| D | min. | Đường kính tối thiểu ở phần đầu của khớp nối hình nón cái | 4,270 | 4,270 | |
| max. | Đường kính tối đa ở phần đầu của khớp nối hình nón cái | 4,315 | 4,315 | ||
| E | Chiều dài tối thiểu của khớp nối hình nón đực | 7,500 | 7,500 | ||
| F | Chiều sâu tối thiểu của khớp nối hình nón cái | 7,500 | 7,500 | ||
| G | Đường kính ngoài tối đa của khớp nối hình nón cái | 6,730 | 6,730 | ||
| Kích thước khác | La | Chiều dài ăn khớp tối thiểu | 4,665 | 4,050 | |
| Ma | Dung sai cho chiều dài ăn khớp của khớp nối hình nón cái | 0,750 | 0,750 | ||
| Na | Dung sai cho chiều dài ăn khớp của khớp nối hình nón đực | 1,083 | 1,700 | ||
| Rb | Bán kính cong (tối đa) | 0,5 | 0,5 | ||
| a Các kích thước L, M và N được suy ra từ các kích thước cơ bản. b Hoặc vát mép tương đương mà không có bất kỳ góc nhọn nào | |||||
A.1.2 Thử nghiệm đo
A.1.2.1 Khi được thử theo A.1.2.4, khớp nối hình nón phải thỏa mãn các yêu cầu quy định trong A.1.2.2 và A.1.2.3.
A.1.2.2 Đầu nhỏ của khớp nối hình nón đực phải nằm giữa hai mặt phẳng giới hạn của máy đo và đầu lớn hơn của phần hình côn phải kéo dài ra ngoài mặt phẳng mốc của máy đo. Không được thấy hiện tượng rung lắc giữa máy đo và khớp nối làm bằng vật liệu cứng đang được thử nghiệm.
A.1.2.3 Mặt phẳng có đường kính lớn nhất tại lỗ mở của khớp nối hình nón cái phải nằm giữa hai mặt phẳng giới hạn của máy đo. Không được thấy hiện tượng rung lắc giữa máy đo và khớp nối làm bằng vật liệu cứng đang được thử nghiệm.
A.1.2.4 Quy trình nên được thực hiện như quy định trong A.1.2.4.1 đến A.1.2.4.4.
A.1.2.4.1 Tiến hành thử nghiệm bằng máy đo bằng thép như minh họa trong Hình A.3.
A.1.2.4.2 Tiến hành thử nghiệm ở nhiệt độ (20 ± 5) °C.
A.1.2.4.3 Trước khi thử nghiệm, điều kiện sản phẩm làm từ vật liệu hút ẩm ở (20 ± 5) °C và (50 ± 10) % độ ẩm tương đối trong thời gian không ít hơn 24 h. Không cần ổn định đối với các sản phẩm làm từ vật liệu không hút ẩm.
A.1.2.4.4 Tác dụng máy đo lên khớp nối hình nón với tổng lực dọc trục là 5 N, không sử dụng mômen xoắn. Bỏ tải dọc trục.
Kích thước tính bằng milimét
| | | |
| a) Máy đo thử nghiệm khớp nối hình nón đực cứng | b) Máy đo thử nghiệm các khớp nối hình nón bán cứng | c) Máy đo thử nghiệm các khớp nối hình nón cái của tất cả các vật liệu |
CHÚ THÍCH: Độ côn hình nón (0,06;1)
Hình A.3 - Máy đo thử nghiệm khớp nối hình nón 6 % (Luer)
A.1.3 Khớp nối thép tham chiếu
A.1.3.1 Hình A.4 và A.5 mô tả các khớp nối thép tham chiếu đực và cái.
Kích thước tính bằng milimét
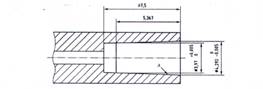
CHÚ THÍCH: Độ côn hình nón (0,06:1)
Hình A.4 - Khớp nối hình nón cái thép tham chiếu
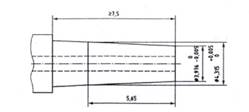
CHÚ THÍCH: Độ côn hình nón (0,06:1)
Hình A.5 - Khớp nối hình nón đực thép tham chiếu
A.2 Khớp nối khóa Luer
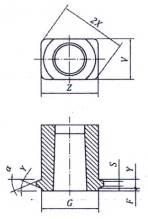
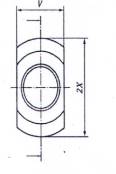
A.2.1 Hình A.6 đến A.9 mô tả khớp nối khóa Luer trong khi Hình A.10 và A.11 mô tả khớp nối thép tham chiếu để thử nghiệm khớp nối khóa đực 6 % (Luer). Đối với các kích thước tương ứng, xem Bảng A.2.
CHÚ THÍCH 1: Nếu khớp nối khóa hình nón cái 6 % (Luer) như trong Hình A.8 có các vấu nằm trên mặt phẳng nghiêng với trục của khớp nối, các vấu phải tạo thành một phần của dạng ren như trong Hình A.9. Trong trường hợp này, ‘V’ không áp dụng.
CHÚ THÍCH 2: Tất cả các cạnh bên ngoài của vấu hoặc dạng ren như trong Hình A.10 và A.11 nên có bán kính giữa 0,15 mm và 0,2 mm (trừ khi có quy định khác).
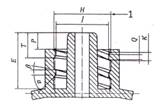
CHÚ DẪN:
1 khởi động kép, ren bên phải có bước sóng 2,5 mm
CHÚ THÍCH: Xem chú dẫn và các kích thước trong Bảng A.2
Hình A.6 - Khớp nối khóa hình nón đực 6 % (Luer) với vòng ren bên trong được kết nối cố định
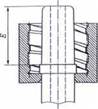
CHÚ THÍCH 1: Đối với các kích thước khác, xem Hình A.6.
CHÚ THÍCH 2: Xem chú dẫn và các kích thước trong Bảng A.2
Hình A.7 - Khớp nối khóa hình nón đực 6 % (Luer) với vòng ren trong có thể xoay được
|
|
|
|
| a) Biến thể A | b) Biến thể B | c) Biến thể C |
CHÚ THÍCH 1: Các biến thể B và C chỉ được sử dụng để thiết kế các khớp nối cứng.
CHÚ THÍCH 2: Để đảm bảo tính tương thích với các khớp nối cứng hiện có, ưu tiên K = 0,8 mm tối đa.
CHÚ THÍCH 3: Xem chú dẫn và kích thước trong Bảng A.2.
Hình A.8 - Khớp nối khóa hình nón cái 6 % (Luer) với các vấu trong mặt phẳng vuông góc với trục của khớp nối
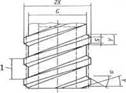
CHÚ DẪN:
1 Bước răng
CHÚ THÍCH 1: Đối với các kích thước khác, xem Hình A.8.
CHÚ THÍCH 2: Xem Chú dẫn và kích thước cho trong Bảng A.2.
Hình A.9 - Khớp nối hình nón khóa cái 6 % (Luer) với ren ngoài
Bảng A.2 - Kích thước của khớp nối khóa hình nón cứng 6 % (Luer)
| Ký hiệu | Quy định | Kích thước (chiều dài tính bằng milimét) | |
| Hình A.6, A.7, A.8 và A.9 | Hình A.8 b) và A.8 c) | ||
| α | Góc của ren hoặc bề mặt mang vấu chống lại sự phân tách với mặt phẳng vuông góc với trục của khớp nối khóa | | |
| β | Góc nhỏ nhất của bề mặt không chịu lực ren trong chống lại sự phân tách với mặt phẳng vuông góc với trục của khớp nối khóa | 25° | — |
| γ | Góc nhỏ nhất của ren ngoài hoặc bề mặt không chịu lực vấu chống lại sự phân tách với mặt phẳng vuông góc với trục của khớp nối khóa | 0° | 0° |
| E | Chiều dài tối thiểu của đầu nối khóa đực | 7,5 | — |
| F | Khoảng cách danh nghĩa từ mặt của khớp nối đến đế của vấu | — | 0,20 |
| G | Đường kính ngoài tối đa của khớp nối khóa cái lắp ở đế vấu hoặc đường kính trong tối đa của ren ngoài; Đường kính này không nên được tăng lên trong khoảng cách từ mặt trục là 5,5 mm | 6,73 | 5,7 |
| H | Đường kính gốc của ren của khớp nối khóa đực | 8,0 ±0,1 | — |
| J | Đường kính đỉnh của ren của khớp nối khóa đực | 7,0 ± 0,2 | — |
| K | Chiều rộng ren tối đa của khớp nối khóa đực ở gốc | 1 | — |
| P | Hình chiếu tối thiểu của vòi phun từ vành | 2,1 | — |
| Q | Chiều rộng đỉnh ren tối thiểu của khớp nối khóa đực | 0,3 | — |
| S | Chiều rộng đỉnh vấu hoặc chiều rộng đính ren của khớp nối khóa cái với vấu hoặc ren ngoài | tối thiểu 0,3 | tối đa 0,27 |
| T | Khoảng cách tối đa từ đầu của khớp nối khóa đực đến đáy của dạng ren hoàn chỉnh đầu tiên của ren trong | 3,2 | — |
| V | Chiều dài dây tối đa tại đáy của vấu trong mặt phẳng chỉ vuông góc với trục của khớp nối, được đo trên dây của một đường tròn có đường kính tối thiểu là J (7,0 mm) | 3,5 | 5,0 |
| W | Chiều dài dây tối thiểu tại cực điểm của vấu trong một mặt phẳng chỉ vuông góc với trục của khớp nối (W không được lớn hơn V) | 2,71 | — |
| X | Khoảng cách từ trục của khớp nối khóa cái đến cực điểm của vấu | — | — |
| 2X | Đường kính ngoài qua vấu hoặc ren ngoài | 7,830-0,1 | 7,830-0,1 |
| Y | Chiều rộng tối đa của đế vấu (trục) hoặc ren ở đế, của khớp nối khóa cái được đo tại điểm tương ứng với đường kính ngoài bằng G (tối đa 6,73) | 1,2 | 1,30 |
| Z | Chiều rộng trên các vấu ở ren ngoài | — | 6,500-0,1 |
| Bước răng | Bước danh nghĩa của ren khởi động kép, bên phải của khớp nối khóa cái - dây dẫn 5 mm | 2,5 | — |
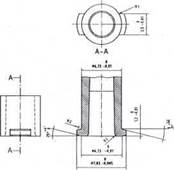
CHÚ DẪN:
R1 Bán kính tối đa 0,5 mm
R2 Bán kính tối đa 0,2 mm
Hình A.10 - Khớp nối hình nón cái tham chiếu để thử nghiệm các khớp nối khóa đực 6 % (Luer) về khả năng rò rỉ, dễ lắp ráp, mô-men xoắn tháo xoắn và nứt ứng suất
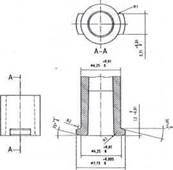
CHÚ DẪN:
R1 Bán kính tối đa 0,5 mm
R2 bán kính tối đa 0,2 mm
Hình A.11 - Khớp nối hình nón cái tham chiếu để thử nghiệm các khớp nối đực khóa 6 % (Luer) cho lực tách và khả năng chống đè
Thư mục tài liệu tham khảo
[1] TCVN ISO 13485, Thiết bị y tế - Hệ thống quản lý chất lượng - Yêu cầu đối với các mục đích chế định.
[2] TCVN 8023 (ISO 14971), Trang thiết bị y tế - Áp dụng quản lý rủi ro đối với trang thiết bị y tế.
[3] ISO 594-2, Conical fittings with a 6 % (Luer) taper for syringes, needles and certain other medical equipment - Part 2: Lock fittings (Đầu cắm hình côn với độ côn 6 % (luer) dùng cho các loại bơm tiêm, kim tiêm và một số dụng cụ y tế khác - Phần 2: Đầu cắm có khóa)
[4] ISO 8637:2010, Cardiovascular implants and extracorporeal systems - Haemodialysers, haemodiafilters, haemofilters and haemoconcentrators (Vật cấy ghép tim mạch và các hệ thống ngoài cơ thể - Thiết bị thẩm tách máu, bộ lọc thẩm tách máu, bộ lọc máu và các thiết bị cô máu)
[5] TCVN 13376-1 (ISO 8637-1), Hệ thống lọc máu ngoài cơ thể - Phần 1: Thiết bị thẩm tách máu, thẩm lọc máu và cô máu)
[6] ISO/TS 23810, Cardiovascular implants and artificial organs - Checklist for preoperative extracorporeal circulation equipment setup (Vật cấy ghép tim mạch và các cơ quan nhân tạo - Danh sách danh mục cần kiểm tra để thiết lập thiết bị tuần hoàn ngoài cơ thể trước khi hoạt động)
[7] US Food and Drug Administration. Guidance for Cardiopulmonary Bypass Oxygenators 510 (k), submissions; Final guidance for industry and FDA staff, issued Nov. 13.2000. (Cơ quan Quản lý Thực phẩm và Thuốc. Chỉ dẫn đối với các thiết bị cung cấp oxy máu đi tắt tim-phổi 510 (k), Các đề xuất: Chỉ dẫn cuối cùng đối với công nghiệp và nhân sự FDA, phát hành ngày 13 tháng 11 năm 2000).
Mục lục
Lời nói đầu
Lời giới thiệu
1 Phạm vi áp dụng
2 Tài liệu viện dẫn
3 Thuật ngữ và định nghĩa
4 Các yêu cầu
5 Các thử nghiệm và đo lường để xác định sự phù hợp với tiêu chuẩn này
6 Thông tin cung cấp bởi nhà sản xuất
7 Bao gói
Phụ lục A (tham khảo) - Ví dụ về các đầu nối :
Thư mục tài liệu tham khảo
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 13405:2021 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 13405:2021 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 13405:2021 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 13405:2021 DOC (Bản Word)