- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 10992:2015 CEN/TS 15606:2009 Thực phẩm-Xác định acesulfame-K, aspartame, neohesperidine-dihydrochalcone và saccharin-Phương pháp sắc ký lỏng hiệu năng cao
| Số hiệu: | TCVN 10992:2015 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
31/12/2015 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 10992:2015
Tiêu chuẩn Quốc gia TCVN 10992:2015: Xác định Acesulfame-K, Aspartame, Neohesperidine-dihydrochalcone và Saccharin trong thực phẩm
Tiêu chuẩn Quốc gia TCVN 10992:2015 được ban hành thay thế tiêu chuẩn CEN/TS 15606:2009. Tiêu chuẩn này quy định phương pháp xác định Acesulfame-K, Aspartame, Neohesperidine-dihydrochalcone và Saccharin trong thực phẩm bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC) với detector UV.
Ngày ban hành và hiệu lực
Tiêu chuẩn TCVN 10992:2015 được công bố bởi Bộ Khoa học và Công nghệ và có hiệu lực áp dụng từ ngày ban hành. Tiêu chuẩn này giúp các cơ sở sản xuất thực phẩm đáp ứng yêu cầu quản lý chất lượng và an toàn thực phẩm đối với các chất tạo ngọt nhân tạo.
Phạm vi áp dụng
Tiêu chuẩn này áp dụng cho việc xác định nồng độ của các chất tạo ngọt như Acesulfame-K (từ 86 mg/l đến 331 mg/l), Aspartame (từ 97 mg/kg đến 610 mg/l), Saccharin (từ 70 mg/l đến 97 mg/kg) và Neohesperidine-dihydrochalcone (từ 27 mg/l đến 57 mg/kg) trong nhiều loại thực phẩm như đồ uống pha từ nước, đồ uống từ trái cây, bánh quy, và súp đóng hộp.
Phương pháp phân tích
Nguyên tắc của phương pháp sắc ký lỏng hiệu năng cao bao gồm: chiết mẫu với nước, tinh sạch dung dịch mẫu bằng các thuốc thử Carrez, và phân tích bằng HPLC với pha đảo và detector UV. Các thuốc thử được yêu cầu sử dụng là loại tinh khiết phân tích. Phương pháp đạt được đảm bảo độ chính xác và độ tin cậy trong việc xác định các chất tạo ngọt này.
Tài liệu viện dẫn
TCVN 4851:1989 (ISO 3696:1987) quy định các yêu cầu kỹ thuật và phương pháp thử cho nước dùng để phân tích trong phòng thí nghiệm. Các tài liệu viện dẫn này cung cấp nền tảng và yêu cầu thiết yếu để áp dụng thành công tiêu chuẩn TCVN 10992:2015.
Kết quả phân tích và báo cáo
Hệ thống HPLC yêu cầu phải phù hợp với bộ tiêu chí cụ thể để đảm bảo độ chính xác trong phân tích. Kết quả phân tích sẽ được báo cáo với đầy đủ thông tin cần thiết như ngày nhận mẫu, kết quả đo đạc và các chỉ số quan sát được trong quá trình thử nghiệm.
Độ chụm và độ lặp lại
Tiêu chuẩn đưa ra các giá trị độ lặp lại cho từng chất tạo ngọt, với các giới hạn cụ thể cho Acesulfame-K tại 331 mg/l, Aspartame 567 mg/l, Saccharin 69,6 mg/l và Neohesperidine-dihydrochalcone 27,3 mg/l. Những giá trị này được sử dụng để đánh giá mức độ chính xác và độ tin cậy của các phương pháp thử nghiệm, cũng như so sánh giữa các phòng thử nghiệm khác nhau.
Tiêu chuẩn TCVN 10992:2015 là công cụ quan trọng giúp nâng cao chất lượng thực phẩm và bảo vệ sức khỏe người tiêu dùng thông qua việc quản lý chặt chẽ các chất tạo ngọt trong thực phẩm.
Tải tiêu chuẩn Việt Nam TCVN 10992:2015
TIÊU CHUẨN QUỐC GIA
TCVN 10992:2015
CEN/TS 15606:2009
THỰC PHẨM - XÁC ĐỊNH ACESULFAME-K, ASPARTAME, NEOHESPERIDIDINE-DIHYDROCHALCONE VÀ SACCHARIN - PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO
Foodstuffs - Determination of acesulfame-K, aspartame, neohesperidine-dihydrochalcone and saccharin - High performance liquid chromatographic method
Lời nói đầu
TCVN 10992:2015 hoàn toàn tương đương với CEN/TS 15606:2009;
TCVN 10992:2015 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F13 Phương pháp phân tích và lấy mẫu biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
THỰC PHẨM - XÁC ĐỊNH ACESULFAME-K, ASPARTAME, NEOHESPERIDIDINE-DIHYDROCHALCONE VÀ SACCHARIN - PHƯƠNG PHÁP SẮC KÝ LỎNG HIỆU NĂNG CAO
Foodstuffs - Determination of acesulfame-K, aspartame, neohesperidine-dihydrochalcone and saccharin - High performance liquid chromatographic method
1. Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp xác định acesulfame-K, aspartame, neohesperidine-dihydrochalcone và saccharin trong thực phẩm bằng sắc kí lỏng hiệu năng cao (HPLC) với detector UV.
Phương pháp này đã được đánh giá xác nhận đầy đủ về quy trình thẩm tách thông qua phép thử cộng tác[1] (xem 8.2, 8.3 và Phụ lục C), theo quy trình IUPAC[2] trên các hỗn hợp nền mẫu phân tích sau đây:
- acesulfame-K (từ 86 mg/l đến 331 mg/l) và aspartame (từ 97 mg/kg đến 610 mg/l) trong đồ uống pha từ nước, đồ uống từ trái cây, bánh quy có phomat, súp đóng hộp và đồ uống socola.
- saccarin (từ 70 mg/l đến 97 mg/kg) trong đồ uống pha từ nước, đồ uống từ trái cây, bánh quy có phomat, súp đóng hộp;
- neohesperidine-dihydrochalcone (từ 27 mg/l đến 57 mg/kg) trong đồ uống pha từ nước, đồ uống từ trái cây, bánh quy có phomat, súp đóng hộp.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau là rất cần thiết cho việc áp dụng tiêu chuẩn. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi (nếu có).
TCVN 4851:1989 (ISO 3696:1987), Nước dùng để phân tích trong phòng thí nghiệm - Yêu cầu kỹ thuật và phương pháp thử.
3. Nguyên tắc
Mẫu được pha loãng hoặc được chiết bằng nước. Nếu cần, dung dịch mẫu có chứa các chất tạo ngọt mạnh được tinh sạch bằng thuốc thử Carrez. Cách khác, các mẫu dạng rắn được hồ hóa trong dung dịch NaCl/HCl và chất tạo ngọt được chiết bằng thẩm tách sử dụng cellulose axetat (ngưỡng khối lượng phân tử xấp xỉ 12 000). Dịch chiết đã tinh sạch được phân tích bằng HPLC pha đảo cặp ion với detector UV.
4. Thuốc thử
4.1. Yêu cầu chung
Chỉ sử dụng thuốc thử loại tinh khiết phân tích và chỉ sử dụng nước cất hoặc ít nhất là nước loại 1 của TCVN 4851 (ISO 3696), trừ khi có quy định khác. Khi chuẩn bị các dung dịch, cần tính đến độ tinh khiết của các chất.
4.2. Metanol, loại dùng cho HPLC.
4.3. Axit clohydric, w(HCl) » 36 %1).
4.4. Axit phosphoric, c(H3PO4) = 5 mol/l2).
4.5. Natri hydroxit, c(NaOH) = 5 mol/l.
4.6. Saccharin, w(C7H5NO3S): 98,0 % đến 101,0 % hoặc w(C7H4NNaO3S.2H2O): 99,0 % đến 101,0 %.
4.7. Neohesperidine-dihydrochalcone, w(C28H34O15) ≥ 99,0 %.
4.8. Acesulfame-K, w(C4H4KNO4S) ≥ 99,0 %.
4.9. Aspartame, w(C14H18N2O5) ≥ 98 %.
4.10. Natri clorua.
4.11. Tetrapropylamoni hydro sulfat (TPrA-HSO4)
4.12. Pha động HPLC
4.12.1. Pha động 1 (5 % metanol trong nước)
Dùng pipet (5.4) lấy 50 ml metanol (4.2) cho vào bình định mức 1 lít (5.2), thêm nước đến vạch. Thêm 0,24 g ± 0,01 g TPrA-HSO4 (4.11) và lắc. Chỉnh đến pH 3,5 bằng cách thêm từng giọt natri hydroxit 5 mol/l (4.5) hoặc axit phosphoric 5 mol/l (4.4).
4.12.2. Pha động 2 (75 % metanol trong nước)
Chuyển 750 ml metanol (4.2) từ ống đong sang bình định mức 1 lít (5.2) thêm nước đến vạch. Thêm 0,24 g ± 0,01 g TPrA-HSO4 (4.11) và lắc. Chỉnh đến pH 3,5 bằng cách thêm từng giọt natri hydroxit 5 mol/l (4.5) hoặc axit phosphoric 5 mol/l (4.4).
4.12.3. Pha động rửa giải đẳng dòng (15 % metanol trong nước)
Chuyển 150 ml metanol (4.2) từ ống đong vào bình định mức 1 lít (5.2) và thêm nước đến vạch. Thêm 0,24 g ± 0,01 g TPrA-HSO4 (4.11) và lắc. Chỉnh đến pH 3,5 bằng cách thêm từng giọt natri hydroxit 5 mol/l (4.5) hoặc axit phosphoric 5 mol/l (4.4).
Lọc các dung dịch qua bộ lọc (5.5) và siêu âm trong bể siêu âm (5.9) trong 30 min.
4.13. Dung dịch dùng để thẩm tách, 1,71 mol/l NaCl và 0,01 mol/l HCl, tùy chọn.
Hòa tan 100 g NaCl (4.10) và 1 ml axit HCl đặc (4.3) trong nước đựng trong bình định mức 1 lít (5.2).
4.14. Dung dịch chất thẩm tách, 0,01 mol/l HCl, tùy chọn.
Hòa tan 1 ml axit HCl đặc (4.3) trong nước đựng trong bình định mức 1 lít (5.2).
4.15. Dung dịch gốc acesulfame-K, aspartame, saccharin và neohesperidine-dihydrochalcone
Chuẩn bị các dung dịch 1 000 mg/l của acesulfame-K (4.8) và aspartame (4.9) trong nước. Chuẩn bị dung dịch saccharin (4.6) tương ứng với imit tự do 1 000 mg/l (ví dụ: muối natri khan 1126 mg/l) trong nước và neohesperidine-dihydrochalcone 1 000 mg/l (4.7) trong hỗn hợp 50 % metanol (4.2) và 50 % nước.
4.16. Các dung dịch hiệu chuẩn hỗn hợp có chứa acesulfame-K, aspartame, saccharin và neohesperidine-dihydrochalcone
Từ các dung dịch gốc (4.15) chuẩn bị một dãy các dung dịch chuẩn hỗn hợp có chứa các chất tạo ngọt ở các nồng độ tương ứng với mức tối đa 150 % của giới hạn thích hợp (ví dụ: các mức tối đa theo quy định hiện hành) trong khi đó đã tính đến các bước pha loãng.
VÍ DỤ: Các chất chuẩn hiệu chuẩn phép đo các chất tạo ngọt trong sản phẩm tráng miệng từ sữa.
Các giới hạn hiện hành của EU đối với bốn chất tạo ngọt trong các sản phẩm tráng miệng chứa sữa là:
- acesulfame-K: 350 mg/kg;
- saccharin: 100 mg/kg (imit tự do);
- aspartame: 1 000 mg/kg;
- neohesperidine-dihydrochalcone 50 mg/kg.
150 % của các giới hạn trên là:
- acesulfame-K: 525 mg/kg;
- saccharin: 150 mg/kg (imit tự do);
- aspartame: 1 500 mg/kg;
- neohesperidine-dihydrochalcone 75 mg/kg.
Các chất tạo ngọt từ 20 g mẫu được chiết trong 200 ml chất thẩm tách (độ pha loãng 10:1). Do đó, việc hiệu chuẩn cần được thực hiện đối với các dịch chiết có chứa các nồng độ chất tạo ngọt sau đây:
- acesulfame-K: 50 mg/l;
- saccharin: 15 mg/l (imit tự do);
- aspartame: 150 mg/l;
- neohesperidine-dihydrochalcone 7 mg/l.
Để hiệu chuẩn bảy điểm, lấy các thể tích từ các dung dịch gốc 1 000 mg/l (4.15) như trong Bảng 1 và thêm nước đến vạch 50 ml trong bình định mức (5.2).
Bảng 1 - Chuẩn bị đường chuẩn
|
| Acesulfame-K ml | Saccharin ml | Aspartame ml | Neohesperidine-dihydrochalcone ml |
| 1 | 0,25 | 75 | 0,75 | 50 |
| 2 | 0,50 | 150 | 1,50 | 100 |
| 3 | 0,75 | 225 | 2,25 | 150 |
| 4 | 1,00 | 300 | 3,00 | 200 |
| 5 | 1,50 | 450 | 4,50 | 250 |
| 6 | 2,00 | 600 | 6,00 | 300 |
| 7 | 2,50 | 750 | 7,50 | 350 |
Bảng 2 đưa ra nồng độ chất tạo ngọt trong mỗi dung dịch hiệu chuẩn pha loãng sau:
Bảng 2 - Nồng độ chất tạo ngọt trong mỗi dung dịch hiệu chuẩn
|
| Acesulfame-K mg/l | Saccarin (imit tự do) mg/l | Aspartame mg/l | Neohesperidine-dihydrochalcone mg/l |
| 1 | 5 | 1,5 | 15 | 1 |
| 2 | 10 | 3 | 30 | 2 |
| 3 | 15 | 4,5 | 45 | 3 |
| 4 | 20 | 6 | 60 | 4 |
| 5 | 30 | 9 | 90 | 5 |
| 6 | 40 | 12 | 120 | 6 |
| 7 | 50 | 15 | 150 | 7 |
4.17. Mẫu trắng và mẫu thêm chuẩn để xác định độ thu hồi
Nếu thực hiện chuẩn bị mẫu bằng thẩm tách thì cần chuẩn bị mẫu đồng nhất của cùng loại mẫu thử. Chia mẫu thử thành hai phần. Bổ sung một lượng đã biết các chất tạo ngọt vào một phần (tính theo khối lượng với chất rắn hoặc thể tích với dung dịch là phù hợp).
4.18. Dung dịch Carrez số 1
Hòa tan 15 g kali hexacyanoferat (II) (K4[Fe(CN)6]×3H2O) trong nước và pha loãng đến 100 ml.
4.19. Dung dịch Carrez số 2
Hòa tan 30 g kẽm sulfat (ZnSO4×7H2O) trong nước và pha loãng đến 100 ml.
5. Thiết bị, dụng cụ
5.1. Yêu cầu chung
Sử dụng các thiết bị, dụng cụ thủy tinh của phòng thử nghiệm thông thường và cụ thể như sau:
5.2. Bình định mức, dung tích 50 ml và nhỏ hơn.
5.3. Lọ đựng mẫu dùng cho HPLC, trong suốt, dung tích 2 ml.
5.4. Pipet, dung tích 50 ml và nhỏ hơn.
5.5. Bộ lọc thủy tinh dùng cho pha động.
5.6. Chai có nắp vặn, dung tích 250 ml.
5.7. Phễu thủy tinh.
5.8. Bộ đồng hóa, Ultra Turrax® hoặc loại tương đương.
5.9. Bể siêu âm.
5.10. Bộ khuấy từ thích hợp để khuấy (hoặc máy trộn trục lăn hoặc một vài dụng cụ khác thích hợp cho việc khuấy trộn chất thẩm tách).
5.11. Thanh nam châm mini.
5.12. Bộ lọc màng xyranh, 13 mm, cỡ lỗ 0,45 mm (PVDF hoặc tương đương).
5.13. Bộ lọc pha động, đường kính 4,8 cm, cỡ lỗ 0,45 mm.
5.14. Ống thẩm tách, bằng cellulose axetat, chiều rộng cắt ngang 4,8 cm; ngưỡng khối lượng phân tử xấp xỉ 12 000, tùy chọn.
5.15. Máy đo pH.
5.16. Máy sắc ký lỏng hiệu năng cao (HPLC), được trang bị cột phân tích (5.17), hệ thống bơm gradient, bộ lấy mẫu tự động, detector (UV) (có thể phát hiện ở bước sóng 220 nm đến 280 nm, tốt nhất là detector mảng diot) và được trang bị máy ghi và/hoặc máy tích phân để có thể đo chiều cao và diện tích pic.
5.17. Cột HPLC pha đảo, ví dụ: ODS3 10 mm; 250 mm x 3,2 mm hoặc loại tương tự (cỡ hạt 10 mm, kích thước 250 mm x 3,2 mm).
CHÚ THÍCH: Có thể sử dụng cột có các kích thước khác với quy định nêu trên (ví dụ: đường kính 3,0 mm đến 4,6 mm, dài từ 100 mm đến 250 mm). Các thông số tách (tốc độ dòng, thể tích bơm) cần đảm bảo cho kết quả tương tự.
5.18. Sự phù hợp của hệ thống HPLC
Các chất tạo ngọt acesulfame-K, saccharin, aspartame và neohesperidine-dihydrochalcone cần được phân giải (Rs = 1,3) ra khỏi nhau và ra khỏi các thành phần khác của nền mẫu. Hai thành phần thường gặp phải là các cặp tới hạn: (a) acesulfame-K với theobromine và (b) aspartame với caffeine.
6. Cách tiến hành
6.1. Chuẩn bị mẫu thử không thẩm tách
6.1.1. Các sản phẩm dạng lỏng trong suốt như nước chanh, nước cola hoặc đồ uống
Pha loãng 20 ml mẫu thử bằng nước đựng trong bình định mức 100 ml. Lọc dung dịch qua bộ lọc màng cỡ lỗ 0,45 mm trước khi bơm.
6.1.2. Các sản phẩm dạng lỏng màu đục như nước trái cây hoặc đồ uống từ sữa có bổ sung hương liệu
Pha loãng 20 ml mẫu thử đã đồng nhất trong 50 ml nước đựng trong bình định mức 100 ml, thêm 2 ml dung dịch thuốc thử Carrez số 1 (4.18), trộn và thêm 2 ml dung dịch thuốc thử Carrez số 2 (4.19). Lắc mạnh và để yên dung dịch 10 min ở nhiệt độ phòng. Pha loãng bằng nước đến vạch. Lọc dung dịch qua giấy lọc gấp nếp, loại bỏ 10 ml dịch lọc đầu tiên. Cho dịch lọc đi qua bộ lọc màng cỡ lỗ 0,45 mm trước khi bơm dung dịch mẫu thử vào hệ thống HPLC.
Để yên cho dung dịch kết tủa hết, nếu chất không tan không chứa chất béo có trong thể tích mẫu (trường hợp này là 20 ml) vượt quá khoảng 3 g, thì nên ly tâm hỗn hợp mẫu đã lọc 10 min ở ít nhất 1 400g trước khi lọc dung dịch sang bình định mức 100 ml. Rửa phần kết tủa hai lần với nước và ly tâm lại, mỗi lần thu lấy phần nổi phía trên cho vào bình định mức 100 ml và pha loãng dung dịch bằng nước đến vạch. Quy trình này cũng có thể thực hiện khi lượng chất không tan ít hơn 3 g.
6.1.3. Mứt nhuyễn, mứt, mứt quả nghiền và các sản phẩm có liên quan, trừ trái cây đông lạnh
Cân khoảng 20 g mẫu đồng nhất, chính xác đến 1 mg, cho vào bình định mức 100 ml. Thêm khoảng 60 ml nước và đặt bình cầu vào bể siêu âm ở 40 °C trong 20 min. Nhiệt độ không được vượt quá 40 °C vì aspartame có thể bị phân hủy.
Làm nguội dung dịch đến nhiệt độ phòng. Thêm 2 ml dung dịch Carrez số 1 (4.18), trộn và thêm 2 ml dung dịch Carrez số 2 (4.19). Lắc mạnh và để yên dung dịch ở nhiệt độ phòng 10 min. Pha loãng bằng nước đến vạch. Lọc dung dịch qua giấy lọc gấp nếp và loại bỏ 10 ml dịch lọc đầu tiên. Cho dịch lọc đi qua bộ lọc màng cỡ lỗ 0,45 mm trước khi bơm dung dịch mẫu vào hệ thống HPLC.
Để yên cho dung dịch kết tủa hết, nếu chất không tan không chứa chất béo có trong khối lượng mẫu ban đầu vượt quá khoảng 3 g, thì nên ly tâm hỗn hợp mẫu 10 min ở ít nhất 1 400g trước khi lọc dung dịch sang bình định mức 100 ml. Rửa phần kết tủa hai lần với nước và ly tâm lại, mỗi lần thu lấy phần nổi phía trên cho vào bình định mức 100 ml và pha loãng dung dịch bằng nước đến vạch. Quy trình này cũng có thể thực hiện khi lượng chất không tan ít hơn 3 g.
6.1.4. Sản phẩm bán đặc và sản phẩm đặc như món tráng miệng chứa phomat, sữa chua yoghurt hoặc salad, trừ bột custard
Cân từ 10 g đến 20 g, chính xác đến 1 mg, mẫu thử đã đồng hóa kỹ, cho vào bình định mức 100 ml. Thêm khoảng 50 ml nước và đặt bình vào bể siêu âm ở 40 °C trong 20 min. Không để nhiệt độ vượt quá 40 °C vì aspartame có thể bị phân hủy.
Làm nguội dung dịch đến nhiệt độ phòng. Thêm 2 ml dung dịch Carrez số 1 (4.18), trộn, thêm tiếp 2 ml dung dịch Carrez số 2 (4.19). Lắc mạnh và để yên dung dịch ở nhiệt độ phòng trong 10 min. Pha loãng bằng nước đến vạch. Lọc dung dịch qua giấy lọc gấp nếp và loại bỏ 10 ml dịch lọc đầu tiên.
Trong trường hợp nền mẫu phức hợp, dùng cột chiết pha rắn (ví dụ: cột C18-SPE) tinh sạch thêm dung dịch để bảo vệ cột chiết, vì các chất màu, hương liệu và chất béo không thể tách được bằng thuốc thử Carrez. Trong trường hợp này, cho 2 ml dịch lọc đã làm trong vào cột, đã được hoạt hóa bằng 3 ml metanol (4.2) và 20 ml nước, rửa giải bằng khoảng 20 ml pha động (4.12). Cho dịch lọc đi qua bộ lọc màng cỡ lỗ 0,45 mm trước khi bơm dung dịch mẫu thử vào hệ thống HPLC.
Để yên cho dung dịch kết tủa hết, nếu chất không tan không chứa chất béo có trong khối lượng mẫu ban đầu vượt quá khoảng 3 g, thì nên ly tâm hỗn hợp mẫu 10 min ở ít nhất 1 400g trước khi lọc dung dịch sang bình định mức 100 ml. Rửa phần kết tủa hai lần với nước và ly tâm lại, mỗi lần thu lấy phần nổi phía trên cho vào bình định mức 100 ml và pha loãng dung dịch bằng nước đến vạch. Quy trình này cũng có thể thực hiện khi lượng chất không tan ít hơn 3 g.
6.1.5. Bột custard
Cân khoảng 10 g mẫu thử, chính xác đến 1 mg, cho vào bình định mức 500 ml. Thêm khoảng 400 ml nước và thực hiện như trên, nghĩa là thêm 6 ml dung dịch thuốc thử Carrez số 1 (4.18), trộn, thêm 6 ml dung dịch thuốc thử Carrez số 2 (4.19) để làm trong.
Để yên cho dung dịch kết tủa hết, nếu chất không tan không chứa chất béo có trong khối lượng mẫu ban đầu vượt quá khoảng 3 g, thì nên ly tâm hỗn hợp mẫu 10 min ở ít nhất 1 400g trước khi lọc dung dịch sang bình định mức 500 ml. Rửa phần kết tủa hai lần với nước và ly tâm lại, mỗi lần thu lấy phần nổi phía trên cho vào bình định mức 500 ml và pha loãng dung dịch bằng nước đến vạch. Quy trình này cũng có thể thực hiện khi lượng chất không tan ít hơn 3 g.
6.2. Chuẩn bị mẫu thử có thẩm tách
6.2.1. Mẫu dạng bán rắn và mẫu dạng rắn
Cân 20 g mẫu đồng nhất cho vào cốc mỏ 100 ml. Thêm 20 g dung dịch thẩm tách (4.13) và trộn kỹ để tạo hồ nhão. Cắt một đoạn 25 cm chiều dài ống thẩm tách (5.14) và đặt vào nước lạnh 20 min để mềm ra. Chuẩn bị ống thẩm tách bằng cách thắt nút một đầu. Nạp mẫu vào ống thẩm tách, nếu cần, sử dụng dung dịch thẩm tách (4.13) để chuyển mẫu vào. Thắt nút đầu còn lại càng sát với mẫu càng tốt. Cắt bỏ phần ống thừa.
Đặt túi đựng mẫu vào chai có nắp vặn (5.6) và thêm 200 ml (V1) dung dịch chất thẩm tách (4.14). Đặt thêm thanh nam châm (5.11) vào. Đặt chai này lên bộ khuấy từ (5.10) đảm bảo rằng tất cả mẫu ngập trong dung dịch thẩm tách và để cho thẩm tách trong 40 h. Cách khác, có thể đặt chai lên máy trộn lăn (hoặc thiết bị khuấy trộn khác) và thẩm tách trong 40 h. Lọc dịch thẩm tách qua bộ lọc màng xyranh (5.12).
6.2.2. Nước quả
Đong 20 ml mẫu đã lắc trộn kỹ cho vào cốc có mỏ, thêm 20 ml dung dịch thẩm tách (4.13). Lắc kỹ. Cho vào ống thẩm tách (5.14) và để cho thẩm tách 24 h như trên. Lọc dịch thẩm tách qua bộ lọc màng xyranh (5.12).
6.3. Phân tích bằng HPLC
Bơm dung dịch mẫu thử đã chuẩn bị trong 6.1 hoặc 6.2 vào hệ thống HPLC (5.16).
Các gradient HPLC sau đây đã chứng minh là phù hợp.
Bảng 3 - Gradient HPLC I, tốc độ dòng 0,8 ml/min
| Thời gian (min) | Pha động 1 (%) | Pha động 2 (%) |
| 0 | 100 | 0 |
| 30 | 0 | 100 |
| 35 | 0 | 100 |
| 40 | 100 | 0 |
Sử dụng các điều kiện trong Bảng 3, cần cài đặt bước sóng ở 220 nm từ 0 min đến 25 min để thẩm tách acesulfame-K, aspartame và saccharin. Cần cài đặt lại bước sóng ở 280 nm để phân tích neohesperidine-dihydrochalcone. Gradient có thể dài hơn để tách tốt hơn.
Bảng 4 - Gradient HPLC II, tốc độ dòng 0,8 ml/min
| Thời gian (min) | Pha động 1 (%) | Pha động 2 (%) |
| 0 | 100 | 0 |
| 25 | 50 | 50 |
| 30 | 0 | 100 |
| 35 | 0 | 100 |
| 40 | 100 | 0 |
Nếu chỉ phân tích acesulfame-K, aspartame và saccharin thì có thể áp dụng các điều kiện đẳng dòng (4.12.3).
6.4. Diễn giải dữ liệu sắc ký
Nhận biết acesulfame-K, aspartame, saccharin và neohesperidine-dihydrochalcone trong mẫu bằng cách so sánh thời gian lưu của các chất tạo ngọt quan sát được khi phép phân tích dung dịch chuẩn (4.16) được phân tích trong cùng mẻ mẫu với thời gian lưu của hợp chất rửa giải trong phép phân tích mẫu.
Đo diện tích pic quan sát được của từng chất tạo ngọt trong mỗi dung dịch.
Nếu diện tích pic của chất phân tích bất kỳ trong dịch chiết mẫu lớn hơn đặc trưng diện tích pic của dung dịch chuẩn có nồng độ cao nhất thì cần pha loãng dịch chiết mẫu bằng dung dịch thẩm tách (4.14) và phân tích lại dịch chiết đã pha loãng.
Dựng đường chuẩn đối với từng chất tạo ngọt từ các kết quả phân tích các dung dịch chuẩn (4.16). Nồng độ của dung dịch chuẩn được thể hiện trên trục x và đặc trưng diện tích pic thể hiện trên trục y.
Nếu các kết quả thu được của các dung dịch chuẩn là tuyến tính và nồng độ của chất tạo ngọt nằm giữa nồng độ cao nhất và thấp nhất của các dung dịch chuẩn thì đường chuẩn có thể được dùng để tính nồng độ chất tạo ngọt trong dịch chiết mẫu. Xác định độ dốc (g) và giao điểm (I) của đường chuẩn.
7. Tính kết quả
7.1. Tính hàm lượng chất tạo ngọt có trong mẫu
Tính phần khối lượng, w, bằng miligam trên kilogam (mg/kg) hoặc nồng độ khối lượng, p, bằng miligam trên lít mẫu (mg/l), của chất tạo ngọt theo Công thức (1) sau đây:
w hoặc p = ![]() (1)
(1)
Trong đó:
A là đặc trưng diện tích pic;
I là giao điểm của đường chuẩn;
g là độ dốc của đường chuẩn;
m0 là khối lượng mẫu thử, tính bằng mililit (ml) hoặc gam (g);
F là hệ số pha loãng.
7.2. Độ thu hồi chất tạo ngọt
Tính độ thu hồi chất tạo ngọt từ mẫu thêm chuẩn theo Công thức (2) và Công thức (3):
![]() (2)
(2)
Nếu cần, hiệu chính các kết quả đo độ thu hồi sử dụng Công thức (3):
![]() (3)
(3)
Trong đó:
C là kết quả chưa hiệu chính của phép đo nồng độ chất tạo ngọt;
CF là kết quả đo nồng độ chất tạo ngọt trong mẫu thêm chuẩn;
CB là kết quả đo nồng độ chất tạo ngọt trong mẫu trắng được dùng để tạo mẫu thêm chuẩn;
CS là nồng độ chất tạo ngọt đã bổ sung trong mẫu thêm chuẩn;
R là độ thu hồi chất tạo ngọt từ mẫu thêm chuẩn được biểu thị theo tỷ lệ phần trăm;
CR là kết quả đo độ thu hồi đã hiệu chính
7.3. Biểu thị kết quả
Đối với các mẫu được chuẩn bị bằng thẩm tách thì dữ liệu của mẫu là độ thu hồi đã hiệu chính sử dụng giá trị độ thu hồi thu được bằng cách đo các chất tạo ngọt trong mẫu thêm chuẩn được phân tích cùng thời điểm với mẫu thử.
8. Độ chụm
8.1. Yêu cầu chung
Chi tiết của phép thử liên phòng về độ chụm của phương pháp được nêu trong Phụ lục C. Các dữ liệu thu được từ phép nghiên cứu cộng tác này có thể không áp dụng được cho các dải nồng độ chất phân tích và các nền mẫu khác với các dải nồng độ chất phân tích và các nền mẫu nêu trong Phụ lục C.
8.2. Độ lặp lại
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ, thu được khi tiến hành trên vật liệu thử giống hệt nhau, do một người thực hiện, sử dụng cùng thiết bị, trong một khoảng thời gian ngắn như nhau, không quá 5 % các trường hợp vượt quá giới hạn lặp lại r.
Các giá trị đối với acesulfame-K là:
| Đồ uống từ nước |
| r = 21,8 mg/l |
| Đồ uống từ trái cây |
| r = 15,3 mg/l |
| Bánh quy chứa phomat |
| r = 6,2 mg/kg |
| Súp đóng hộp |
| r = 7,9 mg/kg |
| Đồ uống chứa socola uống liền |
| r = 20,8 mg/l |
Các giá trị đối với aspartame là:
| Đồ uống từ nước |
| r = 43,5 mg/l |
| Đồ uống từ trái cây |
| r = 47,4 mg/l |
| Bánh quy chứa phomat |
| r = 22,1 mg/kg |
| Súp đóng hộp |
| r = 11,8 mg/kg |
| Đồ uống chứa socola uống liền |
| r = 43,4 mg/l |
| Các giá trị đối với saccharin là: | ||
| Đồ uống từ nước |
| r = 5,4 mg/l |
| Đồ uống từ trái cây |
| r = 14 mg/l |
| Bánh quy chứa phomat |
| r = 7,4 mg/kg |
| Súp đóng hộp |
| r = 4,5 mg/kg |
Các giá trị đối với neohesperidine-dihydrochalcone là:
| Đồ uống từ nước |
| r = 3,8 mg/l |
| Đồ uống từ trái cây |
| r = 5,2 mg/l |
| Súp đóng hộp |
| r = 23,5 mg/kg |
8.3. Độ tái lập
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ, thu được bởi hai phòng thử nghiệm khi tiến hành trên vật liệu thử giống hệt nhau, không quá 5 % các trường hợp vượt quá giới hạn tái lập R.
Các giá trị đối với acesulfame-K là:
| Đồ uống từ nước |
| R = 56,9 mg/l |
| Đồ uống từ trái cây |
| R = 46,4 mg/l |
| Bánh quy chứa phomat |
| R = 103 mg/kg |
| Súp đóng hộp |
| R = 18,2 mg/kg |
| Đồ uống chứa socola uống liền |
| R = 40,0 mg/l |
| Các giá trị đối với aspartame là: | ||
| Đồ uống từ nước |
| R = 161 mg/l |
| Đồ uống từ trái cây |
| R = 207 mg/l |
| Bánh quy chứa phomat |
| R = 217 mg/kg |
| Súp đóng hộp |
| R = 37,4 mg/kg |
| Đồ uống chứa socola uống liền |
| R = 106 mg/l |
| Các giá trị đối với saccharin là: | ||
| Đồ uống từ nước |
| R = 17,5 mg/l |
| Đồ uống từ trái cây |
| R = 31,2 mg/l |
| Bánh quy chứa phomat |
| R = 44,4 mg/kg |
| Súp đóng hộp |
| R = 16,9 mg/kg |
| Các giá trị đối với neohesperidine-dihydrochalcone là: | ||
| Đồ uống từ nước |
| R = 9,9 mg/l |
| Đồ uống từ trái cây |
| R = 20,0 mg/l |
| Súp đóng hộp |
| R = 34,9 mg/kg |
9. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải nêu rõ các thông tin sau:
- mọi thông tin cần thiết để nhận biết đầy đủ về mẫu thử;
- viện dẫn tiêu chuẩn này và phương pháp đã sử dụng;
- ngày và phương pháp lấy mẫu đã sử dụng (nếu biết);
- ngày nhận mẫu;
- ngày thử nghiệm;
- kết quả thu được và đơn vị biểu thị;
- các điểm cụ thể quan sát được trong khi thử nghiệm;
- mọi chi tiết thao tác không quy định trong tiêu chuẩn này, hoặc được xem là tùy chọn, có thể ảnh hưởng đến kết quả.
Ghi lại tất cả các dữ liệu định tính và định lượng. Trừ khi có các yêu cầu khác, tất cả các kết quả phải được hiệu chính để phục hồi. Báo cáo phải trình bày các kết quả đã được hiệu chính để phục hồi và cung cấp các giá trị của dữ liệu này.
Phụ lục A
(Quy định)
Ví dụ về các điều kiện sắc ký cho kết quả thỏa đáng
A.1. Cột sắc ký
| Kiểu: | Pha đảo (RP) |
| Pha tĩnh và chiều dài cột: | cỡ hạt hình cầu 10 mm dùng cho cột dài 250 mm (phù hợp với các tiêu chí thực hành đã quy định) |
| Đường kính trong: Cột bảo vệ: Ví dụ: | 3,2 mm nên dùng (tùy chọn) Partisil ODS 33) |
A.2. Tốc độ dòng: 0,8 ml/min
A.3. Thể tích bơm: từ 10 ml đến 20 ml
A.4. Detector: UV phát hiện ở bước sóng 220 nm từ 0 min đến 25 min để phân tích acesulfame-K, aspartame, saccharin và ở bước sóng 280 nm để phân tích neohesperidine dihydrochalcone.
A.5. Pha động
Phân tích gradient như 6.3.
Phụ lục B
(Tham khảo)
Sắc ký đồ
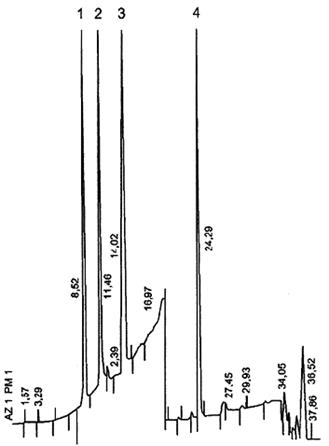
CHÚ DẪN
1. Acesulfeme-K
2. Saccharin
3. Aspartame
4. Neohesperidine-dihydrochalcone
Hình B.1 - Sắc ký đồ của dung dịch chuẩn các chất tạo ngọt
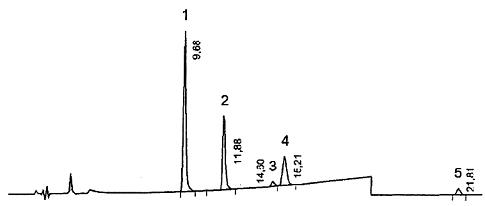
CHÚ DẪN
1. Acesulfame-K
2. Saccharin
3. Caffeine
4. Aspartame
5. Neohesperidine-dihydrochalcone
Hình B.2 - Sắc ký đồ của các chất tạo ngọt trong đồ uống có chứa caffeine
Phụ lục C
(Tham khảo)
Dữ liệu về độ chụm
Các dữ liệu trong Bảng C.1, C.2 và C.3 thu được từ phép thử liên phòng thực hiện theo quy định của IUPAC Harmonised Protocol [2] do Vụ Môi trường, Thực phẩm và Nông nghiệp (DEFRA), Phòng thí nghiệm Khoa học Trung tâm (CSL) thực hiện trên nước uống, nước trái cây, bánh quy chứa phomat, súp đóng hộp và đồ uống chứa socola uống liền.
Mười bảy phòng thử nghiệm tham gia trong các phép thử liên phòng. Các đơn vị tham gia vào phép thử sơ bộ để đánh giá mọi trở ngại có thể xảy ra trước khi tham gia xác định chính thức. Trong suốt quá trình đánh giá sơ bộ, các đơn vị tham gia được giao ba loại mẫu thử: a) mẫu thử của hỗn hợp sản phẩm sữa hoặc sản phẩm bánh có chứa chất béo; b) các mẫu kép được bổ sung các chất tạo ngọt và c) mẫu trắng. Mẫu trắng được chia thành hai phần cho các đơn vị tham gia và một phần được dùng làm mẫu trắng. Một phần mẫu trắng còn lại được thêm các chất tạo ngọt để đánh giá độ thu hồi.
Trong quá trình đánh giá thử nghiệm chính thức, các đơn vị tham gia được nhận mười mẫu thử (năm mẫu kép mù) từ nước uống, nước trái cây, bánh quy chứa phomat, súp và bột socola nóng để phân tích sử dụng phương pháp nêu trong Điều 6.
Bảng C.1 - Acesulfame-K
|
| Nước uống | Nước trái cây | Bánh quy chứa phomat | Súp đóng hộp | Đồ uống chứa socola uống liền |
| Năm thử nghiệm | 2003 | 2003 | 2003 | 2003 | 2003 |
| Số phòng thử nghiệm | 17 | 17 | 17 | 17 | 17 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 15 | 15 | 13 | 14 | 13 |
| Số phòng thử nghiệm ngoại lệ | 2 | 0 | 2 | 3 | 1 |
| Số lượng kết quả được chấp nhận | 30 | 30 | 26 | 28 | 26 |
| Giá trị trung bình | 331 | 219 | 239 | 95,9 | 85,6 |
| Độ lệch chuẩn lặp lại sr, mg/kg hoặc mg/l | 7,8 | 5,5 | 2,2 | 2,8 | 7,4 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 2,4 | 2,5 | 0,9 | 3,0 | 8,7 |
| Giới hạn lặp lại, r [mg/kg hoặc mg/l] | 21,8 | 15,3 | 6,2 | 7,9 | 20,8 |
| Độ lệch chuẩn tái lập sR, mg/kg hoặc mg/l | 20,3 | 16,6 | 36,9 | 6,4 | 14,3 |
| Độ lệch chuẩn tương đối tái lập, RSDR, % | 6,1 | 7,1 | 15,5 | 6,8 | 16,7 |
| Giới hạn tái lập, R (R = 2,8 x sR), mg/kg hoặc mg/l | 56,9 | 46,4 | 103 | 18,2 | 40,0 |
| Giá trị Horrat | 0,9 | 1,1 | 2,2 | 0,8 | 2,0 |
Bảng C.2 - Aspartame
|
| Nước uống | Nước trái cây | Bánh quy chứa phomat | Súp đóng hộp | Đồ uống chứa socola uống liền |
| Năm thử nghiệm | 2003 | 2003 | 2003 | 2003 | 2003 |
| Số phòng thử nghiệm | 17 | 17 | 17 | 17 | 17 |
| Số lượng mẫu thử | 2 | 2 | 2 | 3 | 2 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 16 | 16 | 11 | 13 | 12 |
| Số phòng thử nghiệm ngoại lệ | 1 | 1 | 2 | 3 | 3 |
| Số lượng kết quả được chấp nhận | 32 | 32 | 22 | 26 | 24 |
| Giá trị trung bình | 567 | 610 | 501 | 96,9 | 153 |
| Độ lệch chuẩn lặp lại sr, mg/kg hoặc mg/l | 15,5 | 16,9 | 7,9 | 4,2 | 15,5 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 2,73 | 2,8 | 1,6 | 4,4 | 10,1 |
| Giới hạn lặp lại, r [mg/kg hoặc mg/l] | 43,5 | 47,4 | 22,1 | 11,8 | 43,4 |
| Độ lệch chuẩn tái lập sR, mg/kg hoặc mg/l | 57,6 | 74,1 | 77,6 | 13,4 | 37,8 |
| Độ lệch chuẩn tương đối tái lập, RSDR, % | 10,2 | 12,1 | 15,5 | 14,1 | 24,7 |
| Giới hạn tái lập, R (R = 2,8 x sR), mg/kg hoặc mg/l | 161 | 207 | 217 | 37,4 | 106 |
| Giá trị Horrat | 1,7 | 2,0 | 2,5 | 1,7 | 3,3 |
Bảng C.3 - Saccharin
|
| Nước uống | Nước trái cây | Bánh quy chứa phomat | Súp đóng hộp |
| Năm thử nghiệm | 2003 | 2003 | 2003 | 2003 |
| Số phòng thử nghiệm | 17 | 17 | 17 | 17 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 15 | 14 | 8 | 12 |
| Số phòng thử nghiệm ngoại lệ | 2 | 1 | 1 | 3 |
| Số lượng kết quả được chấp nhận | 30 | 28 | 16 | 24 |
| Giá trị trung bình | 69,6 | 91,4 | 83,1 | 96,7 |
| Độ lệch chuẩn lặp lại sr, mg/kg hoặc mg/l | 1,9 | 1,4 | 2,6 | 1,6 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 2,8 | 1,5 | 3,2 | 1,7 |
| Giới hạn lặp lại, r [mg/kg hoặc mg/l] | 5,4 | 3,9 | 7,4 | 4,5 |
| Độ lệch chuẩn tái lập sR, mg/kg hoặc mg/l | 6,2 | 11,1 | 15,9 | 6,0 |
| Độ lệch chuẩn tương đối tái lập, RSDR, % | 9,0 | 12,2 | 19,1 | 6,2 |
| Giới hạn tái lập, R (R = 2,8 x sR), mg/kg hoặc mg/l | 17,5 | 31,2 | 44,4 | 16,9 |
| Giá trị Horrat | 1,1 | 1,5 | 2,3 | 0,8 |
Bảng C.4 - Neohesperidine-dihydrochalcone
|
| Nước uống | Nước trái cây | Súp đóng hộp |
| Năm thử nghiệm | 2003 | 2003 | 2003 |
| Số phòng thử nghiệm | 17 | 17 | 17 |
| Số lượng mẫu thử | 2 | 2 | 2 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 16 | 15 | 14 |
| Số phòng thử nghiệm ngoại lệ | 1 | 0 | 0 |
| Số lượng kết quả được chấp nhận | 32 | 30 | 28 |
| Giá trị trung bình | 27,3 | 34,1 | 56,5 |
| Độ lệch chuẩn lặp lại sr, mg/kg hoặc mg/l | 1,4 | 1,8 | 8,4 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 5,0 | 5,4 | 14,9 |
| Giới hạn lặp lại, r [mg/kg hoặc mg/l] | 3,8 | 5,2 | 23,5 |
| Độ lệch chuẩn tái lập sR, mg/kg hoặc mg/l | 3,6 | 7,1 | 12,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR, % | 5,0 | 20,9 | 22,0 |
| Giới hạn tái lập, R (R = 2,8 x sR), mg/kg hoặc mg/l | 9,9 | 20,0 | 34,9 |
| Giá trị Horrat | 1,3 | 2,2 | 2,5 |
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] Willetts, P., Anderson, S., Brereton, P., and Wood, R.: Determination of intense sweeteners in foodstuffs. Collaborative trial, J Assoc Publ Analysts, 1996, 32, 53 - 97
[2] IUPAC Harmonised Protocol for the Design, Conduct and Interpretation of method-Performance Studies. Pure & Appl. Chem., Vol. 67, No., 2, pp.331-343
1) w là khối lượng.
2) c là nồng độ chất.
3) Partisil ODS 3 là ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra để thuận tiện cho người sử dụng tiêu chuẩn mà không ấn định sử dụng sản phẩm này.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 10992:2015 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 10992:2015 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 10992:2015 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 10992:2015 DOC (Bản Word)