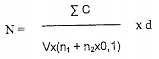- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn quốc gia TCVN 8685-43:2023 Quy trình kiểm nghiệm vắc xin – Phần 43
| Số hiệu: | TCVN 8685-43:2023 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Nông nghiệp-Lâm nghiệp |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
05/09/2023 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 8685-43:2023
TCVN 8685-43:2023: Quy trình kiểm nghiệm vắc xin vô hoạt phòng bệnh viêm phổi do Pasteurella multocida type A ở lợn
Tiêu chuẩn Quốc gia TCVN 8685-43:2023 được ban hành bởi Trung tâm Kiểm nghiệm thuốc Thú y Trung Ương 1 - Cục Thú y, Bộ Nông nghiệp và Phát triển nông thôn, và đã được Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định. Văn bản này có hiệu lực từ ngày ban hành, quy định quy trình kiểm nghiệm vắc xin vô hoạt phòng bệnh viêm phổi do Pasteurella multocida type A ở lợn.
Tiêu chuẩn đưa ra một số hướng dẫn quan trọng về cách thức kiểm nghiệm vắc xin, trong đó bao gồm các phần về cảm quan, độ vô trùng, độ thuần khiết, độ vô hoạt, độ an toàn, và hiệu lực của vắc xin. Các chỉ tiêu này sẽ được kiểm tra một cách nghiêm ngặt, đảm bảo chất lượng vắc xin trước khi được đưa vào sử dụng.
Trong quy trình kiểm nghiệm bao gồm các bước cơ bản như kiểm tra cảm quan (mức độ đồng đều của hỗn dịch vắc xin), kiểm tra độ vô trùng, kiểm tra độ vô hoạt (không phát hiện vi khuẩn tồn tại trong mẫu vắc xin), cũng như thông qua nhiều phép thử trên động vật, bao gồm lợn, chuột lang và chuột nhắt trắng.
Đối với việc kiểm tra độ an toàn, có thể chọn phương pháp kiểm tra trên lợn hoặc thay thế bằng chuột lang và chuột nhắt trắng. Kết quả sẽ được coi là đạt yêu cầu khi không có dấu hiệu phản ứng bất lợi nào xuất hiện sau khi tiêm.
Ngoài ra, quy trình cũng quy định về việc kiểm tra hiệu lực của vắc xin. Có hai phương pháp được áp dụng là phương pháp công cường độc trên chuột nhắt trắng và phương pháp huyết thanh học. Đối với phương pháp đầu tiên, vắc xin sẽ được thử nghiệm để xác định LD50, trong đó yêu cầu LD50 của nhóm được tiêm vắc xin phải cao hơn nhóm đối chứng ít nhất 100 lần. Đối với phương pháp huyết thanh học, yêu cầu ít nhất 80% mẫu huyết thanh cần đạt hiệu giá kháng thể ≥ 4 log2.
Cuối cùng, báo cáo kết quả kiểm nghiệm phải đầy đủ thông tin về mẫu thử, phương pháp thử đã sử dụng, các điều kiện thao tác khác cùng với mọi tình huống bất thường có thể ảnh hưởng đến kết quả để đảm bảo tính chính xác và độ tin cậy của vắc xin. Tiêu chuẩn này không chỉ mang lại hướng dẫn rõ ràng cho các cơ sở sản xuất mà còn giúp bảo vệ sức khỏe cho đàn lợn, góp phần nâng cao chất lượng nông sản trong ngành chăn nuôi.
Tải tiêu chuẩn Việt Nam TCVN 8685-43:2023
TIÊU CHUẨN QUỐC GIA
TCVN 8685-43:2023
QUY TRÌNH KIỂM NGHIỆM VẮC XIN –
PHẦN 43: VẮC XIN VÔ HOẠT PHÒNG BỆNH VIÊM PHỔI DO
PASTEURELLA MULTOCIDA TYPE A Ở LỢN
Vaccine testing procedure - Part 43: Swine pasteurella multocida type A Vaccine, Inactivated
Lời nói đầu
TCVN 8685-43:2023 do Trung tâm Kiểm nghiệm thuốc Thú y Trung Ương 1 - Cục Thú y biên soạn, Bộ Nông nghiệp và Phát triển nông thôn đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
Bộ TCVN 8685 Quy trình kiểm nghiệm Vắc xin gồm các phần:
- TCVN 8685-1:2011, Phần 1: Vắc xin phó thương hàn lợn nhược độc;
- TCVN 8685-2:2011, Phần 2: Vắc xin viêm gan siêu vi trùng vịt;
- TCVN 8685-3:2011, Phần 3: Vắc xin E.coli của lợn;
- TCVN 8685-4:2011, Phần 4: Vắc xin vô hoạt phòng hội chứng giảm đẻ ở gà;
- TCVN 8685-5:2011, Phần 5: Vắc xin ung khí thán;
- TCVN 8685-6:2011, Phần 6: Vắc xin Gumboro nhược độc;
- TCVN 8685-7:2011, Phần 7: Vắc xin nhiệt thán nha bào vô độc chủng 34 F2;
- TCVN 8685-8:2011, Phần 8: Vắc xin dịch tả lợn nhược độc;
- TCVN 8685-9:2022, Phần 9: Vắc xin vô hoạt phòng bệnh Cúm gia cầm A/H5N1 (xuất bản lần 2);
- TCVN 8685-10:2022, Phần 10: Vắc xin vô hoạt phòng bệnh Lở mồm long móng (FMD) (xuất bản lần 2);
- TCVN 8685-11:2014, Phần 11: Vắc xin vô hoạt phòng bệnh Phù đầu gà (coryza);
- TCVN 8685-12:2014, Phần 12: Vắc xin nhược độc, đông khô phòng hội chứng rối loạn hô hấp và sinh sản ở lợn (PRRS);
- TCVN 8685-13:2014, Phần 13: Vắc xin vô hoạt phòng hội chứng rối loạn hô hấp và sinh sản ở lợn (PRRS);
- TCVN 8685-14:2017, Phần 14: Vắc xin vô hoạt phòng bệnh viêm phổi thể kính ở lợn;
- TCVN 8685-15:2017, Phần 15: Vắc xin vô hoạt phòng bệnh viêm phổi do pasteurella multocida type D gây ra ở lợn;
- TCVN 8685-16:2017, Phần 16: Vắc xin vô hoạt phòng bệnh viêm teo mũi truyền nhiễm ở lợn;
- TCVN 8685-17:2017, Phần 17: Vắc xin vô hoạt phòng bệnh viêm màng phổi ở lợn;
- TCVN 8685-18:2017, Phần 18: Vắc xin vô hoạt phòng bệnh Newcastle;
- TCVN 8685-19:2017, Phần 19: Vắc xin vô hoạt phòng bệnh Gumboro;
- TCVN 8685-20:2018, Phần 20: Vắc xin nhược độc phòng bệnh Newcastle;
- TCVN 8685-21:2018, Phần 21: Vắc xin phòng bệnh đậu gà;
- TCVN 8685-22:2018, Phần 22: Vắc xin vô hoạt phòng bệnh tụ huyết trùng ở gia cầm;
- TCVN 8685-23:2018, Phần 23: Vắc xin vô hoạt phòng bệnh Salmonella enteritidis ở gà;
- TCVN 8685-24:2018, Phần 24: Vắc xin vô hoạt phòng bệnh Salmonella typhimurium ở gà;
- TCVN 8685-25:2018, Phần 25: Vắc xin phòng bệnh giả dại ở lợn;
- TCVN 8685-26:2018, Phần 26: Vắc xin nhược độc phòng bệnh viêm thanh khí quản truyền nhiễm ở gà;
- TCVN 8685-27:2018, Phần 27: Vắc xin nhược độc phòng bệnh viêm phế quản truyền nhiễm ở gà;
- TCVN 8685-28:2019, Phần 28: Vắc xin vô hoạt phòng bệnh Tụ huyết trùng ở lợn;
- TCVN 8685-29:2019, Phần 29: Vắc xin vô hoạt phòng bệnh Viêm phế quản truyền nhiễm (IB) ở gà;
- TCVN 8685-30:2019, Phần 30: Vắc xin nhược độc phòng bệnh Viêm não tủy truyền nhiễm ở gà;
- TCVN 8685-31:2019, Phần 31 Vắc xin phòng bệnh Dại ở chó;
- TCVN 8685-32:2019, Phần 32: Vắc xin vô hoạt phòng bệnh Mycoplasma gallisepticum ở gia cầm;
- TCVN 8685-33:2019, Phần 33: Vắc xin vô hoạt phòng bệnh Riermerella anatipestifer;
- TCVN 8685-34:2020, Phần 34: Vắc xin phòng bệnh tiêu chảy thành dịch do Porcine epidemic diarrhea virus (PEDV) gây ra ở lợn;
- TCVN 8685-35:2020, Phần 35: Vắc xin vô hoạt phòng bệnh tụ huyết trùng ở trâu bò;
- TCVN 8685-36:2020, Phần 36: Vắc xin vô hoạt phòng bệnh tụ huyết trùng và bệnh đóng dấu ở lợn;
- TCVN 8685-37:2020, Phần 37: Vắc xin nhược độc phòng bệnh Marek ở gà;
- TCVN 8685-38:2020, Phần 38: Vắc xin vô hoạt phòng bệnh do Leptospira gây ra;
- TCVN 8685-39:2020, Phần 39: Vắc xin vô hoạt phòng hội chứng còi cọc do Circovirus gây ra ở lợn;
- TCVN 8685-40:2023, Phần 40: Vắc xin vô hoạt phòng bệnh viêm não tủy truyền nhiễm do Avian Encephalomyelitis Virus ở gà;
- TCVN 8685-41:2023, Phần 41: Vắc xin phòng bệnh viêm khớp do Avian Reovirus ở gà;
- TCVN 8685-42:2023, Phần 42: Vắc xin phòng bệnh E.coli ở gia cầm;
- TCVN 8685-43:2023, Phần 43: Vắc xin vô hoạt phòng bệnh viêm phổi do Pasteurella multocida type A ở lợn.
QUY TRÌNH KIỂM NGHIỆM VẮC XIN –
PHẦN 43: VẮC XIN VÔ HOẠT PHÒNG BỆNH VIÊM PHỔI DO
PASTEURELLA MULTOCIDA TYPE A Ở LỢN
Vaccine testing procedure - Part 43: Swine Pasteurella multocida type A Vaccine, Inactivated
1 Phạm vi áp dụng
Tiêu chuẩn này quy định quy trình kiểm nghiệm Vắc xin vô hoạt phòng bệnh viêm phổi do Pasteurella multocida type A ở lợn.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các bản sửa đổi, bổ sung (nếu có).
TCVN 8684: 2022 Vắc xin và chế phẩm sinh học dùng trong thú y - Phép thử độ thuần khiết
3 Chữ viết tắt
- BAB (Blood Agar Base): Môi trường thạch máu cơ bản.
- BHI (Brain Heart Infusion): Môi trường canh thang não tim.
- ELISA (Enzyme-linked Immunosorbent Assay): Phản ứng miễn dịch gắn enzym.
- LD50 (Lethal Dose, 50%): Liều gây chết trung bình 50%.
- PBS (Phosphate Buffered Saline): Dung dịch muối đệm photphat.
4 Nguyên tắc
Vắc xin được kiểm tra các chỉ tiêu cảm quan, độ vô trùng, độ thuần khiết, độ vô hoạt bằng các phương pháp phân tích trong phòng thí nghiệm, các chỉ tiêu độ an toàn và hiệu lực được đánh giá trên động vật thí nghiệm.
5 Vật liệu thử và thuốc thử
5.1 Lợn, từ 3 tuần tuổi đến 4 tuần tuổi, khỏe mạnh không có kháng thể Pasteurella multocida type A.
5.2 Thỏ, trọng lượng từ 1,8 kg đến 2 kg, khỏe mạnh.
5.3 Chuột lang, trọng lượng từ 350 g đến 400 g, khỏe mạnh.
5.4 Chuột nhắt trắng, trọng lượng từ 18 g đến 20 g, khỏe mạnh.
5.5 Vi khuẩn Pasteurella multocida type A cường độc.
5.6 Nước muối sinh lý, vô trùng (dung dịch NaCl 0,9 %).
5.7 Môi trường canh thang não tim (BHI), đã được hấp tiệt trùng.
5.8 Kit ELISA phát hiện kháng thể Pasteurella multocida type A.
6 Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ của phòng thí nghiệm thông thường và cụ thể như sau:
6.1 Tủ ấm có thể duy trì nhiệt độ 37 °C ± 0,5 °C.
6.2 Kính hiển vi, có vật kính với độ phóng đại 100 X.
6.3 Tủ lạnh có thể duy trì nhiệt độ từ 2 °C đến 8 °C.
6.4 Vortex mixer (máy lắc trộn) có tốc độ lắc từ 50 vòng/phút đến 2400 vòng/phút.
6.5 Pipet đơn kênh, thể tích từ 50 μl đến 200 μl, từ 100 μl đến 1000 μl.
6.6 Xyranh vô trùng có dung tích 1 ml, 5 ml, 10 ml.
6.7 Đầu tip phù hợp với pipet.
7 Cách tiến hành
7.1 Kiểm tra cảm quan
- Lắc nhẹ lọ vắc xin và quan sát độ đồng đều của hỗn dịch bằng mắt thường.
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra cảm quan đạt yêu cầu khi có hỗn dịch đồng đều, không đông vón, không lắng cặn.
7.2 Kiểm tra độ vô trùng
- Kiểm tra tạp nhiễm vi khuẩn, tạp nhiễm nấm mốc, tạp nhiễm Mycoplasma sp và tạp nhiễm Salmonella theo quy định tại mục 6.2.1, 6.2.2, 6.2.3 và 6.2.4 của TCVN 8684:2022.
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra độ vô trùng đạt yêu cầu khi không có bất cứ tạp khuẩn, nấm mốc, Mycoplasma và Salmonella mọc trên môi trường kiểm tra trong thời gian theo dõi.
7.3 Kiểm tra độ vô hoạt
- Dùng pipet đơn kênh (6.5) nhỏ 100 μl vắc xin vào môi trường BHI (5.7) rồi ủ ở tủ ấm (6.1) trong 24 h đến 48 h.
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra độ vô hoạt đạt yêu cầu khi không phát hiện vi khuẩn Pasteurella multocida phát triển trên môi trường nuôi cấy.
7.4 Kiểm tra độ thuần khiết
- Kiểm tra hình thái vi khuẩn bằng phương pháp nhuộm Gram. Phương pháp nhuộm Gram được nêu tại phụ lục A.
- Quan sát hình thái vi khuẩn dưới kính hiển vi (6.2).
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra độ thuần khiết đạt yêu cầu khi trên tiêu bản nhuộm Gram chỉ quan sát thấy hình thái vi khuẩn Pasteurella multocida.
7.5 Kiểm tra độ an toàn
Chọn 1 trong 2 phương pháp sau:
7.5.1 Kiểm tra trên lợn
- Tiêm bắp hoặc tiêm dưới da cho ít nhất 03 lợn (5.1), mỗi con 02 liều vắc xin ghi trên nhãn.
- Theo dõi lợn trong 21 ngày.
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra an toàn đạt yêu cầu khi tất cả lợn sống khỏe và không có bất kỳ dấu hiệu phản ứng bất lợi nào.
7.5.2 Phương pháp thay thế
- Tiêm cho ít nhất 02 chuột lang (5.3), mỗi con 2 ml vắc xin và tiêm cho ít nhất 10 chuột nhắt trắng (5.4), mỗi con 0,5 ml vắc xin theo đường tiêm dưới da.
- Theo dõi chuột lang và chuột nhắt trắng ít nhất trong 14 ngày.
- Đánh giá kết quả: Vắc xin có kết quả kiểm tra an toàn đạt yêu cầu khi tất cả chuột lang và chuột nhắt trắng sống khỏe và không có bất kỳ dấu hiệu phản ứng bất lợi nào.
7.6 Kiểm tra hiệu lực
Chọn 1 trong 2 phương pháp sau:
7.6.1 Phương pháp công cường độc trên chuột nhắt trắng
7.6.1.1 Cách tiến hành
- Sử dụng ít nhất 60 chuột nhắt trắng (5.4), chia làm 02 nhóm:
+ Nhóm 1: Gồm ít nhắt 30 chuột nhắt trắng (5.4), mỗi con được tiêm dưới da một liều bằng 1/20 liều vắc xin ghi trên nhãn;
+ Nhóm 2: Gồm ít nhất 30 chuột nhắt trắng (5.4), đối chứng không tiêm vắc xin.
- Ba tuần sau tiêm, toàn bộ chuột nhắt trắng nhóm 1 và nhóm 2 được thử thách với vi khuẩn Pasteurelia muitocida type A (5.5) chủng cường độc tương ứng với các liều từ 103, 104, 105, 106, 107, 108 CFU/ml mỗi liều tiêm cho 5 chuột nhắt trắng, mỗi chuột nhắt trắng tiêm 0,1 ml vào phúc xoang.
- Theo dõi chuột trong 10 ngày.
- Liều LD50 của cả 2 nhóm chuột được tính toán tính theo công thức Reed - Muench:
Lg LD50 = LgA + Xlgf (7.1)

Trong đó:
X: Khoảng cách tỷ lệ.
A: Độ pha loãng vi khuẩn gây chết chuột nhắt trắng cận trên 50 %.
A': Tỷ lệ % chuột nhắt trắng chết cận trên 50%.
B': Tỷ lệ % chuột nhắt trắng chết cận dưới 50%.
f: Hệ số pha loãng vi khuẩn.
7.6.1.2 Đánh giá kết quả
Vắc xin có kết quả kiểm tra hiệu lực đạt yêu cầu khi LD50 của nhóm 1 lớn hơn nhóm 2 ít nhất 10 2.0.
7.6.2 Phương pháp huyết thanh học
7.6.2.1 Cách tiến hành
- Sử dụng ít nhất 08 lợn (5.1) hoặc 08 thỏ (5.2), chia làm 2 nhóm:
+ Nhóm 1: Gồm ít nhất 05 lợn hoặc 05 thỏ, mỗi con được tiêm bắp hoặc dưới da 1 liều vắc xin ghi trên nhãn;
+ Nhóm 2: Gồm ít nhất 03 lợn hoặc 03 thỏ, đối chứng không tiêm vắc xin.
- Sau khi tiêm vắc xin 21 ngày (hoặc gây miễn dịch theo hướng dẫn của nhà sản xuất), toàn bộ lợn hoặc thỏ ở nhóm 1 và nhóm 2 được lấy máu chắt huyết thanh để kiểm tra kháng thể bằng 1 trong 2 phương pháp sau:
+ Phản ứng ngưng kết chậm: Các bước kiểm tra hiệu giá kháng thể kháng Pasteurella multocida type A bằng phản ứng ngưng kết chậm được nêu tại Phụ lục B;
+ Hoặc phản ứng ELISA (áp dụng cho huyết thanh lợn), sử dụng kit ELISA (5.8) phát hiện kháng thể Pasteurella multocida type A.
CHÚ THÍCH: Hiện nay có nhiều bộ KIT ELISA phát hiện kháng thể Pasteurella multocida type A bán sẵn trên thị trường. Khi sử dụng phương pháp ELISA cần theo đúng hướng dẫn của nhà sản xuất. Ví dụ về phản ứng ELISA sử dụng KIT thương mại được nêu trong phụ lục C.
7.6.2.2 Đánh giá kết quả
Vắc xin có kết quả kiểm tra hiệu lực đạt yêu cầu khi:
- Phương pháp ngưng kết chậm:
+ Nhóm 1: Ít nhất 80 % mẫu huyết thanh cho kết quả hiệu giá kháng thể ≥ 4 log2;
+ Nhóm 2: 100 % mẫu huyết thanh có kết quả âm tính hoặc hiệu giá kháng thể < 3log2.
- Phương pháp ELISA:
+ Nhóm 1: Ít nhất 80 % mẫu huyết thanh đạt kết quả dương tính theo qui định của bộ Kít sử dụng;
+ Nhóm 2: 100 % mẫu huyết thanh có kết quả âm tính theo quy định của bộ Kit sử dụng.
8 Kết luận
Vắc xin đạt yêu cầu kiểm nghiệm khi đáp ứng được tất cả các yêu cầu về cảm quan, độ vô trùng, độ thuần khiết, độ vô hoạt, độ an toàn và hiệu lực như đã nêu lần lượt ở 7.1, 7.2, 7.3, 7.4, 7.5 và 7.6.
9 Báo cáo kết quả kiểm nghiệm
Báo cáo kiểm nghiệm phải nêu rõ:
- Mọi thông tin cần thiết về nhận biết đầy đủ về mẫu thử;
- Phương pháp lấy mẫu đã sử dụng, nếu biết;
- Phương pháp thử đã sử dụng, viện dẫn tiêu chuẩn này;
- Tất cả các điều kiện thao tác không quy định trong tiêu chuẩn này, hoặc được xem là tùy ý, cùng với mọi tình huống bất thường có thể ảnh hưởng đến kết quả;
- Kết quả kiểm nghiệm thu được.
Phụ lục A
(Quy định)
Phương pháp nhuộm Gram
A.1 Hóa chất
A.1.1 Dung dịch tím gentians, sản phẩm thương mại.
A.1.2 Dung dịch lugol, sản phẩm thương mại.
A.1.3 Dung dịch cồn 90 %.
A.1.4 Dung dịch fuchsin kiềm, sản phẩm thương mại.
A.2 Thiết bị và dụng cụ
A.2.1 Phiến kính sạch.
A.2.2 Que cấy vô trùng.
A.2.3 Đèn cồn
A.3 Chuẩn bị tiêu bản
Bước 1: Dùng pipet đơn kênh (6.5) nhỏ một giọt vắc xin lên phiến kính (A.2.1) rồi dùng que cấy (A.2.2) dàn đều, để khô trong phòng thí nghiệm.
Bước 2: Cố định tiêu bản bằng cách hơ nhanh trên ngọn lửa đèn cồn (A.2.3) từ 2 lần đến 3 lần.
A.4 Cách tiến hành
Bước 1: Dùng pipet đơn kênh (6.5) nhỏ một lượng dung dịch tím gentians (A.1.1) lên tiêu bản sao cho dung dịch phủ đều chỗ phết vi khuẩn, để từ 1 phút đến 2 phút sau đó rửa nhanh bằng nước và làm khô tiêu bản.
Bước 2: Dùng pipet đơn kênh (6.5) nhỏ một lượng dung dịch lugol (A.1.2) lên tiêu bản sao cho dung dịch phủ đều chỗ phết vi khuẩn, để 1 phút, sau đó rửa nhanh bằng nước và làm khô tiêu bản.
Bước 3: Dùng pipet đơn kênh (6.5) nhỏ một lượng dung dịch cồn (A.1.3) lên tiêu bản sao cho dung dịch phủ đều chỗ phết vi khuẩn, rửa nhanh bằng nước cất và làm khô tiêu bản.
Bước 4: Dùng pipet đơn kênh (6.5) nhỏ một lượng dung dịch fuchsin sao cho dung dịch phủ đều chỗ phết vi khuẩn, để 1 phút, sau đó rửa nhanh bằng nước và làm khô tiêu bản.
Bước 5: Xem tiêu bản dưới kính hiển vi (6.2) ở vật kính dầu 100 X.
A.5 Đọc kết quả
Vi khuẩn Pasteurella multocida type A bắt màu hồng (Gram âm), hình cầu, hình cầu trực khuẩn, hình trực khuẩn ngắn), thường đứng riêng lẻ hay thành cặp.
Phụ lục B
(Tham khảo)
Kiểm tra hiệu giá kháng thể kháng Pasteurella multocida type A bằng phản ứng ngưng kết chậm
B.1 Vật liệu và thuốc thử
B.1.1 Môi trường thạch máu cơ bản (BAB), sản phẩm thương mại.
B.1.2 Môi trường canh thang não tim (BHI), sản phẩm thương mại.
B.1.3 Máu thỏ vô trùng.
B.1.4 Dung dịch acid chlohydric (HCl) 1 N.
B.1.5 Dung dịch formaldehyde (HCHO) 37 %.
B.1.6 Dung dịch PBS 1 X, pH = 7,2 ± 0,2
B.2 Thiết bị, dụng cụ
B.2.1 Máy ly tâm có thể quay với tốc độ 12000 vòng/phút.
B.2.2 Nồi hấp ướt có thể duy trì ở nhiệt độ 121 °C trong thời gian 15 phút.
B.2.3 Bể ủ nhiệt, duy trì nhiệt độ 56 °C.
B.2.4 Đĩa lồng Ø 20, ống nghiệm thủy tinh 12 x 120 mm vô trùng.
B.2.5 Pipet đa kênh, thể tích từ 5 μl đến 50 μl, từ 50 μl đến 200 μl.
B.2.6 Máy ly tâm, có thể quay với tốc độ từ 10000 vòng/phút đến 12000 vòng/phút.
B.2.7 Nồi ủ nhiệt có thể duy trì ở các nhiệt độ 100 °C, 110 °C, 121 °C trong thời gian 10 phút, 15 phút, 20 phút.
B.2.8 Bình tam giác 100 ml, 200 ml vô trùng.
B.2.9 Đĩa nhựa 96 giếng đáy chữ U.
B.2.10 Cân phân tích có dải đo từ 0 g đến 30 g.
B.3 Chuẩn bị
B.3.1 Môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ
Môi trường thạch máu cơ bản (B.1.1) được pha theo hướng dẫn của nhà sản xuất, chỉnh pH = 7,4 ± 0 2 ở 25 °C. Sau đó đem hấp tiệt trùng ở nồi hấp (B.2.2) ở nhiệt độ 121 °C trong 15 phút, để nguội đến 45 °C rồi bổ sung từ 5 % đến 8 % máu thỏ (B.1.3) và đổ ra đĩa lồng vô trùng (B.2.4).
Ví dụ: Dùng môi trường thạch máu cơ bản của hãng Merck (Cat. No.1.1886.0500).
B.3.2 Ống môi trường BHI
Môi trường BHI (B.1.2) được pha theo hướng dẫn của nhà sản xuất, chỉnh pH = 7,4 ± 0,2 ở 25 °C, lắc đều và chia ra các ống nghiệm thủy tinh vô trùng (B.2.4) (4 ml/ ống), sau đó đem hấp tiệt trùng ở nồi hấp (B.2.2) nhiệt độ 121 °C trong 15 phút.
Ví dụ: Dùng môi trường canh thang não tim của hãng Merck (Cat. No.1.10493.0500).
B.3.3 Chế kháng nguyên thân (Kháng nguyên O - Kháng nguyên được xử lý bằng dung dịch acid chlohydric1N)
- Dùng pipet đơn kênh (6.5) hút 0,01 ml canh khuẩn chứa vi khuẩn P.multocida type A cường độc (5.5) vào môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ (B.3.1), ủ ở tủ ấm (6.1) trong 24 giờ.
- Dùng que cấy lấy 1 đến 2 khuẩn lạc cấy vào ống môi trường BHI (B.3.2), rồi ủ ở tủ ấm (6.1) trong 24 giờ. Sau đó dùng pipet đơn kênh (6.6) hút 0,1 ml canh trùng 24 giờ trên láng lên 2 đĩa môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ bằng cách dùng que cấy vô trùng dàn đều trên mặt thạch (B.3.1), tiếp tục ủ ở tủ ấm (6.1) trong 24 giờ.
- Dùng pipet đơn kênh (6.5) hút 5 ml dung dịch PBS (B.1.6) để rửa bề mặt hai đĩa thạch, hút huyễn dịch vi khuẩn thu được vào ống nghiệm thủy tinh vô trùng (B.2.4).
- Dùng pipet đơn kênh (6.6) hút 0,02 ml dung dịch formaldehyde (B.1.5) nhỏ vào huyễn dịch vi khuẩn thu được ở trên rồi ủ ở tủ ấm (6.1) trong 24 giờ, sau đó đem kiểm tra vô trùng huyễn dịch vi khuẩn bằng cách ria trên môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ (B.3.1).
- Huyễn dịch vi khuẩn đạt chỉ tiêu vô trùng (không có vi khuẩn mọc trên đĩa thạch) sẽ được ly tâm bằng máy ly tâm (B.2.1) với tốc độ 12 000 vòng/phút trong 15 phút ở nhiệt độ 4 °C, loại bỏ phần dung dịch nổi bên trên. Sau đó thêm 20 ml dung dịch HCl 1N (B.1.4), lắc đều rồi ủ ở tủ ấm (6.1) trong 24 giờ.
- Huyễn dịch vi khuẩn sau khi ủ ở tủ ấm tiếp tục được ly tâm bằng máy ly tâm (B.2.1) với tốc độ 12 000 vòng/phút trong 15 phút ở nhiệt độ 4 °C, loại bỏ phần dung dịch nổi bên trên, thêm dung dịch PBS (B.1.6) có bổ sung 0,3 % dung dịch formaldehyde (B.1.5). Ly tâm lặp lại 2 lần, loại bỏ phần dung dịch nổi bên trên sau lần ly tâm cuối, cặn thu được sẽ được hoàn nguyên bằng 5 ml dung dịch PBS (B.1.6) để thu hoạch kháng nguyên thân.
- Kháng nguyên đạt yêu cầu khi không có hiện tượng ngưng kết, kháng nguyên lắng tròn nhỏ đáy giếng.
B.3.4 Huyết thanh cần kiểm tra
Lấy máu động vật (7.6.2.1), chắt lấy huyết thanh. Sau đó khử bổ thể bằng cách ủ ở bể ủ nhiệt (B.2.3) trong 30 phút ở nhiệt độ 56 °C.
B.3.5 Chuẩn bị canh trùng 2 x 109 CFU/ml (Canh trùng được bảo quản 2- 8°C)
- Dùng pipet đơn kênh (6.5) hút 0,01 ml canh khuẩn chứa vi khuẩn P.multocida type A cường độc (5.4) vào môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ (B.3.1), ủ ở tủ ấm (6.1) trong 24 giờ.
- Dùng que cấy lấy 1 đến 2 khuẩn lạc cấy vào ống môi trường BHI (B.3.2), rồi ủ ở tủ ấm (6.1) trong 24 giờ. Sau đó dùng pipet đơn kênh (6.5) hút 0,1 ml canh trùng 24 giờ trên láng lên 2 đĩa môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ bằng cách dùng que cấy vô trùng dàn đều trên mặt thạch (B.3.1), tiếp tục ủ ở tủ ấm (6.1) trong 24 giờ.
- Dùng pipet đơn kênh (6.5) hút 5 ml dung dịch PBS (B.1.6) để rửa bề mặt hai đĩa thạch, hút huyễn dịch vi khuẩn thu được vào ống nghiệm thủy tinh vô trùng (B.2.4).
- Từ canh trùng ban đầu (canh trùng này bắt buộc mật độ vi khuẩn phải lớn hơn 2 x 109 CFU/ml) pha thành canh trùng có mật độ 2 x 109 CFU/ml theo các bước sau:
+ Dùng pipet đơn kênh (6.5) hút nước muối sinh lý vô trùng (5.4) vào 7 ống nghiệm thủy tinh vô trùng (B.2.4), mỗi ống 9 ml và đánh số từ 1 đến 7;
+ Dùng pipet đơn kênh (6.5) hút 1 ml canh trùng ban đầu vào ống thứ 1, trộn đều bằng cách lắc đều rồi chuyển 1 ml huyễn dịch từ ống thứ 1 sang ống thứ 2, lặp lại như vậy đến ống thứ 7;
+ Dùng pipet đơn kênh (6.5) hút 0,1 ml huyễn dịch ở 2 nồng độ pha loãng liền nhau, nhỏ lên môi trường thạch máu bổ sung từ 5 % đến 8 % máu thỏ (B.3.1) (mỗi nồng độ 2 đĩa, mỗi đĩa 0,1 ml), rồi dùng que trang dàn đều mẫu và ủ ở tủ ấm (6.1) trong 18 giờ đến 20 giờ;
+ Đếm số khuẩn lạc mọc trên mỗi đĩa và tính mật độ vi khuẩn theo công thức sau:
|
| (B.1) |
Trong đó:
N: tổng số vi khuẩn trong 1 ml canh trùng.
C: số khuẩn lạc đếm được ở các đĩa có nồng độ liền nhau.
V: thể tích (ml) cấy ở mỗi đĩa.
n1: số đĩa của độ pha loãng ban đầu (2 đĩa).
n2: số đĩa của độ pha loãng tiếp theo (2 đĩa).
d: độ pha loãng ban đầu.
- Pha canh trùng 2 x 109 CFU/ml như sau:
Lấy số vi khuẩn đã tính được ở trên (N - theo công thức B.1) chia cho số vi khuẩn cần dùng (2 x 109 CFU/mI) ta được một thông số (X). Sau đó ta lấy 1ml canh trùng nguyên ban đầu cộng với số ml (Y) nước muối sinh lý. Số ml của Y = X - 1 (điều kiện X ≥ 1), (B.2).
Ví dụ: Có canh trùng 3 x 109 CFU/ml muốn pha thành canh trùng 2 x 109 CFU/ml thì làm như sau:
Lấy 3 x 109 CFU/ml chia cho 2 x 109 CFU/ml được thông số là 1,5. Để được canh trùng 2 x 109 CFU/ml ta sẽ lấy 1 ml canh trùng 3 x 109 CFU/ml và thêm vào 0,5 ml nước muối sinh lý. Hỗn dịch cuối cùng là canh trùng cần pha.
B.3.6 Chế huyết thanh tối miễn dịch
- Ngày thứ 1: tiêm 2 ml canh trùng (B.3.5) cho thỏ (5.2) theo đường dưới da.
- Ngày thứ 7: tiêm tiếp 0,2 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 11: tiêm tiếp 0,5 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 15: tiêm tiếp 1 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 19: tiêm tiếp 1,5 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 23: tiêm tiếp 2 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 27: tiêm tiếp 2,5 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 31: tiêm tiếp 3 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 35: tiêm tiếp 3,5 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Ngày thứ 39: tiêm tiếp 4 ml canh trùng (B.3.5) cho thỏ theo đường tĩnh mạch tai.
- Một tuần sau mũi tiêm cuối cùng tiến hành lấy máu thỏ, chắt huyết thanh. Đó chính là huyết thanh tối miễn dịch.
B.4 Cách tiến hành
Quy trình cho phản ứng ngưng kết chậm với kháng nguyên thân (B.3.3) thực hiện trên đĩa nhựa 96 giếng đáy chữ U (B.2.9).
- Bố trí thí nghiệm.
+ Giếng thí nghiệm: A1 đến H8;
+ Giếng đối chứng âm: A9 đến H10;
+ Giếng đối chứng dương: A11 đến H12.
Bảng B.1 - Sơ đồ bố trí mẫu cho phản ứng ngưng kết chậm
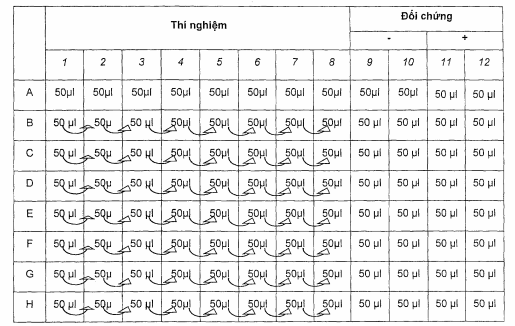
- Thực hiện thí nghiệm theo sơ đồ phản ứng ngưng kết chậm như trên.
- Đối với các giếng thí nghiệm:
+ Dùng pipet đa kênh (B.2.5) hút 50 μl dung dịch PBS vào mỗi giếng thí nghiệm (A1 đến H8);
+ Dùng pipet đơn kênh (6.5) hút 50 μl huyết thanh (B.3.4) cho vào giếng đầu tiên và pha loãng theo cơ số 2 bằng cách trộn đều rồi chuyển 50 μl sang giếng thứ 2, cứ như vậy đến giếng số 8 trộn đều rồi hút bỏ đi 50 μl;
+ Dùng pipet đa kênh (B.2.5) hút 50 μl kháng nguyên thân (B.3.3) cho vào các giếng (A1 đến H8);
- Đối với các giếng đối chứng:
+ Đối chứng âm (A9 đến H10): Dùng pipet đơn kênh (6.5) hút 50 μl dung dịch PBS (B.1.6) và 50 μl kháng nguyên thân (B.3.3);
+ Đối chứng dương (A11 đến H12): Dùng pipet đơn kênh (6.5) hút 50 μl huyết thanh tối miễn dịch (B.3.6) và 50 μl kháng nguyên thân (B.3.3);
- Lắc nhẹ rồi đậy nắp, để ở tủ ấm (6.1) qua đêm.
- Đọc kết quả:
+ Phản ứng âm tính: Kháng nguyên lắng tròn đáy giếng;
+ Phản ứng dương tính: Xảy ra phản ứng ngưng kết, kháng nguyên ngưng kết thành cụm lấm tấm đều ở đáy giếng;
+ Đọc hiệu giá ngưng kết: Hiệu giá ngưng kết được đánh giá ở độ pha loãng cao nhất còn có phản ứng ngưng kết xảy ra.
Phụ lục C
(Tham khảo)
Ví dụ phản ứng ELISA kiểm tra kháng thể Pasteurella multocida type A
C.1 Vật liệu thử
C.1.1 Huyết thanh cần kiểm tra.
C.1.2 Nước cất 2 lần.
C.1.3 Bộ Kit ELISA.
C.2 Thiết bị và dụng cụ
C.2.1 Tủ ấm có thể duy trì nhiệt độ 37 °C ± 0,5 °C.
C.2.2 Pipet đơn kênh, thể tích từ 50 μl đến 200 μl, từ 100 μl đến 1000 μl.
C.2.3 Pipet đa kênh, thể tích từ 5 μl đến 50 μl, từ 50 μl đến 200 μl.
C.2.4 Máy lắc trộn (vortex mixer) có tốc độ lắc từ 50 vòng/phút đến 2400 vòng/phút.
C.2.5 Máy đọc ELISA, có bước sóng 405 nm đến 650 nm.
C.3 Cách tiến hành
C.3.1 Đặt lần lượt 2 giếng đối chứng dương, đối chứng âm, mẫu kiểm tra và giếng blank trên đĩa phủ trước kháng nguyên theo thứ tự định sẵn.
C.3.2 Nhỏ 50 μl đối chứng âm và 50 μl đối chứng dương vào các giếng đã định sẵn. Để trống 1 giếng làm giếng blank.
C.3.3 Nhỏ 50 μl mẫu đã được pha loãng thích hợp (độ pha loãng 1:5, ví dụ: 10 μl mẫu pha với 40 μl Samμle Diluent Buffer) vào các giếng có mẫu thử nghiệm. Gõ nhẹ vào đĩa (hoặc sử dụng máy lắc) để trộn.
C.3.4 Dán và ủ đĩa ở 37 °C trong 30 phút.
C.3.5 Tháo miếng dán và đổ bỏ dung dịch trong đĩa. Rửa đĩa 5 lần với dung dịch rửa 1X. Làm đầy vào từng giếng 300 μl bằng cách sử dụng pipet đa kênh (C.2.3) hoặc máy rửa tự động (khuyến cáo thời gian ngâm khoảng 1 đến 2 phút). Việc loại bỏ hoàn toàn chất lỏng ở mỗi bước là điều cần thiết để đạt được hiệu quả tốt. Sau lần rửa cuối cùng, loại bỏ phần còn lại bằng cách hút hoặc gạn. Lật ngược đĩa và thấm vào khăn giấy sạch thấm nước.
C.3.6 Nhỏ 50 μl dung dịch HRP conjugate reagent vào mỗi giếng (trừ giếng đối chứng).
C.3.7 Dán đĩa và ủ ở 37 °C trong 30 phút.
C.3.8 Tháo miếng dán, loại bỏ dung dịch và lặp lại bước (C.3.5).
C.3.9 Nhỏ 50 μl cơ chất A và 50 μl cơ chất B vào mỗi giếng. Gõ nhẹ đĩa để trộn đều. Dán đĩa và ủ ở 37 °C trong 10 phút. Tránh để đĩa tiếp xúc với ánh sáng.
C.3.10 Nhỏ 50 μl dung dịch dừng phản ứng vào mỗi giếng, nên trộn đều và nhanh để bất hoạt hoàn toàn hoạt tính của enzym.
C.3.11 Đảm bảo không có dấu vân tay hoặc nước dưới đáy đĩa. Chất lỏng trong giếng không có bọt. Đặt đĩa vào máy đọc ELISA (C.2.5) và đọc ở bước sóng 450 nm để thu được các giá trị mật độ quang học (Optical density - OD) của các mẫu trong đĩa phản ứng.
C.4 Công thức tính kết quả
| - Đối chứng dương trung bình (PCx) = |
| (C.1) |
| - Đối chứng âm trung binh (NCx) = |
| (C.2) |
| - OD mẫu trung bình (ODtb) = |
| (C.3) |
Giá trị CUT OFF = Đối chứng âm (C.1) + 0,15.
C.5 Điều kiện kết quả
PCx (C.2) ≥ 1,0.
NCx (C.1) ≤ 0,10.
Nếu PCx ≥ 1,0, NCx ≤ 0,10, kết quả hợp lệ, nếu ngược lại thì kết quả không hợp lệ.
C.6 Diễn giải kết quả
Nếu OD mẫu (C.3) < CUT OFF, mẫu kiểm tra âm tính.
Nếu OD mẫu (C.3) ≥ CUT OFF, mẫu kiểm tra dương tính.
Thư mục tài liệu tham khảo
[1] ASEAN, (2018). Asean Standard Requirements for Swine Pasteurella multocida, Inactivated, p64-65.
[2] Trung tâm Kiểm nghiệm thuốc thú y Trung ương I, (2010). 12 VT - 10/KN1 - Quy trình kiểm nghiệm vắc xin Pasteurella multocida type A.
[3] Code of Federal Regualtions, (2021). 9 CFR 113.33: Mouse safety test, p691 ; 9 CFR 113.38: Guinea pig safety tests, p694.
[4] Hồ sơ vắc xin Biofors ARPM, p74-86.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 8685-43:2023 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 8685-43:2023 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 8685-43:2023 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 8685-43:2023 DOC (Bản Word)