- Tổng quan
- Nội dung
- VB gốc
- Tiếng Anh
- Hiệu lực
- VB liên quan
- Lược đồ
-
Nội dung hợp nhất
Tính năng này chỉ có tại LuatVietnam.vn. Nội dung hợp nhất tổng hợp lại tất cả các quy định còn hiệu lực của văn bản gốc và các văn bản sửa đổi, bổ sung, đính chính... trên một trang. Việc hợp nhất văn bản gốc và những văn bản, Thông tư, Nghị định hướng dẫn khác không làm thay đổi thứ tự điều khoản, nội dung.
Khách hàng chỉ cần xem Nội dung hợp nhất là có thể nắm bắt toàn bộ quy định hiện hành đang áp dụng, cho dù văn bản gốc đã qua nhiều lần chỉnh sửa, bổ sung.
- Tải về
Quyết định 5772/QĐ-BYT 2021 Biểu mẫu và quy trình cấp “Hộ chiếu vắc xin”
| Cơ quan ban hành: | Bộ Y tế |
Số công báo:
Số công báo là mã số ấn phẩm được đăng chính thức trên ấn phẩm thông tin của Nhà nước. Mã số này do Chính phủ thống nhất quản lý.
|
Đang cập nhật |
| Số hiệu: | 5772/QĐ-BYT | Ngày đăng công báo: | Đang cập nhật |
| Loại văn bản: | Quyết định | Người ký: | Trần Văn Thuấn |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
20/12/2021 |
Ngày hết hiệu lực:
Ngày hết hiệu lực là ngày, tháng, năm văn bản chính thức không còn hiệu lực (áp dụng).
|
Đang cập nhật |
|
Áp dụng:
Ngày áp dụng là ngày, tháng, năm văn bản chính thức có hiệu lực (áp dụng).
|
Đã biết
|
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
| Lĩnh vực: | Y tế-Sức khỏe COVID-19 |
TÓM TẮT QUYẾT ĐỊNH 5772/QĐ-BYT
Cụ thể, quy trình cấp "Hộ chiếu vắc xin" cho người dân gồm 03 bước: Các cơ sở tiêm chủng rà soát, xác minh, xác thực thông tin người dân tiêm chủng vắc xin COVID-19 theo quy định pháp luật; Các cơ sở tiêm chủng thực hiện ký số dữ liệu tiêm chủng vắc xin COVID-19 trên Nền tảng Quản lý tiêm chủng COVID-19; Cục Y tế dự phòng - Bộ Y tế thực hiện ký số giấy xác nhận tiêm chủng vắc xin phòng COVID-19 tập trung.
Bên cạnh đó, "Hộ chiếu vắc xin" sẽ hiển thị các trường thông tin: Họ và tên; Ngày tháng năm sinh; Quốc tịch; Bệnh dịch mà chứng nhận nhắm tới; Số mũi tiêm đã nhận; Ngày tiêm; Liều số; Vắc xin; Sản phẩm vắc xin; Nhà cung cấp hoặc sản xuất vắc xin; Mã số của chứng nhận. Các thông tin trên sẽ được ký số, mã hoá và được đóng gói dưới dạng mã QR định dạng 2D. Mã QR hết hạn sau 12 tháng kể từ ngày khởi tạo.
Ngoài ra, Bộ Y tế còn hướng dẫn việc Chuẩn hóa dữ liệu tiêm chủng vắc xin COVID-19; Quy trình kỹ thuật tạo mã QR; Danh mục các bảng mã quốc tế về loại Vắc xin; Tên nhà sản xuất/thương hiệu...
Quyết định này có hiệu lực kể từ ngày ký.
Xem chi tiết Quyết định 5772/QĐ-BYT có hiệu lực kể từ ngày 20/12/2021
Tải Quyết định 5772/QĐ-BYT
| BỘ Y TẾ ______ Số: 5772/QĐ-BYT | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập - Tự do - Hạnh phúc _____________________ Hà Nội, ngày 20 tháng 12 năm 2021 |
QUYẾT ĐỊNH
Ban hành Biểu mẫu và quy trình cấp “Hộ chiếu vắc xin”
_______
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Luật Phòng, chống bệnh truyền nhiễm năm 2007;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ Quy định Chức năng, nhiệm vụ quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Theo đề nghị của Cục trưởng Cục Công nghệ thông tin,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này Biểu mẫu và quy trình cấp “Hộ chiếu vắc xin”.
Điều 2. Biểu mẫu và quy trình cấp “Hộ chiếu vắc xin” ban hành theo Quyết định này được áp dụng thống nhất tại tất cả các cơ sở tiêm chủng trên cả nước.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký, ban hành.
Điều 4. Các Ông, Bà: Cục trưởng Cục Công nghệ thông tin, Cục trưởng Cục Y tế dự phòng, Chánh Văn phòng Bộ, Chánh Thanh tra Bộ, Vụ trưởng, Cục trưởng, Tổng Cục trưởng các Vụ, Cục, Tổng cục thuộc Bộ Y tế; Thủ trưởng các đơn vị trực thuộc Bộ Y tế; Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương; Thủ trưởng y tế các ngành và các đơn vị có liên quan chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: - Như điều 4; - PTTg. Vũ Đức Đam (để báo cáo); - Bộ trưởng Nguyễn Thanh Long (để báo cáo); - Các bộ: Ngoại giao, Công an, Thông tin và Truyền thông (để phối hợp); - Các Thứ trưởng Bộ Y tế; - Lưu: VT, CNTT. | KT. BỘ TRƯỞNG THỨ TRƯỞNG
Trần Văn Thuấn |
| BỘ Y TẾ _______
| CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập - Tự do - Hạnh phúc ________________________
|
BIỂU MẪU VÀ QUY TRÌNH CẤP “HỘ CHIẾU VẮC XIN”
(Ban hành kèm theo Quyết định số 5772/QĐ-BYT ngày 20 tháng 12 năm 2021 của Bộ Y tế)
1. Biểu mẫu “Hộ chiếu vắc xin”
1.1. Các trường thông tin hiển thị:
1. Họ và tên;
2. Ngày tháng năm sinh;
3. Quốc tịch;
4. Bệnh dịch mà chứng nhận nhắm tới;
5. Số mũi tiêm đã nhận;
6. Ngày tiêm;
7. Liều số;
8. Vắc xin;
9. Sản phẩm vắc xin;
10. Nhà cung cấp hoặc sản xuất vắc xin;
11. Mã số của chứng nhận.
Các thông tin trên sẽ được ký số, mã hoá và được đóng gói dưới dạng mã QR định dạng 2D. Yêu cầu cụ thể sẽ được mô tả tại Mục 4.
1.2. Các thông tin trên bao gồm họ và tên và ngày sinh kết hợp với giấy tờ định danh khác như CMND, CCCD hay hộ chiếu để giúp định danh người sở hữu.
1.3. Các thông tin về bệnh dịch mà chứng nhận nhắm tới, vắc xin, loại vắc xin và nhà cung cấp hoặc sản xuất sẽ được hiển thị tương ứng với tài liệu “COVID-19 vaccine tracker and landscape” của WHO được cập nhật trên Cổng thông tin điện tử của WHO và “Value Sets for EU Digital COVID Certificates” do Liên minh Châu Âu (EU) ban hành.
1.4. Ngày tiêm và số mũi tiêm đã nhận để xác định thông tin tiêm chủng.
1.5. Mã QR hết hạn sau 12 tháng kể từ ngày khởi tạo.

Hình 1: Minh họa Chứng nhận điện tử đã tiêm vắc xin COVID-19 của Việt Nam trên thiết bị di động
2. Quy trình cấp “Hộ chiếu vắc xin”
2.1. Sơ đồ quy trình
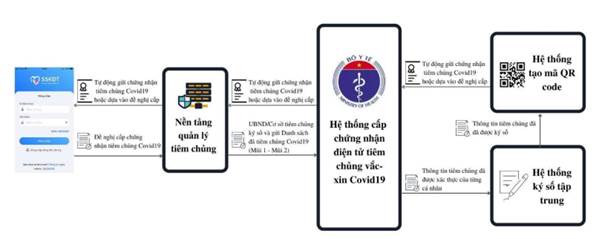
2.2. Mô tả quy trình
- Bước 1: Các cơ sở tiêm chủng rà soát, xác minh, xác thực thông tin người dân tiêm chủng vắc xin COVID-19 theo hướng dẫn tại Công văn số 8938/BYT-DP ngày 21/10/2021 của Bộ Y tế về việc hướng dẫn quy trình xác minh thông tin và tiêm chủng vắc xin COVID-19 và Công văn số 9438/BYT-CNTT ngày 5/11/2021 của Bộ Y tế về việc hướng dẫn Quy trình xác thực thông tin người dân trên Nền tảng Quản lý tiêm chủng COVID-19.
- Bước 2: Các cơ sở tiêm chủng thực hiện ký số dữ liệu tiêm chủng vắc xin COVID-19 trên Nền tảng Quản lý tiêm chủng COVID-19. Nền tảng Quản lý tiêm chủng COVID-19 kết nối, chia sẻ dữ liệu tiêm chủng với Hệ thống Quản lý cấp chứng nhận tiêm chủng vắc xin COVID-19 đáp ứng theo các quy định về kết nối dữ liệu y tế do Bộ Y tế ban hành.
Dữ liệu tiêm chủng vắc xin COVID-19 trên Nền tảng Quản lý tiêm chủng COVID-19 cần đáp ứng quy định tại Mục 3 và Mục 4.
- Bước 3: Cục Y tế dự phòng - Bộ Y tế thực hiện ký số giấy xác nhận tiêm chủng vắc xin phòng COVID-19 tập trung. Chứng nhận được cấp sử dụng định dạng mã QR theo tiêu chuẩn của EU quy định tại Mục 5.
Các ứng dụng phòng chống dịch quốc gia và các ứng dụng tiện ích khác (nếu được sự đồng ý của cá nhân người sử dụng) tiếp nhận và lưu giữ xác nhận tiêm chủng vắc xin phòng COVID-19 dạng mã QR theo hướng dẫn trao đổi dữ liệu y tế do Bộ Y tế ban hành.
3. Chuẩn hóa dữ liệu tiêm chủng vắc xin COVID-19
| TT | Thông tin | Ví dụ |
| Thông tin cá nhân | ||
| 1 | Họ và tên | Nguyễn Văn A |
| 2 | Ngày sinh | 20/10/1999 |
| 3 | Số điện thoại | 0912345678 |
| 4 | Số Chứng minh thư nhân dân/Căn cước công dân | 001123456789 |
| 5 | Số hộ chiếu | Nếu có |
| 6 | Quốc tịch | Việt Nam |
| Mũi tiêm số 1 | ||
| 7 | Vắc xin* | EU/1/20/1528 |
| 8 | Loại vắc xin* | 1119305005 |
| 9 | Nhà cung cấp/sản xuất* | ORG-100030215 |
| 10 | Mũi tiêm số | 1 |
| 11 | Ngày tiêm | 20/6/2021 |
| 12 | Tên đơn vị tiêm chủng |
|
| 13 | Tên cơ sở quản lý |
|
| Mũi tiêm số 2 | ||
| 14 | Vắc xin* | EU/1/20/1528 |
| 15 | Loại vắc xin* | 1119305005 |
| 16 | Nhà cung cấp/sản xuất* | ORG-100030215 |
| 17 | Mũi tiêm số | 2 |
| 18 | Ngày tiêm | 20/7/2021 |
| 19 | Tên đơn vị tiêm chủng |
|
| 20 | Tên cơ sở quản lý |
|
| 21 | Tổng số liều đã tiêm | 2 |
| Chữ ký số của cơ sở tiêm chủng | ||
*Vắc xin, loại vắc xin và nhà cung cấp hoặc sản xuất điền theo thông tin tại Mục 4. Danh mục các bảng mã quốc tế
4. Danh mục các bảng mã quốc tế
4.1. Bệnh dịch
| Code | Tên bệnh dịch |
| 840539006 | COVID-19 |
4.2. Loại Vắc xin
| Code | Tên loại vắc xin |
| 1119305005 | Vắc xin antigen SARS-CoV-2 |
| 1119349007 | Vắc xin mRNA SARS-CoV-2 |
| J07BX03 | Vắc xin Covid-19 khác |
4.3. Sản phẩm Vắc xin
| Code | Tên sản phẩm vắc xin/ tên vắc xin |
| EU/1/20/1528 | Comirnaty/ Pfizer |
| EU/1/20/1507 | Spikevax (previously COVID-19 Vaccine Moderna)/Moderna |
| EU/1/21/1529 | Vaxzevria/ Astrazeneca |
| EU/1/20/1525 | COVID-19 Vaccine Janssen/ Janssen |
| Hayat-Vax | Hayat-Vax/ Hayat-Vax |
| BBIBP-CorV | BBIBP-CorV/ Vero-Cell |
| Sputnik-V | Sputnik-V/ Sputnik |
| Abdala | Abdala/ Abdala |
4.4. Tên nhà sản xuất/thương hiệu
| Code | Tên nhà sản xuất/thương hiệu |
| ORG-100030215 | BioNTech Manufacturing GmbH |
| ORG-100031184 | Rovi Pharma Industrial Services, S.A, Spain Recipharm Monts, France |
| ORG-100001699 | AstraZeneca, AB |
| ORG-100001417 | Janssen-Cilag International NV |
| ORG-100023050 | Gulf Pharmaceutical Industries |
| ORG-100020693 | Beijing Institute of Biological Products Co., Ltd |
| CIGB | Cuba CIGB (Center for Genetic Engineering and Biotechnology) |
5. Quy trình kỹ thuật tạo mã QR
5.1. Quy trình khởi tạo mã QR
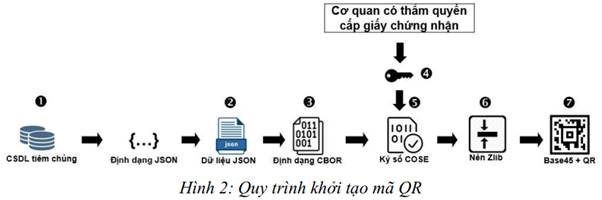
5.2. Yêu cầu kỹ thuật với các bước trong quy trình khởi tạo mã QR
| STT | Nội dung | Yêu cầu kỹ thuật |
| 1 | Định dạng dữ liệu tại phần II | Định dạng Json (theo RFC 7159) |
| 2 | Chuyển dữ liệu JSON thành CBOR | Sử dụng thuật toán chuyển đổi định dạng JSON thành định dạng CBOR (theo RFC 8392) |
| 3 | Ký số | Sử dụng thuật toán ký số RSA (theo RFC 8230) 2048 bits cùng thuật toán băm SHA-256 (theo ISO/IEC 101183:2004) |
| 4 | Mã hoá và nén dữ liệu CBOR | Sử dụng giao thức COSE (theo RFC 8152) |
| 5 | Nén dữ liệu đã được COSE | Sử dụng thuật toán Zlib (theo RFC 1950) |
| 6 | Thay đổi cấu trúc dữ liệu | Sử dụng thuật toán BASE45 |
| 7 | Tạo hình ảnh 2D | Sử dụng thuật toán ASCII (theo phần 3 tài liệu ICAO 9303) và hình thành mã vạch QR (theo ISO/IEC 18004:2015) |
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Quyết định 5772/QĐ-BYT PDF (Bản có dấu đỏ)
Quyết định 5772/QĐ-BYT PDF (Bản có dấu đỏ) Quyết định 5772/QĐ-BYT DOC (Bản Word)
Quyết định 5772/QĐ-BYT DOC (Bản Word)