- Tổng quan
- Nội dung
- VB gốc
- Tiếng Anh
- Hiệu lực
- VB liên quan
- Lược đồ
-
Nội dung hợp nhất
Tính năng này chỉ có tại LuatVietnam.vn. Nội dung hợp nhất tổng hợp lại tất cả các quy định còn hiệu lực của văn bản gốc và các văn bản sửa đổi, bổ sung, đính chính... trên một trang. Việc hợp nhất văn bản gốc và những văn bản, Thông tư, Nghị định hướng dẫn khác không làm thay đổi thứ tự điều khoản, nội dung.
Khách hàng chỉ cần xem Nội dung hợp nhất là có thể nắm bắt toàn bộ quy định hiện hành đang áp dụng, cho dù văn bản gốc đã qua nhiều lần chỉnh sửa, bổ sung.
- Tải về
Quyết định 1271/QĐ-BYT của Bộ Y tế về việc ban hành "Hướng dẫn giám sát nhiễm trùng đường hô hấp cấp tính nặng (SARI)"
| Cơ quan ban hành: | Bộ Y tế |
Số công báo:
Số công báo là mã số ấn phẩm được đăng chính thức trên ấn phẩm thông tin của Nhà nước. Mã số này do Chính phủ thống nhất quản lý.
|
Đang cập nhật |
| Số hiệu: | 1271/QĐ-BYT | Ngày đăng công báo: | Đang cập nhật |
| Loại văn bản: | Quyết định | Người ký: | Nguyễn Thanh Long |
| Trích yếu: | Về việc ban hành "Hướng dẫn giám sát nhiễm trùng đường hô hấp cấp tính nặng (SARI)" | ||
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
03/04/2017 |
Ngày hết hiệu lực:
Ngày hết hiệu lực là ngày, tháng, năm văn bản chính thức không còn hiệu lực (áp dụng).
|
Đang cập nhật |
|
Áp dụng:
Ngày áp dụng là ngày, tháng, năm văn bản chính thức có hiệu lực (áp dụng).
|
Đã biết
|
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
| Lĩnh vực: | Y tế-Sức khỏe | ||
TÓM TẮT QUYẾT ĐỊNH 1271/QĐ-BYT
Nội dung tóm tắt đang được cập nhật, Quý khách vui lòng quay lại sau!
Tải Quyết định 1271/QĐ-BYT
| BỘ Y TẾ Số: 1271/QĐ-BYT | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Hà Nội, ngày 03 tháng 4 năm 2017 |
QUYẾT ĐỊNH
Về việc ban hành “Hướng dẫn giám sát nhiễm trùng đường hô hấp cấp tính nặng (SARI)”
____________
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Nghị định số 63/2012/NĐ-CP ngày 31 tháng 8 năm 2012 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức Bộ Y tế;
Theo đề nghị của Cục trưởng Cục Y tế dự phòng, Bộ Y tế,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này “Hướng dẫn giám sát nhiễm trùng đường hô hấp cấp tính nặng (SARI)”.
Điều 2. “Hướng dẫn giám sát nhiễm trùng đường hô hấp cấp tính nặng (SARI)” là tài liệu hướng dẫn được áp dụng trong các cơ sở y tế dự phòng và các cơ sở khám bệnh, chữa bệnh trong hệ thống giám sát trọng điểm nhiễm trùng đường hô hấp cấp tính nặng.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký, ban hành.
Điều 4. Các ông, bà: Chánh Văn phòng Bộ; Cục trưởng Cục Y tế dự phòng; Cục trưởng Cục Quản lý Khám, chữa bệnh; Viện trưởng các Viện Vệ sinh dịch tễ, Viện Pasteur; Giám đốc Sở Y tế, Bệnh viện, Trung tâm Y tế dự phòng tỉnh, thành phố trong hệ thống giám sát trọng điểm nhiễm trùng đường hô hấp cấp tính nặng (SAKI); Thủ trưởng các đơn vị liên quan chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: | KT. BỘ TRƯỞNG |
HƯỚNG DẪN GIÁM SÁT
NHIỄM TRÙNG ĐƯỜNG HÔ HẤP CẤP TÍNH NẶNG
(SARI)
(Ban hành kèm theo Quyết định số 1271/QĐ-BYT ngày 03 tháng 4 năm 2017 của Bộ trưởng Bộ Y tế)
MỤC LỤC
Phần 1 ĐẶT VẤN ĐỀ
Phần 2 MỤC TIÊU
I. Mục tiêu chung
II. Mục tiêu cụ thể
Phần 3 NỘI DUNG VÀ QUY TRÌNH GIÁM SÁT
I. Nội dung giám sát
1. Đặc điểm dịch tễ học SARI tại Việt Nam
2. Sự lưu hành của vi rút cúm và một số vi rút thường gặp khác gây SARI tại Việt Nam
II. Lựa chọn điểm giám sát
III. Quy trình giám sát
1. Lựa chọn trường hợp bệnh
2. Điền phiếu điều tra trường hợp bệnh SAKI
3. Lấy mẫu, bảo quản, vận chuyển bệnh phẩm của bệnh nhân SARI
4. Tổ chức xét nghiệm bệnh phẩm và phản hồi, báo cáo kết quả xét nghiệm
5. Quản lý dữ liệu và quy định về báo cáo
Phụ lục
PHỤ LỤC 1: DANH SÁCH CÁC ĐIỂM GIÁM SÁT SARI NĂM 2017
PHỤ LỤC 2: HƯỚNG DẪN GHI MÃ SỐ
1. Mã số bệnh nhân
2. Mã số báo cáo tuần
PHỤ LỤC 3: HƯỚNG DẪN LẤY MẪU, BẢO QUẢN, VẬN CHUYỂN BỆNH PHẨM SARI
1. Lấy mẫu
2. Bảo quản, đóng gói, vận chuyển và nhận mẫu
PHỤ LỤC 4: HƯỚNG DẪN LƯU TRỮ, XÉT NGHIỆM BỆNH PHẨM SARI
1. Lưu trữ mẫu bệnh phẩm
2. Quy trình xét nghiệm
PHỤ LỤC 5: CÁC MẪU PHIẾU, BÁO CÁO, SỔ THEO DÕI
PHỤ LỤC 6: SƠ ĐỒ QUY TRÌNH GIÁM SÁT SARI
DANH MỤC VIẾT TẮT
| Adv | Adenovirus |
|
| Vi rút Adeno |
| ARI | Acute Respiratory Infection Nhiễm trùng đường hô hấp cấp tính |
| BVĐK | Bệnh viện đa khoa |
| CDC | Centers for Disease Control and Prevention Trung tâm Dự phòng và Kiểm soát bệnh tật Hoa Kỳ |
| hMPV | Human metapneumovirus |
| ILI | Influenza-like illness Hội chứng cúm |
| NISS | National influenza Surveillance System Hệ thống giám sát cúm quốc gia |
| RSV | Respiratory Syncytial Virus Vi rút hợp bào đường hô hấp |
| RV | Rhinovirus |
|
| Vi rút Rhino |
| SARI | Severe Acute Respiratory Infection Nhiễm trùng đường hô hấp cấp tính nặng |
| TP HCM | Thành phố Hồ Chí Minh |
| VPN | Viêm phổi nặng |
| VSDT | Vệ sinh dịch tễ |
| WHO | World Health Organization Tổ chức Y tế Thế giới |
Phần 1
ĐẶT VẤN ĐỀ
Hệ thống giám sát cúm quốc gia của Việt Nam (NISS) dược hình thành từ năm 2006, do Trung tâm Dự phòng và Kiểm soát bệnh tật Hoa Kỳ (CDC) hỗ trợ. Thời gian đầu, hệ thống bao gồm 15 điểm giám sát hội chứng cúm (ILI) và 5 điểm giám sát nhiễm trùng đường hô hấp cấp tính nặng (SAKI), cùng với hệ thống giám sát viêm phổi nặng nghi do vi rút (VPN) tại tất cả các bệnh viện tuyến tỉnh và tuyến trung ương ở Việt Nam, NISS đã cung cấp nhiều thông tin về dịch tễ học và vi rút học cần thiết cho việc hướng dẫn và định hướng cho các hoạt động và chính sách phòng chống bệnh cúm tại Việt Nam. Các số liệu trong vòng 10 năm giám sát hội chứng cúm (từ năm 2006) cho thấy các vi rút cúm lưu hành quanh năm ở Việt Nam, với tỷ lệ mắc cúm hàng năm khoảng 21%; trong khi đó, tỉ lệ nhiễm cúm ở các bệnh nhân SARI và bệnh nhân viêm phổi nặng nghi do vi rút dao động, trong khoảng từ 12% đến 17%.
Tuy nhiên, ngoài sự lưu hành của các vi rút cúm, có rất ít thông tin về các tác nhân khác ngoài cúm gây ra các nhiễm trùng hô hấp cấp tính (ARI). Một số ít các nghiên cứu đã được tiến hành để tìm hiểu về các tác nhân vi rút gây ra ARI ở trẻ em nhập viện tại Việt Nam, kết quả cho thấy, bên cạnh vi rút cúm, các vi rút hô hấp khác như vi rút hợp bào hô hấp (RSV), vi rút Adeno và vi rút Rhino trên người cũng thường thấy trên các nhóm bệnh nhân này. Tuy nhiên, vì nhiều lý do khác nhau cũng như vì nguồn lực có hạn, các chương trình giám sát hiện hành mới chỉ chú trọng đến vi rút cúm, trong khi đó chúng ta vẫn cần hiểu thêm về đặc điểm lâm sàng và dịch tễ của các bệnh nhiễm trùng hô hấp cấp tính, đặc biệt là nhiễm trùng hô hấp cấp tính nặng ở những bệnh nhân có yêu cầu phải nhập viện.
Nhằm mục đích tìm hiểu sự lưu hành của vi rút cúm và các vi rút đường hô hấp khác, cũng như xác định tỷ lệ mắc bệnh và tỷ lệ tử vong, do vi rút cúm và các vi rút đường hô hấp khác gây ra cho các bệnh nhân SARI nhập viện, chương trình giám sát trọng điểm SARI được đề xuất dựa trên nền tảng của hệ thống giám sát cúm quốc gia. Đây cũng là một phần của mạng lưới giám sát trọng điểm của Bộ Y tế với sự hỗ trợ từ các đối tác trong việc giám sát các bệnh truyền nhiễm ưu tiên tại Việt Nam. Trong chương trình giám sát trọng điểm SARI, các bệnh nhân sẽ được lựa chọn từ các bệnh viện trọng điểm trên toàn quốc theo một định nghĩa trường hợp bệnh thống nhất sẽ được đề nghị lấy mẫu ngoáy mũi và ngoáy họng. Các mẫu này sẽ được xét nghiệm tìm căn nguyên vi rút cúm và các vi rút đường hô hấp phổ biến khác bằng phương pháp real-time RT- PCR.
Phần 2
MỤC TIÊU
I. Mục tiêu chung
Giám sát, thu thập các thông tin cần thiết về dịch tễ học, vi rút học của nhiễm trùng đường hô hấp cấp tính nặng do một số vi rút gây bệnh hô hấp phổ biến làm cơ sở đề xuất các chính sách và biện pháp phòng chống dịch bệnh tại Việt Nam, từng bước hoàn thiện hệ thống giám sát nhiễm trùng đường hô hấp cấp tính nặng tại Việt Nam và chia sẻ thông tin về đặc điểm dịch tễ học, vi rút học của SARI cho mạng lưới giám sát toàn cầu.
II. Mục tiêu cụ thể
1. Thu thập, phân tích một cách hệ thống và thường xuyên dữ liệu dịch tễ học của các trường hợp SARI tại một số bệnh viện trọng điểm.
2. Xác định sự lưu hành của các chủng vi rút cúm và một số vi rút thường gặp khác gây SARI tại Việt Nam.
3. Xây dựng cơ sở dữ liệu về mức độ hoạt động của vi rút cúm và một số vi rút thường gặp khác gây SARI sử dụng cho việc ước tính, dự báo dịch bệnh cúm và nhiễm trùng đường hô hấp cấp tính nặng.
Phần 3
NỘI DUNG VÀ QUY TRÌNH GIÁM SÁT
I. Nội dung giám sát
1. Đặc điểm dịch tễ học SARI tại Việt Nam
Thu thập và phân tích các chỉ số sau:
- Tỷ lệ mắc SARI trên tổng số lượt bệnh nhân nhập viện.
- Tỷ lệ, phân bố số mắc và tử vong do SARI theo thời gian, địa điểm, con người.
- Tỷ lệ tử vong do SARI trong tổng số lượt bệnh nhân SARI nhập viện.
- Tỷ lệ tử vong do SARI trong tổng số tử vong do tất cả các nguyên nhân.
2. Sự lưu hành của vi rút cúm và một số vi rút thường gặp khác gây SARI tại Việt Nam
Thu thập và phân tích các chỉ số sau:
- Tỷ lệ phần trăm từng tác nhân vi rút gây SARI trong tổng số những trường hợp SARI được xét nghiệm theo thời gian, địa điểm, con người.
- Tỷ lệ phần trăm các phân típ vi rút cúm trong tổng số trường hợp SARI nhiễm vi rút cúm theo thời gian, địa điểm, con người.
II. Lựa chọn điểm giám sát
Viện VSDT/ Pasteur khu vực phối hợp với Cục Y tế dự phòng thực hiện lựa chọn điểm giám sát theo các nội dung sau:
a) Số lượng: chọn từ 1 đến 2 điểm giám sát (bệnh viện) tại mỗi vùng trong 8 vùng sinh thái (Phụ lục 1).
b) Tiêu chuẩn lựa chọn:
- Các bệnh viện đa khoa tuyến tỉnh, trung ương có số lượng bệnh nhân SARI nhập viện đủ lớn (trung bình ≥ 10 bệnh nhân SARI/tuần).
- Có mô hình bệnh tật đa dạng.
- Có đủ điều kiện, trang thiết bị, đội ngũ cán bộ có đủ khả năng thực hiện các hoạt động chuyên môn giám sát SARI.
- Phối hợp chặt chẽ và cam kết duy trì hoạt động giám sát lâu dài.
c) Quy trình lựa chọn điểm giám sát:
- Liệt kê các bệnh viện tuyến tỉnh, trung ương tại mỗi vùng sinh thái
- Đánh giá từng bệnh viện dựa trên các tiêu chí nêu trên
- Chọn các bệnh viện theo thứ tự ưu tiên từ cao xuống thấp cho mỗi vùng sinh thái.
Số lượng điểm và địa điểm giám sát SARI có thể thay đổi dựa trên sự ưu tiên, khả năng và nhu cầu của hệ thống giám sát SARI.
III. Quy trình giám sát
1. Lựa chọn trường hợp bệnh
1.1. Định nghĩa trường hợp bệnh
Áp dụng định nghĩa trường hợp bệnh SARI của Tổ chức Y tế Thế giới năm 2014 như sau (cho tất cả các độ tuổi):
Một trường hợp nhiễm trùng đường hô hấp cấp tính nặng với các tiêu chí sau:
- Tiền sử bị sốt hoặc sốt với nhiệt độ đo được ≥ 38°C; và
- Ho; và
- Khởi phát trong vòng 10 ngày; và
- Yêu cầu nhập viện (Bệnh nhân nội trú).
1.2. Lựa chọn bệnh nhân phỏng vấn, lấy mẫu
a) Số lượng: 10 bệnh nhân/ tuần.
b) Cách chọn: Hàng ngày cán bộ tham gia giám sát SARI của các khoa lâm sàng thực hiện việc lựa chọn bệnh nhân theo các bước sau:
Bước 1: Kiểm tra bệnh án các trường hợp mới nhập viện, lựa chọn những bệnh nhân có đủ các tiêu chuẩn theo định nghĩa trường hợp bệnh đã nêu trên. Lưu tổng số trường hợp mắc và tử vong SARI theo ngày trong Báo cáo tuần của khoa (Mẫu 2A).
Bước 2: Chọn 02 bệnh nhân SARI đầu tiên nhập viện vào ngày hôm đó để lấy mẫu, điền phiếu và lưu thông tin vào Báo cáo tuần của khoa (Mẫu 2A).
Lưu ý:
- Nếu trong ngày không có đủ 02 bệnh nhân SARI để lấy mẫu, có thể lấy bù trong các ngày tiếp theo cho đến thứ Sáu của tuần đó, nếu đến thứ Sáu không đủ thì dừng lại (không lấy bù vào thứ Bảy, Chủ nhật và các tuần sau).
- Tùy vào tình hình thực tế tại điểm giám sát, Viện VSDT/ Pasteur khu vực phối hợp với điểm giám sát và Trung tâm Y tế dự phòng tỉnh, thành phố thống nhất quy trình giám sát SAKI của từng điểm giám sát, trong đó quy định rõ về:
+ Các khoa lâm sàng tham gia giám sát SARI và cách phân bố lấy mẫu bệnh phẩm giữa các khoa để mẫu được lấy đại diện cho các khoa lâm sàng (Nội, Nhi, Truyền nhiễm, Hồi sức cấp cứu, ...) có điều trị bệnh nhân SARI, đại diện cho nhóm tuổi (người lớn và trẻ em, trừ bệnh viện chuyên khoa Nhi).
+ Quy trình bảo quản, vận chuyển mẫu, điền phiếu, ghi số, báo cáo kết quả... để đảm bảo các yêu cầu kỹ thuật về chất lượng mẫu, thông tin được thu thập, xét nghiệm và báo cáo theo đúng yêu cầu.
2. Điền phiếu điều tra trường hợp bệnh SARI
- Sau khi lựa chọn bệnh nhân, cán bộ giám sát SARI của khoa thu thập thông tin về trường hợp bệnh theo Mẫu 1 - Phiếu điều tra trường hợp bệnh SARI. Mỗi bệnh nhân SARI có một mã số riêng để quản lý thông tin dịch tễ và kết quả xét nghiệm. Mã số bệnh nhân là mã số duy nhất, không trùng lặp, được quy định tại Phụ lục 2.
- Thông tin trong phiếu điều tra trường hợp bệnh thu thập qua phỏng vấn bệnh nhân hoặc người nhà, người chăm sóc bệnh nhân phải được điền đầy đủ, chính xác. Cán bộ điều phối tại bệnh viện cần kiểm tra phiếu trước khi gửi về các Viện VSDT/ Pasteur khu vực.
- Một số vấn đề cần lưu ý khi kiểm tra:
+ Tất cả các câu hỏi đều được trả lời.
+ Tính hợp lý của số liệu (Ví dụ: ngày khởi phát, ngày nhập viện, nghề nghiệp có tương ứng với tuổi không, chỉ có phụ nữ mới mang thai,...).
3. Lấy mẫu, bảo quản, vận chuyển bệnh phẩm của bệnh nhân SARI
Một mẫu bệnh phẩm hợp lệ sẽ bao gồm cả mẫu dịch ngoáy mũi và dịch ngoáy họng của một bệnh nhân được lấy tại cùng một thời điểm. Hai mẫu này được bảo quản trong cùng một ống đựng môi trường vận chuyển. Tuy nhiên, đối với bệnh nhân thở máy và phải đặt nội khí quản, có thể lấy mẫu dịch nội khí quản thay thế cả hai bệnh phẩm trên.
- Lấy mẫu, bảo quản, vận chuyển bệnh phẩm được thực hiện theo đúng Hướng dẫn lấy mẫu, bảo quản, vận chuyển bệnh phẩm SARI (Phụ lục 3).
Ngoài ra:
- Sau khi lấy mẫu bệnh phẩm, cán bộ phụ trách SARI của khoa ghi thông tin các trường hợp được lấy mẫu vào Báo cáo tuần của khoa (Mẫu 2A).
- Nếu mẫu bệnh phẩm được bảo quản tại Khoa xét nghiệm của bệnh viện hoặc Trung tâm Y tế dự phòng tỉnh, thành phố thì thông tin của mẫu bệnh phẩm nhận từ các khoa phải được lưu vào số quản lý bệnh phẩm SARI (Mẫu 6) và sổ này được lưu tại Khoa xét nghiệm của bệnh viện hoặc Trung tâm Y tế dự phòng tỉnh, thành phố.
4. Tổ chức xét nghiệm bệnh phẩm và phản hồi, báo cáo kết quả xét nghiệm
Khi bệnh phẩm, phiếu điều tra trường hợp bệnh (Mẫu 1) và phiếu yêu cầu xét nghiệm (Mẫu 3) được chuyển đến phòng xét nghiệm của Viện VSDT/ Pasteur khu vực, bên giao và bên nhận phải ký xác nhận vào sổ giao nhận bệnh phẩm, Phiếu điều tra trường hợp bệnh, Báo cáo tuần (Mẫu 5).
4.1. Xét nghiệm bệnh phẩm
- Sau khi nhận được bệnh phẩm từ các điểm giám sát được phản công phụ trách (Phụ lục 1), phòng xét nghiệm tại các Viện khu vực sẽ tiến hành xét nghiệm các mẫu bệnh phẩm trước thứ Năm hàng tuần theo Hướng dẫn lưu trữ, xét nghiệm bệnh phẩm SARI (Phụ lục 4) để đảm bảo kết quả xét nghiệm được gửi đến các đơn vị liên quan đúng thời gian quy định tại mục 4.2.
4.2. Phản hồi, báo cáo kết quả xét nghiệm
- Sau khi hoàn thành xét nghiệm, phòng xét nghiệm của Viện VSDT/Pasteur sẽ điền kết quả vào phần trả lời kết quả xét nghiệm trong Mẫu 3 và Bảng tổng hợp kết quả xét nghiệm (Mẫu 4). Mẫu 4 sẽ được gửi đến các điểm giám sát và các khoa dịch tễ tại các Viện VSDT/Pasteur trước 16h00 thứ Sáu hàng tuần. Trong trường hợp cần xác định lại kết quả thì phòng xét nghiệm của Viện VSDT/Pasteur sẽ thông báo cho các đơn vị nhận kết quả xét nghiệm về các mẫu cần xác định lại, đồng thời báo cáo kết quả phải được gửi đến các đơn vị này trước 16h00 thứ Hai của tuần kế tiếp.
- Đối với các tác nhân mới hoặc quan trọng, trong đó có vi rút cúm A/H5 và A/H7, kết quả phải được thông báo ngay theo quy định hiện hành. Trong trường hợp kết quả xét nghiệm không được gửi trả cho các điểm giám sát theo thời gian quy định, phòng xét nghiệm của Viện VSDT/Pasteur cần thông báo cho các đơn vị khi nào họ có thể nhận được kết quả và giải thích lý do tại sao.
5. Quản lý dữ liệu và quy định về báo cáo
5.1. Tại các bệnh viện
- Phiếu điều tra trường hợp bệnh (Mẫu 1) và Phiếu yêu cầu xét nghiệm (Mẫu 3) cần được gửi kèm với mẫu bệnh phẩm về phòng xét nghiệm của các Viện VSDT/Pasteur ít nhất một lần/tuần để đảm bảo yêu cầu về kỹ thuật và thời gian báo cáo.
- Hàng ngày cán bộ tham gia hoạt động giám sát SARI tại các khoa lâm sàng tổng hợp số liệu bệnh nhân nhập khoa nói chung và bệnh nhân SARI theo mẫu 2A. Các thông tin này sẽ được lưu tại khoa giám sát và chuyển tới cán bộ điều phối SARI của bệnh viện trước 16h00 ngày thứ Hai tuần tiếp theo.
Lưu ý: mỗi tuần được tính từ thứ Hai đến Chủ nhật. Mã số tuần được quy định theo lịch tuần tại Phụ lục 2.
- Hàng tuần, Điều phối viên SARI tại các bệnh viện sẽ tổng hợp các thông tin từ mẫu 2A của các khoa tham gia giám sát gửi lên và điền vào Báo cáo tuần của bệnh viện (Mẫu 2B). Báo cáo này cần gửi tới các Viện VSDT/Pasteur khu vực trước 16h00 ngày thứ Ba của tuần kế tiếp.
5.2. Tại các Viện VSDT/ Pasteur khu vực
- Phòng xét nghiệm của các Viện VSDT/Pasteur sau khi nhận được Phiếu điều tra trường hợp bệnh (Mẫu 1) từ các bệnh viện cần chuyển ngay cho khoa Dịch tễ của Viện VSDT/Pasteur.
- Các thông tin từ Phiếu điều tra trường hợp bệnh (Mẫu 1) cần được khoa Dịch tễ của Viện VSDT/Pasteur nhập vào phần mềm báo cáo SARI ngay trong ngày sau khi nhận được phiếu.
- Các thông tin từ Báo cáo tuần của bệnh viện (Mẫu 2B) được tổng hợp tại đơn vị Dịch tễ của Viện VSDT/Pasteur.
- Kết quả xét nghiệm (Mẫu 4) được Phòng xét nghiệm của các Viện VSDT/Pasteur gửi đến khoa Dịch tễ tại các Viện VSDT/Pasteur trước 16h00 thứ Sáu hàng tuần. Các Viện sẽ gửi kết quả đến các điểm giám sát ngay sau đó. Trường hợp cần xác định lại kết quả thì báo cáo kết quả phải được gửi đến các đơn vị này trước 16h00 thứ Hai của tuần kế tiếp.
- Các dữ liệu từ báo cáo tuần và kết quả xét nghiệm trong tuần trước của các bệnh viện thuộc khu vực phụ trách được Viện VSDT/Pasteur tổng hợp theo Mẫu 7 gửi về Viện Vệ sinh dịch tễ Trung ương và Cục Y tế dự phòng trước 16hoo thứ Tư hàng tuần.
- Viện Vệ sinh dịch tễ Trung ương sẽ tổng hợp thông tin từ báo cáo tuần của các Viện VSDT/Pasteur và gửi về Cục Y tế dự phòng trước 16h00 thứ Năm hàng tuần.
- Cục Y tế dự phòng sẽ chia sẻ kết quả giám sát SARI cả nước đến các Viện VSDT/Pasteur và các đối tác liên quan.
- Tất cả các phiếu điều tra và phiếu xét nghiệm (thu thập mẫu bệnh phẩm và kết quả xét nghiệm) bản gốc sẽ được giữ tại Viện VSDT/Pasteur khu vực và chuyển về Cục Y tế dự phòng khi có yêu cầu. Phiếu điều tra trường hợp bệnh và phiếu kết quả xét nghiệm của mỗi bệnh nhân phải được gắn kèm với nhau.
- Hàng tháng, Viện VSDT/ Pasteur khu vực gửi file kết xuất dữ liệu từ Phiếu điều tra trường hợp bệnh về Cục Y tế dự phòng và Viện Vệ sinh dịch tễ Trung ương trước ngày 05 của tháng kế tiếp và báo cáo tháng phân tích theo các chỉ số giám sát quy định tại Phần 3, mục I: Nội dung giám sát./.
Phụ lục
1. Phụ lục 1: Danh sách các điểm giám sát SARI năm 2017
2. Phụ lục 2: Hướng dẫn ghi mã số
3. Phụ lục 3: Hướng dẫn lấy mẫu, bảo quản, vận chuyển bệnh phẩm SARI
4. Phụ lục 4: Hướng dẫn lưu trữ, xét nghiệm bệnh phẩm SARI
5. Phụ lục 5: Các mẫu phiếu, báo cáo, sổ theo dõi
- Phiếu điều tra trường hợp bệnh SARI (Mẫu 1)
- Báo cáo tuần của khoa (Mẫu 2A)
- Báo cáo tuần của bệnh viện (Mẫu 2B)
- Phiếu yêu cầu xét nghiệm và trả lời kết quả xét nghiệm bệnh nhân SARI (Mẫu 3)
- Bảng tổng hợp kết quả xét nghiệm bệnh nhân SARI (Mẫu 4)
- Sổ giao nhận bệnh phẩm, Phiếu điều tra trường hợp bệnh, Báo cáo tuần (Mẫu 5)
- Số quản lý bệnh phẩm SARI (Mẫu 6)
- Báo cáo tuần SAKI của Viện VSDT/ Pasteur khu vực (Mẫu 7)
6. Phụ lục 6: Sơ đồ quy trình thực hiện giám sát SARI
PHỤ LỤC 1:
DANH SÁCH CÁC ĐIỂM GIÁM SÁT SARI NĂM 2017
| Vùng | Điểm giám sát | Viện khu vực phụ trách |
| Đông Bắc | Bệnh viện đa khoa Quảng Ninh | Viện Vệ sinh Dịch tễ Trung ương |
| Tây Bắc | Bệnh viện đa khoa Điện Biên | |
| Đồng bằng sông Hồng | Bệnh viện Nhi Trung ương Bệnh viện đa khoa Thanh Hóa | |
| Duyên hải Nam Trung bộ | Bệnh viện đa khoa Trung ương Huế Bệnh viện đa khoa Khánh Hòa | Viện Pasteur Nha Trang |
| Tây Nguyên | Bệnh viện đa khoa Đắk Lắk | Viện Vệ sinh Dịch tễ Tây Nguyên |
| Đông Nam bộ | Bệnh viện Bệnh Nhiệt đới TP. HCM |
|
| Bệnh viện Nhi đồng 1 TP. HCM | Viên Pasteur TP. Hồ Chí Minh | |
| Tây Nam bộ | Bệnh viện đa khoa An Giang | |
| Bệnh viện đa khoa Đồng Tháp |
Lưu ý: Danh sách sẽ được cập nhật theo từng năm
PHỤ LỤC 2:
HƯỚNG DẪN GHI MÃ SỐ
1. Mã số bệnh nhân
- Mỗi bệnh nhân SARI sẽ có một mã số riêng để quản lý thông tin dịch tễ và kết quả xét nghiệm. Mã số bệnh nhân là mã số duy nhất, không trùng lặp. Cấu trúc của mỗi mã số bệnh nhân bao gồm các thành phần như sau:
SARI/Mã bệnh viện/ hai số cuối của năm/tên viết tắt khoa/ số thứ tự trường hợp bệnh (3 chữ số)
Ví dụ: SARI/05/15/TN/034 là mã số bệnh nhân của trường hợp bệnh thứ 34, khoa Truyền nhiễm (TN), năm 2015 tại Bệnh viện đa khoa tỉnh Khánh Hòa.
Mã số các bệnh viện trọng điểm được quy định như sau:
| Mã bệnh viện | Tên điểm giám sát |
| 02 | BV Nhi Trung ương |
| 03 | BV Nhi Đồng 1, TP HCM |
| 04 | BV Bệnh Nhiệt đới TP HCM |
| 05 | BVĐK tỉnh Khánh Hòa |
| 06 | BVĐK tỉnh Đắk Lắk |
| 18 | BVĐK tỉnh Quảng Ninh |
| 22 | BV Trung ương Huế |
| 24 | BVĐK tỉnh Đồng Tháp |
| 26 | BVĐK tỉnh An Giang |
| 27 | BVĐK tỉnh Thanh Hóa |
| 29 | BVĐK tỉnh Điện Biên |
Lưu ý: Mã số bệnh nhân phải được ghi trên phiếu điều tra trường hợp bệnh (Mẫu 1), Phiếu yêu cầu xét nghiệm và trả lời kết quả xét nghiệm (Mẫu 3), ghi trên ống đựng bệnh phẩm và trên danh sách bệnh nhân đối với các bệnh nhân được chọn lấy mẫu xét nghiệm.
2. Mã số báo cáo tuần
Mã số Báo cáo tuần (Mẫu 2A và 2B) là mã số duy nhất cho một tuần đối với một điểm giám sát trong hệ thống, cấu trúc của mã số báo cáo tuần bao gồm 3 thành phần sau:
BCT/mã bệnh viện /số tuần
Ví dụ: BCT/02/201726 là tuần thứ 26 năm 2017 của điểm giám sát bệnh viện Nhi Trung ương. Cách ghi số tuần được ghi trong bảng lịch tuần 2017 như sau:
| Số tuần | Từ ngày | Đến ngày |
| Số tuần | Từ ngày | Đến ngày |
| 201701 | 02/01/2017 | 08/01/2017 |
| 201727 | 03/07/2017 | 09/07/2017 |
| 201702 | 09/01/2017 | 15/01/2017 |
| 201728 | 10/07/2017 | 16/07/2017 |
| 201703 | 16/01/2017 | 22/01/2017 |
| 201729 | 17/07/2017 | 23/07/2017 |
| 201704 | 23/01/2017 | 29/01/2017 |
| 201730 | 24/07/2017 | 30/07/2017 |
| 201705 | 30/01/2017 | 05/02/2017 |
| 201731 | 31/07/2017 | 06/08/2017 |
| 201706 | 06/02/2017 | 12/02/2017 |
| 201732 | 07/08/2017 | 13/08/2017 |
| 201707 | 13/02/2017 | 19/02/2017 |
| 201733 | 14/08/2017 | 20/08/2017 |
| 201708 | 20/02/2017 | 26/02/2017 |
| 201734 | 21/08/2017 | 27/08/2017 |
| 201709 | 27/02/2017 | 05/03/2017 |
| 201735 | 28/08/2017 | 03/09/2017 |
| 201710 | 06/03/2017 | 12/03/2017 |
| 201736 | 04/09/2017 | 10/09/2017 |
| 20171I | 13/03/2017 | 19/03/2017 |
| 201737 | 11/09/2017 | 17/09/2017 |
| 201712 | 20/03/2017 | 26/03/2017 |
| 201738 | 18/09/2017 | 24/09/2017 |
| 201713 | 27/03/2017 | 02/04/2017 |
| 201739 | 25/09/2017 | 01/10/2017 |
| 201714 | 03/04/2017 | 09/04/2017 |
| 201740 | 02/10/2017 | 08/10/2017 |
| 201715 | 10/04/2017 | 16/04/2017 |
| 201741 | 09/10/2017 | 15/10/2017 |
| 201716 | 17/04/2017 | 23/04/2017 |
| 201742 | 16/10/2017 | 22/10/2017 |
| 201717 | 24/04/2017 | 30/04/2017 |
| 201743 | 23/10/2017 | 29/10/2017 |
| 201718 | 01/05/2017 | 07/05/2017 |
| 201744 | 30/10/2017 | 05/11/2017 |
| 201719 | 08/05/2017 | 14/05/2017 |
| 201745 | 06/11/2017 | 12/11/2017 |
| 201720 | 15/05/2017 | 21/05/2017 |
| 201746 | 13/11/2017 | 19/11/2017 |
| 201721 | 22/05/2017 | 28/05/2017 |
| 201747 | 20/11/2017 | 26/11/2017 |
| 201722 | 29/05/2017 | 04/06/2017 |
| 201748 | 27/11/2017 | 03/12/2017 |
| 201723 | 05/06/2017 | 11/06/2017 |
| 201749 | 04/12/2017 | 10/12/2017 |
| 201724 | 12/06/2017 | 18/06/2017 |
| 201750 | 11/12/2017 | 17/12/2017 |
| 201725 | 19/06/2017 | 25/06/2017 |
| 201751 | 18/12/2017 | 24/12/2017 |
| 201726 | 26/06/2017 | 02/07/2017 |
| 201752 | 25/12/2017 | 31/12/2017 |
PHỤ LỤC 3:
HƯỚNG DẪN LẤY MẪU, BẢO QUẢN, VẬN CHUYỂN BỆNH PHẨM SARI
1. Lấy mẫu
Một mẫu bệnh phẩm hợp lệ sẽ bao gồm cả mẫu dịch ngoáy mũi và dịch ngoáy họng của một bệnh nhân được lấy tại cùng một thời điểm. Hai mẫu này được bảo quản trong cùng một ống đựng môi trường vận chuyển. Tuy nhiên, đối với bệnh nhân thở máy và phải đặt nội khí quản, có thể lấy mẫu dịch nội khí quản thay thế cả hai bệnh phẩm trên. Bệnh phẩm nên được lấy sớm ngay khi bệnh nhân vừa vào khoa và tốt nhất là trước khi sử dụng bất cứ loại thuốc nào (đặc biệt là thuốc kháng vi rút) theo chỉ định của bác sỹ tại khoa điều trị.
Lưu ý: Mã số bệnh nhân được cung cấp trong phiếu điều tra trường hợp bệnh (Mẫu 1) phải được ghi vào phiếu yêu cầu xét nghiệm (Mẫu 3) và trên ống đựng bệnh phẩm. Ngoài mã số bệnh nhân, trên ống đựng bệnh phẩm cũng phải ghi thêm họ tên và tuổi của bệnh nhân, loại bệnh phẩm và ngày lấy mẫu được quy định theo tiêu chuẩn của Bộ Y tế tại Thông tư 43/2011/TT-BYT ngày 05/12/2011 quy định chế độ quản lý mẫu bệnh phẩm bệnh truyền nhiễm.
1.1. Dụng cụ lấy mẫu
- Găng tay
- Dụng cụ đè lưỡi
- Khẩu trang
- Áo choàng y tế
- Tăm bông y tế được làm bằng sợi polyester hoặc sợi tơ (Không nên sử dụng tăm bông có đầu làm bằng cotton và có cán cầm bằng gỗ vì chúng có thể ức chế phản ứng PCR)
- Ống đựng bệnh phẩm có chứa môi trường vận chuyển (VTM)
- Túi chống thấm
- Cồn sát trùng, bút ghi
- Túi giữ lạnh/đá khô
- Phích lạnh bảo quản mẫu
- Dây nhựa mềm (đường kính 10 FG) để lấy dịch nội khí quản.
1.2. Loại bệnh phẩm và kỹ thuật lấy mẫu bệnh phẩm
Trước khi tiến hành lấy mẫu cần điền đầy đủ thông tin về họ tên, tuổi và ngày lấy mẫu trên nhãn ống đựng mẫu. Lấy đồng thời dịch ngoáy họng và ngoáy mũi của bệnh nhân.
a) Dịch ngoáy họng
- Yêu cầu bệnh nhân há miệng to
- Dùng dụng cụ đè nhẹ nhàng lưỡi bệnh nhân
- Đưa tăm bông vào vùng hầu họng, miết và xoay tròn nhẹ 3 đến 4 lần tại khu vực 2 bên vùng a-mi-đan và thành sau họng để lấy được dịch và tế bào vùng họng.
- Sau khi lấy bệnh phẩm, que tăm bông được chuyển vào ống chứa 3ml môi trường vận chuyển (VTM hoặc UTM) để bảo quản. Lưu ý, đầu tăm bông phải nằm ngập hoàn toàn trong môi trường vận chuyển, và nếu que tăm bông dài hơn ống đựng môi trường vận chuyển cần bẻ/cắt cán tăm bông cho phù hợp với độ dài của ống nghiệm chứa môi trường vận chuyển.
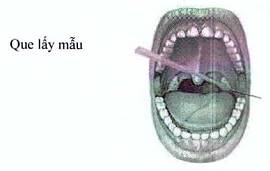
Miết vào 2 bên amidan và thành bên họng
Hình1: Lấy dịch ngoáy họng
b) Dịch ngoáy mũi
- Yêu cầu bệnh nhân ngồi yên, mặt hơi ngửa, trẻ nhỏ thì phải có người lớn giữ.
- Người lấy bệnh phẩm nghiêng đầu bệnh nhân ra sau khoảng 70o, tay đỡ phía sau cổ bệnh nhân.
- Tay kia đưa nhẹ nhàng tăm bông vào mũi, vừa đẩy vừa xoay giúp tăm bông đi dễ dàng vào sâu 1 khoảng bằng 1/2 độ dài từ cánh mũi đến dái tai cùng phía.
Lưu ý: nếu chưa đạt được độ sâu như vậy mà cảm thấy có lực cản rõ thì rút tăm bông ra và thử lấy mũi bên kia. Khi cảm thấy tăm bông chạm vào thành sau họng mũi thì dừng lại, xoay tròn rồi từ từ rút tăm bông ra
- Giữ tăm bông tại chỗ lấy mẫu trong vòng 5 giây để đảm bảo dịch thấm tối đa.
- Từ từ xoay và rút tăm bông ra.
- Đặt đầu tăm bông vào ống đựng bệnh phẩm có chứa môi trường vận chuyển và bẻ cán tăm bông tại điểm đánh dấu để có độ dài phù hợp với độ dài của ống nghiệm chứa môi trường vận chuyển. Que tăm bông sau khi lấy dịch ngoáy mũi sẽ được để chung vào ống môi trường chứa que tăm bông lấy dịch ngoáy họng.
- Đóng nắp, xiết chặt, bọc ngoài bằng giấy parafin (nếu có).
- Bảo quản mẫu trong điều kiện nhiệt độ 2-8°C trước khi chuyển về phòng xét nghiệm của Viện VSDT/Pasteur. Nếu bệnh phẩm không được vận chuyển đến phòng xét nghiệm của Viện VSDT/Pasteur trong vòng 72 giờ kể từ khi lấy mẫu, các mẫu bệnh phẩm phải được bảo quản trong âm 70°C (-70°C) và sau đó phải được giữ đông trong quá trình vận chuyển đến phòng xét nghiệm.
Lưu ý: Đối với trẻ nhỏ đặt ngồi trên đùi của cha/mẹ, lưng của trẻ đối diện với phía ngực cha mẹ. Cha/mẹ cần ôm trẻ giữ chặt cơ thể và tay trẻ. Yêu cầu cha/mẹ ngã đầu trẻ ra phía sau.

Hình 2: Lấy dịch ngoáy mũi
c) Dịch nội khí quản:
- Chỉ áp dụng cho những bệnh nhân đang thở máy và đặt nội khí quản
- Dùng ống hút dịch đặt theo đường nội khí quản, và dùng bơm tiêm hút dịch nội khí quản theo đường ống đã đặt.
- Chuyển dịch nội khí quản vào ống nhựa chứa môi trường vận chuyển vi rút.
- Đóng nắp ống, xiết chặt, bọc ngoài bằng giấy paraffin (nếu có) và bảo quản trong điều kiện nhiệt độ 2-8°C trước khi chuyển về phòng xét nghiệm. Nếu bệnh phẩm không được vận chuyển đến phòng xét nghiệm của Viện VSDT/Pasteur trong vòng 72 giờ kể từ khi lấy mẫu, các mẫu bệnh phẩm phải được bảo quản trong âm 70°C (-70°C) và sau đó phải được giữ đông trong quá trình vận chuyển đến phòng xét nghiệm của Viện VSDT/ Pasteur.
2. Bảo quản, đóng gói, vận chuyển và nhận mẫu
2.1. Bảo quản mẫu:
- Các mẫu bệnh phẩm cần được bảo quản ở nhiệt độ 2-8°C trong vòng 72 giờ kể từ khi lấy mẫu đến khi tới phòng xét nghiệm của các Viện VSDT/Pasteur.
Lưu ý: Nếu bệnh phẩm không được vận chuyển đến phòng xét nghiệm của các Viện VSDT/Pasteur trong vòng 72 giờ kể từ khi lấy mẫu, các mẫu bệnh phẩm phải được bảo quản trong tủ âm 70°C (-70°C) và sau đó phải được bảo quản đông trong quá trình vận chuyển đến phòng xét nghiệm của các Viện VSDT/Pasteur.
2.2. Đóng gói
- Bệnh phẩm thu thập cho chẩn đoán tác nhân gây bệnh được đóng gói theo nguyên tắc 3 lớp được quy định theo tiêu chuẩn của Bộ Y tế tại Thông tư 43/2011/TT-BYT ngày 05/12/2011 quy định chế độ quản lý mẫu bệnh phẩm bệnh truyền nhiễm.
- Kiểm tra xem ống đựng mẫu bệnh phẩm đã được nắp chặt hay chưa, bọc ống bằng giấy paraffin (nếu có) hoặc giấy thấm, trong trường hợp để nhiều ống mẫu trong một kiện hàng cần bọc giấy thấm quanh mỗi ống để tránh tiếp xúc.
- Đặt ống đựng mẫu bệnh phẩm trong túi chống thấm/ túi nylon hoặc hộp đựng có nắp và đóng kín theo quy định.
- Đặt túi/hộp chứa ống đựng mẫu bệnh phẩm vào phích lạnh bảo quản mẫu hoặc thùng cứng.
- Bổ sung đủ túi /bình tích lạnh vào trong phích/thùng đựng mẫu để mẫu được bảo quản ở nhiệt độ từ 2-8°C, trong suốt quá trình vận chuyển mẫu.
- Đối với mẫu lưu tại nhiệt độ -70°C, bổ sung đủ đá khô hoặc túi /bình tích lạnh để mẫu đông được bảo quản ở nhiệt độ -70°C trong suốt quá trình vận chuyển mẫu (trong trường hợp dùng đá khô thì lớp đóng gói ngoài cùng cần có thông khí; nếu sử dụng bình tích lạnh thì phải đặt bình tích lạnh trong tủ lạnh âm sâu -70°C hoặc thấp hơn trước khi sử dụng).
- Phiếu yêu cầu xét nghiệm được đặt trong túi chống thấm / túi nylon khác (không để chung phiếu với mẫu bệnh phẩm) và đặt trong phích/thùng đựng mẫu có biểu tượng nguy hiểm sinh học (hazard) được quy định bởi WHO cho việc vận chuyển mẫu phẩm sinh học.

Hình 3: Đóng gói và bảo quản bệnh phẩm
2.3. Vận chuyển mẫu
- Hàng tuần, các mẫu bệnh phẩm cần được gửi kèm Phiếu điều tra trường hợp bệnh (Mẫu 1) và Phiếu yêu cầu xét nghiệm (Mẫu 3) về phòng xét nghiệm của các Viện VSDT/Pasteur ít nhất 01 lần/tuần. Tùy vào điều kiện của từng điểm giám sát.
Viện VSDT/Pasteur có quy định hướng dẫn cho từng điểm về số lần và thời gian vận chuyển mẫu để đảm bảo mẫu được bảo quản, vận chuyển theo đúng quy định. Các quy định này cần được ghi tại quy trình giám sát của từng điểm giám sát.
- Mẫu bệnh phẩm phải được bảo quản trong nhiệt độ từ 2-8°C (hoặc tại -70°C nếu là mẫu đông) trong suốt quá trình vận chuyển.
- Phiếu yêu cầu xét nghiệm (Mẫu 3) và phiếu điều tra trường hợp bệnh (Mẫu 1) sẽ được đính kèm với mẫu bệnh phẩm.
- Các cơ sở gửi mẫu cần thông báo ngay cho phòng xét nghiệm khoảng thời gian dự kiến phòng xét nghiệm sẽ nhận được bệnh phẩm để cán bộ phòng xét nghiệm có thể chuẩn bị cho việc nhận mẫu.
- Lựa chọn các phương tiện, hình thức vận chuyển để đảm bảo thời gian vận chuyển ngắn nhất, trong khi vẫn phải đảm bảo điều kiện bảo quản mẫu trong suốt quá trình vận chuyển.
2.4. Nhận mẫu
Khi bệnh phẩm và phiếu yêu cầu xét nghiệm (Mẫu 3) được chuyển đến phòng xét nghiệm của Viện VSDT/Pasteur, bên giao và bên nhận phải ký xác nhận vào Sổ giao nhận bệnh phẩm (Mẫu 5). Các mẫu bệnh phẩm sẽ không được chấp nhận nếu có một trong các vấn đề sau:
- Có hiện tượng rò rỉ bệnh phẩm;
- Không đủ lượng bệnh phẩm yêu cầu;
- Loại bệnh phẩm không phù hợp;
- Ống đựng bệnh phẩm không có môi trường vận chuyển;
- Ống đựng bệnh phẩm chứa môi trường vận chuyển hết hạn sử dụng;
- Nhiệt độ của phích lạnh không đảm bảo yêu cầu;
- Bệnh phẩm được bảo quản ở nhiệt độ 2-8oC nhưng được chuyển đến phòng xét nghiệm của các Viện VSDT/ Pasteur hơn 72 giờ sau khi lấy mẫu;
- Thông tin của bệnh nhân (tên, mã số bệnh nhân, tuổi...) hoặc/và thời gian thu thập mẫu trên ống đựng mẫu bị mất hoặc không trùng với phiếu yêu cầu xét nghiệm.
Lưu ý: Các mẫu bệnh phẩm bị từ chối xét nghiệm phải được giữ tại phòng xét nghiệm của các Viện VSDT/Pasteur khu vực theo quy định của từng phòng xét nghiệm. Lý do từ chối xét nghiệm được ghi vào cột Ghi chú tại Sổ giao nhận bệnh phẩm, Phiếu điều tra trường hợp bệnh, Báo cáo tuần (Mẫu 5) và phần Kết quả xét nghiệm ở Mẫu 3.
PHỤ LỤC 4:
HƯỚNG DẪN LƯU TRỮ, XÉT NGHIỆM BỆNH PHẨM SARI
1. Lưu trữ mẫu bệnh phẩm
- Các dụng cụ và môi trường dùng để vận chuyển, bảo quản mẫu cần tuân thủ nguyên tắc vô trùng của thực hành vi sinh tốt.
- Các bệnh phẩm phải được bảo quản tại nhiệt độ 2-8°C trong vòng 72 giờ sau khi lấy mẫu bệnh phẩm.
- Trường hợp phòng xét nghiệm của Viện khu vực không tiến hành xét nghiệm mẫu bệnh phẩm trong vòng 72 giờ sau khi lấy mẫu thì bảo quản mẫu ở tủ âm 70°C (-70°C) hoặc thấp hơn.
- Các mẫu bệnh phẩm sau khi tách chiết vật liệu di truyền phải được bảo quản trong tủ âm 70°C (-70°C) hoặc thấp hơn tại Viện.
- Tất cả các bệnh phẩm cần được bảo quản ở tủ âm 70°C (-70°C) hoặc thấp hơn trong vòng ít nhất 1 năm sau khi làm xét nghiệm. Sau đó nếu hủy mẫu thì phải tuân theo quy trình hủy mẫu và lưu hồ sơ.
2. Quy trình xét nghiệm
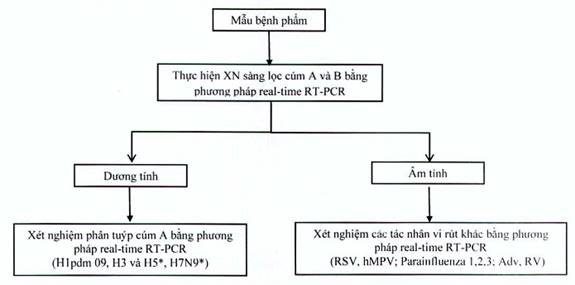
Lưu ý: (*) Nếu mẫu bệnh phẩm có kết quả dương tính với A/H5 và A/H7 thì:
+ Phòng xét nghiệm lại Viện VSDT Tây Nguyên sẽ đóng gói và gửi mẫu về Viện Pasteur TP HCM
+ Phòng xét nghiệm tại Viện Pasteur Nha Trang sẽ đóng gói và gửi mẫu về Viện VSDTTƯ
Hình 4: Sơ đồ quy trình xét nghiệm
Tiến hành xét nghiệm sàng lọc phát hiện vi rút cúm A&B bằng phương pháp real-time RT-PCR cho tất cả các mẫu bệnh phẩm theo quy trình của CDC.
Lưu ý: Khi thực hiện xét nghiệm cúm A và B cần chạy mẫu RNP (human ribonuclease P) cùng với các mẫu bệnh phẩm. Không cần chạy lại mẫu RNP khi thực hiện xét nghiệm phát hiện các tác nhân khác (Other Respiratory Viruses - ORV) không phải cúm nếu phòng xét nghiệm sử dụng cùng mẫu tách triết khi xét nghiệm vi rút cúm. Nếu phòng xét nghiệm sử dụng mẫu tách triết mới thì cần chạy lại RNP.
- Nếu mẫu dương tính với vi rút cúm A, tiến hành làm real-time RT-PCR để xác định phân tuýp cúm A/H1pdm09, A/H3, A/H5 và A/H7
- Nếu mẫu dương tính với vi rút cúm B, không cần làm xác định phân tuýp vi rút cúm.
- Nếu mẫu có kết quả âm tính với cả vi rút cúm A và B, phòng xét nghiệm tiến hành thực hiện xét nghiệm real-time RT-PCR theo quy trình hướng dẫn của CDC để xác định các tác nhân vi rút gây viêm đường hô hấp cấp khác: vi rút hợp bào đường hô hấp (Respiratory syncytial virus - RSV); Human metapneumovirus (hMPV); vi rút Á cúm 1,2,3 (Parainfluenza viruses 1, 2, 3); vi rút Adeno (Adv); và vi rút Rhino (RV).
PHỤ LỤC 5
CÁC MẪU PHIẾU, BÁO CÁO, SỔ THEO DÕI
| Mã số bệnh nhân: SARI /_ _/_ _/_ _/_ _ _ | Số bệnh án #:......................................... | Mẫu 1 |
(Ví dụ: SARI/03/17/CC/001)
PHIẾU ĐIỀU TRA TRƯỜNG HỢP BỆNH
NHIỄM TRÙNG ĐƯỜNG HÔ HẤP CẤP TÍNH NẶNG (SARI)
Tên bệnh viện: ............................. Ngày phỏng vấn (ngày/tháng/năm): ……/……./……
Khoa điều trị: .............................................................................................................
Người điền phiếu: ……………………………………………….ĐT liên hệ: .........................
Người phụ trách SARI: …………………………………………ĐT liên hệ: .........................
Người trả lời: □ Bệnh nhân □ Người nhà bệnh nhân
| THÔNG TIN CHUNG | ||||||||||
| 1. Họ tên bệnh nhân | Họ |
| Tên đệm |
| Tên gọi |
| ||||
| 2. Giới tính | □ Nam □ Nữ | 3. Ngày sinh (ngày/tháng/năm) | ____/_____/______ | 4. Tuổi | ___năm ___tháng (nếu < 2 tuổi) | |||||
| 5. Địa chỉ nơi ở hiện tại | Số nhà:............. Phố/thôn:.......... Phường/ xã:..... | Quận/huyện:........... Tỉnh, thành phố:...... Điện thoại liên lạc: .............................. | 6. Nghề nghiệp* (Xem danh sách nghề nghiệp ở trang sau | (Ghi số) | ||||||
| TÌNH TRẠNG NHẬP VIỆN | ||||||||||
| 7. Ngày nhập viện (ngày/tháng/năm) | _____/_____/______ | 11. Ngày khởi phát (ngày/tháng/năm) | _____/_____/______ | |||||||
| 8. Tiền sử sốt | □ Có □ Không □ Không rõ | 12. Ngày lấy mẫu (ngày/tháng/năm) | _____/_____/______ | |||||||
| 9. Nhiệt độ | ________0C | 13. Chẩn đoán nhập viện ** (Xem danh sách ở trang sau) | (Ghi số) | |||||||
| 10. Ho | □ Có □ Không □ Không rõ | |||||||||
| 14. Tình trạng bệnh lý kèm theo (trước khi bệnh khởi phát) | ||||||||||
| 14.a. Hút thuốc | □ Có □ Không □ Không rõ | 14.f. Các bệnh lý về máu | □ Có □ Không □ Không rõ | |||||||
| 14.b. Bệnh đường hô hấp mạn tính | □ Có □ Không □ Không rõ | 14.g. Suy giảm miễn dịch (do dùng Steroids hoặc do HIV/AIDS | □ Có □ Không □ Không rõ | |||||||
| 14.c. Bệnh hen | □ Có □ Không □ Không rõ | 14.h. Đái tháo đường | □ Có □ Không □ Không rõ | |||||||
| 14.d. Bệnh tim mạch mạn tính | □ Có □ Không □ Không rõ | 14.i. Mang thai | □ Có □ Không □ Không rõ | |||||||
| 14.e. Bệnh thần kinh/ thần kinh - cơ mạn tính | □ Có □ Không □ Không rõ | 14.j. Bệnh lý khác (ghi rõ) |
| |||||||
| CAN THIỆP Y TẾ TRƯỚC KHI NHẬP VIỆN | ||||||||||
| 15. Tiêm vắc xin phòng cúm trong vòng 12 tháng gần nhất | □ Có □ Không □ Không rõ | |||||||||
| 16. Dùng thuốc Oseltamivir (Tamiflu) trong vòng 07 ngày trước khi lấy mẫu | □ Có □ Không □ Không rõ | |||||||||
| TIỀN SỬ DỊCH TỄ TRONG VÒNG 07 NGÀY TRƯỚC KHI KHỞI PHÁT BỆNH | ||||||||||
| 17.a. Du lịch đến nước khác | □ Có □ Không □ Không rõ | Nếu có, ghi cụ thể nước nào: | ||||||||
| 17.b. Tiếp xúc gần (trong vòng 2 mét) với người mắc hoặc tử vong do bệnh đường hô hấp cấp tính | □ Có □ Không □ Không rõ | |||||||||
| 17.c. Là đối tượng trong chùm ca bệnh (2 hoặc nhiều người tiếp xúc gần với nhau) của 1 bệnh hô hấp cấp tính chưa rõ nguyên nhân. | □ Có □ Không □ Không rõ | |||||||||
| 17.d. Giết mổ, chăm sóc, tiếp xúc với một trong những động vật sau: |
| |||||||||
| • Lợn (heo) | □ Có □ Không □ Không rõ | |||||||||
| • Gia cầm, chim | □ Có □ Không □ Không rõ | |||||||||
| • Động vật ăn cỏ (trâu, bò, dê, cừu,…) | □ Có □ Không □ Không rõ | |||||||||
| • Các loài khác (ghi rõ): | □ Có □ Không □ Không rõ | |||||||||
Ghi chú: .............................................................................................................................................................................
| Định nghĩa ca bệnh SARI: Trường hợp nhiễm trùng đường hô hấp cấp tính nặng (SARI) với đầy đủ các triệu chứng sau: • Tiền sử sốt hoặc sốt với nhiệt độ đo được ≥ 38 C°; và • Ho: và • Khởi phát trong vòng 10 ngày; và • Yêu cầu nhập viện (Bệnh nhân nội trú). |
| Danh sách bệnh mạn tính tham khảo: • Bệnh đường hô hấp mạn tính: Bệnh phổi tắc nghẽn mạn tính (COPD), viêm phế quản mạn, khi phế thũng, giãn phế quản, xơ nang, bệnh bụi phổi, hội chứng loạn sàn phối- phế quản. • Bệnh tim mạch mạn tính: bệnh tim bẩm sinh, bệnh cơ tim do tăng huyết áp kéo dài, suy tim mạn, bệnh tim thiếu máu cục bộ • Bệnh thần kinh / thần kinh - cơ mạn tính: đột quỵ, bệnh thần kinh cơ liên quan đến suy yếu chức năng hô hấp, bại não, nhược cơ. |
| *Nghề nghiệp |
| **Chẩn đoán nhập viện: | ||
| 1. | Nhân viên văn phòng |
| 1. | Sốt chưa rõ nguyên nhân |
| 2. | Nhân viên y tế |
| 2. | Viêm phổi |
| 3. | Cán bộ thú y |
| 3. | Viêm phế quản |
| 4. | Làm nông/lâm nghiệp |
| 4. | Viêm tiểu phế quản |
| 5. | Chăn nuôi |
| 5. | Bệnh phổi tắc nghẽn mạn tính |
| 6. | Làm việc tại chợ |
| 6. | Hội chứng nhiễm trùng đường hô hấp cấp tính nặng (SARI) |
| 7. | Lái xe |
| 7. | Cúm |
| 8. | Công nhân |
| 8. | Lao |
| 9. | Nhân viên nhà hàng |
| 9. | Hen |
| 10. | Sinh viên, học sinh |
| 10. | Bệnh tim mạch mạn tính |
| 11. | Nghỉ hưu |
| 11. | Tăng huyết áp |
| 12. | Khác (ghi rõ): |
| 12. | Ung thư |
|
|
|
| 13. | Hội chứng nhiễm trùng |
|
|
|
| 14. | HIV/AIDS |
|
|
|
| 15. | Đái tháo đường |
|
|
|
| 16. | Đột quỵ |
|
|
|
| 17. | Viêm dạ dày ruột |
|
|
|
| 18. | Sốt xuất huyết |
|
|
|
| 19. | Sốt rét |
|
|
|
| 20. | Thương hàn |
|
|
|
| 21. | Suy dinh dưỡng |
|
|
|
| 22. | Thiếu máu |
|
|
|
| 23. | Khác (ghi rõ): |
| Khoa:………………………….. | Bệnh viện……………………………………. | Mẫu 2A |
BÁO CÁO TUẦN CỦA KHOA
(Lưu tại khoa giám sát)
(Tuần …………từ thứ hai, ngày ……/…… /20……. đến chủ nhật, ngày…. / …../20……. )
1. TỔNG HỢP SỐ BỆNH NHÂN NHẬP VIỆN VÀ TỬ VONG
| Ngày | Tổng số nhập viện tại khoa | Tổng số SARI nhập viện tại khoa | Tổng số SARI tử vong tại khoa | Tổng số tử vong do các nguyên nhân khác tại khoa | Tổng số được lấy mẫu tại khoa | |||||
| Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | |
| Thứ 2 |
|
|
|
|
|
|
|
|
|
|
| Thứ 3 |
|
|
|
|
|
|
|
|
|
|
| Thứ 4 |
|
|
|
|
|
|
|
|
|
|
| Thứ 5 |
|
|
|
|
|
|
|
|
|
|
| Thứ 6 |
|
|
|
|
|
|
|
|
|
|
| Thứ 7 |
|
|
|
|
|
|
|
|
|
|
| Chủ nhật |
|
|
|
|
|
|
|
|
|
|
| Tổng số |
|
|
|
|
|
|
|
|
|
|
2. DANH SÁCH BỆNH NHÂN SARI ĐƯỢC LẤY MẪU
| STT | Mã số SARI | Họ tên bệnh nhân | Tuổi | Ngày khởi phát | Ngày nhập viện | Ngày lấy mẫu | |
| Nam | Nữ | ||||||
| 1 |
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
| 4 |
|
|
|
|
|
|
|
| 5 |
|
|
|
|
|
|
|
| 6 |
|
|
|
|
|
|
|
| 7 |
|
|
|
|
|
|
|
| 8 |
|
|
|
|
|
|
|
| 9 |
|
|
|
|
|
|
|
| 10 |
|
|
|
|
|
|
|
Ngày báo cáo: ……../ …../20……
Người làm báo cáo
| Bệnh viện……………………………………. |
| Mẫu 2B |
BÁO CÁO TUẦN CỦA BỆNH VIỆN
(Chuyển về Viện VSDT/ Pasteur trước 16h00 ngày thứ Ba tuần kế tiếp)
(Tuần …………từ thứ hai, ngày ……/…… /20……. đến chủ nhật, ngày…. / …../20……. )
1. TỔNG HỢP SỐ BỆNH NHÂN NHẬP VIỆN VÀ TỬ VONG
| Khoa | Tổng số nhập viện theo khoa | Tổng số SARI nhập viện theo khoa | Tổng số SARI tử vong theo khoa | Tổng số tử vong do các nguyên nhân khác theo khoa | Tổng số được lấy mẫu theo khoa | |||||
| Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. DANH SÁCH BỆNH NHÂN SARI ĐƯỢC LẤY MẪU
| STT | Mã số SARI | Họ tên bệnh nhân | Tuổi | Ngày khởi phát | Ngày nhập viện | Ngày lấy mẫu | |
| Nam | Nữ | ||||||
| 1 |
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
| 4 |
|
|
|
|
|
|
|
| 5 |
|
|
|
|
|
|
|
| 6 |
|
|
|
|
|
|
|
| 7 |
|
|
|
|
|
|
|
| 8 |
|
|
|
|
|
|
|
| 9 |
|
|
|
|
|
|
|
| 10 |
|
|
|
|
|
|
|
Ngày báo cáo: ……../ …../20……
Người làm báo cáo
|
|
| Mẫu 3 |
PHIẾU YÊU CẦU XÉT NGHIỆM
VÀ TRẢ LỜI KẾT QUẢ XÉT NGHIỆM BỆNH NHÂN SARI
Mã số bệnh nhân: SARI_ _/_ _/_ _/_ _ _
Họ và tên:....................................................................................................................
Ngày, tháng, năm sinh: _ _/_ _/_ _ _Tuổi (năm)____ Tuổi theo tháng (nếu dưới 24 tháng)_____
Giới: □ Nam □ Nữ
Điện thoại liên lạc: .......................................................................................................
Địa chỉ: Số nhà/số phòng: ………………………..Xã/phường: .........................................
Quận/huyện: ……………………………………….Tỉnh, thành phố: .....................................
Ngày nhập viện: _ _/_ _/20___ (ngày/tháng/năm)
Ngày khởi phát: _ _/_ _/20___ (ngày/tháng/năm)
Ngày lấy mẫu: _ _/_ _/20___ (ngày/tháng/năm)
Loại bệnh phẩm (khoanh tròn vào số thích hợp):
1. Dịch ngoáy họng 2. Dịch ngoáy mũi 3. Dịch nội khí quản 4. Khác (ghi rõ)……….
Nơi lấy mẫu: ...............................................................................................................
| Bác sỹ yêu cầu xét nghiệm (ký, họ tên) | Người lấy mẫu (ký, họ tên) |
Số điện thoại của bác sỹ yêu cầu xét nghiệm: ................................................................
KẾT QUẢ XÉT NGHIỆM
Viện VSDT/Pasteur: .....................................................................................................
Mã số bệnh nhân: SARI_ _/_ _/_ _/_ _ _
Ngày nhận bệnh phẩm: _ _/_ _/20___ (ngày/tháng/năm)
Tình trạng bệnh phẩm: □ Tốt □ Không tốt □ Từ chối xét nghiệm (lý do:………………)
Ngày xét nghiệm: _ _/_ _/20___ (ngày/tháng/năm)
| Kết quả: | □ A/H1N1/2009 đại dịch | □ A/H3 | □ A/H5 | □ A/H7 | |
|
| □ Cúm B | □ Vi rút Adeno | □ Vi rút cúm khác chưa định được týp | ||
|
| □ HMPV | □ PIV 1 | □ PIV 2 | □ PIV 3 | □ Vi rút Rhino |
|
| □ RSV | □ Âm tính với tất cả các vi rút đường hô hấp được xét nghiệm | |||
| Cán bộ xét nghiệm | ………., ngày….. tháng….. năm ... |
|
| Mẫu 4 |
| Tên Viện VSDT/Pasteur:………………….. Tên khoa/phòng:………………………… | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
| Ngày …. tháng … năm 20….. |
Kính gửi: ………………………………..
KẾT QUẢ XÉT NGHIỆM BỆNH NHÂN NHIỄM TRÙNG ĐƯỜNG HÔ HẤP CẤP TÍNH NẶNG
Từ ngày ……………….Đến …………………..
| STT | Mã số bệnh nhân | Họ và tên | Tuổi* | Giới | Ngày lấy mẫu | Ngày nhận mẫu | Kết quả xét nghiệm** | Ghi chú |
| 1 |
|
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
|
| 4 |
|
|
|
|
|
|
|
|
| 5 |
|
|
|
|
|
|
|
|
| 6 |
|
|
|
|
|
|
|
|
| 7 |
|
|
|
|
|
|
|
|
| 8 |
|
|
|
|
|
|
|
|
| 9 |
|
|
|
|
|
|
|
|
| 10 |
|
|
|
|
|
|
|
|
| Lưu ý: *Đối với trẻ em dưới 2 tuổi cần ghi rõ tháng tuổi ** Quy định viết tắt kết quả: A/H1N1pdm, A/H3N2, B, Cúm khác, Adv, HMPV, PIV1-3. RSV, RV, Âm tính. Kết quả đồng nhiễm ghi cụ thể từng tác nhân, cách nhau bằng dấu phẩy | ||||||||
| Người thực hiện xét nghiệm | Phụ trách phòng xét nghiệm |
|
| Mẫu 4 |
| Bệnh viện……………………………………………… Chương trình giám sát nhiễm trùng hô hấp cấp tính nặng
SỔ GIAO NHẬN Bệnh phẩm, Phiếu điều tra trường hợp bệnh, Báo cáo tuần
NĂM…………. |
|
| Mẫu 5 |
| Số thứ tự tuần | Thời gian thực hiện | Ngày giao - nhận | Số lượng bệnh phẩm | Số phiếu điều tra | Số báo cáo tuần của BV | Chữ ký và tên người giao | Chữ ký và tên người nhận | Ghi chú |
|
| Từ…………….. Đến ……………. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
| ||
|
| Từ…………….. Đến ……………. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
| ||
|
| Từ…………….. Đến ……………. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
| ||
|
| Từ…………….. Đến ……………. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
|
|
| Mẫu 6 |
| Bệnh viện………………………………………….. Chương trình giám sát nhiễm trùng hô hấp cấp tính nặng
SỔ QUẢN LÝ BỆNH PHẨM SARI KHOA……………………………………………………
NĂM……………. |
|
| Mẫu 6 |
THÔNG TIN BỆNH PHẨM SARI
TẠI KHOA…………………………………………………..
| STT | Mã số | Tên bệnh nhân | Ngày/tháng/năm | Loại mẫu | Người giao | Người nhận | ||
| Ngày lấy mẫu |
| |||||||
| Ngày giao mẫu | Dịch khí quản | Dịch hầu họng | ||||||
| 1 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 2 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 3 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 4 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 5 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 6 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 7 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 8 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 9 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
| 10 | SARI/__/__/__ |
| __/__/___ | __/__/___ |
|
|
|
|
|
| Mẫu 7 |
Tên Viện VSDT/Pasteur:………………………………………………………………
BÁO CÁO TUẦN SARI CỦA VIỆN VSDT/PASTEUR KHU VỰC
Tuần….. Năm 201...
Bảng 1: Báo cáo tổng hợp số bệnh nhân nhập viện, tử vong, lấy mẫu trong tuần…. (từ ngày…………. đến ngày……………….)
| STT | Tên Bệnh viện | Tổng số bệnh nhân nhập viện | Tổng số SARI nhập viện | Tổng số SARI tử vong | Tổng số tử vong do nguyên nhân khác | Tổng số mẫu được lấy | |||||
| Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | ||
| 1 |
|
|
|
|
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
|
|
|
|
| 4 |
|
|
|
|
|
|
|
|
|
|
|
| 5 |
|
|
|
|
|
|
|
|
|
|
|
|
| Tổng số |
|
|
|
|
|
|
|
|
|
|
Bảng 2: Báo cáo tổng hợp số bệnh nhân nhập viện, tử vong, lấy mẫu cộng dồn đến tuần………
| STT | Tên Bệnh viện | Tổng số bệnh nhân nhập viện | Tổng số SARI nhập viện | Tổng số SARI tử vong | Tổng số tử vong do nguyên nhân khác | Tổng số mẫu được lấy | |||||
| Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | Nam | Nữ | ||
| 1 |
|
|
|
|
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
|
|
|
|
| 4 |
|
|
|
|
|
|
|
|
|
|
|
| 5 |
|
|
|
|
|
|
|
|
|
|
|
|
| Tổng số |
|
|
|
|
|
|
|
|
|
|
Bảng 3: Kết quả xét nghiệm mẫu được lấy trong tuần……..(từ ngày……………..đến ngày……………)
| Tên bệnh viện | Số mẫu | Số mẫu dương tính với các vi rút cúm | A/ H1N1 pdm | A/ H3N2 | B | Các vi rút cúm khác | Số mẫu âm tính với các vi rút cúm | HMPV | Adv | P1 | P2 | P3 | RSV | RV | Đồng nhiễm | |||||||||||||
| # | # | % | # | % | # | % | # | % | # | % | # | # | % | # | % | # | % | # | % | # | % | # | % | # | % | # | % | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Tổng số |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Thông tin cụ thể về các trường (+) với các vi rút cúm khác (týp, số lượng):…………………………………………………………………………………..
Bảng 4: Kết quả xét nghiệm mẫu cộng dồn đến tuần………
| Tên bệnh viện | Số mẫu | Số mẫu dương tính với các vi rút cúm | A/ H1N1 pdm | A/ H3N2 | B | Các vi rút cúm khác | Số mẫu âm tính với các vi rút cúm | HMPV | Adv | P1 | P2 | P3 | RSV | RV | Đồng nhiễm | |||||||||||||
| # | # | % | # | % | # | % | # | % | # | % | # | # | % | # | % | # | % | # | % | # | % | # | % | # | % | # | % | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Tổng số |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. Số liệu bảng 1, 2 là số liệu ghi nhận tại các khoa giám sát, không bao gồm số liệu nhập viện, tử vong ở các khoa không tham gia giám sát
2. Bảng 3 là kết quả xét nghiệm các mẫu được lấy từ thứ Hai đến thứ Sáu
3. Các vi rút cúm khác: các vi rút cúm hiếm gặp bao gồm Cúm A(H5N1), (H7N9), các vi rút cúm chưa định được typ được ghi cụ thể về typ (nếu có) và số lượng
4. Vì 07 tác nhân ngoài cúm chỉ được làm xét nghiệm trên các mẫu âm tính với cúm nên không có đồng nhiễm giữa các tác nhân cúm và ngoài cúm
5. Các mẫu đồng nhiễm sẽ ghi vào cả ô đồng nhiễm và vào từng tác nhân đồng nhiễm. VD: 01 đồng nhiễm Adeno - RSV sẽ tính thành 01 Adeno, 01 RSV, 01 đồng nhiễm
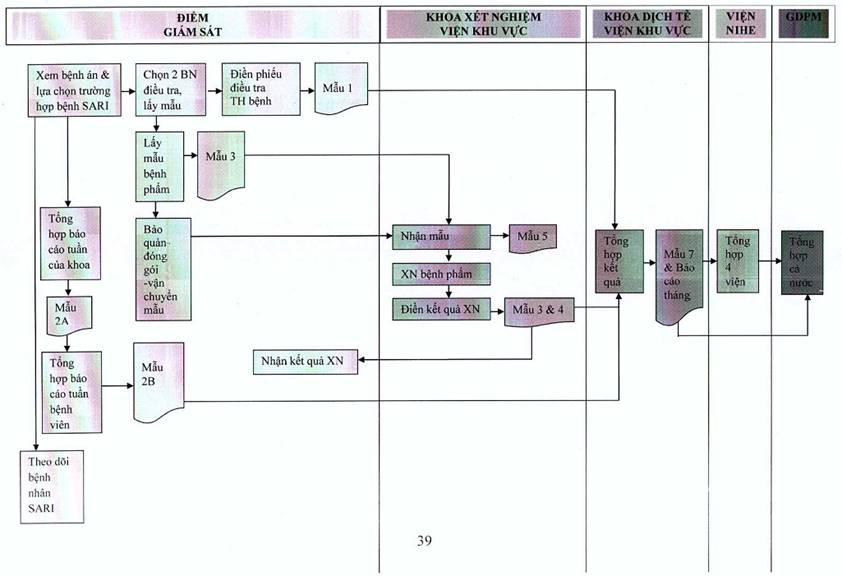
PHỤ LỤC 6:
SƠ ĐỒ QUY TRÌNH GIÁM SÁT SARI
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Quyết định 1271/QĐ-BYT PDF (Bản có dấu đỏ)
Quyết định 1271/QĐ-BYT PDF (Bản có dấu đỏ) Quyết định 1271/QĐ-BYT DOC (Bản Word)
Quyết định 1271/QĐ-BYT DOC (Bản Word)