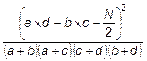- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 11397:2016 Vi sinh vật trong thực phẩm–Phát hiện E.coli O157:H7–Phương pháp 8h
| Số hiệu: | TCVN 11397:2016 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
2016 |
Hiệu lực:
|
Đang cập nhật |
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 11397:2016
Nội dung tóm tắt đang được cập nhật, Quý khách vui lòng quay lại sau!
Tải tiêu chuẩn Việt Nam TCVN 11397:2016
TIÊU CHUẨN VIỆT NAM
TCVN 11397:2016
VI SINH VẬT TRONG THỰC PHẨM - PHÁT HIỆN E.COLI O157:H7 - PHƯƠNG PHÁP 8 H
Microbiology of foods - Detection of E.coli O157:H7 - 8-hour method
Lời nói đầu
TCVN 11397:2016 được xây dựng trên cơ sở tham khảo AOAC 2000.13 Reveal for E. coli O157:H7 test system in selected foods. 8-hour method;
TCVN 11397:2016 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F13 Phương pháp phân tích và lấy mẫu biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
VI SINH VẬT TRONG THỰC PHẨM - PHÁT HIỆN E.COLI O157:H7 - PHƯƠNG PHÁP 8 H
Microbiology of foods - Detection of E.coli O157:H7 - 8 hour method
CẢNH BÁO - Escherichia coli O157 có thể gây một số bệnh nguy hiểm và có liều lây nhiễm thấp. Khả năng lây nhiễm trong phòng thử nghiệm đã ghi nhận.
Để đảm bảo an toàn cho nhân viên phòng thử nghiệm, phương pháp thử này phải được nhân viên có kinh nghiệm thực hiện sử dụng kỹ thuật thực hành phòng thử nghiệm tốt và tốt nhất là tiến hành trong thiết bị có khả năng bảo vệ. Phải tuân thủ các quy định an toàn có liên quan.
Hết sức thận trọng khi hủy bỏ tất cả các vật liệu đã bị lây nhiễm.
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp phát hiện E. coli O157:H7 trong thực phẩm bằng phương pháp 8 h.
Phương pháp này đã được đánh giá liên phòng thử nghiệm về việc xác nhận giá trị sử dụng trên các sản phẩm từ thịt bò và rau diếp. Xem Phụ lục A về thông tin chi tiết của kết quả đánh giá liên phòng.
2 Nguyên tắc
Phương pháp 8 h sử dụng môi trường tăng sinh (môi trường 8 h) và bộ thử kết tủa miễn dịch dòng chảy phụ nhanh để thu đưực kết quả chỉ trong tổng thời gian thử nghiệm 8 h. Môi trường 8 h cung cấp các chất dinh dưỡng có sẵn và các yếu tố khác cần thiết cho sự sinh trưởng và phát triển nhanh của E. coli O157: H7 đến mức phát hiện bằng thiết bị này chỉ trong 8 h. Bộ thử có chứa sẵn kháng thể có độ đặc hiệu cao đối với các kháng nguyên E. coli O157:H7. Các kháng thể này được liên kết với vàng keo (colloidal gold) và riêng rẽ với nền mẫu hỗ trợ đặc. Phần mẫu thử đã tăng sinh được đặt vào cổng mẫu của dòng chảy ban đầu qua thiết bị. Mọi kháng nguyên E. coli O157:H7 có mặt sẽ liên kết với các kháng thể cộng hợp vàng tạo thành phức kháng nguyên-kháng thể-nhiễm sắc thể. Phức này chảy qua màng dòng chảy phụ và sau đó liên kết bởi kháng thể được giữ cố định trên màng tạo ra cộng hợp vàng dạng kết tủa tạo thành một vạch nhìn thấy được là phản ứng dương tính. Phép thử được xác nhận là hợp lệ khi vạch đối chứng xuất hiện phía trên ô đọc kết quả sau khi kết thúc phép thử. Nếu không thấy vạch đối chứng thì phép thử không có hiệu lực.
3 Môi trường và thuốc thử
Chỉ sử dụng thuốc thử loại tinh khiết phân tích và sử dụng nước cất đã khử ion hoặc nước có chất lượng tương đương, trừ khi có quy định khác.
3.1 Môi trường 8 h dùng cho E. coli O157:H7, đã chuẩn bị sẵn (một chai dùng cho một phép thử), có bán sẵn từ Công ty Neogen Corp, Lansing, MI, Hoa Kỳ 1).
Chuyển hết lượng chứa trong chai sang vật chứa vô trùng. Thêm 225 ml nước vô trùng ở 43 oC. Trộn đều môi trường, thêm nước để có nồng độ 39,6 g/l và trộn đều.
3.2 Bộ thử E. coli O157:H7, một bộ thử dùng cho một mẫu, có sẵn từ hãng Neogen Corp 1).
3.3 Chất pha loãng đệm phosphat Butterfield (BPB)
Trộn 34,0 g monokali phosphat trong 500 ml nước. Chỉnh pH đến 7,2 bằng dung dịch natri hydroxit 1 M (40 g/l). Pha loãng đến 1 lít bằng nước. Hấp 15 min trong nồi hấp áp lực ở 121 oC. Cho 1,25 ml dung dịch này vào bình định mức 1 lít (4.8) vô trùng và thêm nước đến vạch.
3.4 Thạch phát hiện E. coli gây xuất huyết đường ruột (HC)
3.4.1 Thành phần
| Trypton | 20,0 g |
| Muối mật số 3 | 1,12 g |
| Natri clorua | 5,0 g |
| Sorbitol | 20,0 g |
| Thuốc thử 4-methylumbelliferyl-β-D-glucuronide (MUG) | 0,1 g |
| Bromocresol tía | 0,015 g |
| Thạch | 15,0 g |
| Nước | 1,0 lít |
3.4.2 Chuẩn bị
Hòa tan các thành phần trong nước bằng cách đun nóng có khuấy.
Hấp 15 min trong nồi hấp áp lực ở 121 o C. pH cuối cùng phải là 7,2 ± 0,2.
3.5 Môi trường thạch sinh màu Biosynth (BCM) O157:H7(+), có sẵn từ Biosynth International, Inc (1665 W. Quincy Ave, Suite 155, Naperville, IL 60504, Hoa Kỳ)1)
3.5.1 Thành phần
| BCM O157: H7(+) | 80,0 g |
| N,N-dimethylformamide (DMF, Sigma, Cat. No. D4254.)1) | 5,0 ml |
| Natri novobiocin (dung dịch 0,2 %, Sigma, Cat. No. N1628.)1) | 5,0 ml |
| Kali tellurit (dung dịch 0,1 %, Sigma, Cat. No. P0677.)1) | 0,2 ml |
| Nước | 1 lít |
3.5.2 Chuẩn bị
Cho DMF vào nước cất, sau đó thêm bột BCM và đun sôi để hòa tan. Chỉnh pH đến 6,8 ± 0,1. Không hấp áp lực. Làm nguội đến nhiệt độ từ 50 oC đến 55 oC trong nồi cách thủy. Lọc qua xyranh (4.3) để khử trùng novobiocin và kali tellurit riêng rẽ và bổ sung vào môi trường một cách vô trùng.
3.6 Môi trường CHROMagar™ O157, có sẵn từ CHROMagar Microbiology (Paris, Pháp)1)
3.6.1 Thành phần
| CHROMagar O157 | 29,2 g |
| Nước | 1 lít |
3.6.2 Chuẩn bị
Hòa bột từ từ vào trong nước bằng cách xoay bình. Đun đến sôi (100 oC) trong khi vẫn xoay bình và thỉnh thoảng khuấy. Nếu sử dụng nồi hấp áp lực, thì không dùng áp lực. Không làm nóng quá 100 oC. Làm nguội đến khoảng 45 oC đến 50 oC trong nồi cách thủy.
3.8 Dung dịch natri hydroxit (NaOH), 1 M
4 Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ thông thường của phòng thử nghiệm và cụ thể các thiết bị, dụng cụ sau:
4.1 Tủ ấm, có thể duy trì nhiệt độ từ 36 oC đến 38 oC và từ 42 oC đến 43 oC
4.2 Nồi cách thủy, có thể duy trì nhiệt độ ở 100 oC ± 5 oC
4.3 Xyranh, được trang bị bộ lọc cỡ lỗ nhỏ hơn hoặc bằng 0,45 μm.
4.4 Ống nghiệm, kích thước 16 mm x 100 mm bằng thủy tinh bo silicat.
4.5 Pipet.
4.6 Micropipet, có thể phân phối chính xác 0,12 ml.
4.7 Túi nhu động.
4.8 Bình định mức, dung tích 1 lít.
4.9 Bình nón, dung tích 500 ml, có nắp vặn.
5 Cách tiến hành
5.1 Chuẩn bị huyền phù mẫu thử
5.1.1 Đối với rau
Cắt mẫu rau một cách vô trùng và chuyển 50 g sang túi vô trùng. Thêm 50 ml chất pha loãng BPB (3.3), đóng nắp túi và lắc bằng tay 15 min. Gạn lấy 25 ml cho vào bình nón 500 ml (4.9) có chứa sẵn 225 ml môi trường 8 h (3.1). Nới lỏng nắp bình, lắc nhẹ để trộn và ủ 8 h ở 42 oC đến 43 oC trong tủ ấm (4.1). Lấy 5 ml môi trường cho vào ống nghiệm (4.4). Đặt ống nghiệm vào nồi cách thủy (4.2) ở 100 oC trong 10 min. Làm nguội đến nhiệt độ phòng.
5.1.2 Đối với thịt nguyên liệu và thịt xay
Cân vô trùng khoảng 25,0 g phần mẫu thử cho vào túi nhu động (4.7) có chứa sẵn 225 ml môi trường 8 h (3.1). Bóp bằng tay để trộn đều và ủ 8 h ở nhiệt độ từ 42 oC đến 43 oC trong tủ ấm (4.1).
Đối với mẫu thử là khối thịt nguyên liệu hoặc khối thịt xay có khối lượng 375 g, cân vô trùng 375 g phần mẫu thử cho vào vật chứa vô trùng có dung tích thích hợp. Thêm 3,375 lít môi trường 8 h (3.1) đã làm ấm đến nhiệt độ 42 oC ± 1 oC. Bóp bằng tay để trộn đều và ủ 12 h ở nhiệt độ 42 oC ± 1 oC trong tủ ấm (4.1).
Đối với cả hai trường hợp nêu trên, sau khi ủ, chuyển 5 ml mới trường vào ống nghiệm (4.4). Đặt ống nghiệm vào nồi cách thủy (4.2) ở 100 oC trong 10 min. Làm nguội đến nhiệt độ phòng.
5.2 Xác định
Mở túi chứa bộ thử (3.2). Sử dụng một bộ thử cho mỗi phép thử. Dùng pipet (4.6) chuyển 0,12 ml chủng cấy đã xử lý nhiệt từ ống nghiệm đã chuẩn bị trong 5.1, đưa mẫu vào cổng của bộ thử. Ủ 15 min ở nhiệt độ phòng.
5.3 Đọc kết quả
Kiểm tra bộ thử ngay sau khi phát triển được 15 min.
Kết quả dương tính nếu trong ô đọc kết quả của bộ thử có 2 vạch khác nhau: một vạch trong vùng phía dưới gần với vạch thử "T" và một vạch trong vùng phía trên gần với vạch đối chứng "C". Các vạch có màu đen tương phản trên nền trắng.
Kết quả âm tính nếu chỉ có một vạch duy nhất trong vùng phía trên (vùng đối chứng) trong ô đọc kết quả.
Kết quả không hợp lệ nếu không có vạch nào trong vùng phía trên (vùng đối chứng) của ô đọc kết quả, cho dù vẫn có một vạch trong vùng phía dưới (vùng thử nghiệm).
5.4 Khẳng định kết quả
Phép thử dương tính giả định (xem 5.3) phải được khẳng định.
a) Đối với mẫu thử là rau, thịt nguyên liệu và thịt xay
Chuẩn bị các dung dịch pha loãng thích hợp từ chủng cấy tăng sinh trong môi trường 8 h và dàn đều vào thạch HC (3.4) và thạch BCM (3.5). Các khuẩn lạc âm tính với thuốc thử sorbitol và MUG được phân lập từ thạch HC cần được khẳng định về mặt huyết thanh học với các kháng huyết thanh O157 và H7.
b) Đối với mẫu thử là khối thịt nguyên liệu hoặc khối thịt xay có khối lượng 375 g
Cấy đĩa các chủng cấy tăng sinh trong môi trường 8 h vào môi trường CHROMagar™ O157 (3.6) và ủ 24 h ± 1 h ở nhiệt độ 37 oC ± 1 oC trong tủ ấm (4.1). Các khuẩn lạc E. coli O157:H7 sẽ có màu tím hoa cà trong khi các vi khuẩn coliform khác có màu xanh, màu xám hoặc không màu. Tiếp tục thực hiện phép thử khẳng định về mặt huyết thanh học.
Khuẩn lạc nghi ngờ được khẳng định nếu đáp ứng ít nhất một trong các tiêu chí sau:
- dương tính với phép thử sinh độc tố Shiga (ST);
- dương tính với phép thử gen độc tố Shiga “stx”;
- được xác định về gen là “H7”.
6 Báo cáo thử nghiệm
Báo cáo thử nghiệm ít nhất phải bao gồm các thông tin sau đây:
a) mọi thông tin cần thiết để nhận biết đầy đủ về mẫu thử;
b) phương pháp thử đã sử dụng, viện dẫn tiêu chuẩn này;
c) kết quả thử nghiệm;
d) ngày kết thúc thử nghiệm;
e) mọi chi tiết thao tác không được quy định trong tiêu chuẩn này hoặc những điều được coi là tùy chọn có thể ảnh hưởng đến kết quả.
Phụ lục A
(Tham khảo)
Kết quả của phép thử liên phòng thử nghiệm
Bảng A.1 - Kết quả của phép thử liên phòng thử nghiệm đối với E. coli O157:H7 trên rau diếp và sản phẩm thịt bò
| Mẫu | Mức | MPN/g | Tổng số mẫu | Kết quả dương tính trên Hệ thống thử 8 h | X2 c | Độ nhạyd, % | Tỷ lệ âm tính giảe, % | Độ đặc hiệuf, % | Tỷ lệ dương tính giảg % | |||||
| Giả địnha | Khẳng địnhb | Thử 8 h | Đối chứng | Thử 8 h | Đối chứng | Thử 8 h | Đối chứng | Thử 8 h | Đối chứng | |||||
| Rau diếp | Thấp | 0,03 | 75 | 48 | 46 | 0,17 | 61,3 | 57,3 | 38,7 | 42,7 | - | - | - | - |
| Cao | 1,1 | 75 | 59 | 52 | 0,54 | 69,3 | 76 | 30,7 | 24 | - | - | - | - | |
| Đối chứng |
| 75 | 1 | 0 | 0 | - | - | - | - | 100 | 100 | 0 | 0 | |
| Thịt bò nguyên liệu | Thấp | 0,24 | 70 | 55 | 48 | 15,4 | 68,6 | 32,9 | 31,4 | 67,1 | - | - | - | - |
| Cao | 2,92 | 70 | 67 | 63 | 21,46 | 90,0 | 50 | 10,0 | 50 | - | - | - | - | |
| Đối chứng |
| 70 | 1 | 0 | 0 | - | - | - | - | 100 | 100 | 0 | 0 | |
| Thịt bò xay nguyên liệu | Thấp | 0,07 | 75 | 67 | 56 | 0,8 | 74,7 | 66,7 | 25,3 | 33,3 | - | - | - | - |
| Cao | 0,28 | 75 | 74 | 72 | 3,86 | 96,0 | 85,3 | 4,0 | 14,7 | - | - | - | - | |
| Đối chứng |
| 75 | 8 | 0 | 0 | - | - | - | - | 100 | 100 | 0 | 0 | |
| CHÚ DẪN: MPN: Số đơn vị hình thành khuẩn lạc có xác suất lớn nhất, tính theo CFU/g (giới hạn tin cậy 95 %). a) Bộ thử cho kết quả dương tính với canh thang tăng sinh 8 h. b) Các chủng cấy tăng sinh của mẫu dương tính giả định được khẳng định theo 5.4a c) Khi bình phương đối với hai mẫu độc lập: X2 = N x Trong đó: a: là số mẫu dương tính trong phép thử 8 h, b: là số mẫu dương tính trong phép thử khẳng định (5.4), c: là số mẫu âm tính trong phép thử 8 h, d: là số mẫu dương tính trong phép thử khẳng định (5.4), N: là tổng số mẫu đã thử với cả hai phương pháp. Giá trị X2 > 3,84 cho thấy sự khác biệt đáng kể ở mức xác suất 5 %. d) Độ nhạy là tỉ lệ phần trăm của tổng số phần mẫu thử dương tính với phép thử khẳng định (5.4) so với tổng số mẫu cấy. e) Tỷ lệ âm tính giả bằng (100 - độ nhạy). Số phép thử dương tính khẳng định là thấp sẽ cho tỷ lệ âm tính giả cao. f) Độ đặc hiệu là tỉ lệ phần trăm của tổng số phần mẫu thử âm tính với phép thử khẳng định (5.4) so với tổng số mẫu chưa cấy. Có thể tính trên số mẫu đối chứng chưa cấy. g) Tỷ lệ âm dương giả bằng (100 - độ đặc hiệu). | ||||||||||||||
Bảng A.2 - Kết quả của phép thử liên phòng thử nghiệm đối với E. coli O157:H7 trên mẫu sản phẩm thịt bò có khối lượng 375 g
| Mẫu | Chủng | MPN/ga | MPN/ phần mẫu thử (375 g)a | Tổng số mẫu | Kết quả trên Hệ thống thử 8 h | X 2 d | Thử 8 h | ||||
| Giả địnhb | Khẳng địnhc | Độ nhạye, % | Tỷ lệ âm tính giảf, % | Độ đặc hiệug, % | Tỷ lệ dương tính giảh, % | ||||||
| Thịt bò xay nguyên liệu | ATCC 35150 | 0,015 | 5,6 (1,4-16) | 20 | 19 | 19 | 3,06 | 100 | 0 | - | - |
| <0,003 | <1,1 (0-3,6) | 5 | 0 | 0 | - | - | - | 100 | 0 | ||
| Thịt bò nguyên liệu | ATCC 43895 | <0,003 | <1,1 | 20 | 18 | 18 | 3,49 | 100 | 0 | - | - |
| <0,003 | <1,1 | 5 | 0 | 0 | - | - | - | 100 | 0 | ||
| CHÚ DẪN: a) MPN: Số đơn vị hình thành khuẩn lạc có xác suất lớn nhất, tính theo CFU/g hoặc CFU/375 g (giới hạn tin cậy 95 %). b) Bộ thử cho kết quả dương tính không được khẳng định tiếp theo. c) Bộ thử cho kết quả dương tính được khẳng định tiếp theo. d) Khi bình phương đối với hai mẫu độc lập: X2 = (N - 1) x Trong đó: a: là số mẫu dương tính trong phép thử 8 h, b: là số mẫu âm tính trong phép thử 8 h, c: là số mẫu dương tính trong phép thử khẳng định (5.4), d: là số mẫu dương tính trong phép thử khẳng định (5.4), N: là tổng số mẫu đã thử với cả hai phương pháp. Giá trị X2 > 3,84 cho thấy sự khác biệt đáng kể ở mức xác suất 5 %. e) Độ nhạy là tỉ lệ phần trăm của tổng số phần mẫu thử dương tính với phép thử khẳng định (5.4) so với tổng số mẫu cấy. f) Tỷ lệ âm tính giả bằng (100 - độ nhạy). g) Độ đặc hiệu là tỉ lệ phần trăm của tổng số phần mẫu thử âm tính với phép thử 8 h so với tổng số mẫu âm tính. Có thể tính trên số mẫu đối chứng chưa khẳng định. h) Tỷ lệ âm dương giả bằng (100 - độ đặc hiệu). | |||||||||||
Thư mục tài liệu tham khảo
[1] United States Food and Drug Administration - Center for Food Safety & Applied Nutrition, Bacteriological Analytical Manual, Chapter 4 : Escherichia coli and the Coliform Bacteria, 2001
[2] United States Department of Agriculture - Food Safety and Inspection Service (FSIS), Office of Public Health Science, MLG 5.09 Detection, Isolation and Identification of Escherichia coli O157:H7 from Meat Products and Carcass and Environmental Sponges, 2015
1) Ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra nhằm tạo thuận lợi cho người sử dụng tiêu chuẩn và không ấn định sử dụng các sản phẩm này. Có thể sử dụng các sản phẩm tương tự nếu cho kết quả tương đương.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 11397:2016 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 11397:2016 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 11397:2016 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 11397:2016 DOC (Bản Word)