- Tổng quan
- Nội dung
- VB gốc
- Tiếng Anh
- Hiệu lực
- VB liên quan
- Lược đồ
-
Nội dung hợp nhất
Tính năng này chỉ có tại LuatVietnam.vn. Nội dung hợp nhất tổng hợp lại tất cả các quy định còn hiệu lực của văn bản gốc và các văn bản sửa đổi, bổ sung, đính chính... trên một trang. Việc hợp nhất văn bản gốc và những văn bản, Thông tư, Nghị định hướng dẫn khác không làm thay đổi thứ tự điều khoản, nội dung.
Khách hàng chỉ cần xem Nội dung hợp nhất là có thể nắm bắt toàn bộ quy định hiện hành đang áp dụng, cho dù văn bản gốc đã qua nhiều lần chỉnh sửa, bổ sung.
- Tải về
Quyết định 696/QĐ-QLD 2021 Sổ tay thực hành tại cơ sở bán lẻ thuốc
| Cơ quan ban hành: | Cục Quản lý Dược |
Số công báo:
Số công báo là mã số ấn phẩm được đăng chính thức trên ấn phẩm thông tin của Nhà nước. Mã số này do Chính phủ thống nhất quản lý.
|
Đang cập nhật |
| Số hiệu: | 696/QĐ-QLD | Ngày đăng công báo: | Đang cập nhật |
| Loại văn bản: | Quyết định | Người ký: | Tạ Mạnh Hùng |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
01/12/2021 |
Ngày hết hiệu lực:
Ngày hết hiệu lực là ngày, tháng, năm văn bản chính thức không còn hiệu lực (áp dụng).
|
Đang cập nhật |
|
Áp dụng:
Ngày áp dụng là ngày, tháng, năm văn bản chính thức có hiệu lực (áp dụng).
|
Đã biết
|
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
| Lĩnh vực: | Thực phẩm-Dược phẩm |
TÓM TẮT QUYẾT ĐỊNH 696/QĐ-QLD
Ngày 01/12/2021, Cục Quản lý Dược đã ra quyết định 696/QĐ-QLD về việc ban hành Sổ tay thực hành tại cơ sở bán lẻ thuốc.
Theo đó, sổ tay hướng dẫn kỹ năng thực hành cho người bán lẻ thuốc bao gồm các kỹ năng cơ bản trong giao tiếp thực hành tại cơ sở bán lẻ thuốc như: kỹ năng hỏi, kỹ năng lắng nghe, kỹ năng phản hồi, kỹ năng tư vấn/khuyên và các kỹ năng giao tiếp với một số đối tượng như: người cao tuổi, khách hàng khó tính, khách hàng trầm cảm.
Ngoài ra, nhằm hỗ trợ người bán lẻ thuốc, sổ tay còn hướng dẫn tư vấn đối với một số triệu chứng bệnh nhẹ thường gặp tại cộng đồng như: ho, cảm lạnh, táo bón, tiêu chảy.
Bên cạnh đó, một số quy trình thao tác chuẩn áp dụng tại cơ sở bán lẻ thuốc được đưa ra nhằm hướng dẫn cụ thể việc thực hiện các hoạt động tại cơ sở bán lẻ thuốc bao gồm: quy trình mua thuốc và kiểm soát thuốc; quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc phải kê đơn; quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc không kê đơn; quy trình bảo quản và theo dõi chất lượng thuốc; quy trình quản lý thuốc kiểm soát đặc biệt (thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất…)
Quyết định này có hiệu lực kể từ ngày ký.
Xem chi tiết Quyết định 696/QĐ-QLD có hiệu lực kể từ ngày 01/12/2021
Tải Quyết định 696/QĐ-QLD
| BỘ Y TẾ | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
| Số: 696/QĐ-QLD | Hà Nội, ngày 01 tháng 12 năm 2021 |
QUYẾT ĐỊNH
VỀ VIỆC BAN HÀNH SỔ TAY THỰC HÀNH TẠI CƠ SỞ BÁN LẺ THUỐC
____________
CỤC TRƯỞNG CỤC QUẢN LÝ DƯỢC
Căn cứ Luật Dược số 105/2016/QH13 ngày 06/4/2016;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 27/6/2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Căn cứ Quyết định số 7868/QĐ-BYT ngày 28/12/2018 của Bộ trưởng Bộ Y tế về việc quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Cục Quản lý Dược thuộc Bộ Y tế;
Theo đề nghị của Trưởng phòng Quản lý Kinh doanh Dược - Cục Quản lý Dược,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này Sổ tay thực hành tại Cơ sở bán lẻ thuốc.
Điều 2. Quyết định này có hiệu lực kể từ ngày ký ban hành.
Điều 3. Các Ông/Bà Chánh Văn phòng, Trưởng phòng Quản lý Kinh doanh Dược, Lãnh đạo các phòng, đơn vị thuộc Cục Quản lý Dược và Thủ trưởng các đơn vị có liên quan chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: | KT. CỤC TRƯỞNG |
SỔ TAY THỰC HÀNH
TẠI CƠ SỞ BÁN LẺ THUỐC
(Ban hành kèm theo Quyết định số 696/QĐ-QLD ngày 01/12/2021)
BAN SOẠN THẢO VÀ TỔ BIÊN TẬP SỔ TAY THỰC HÀNH TẠI CƠ SỞ BÁN LẺ THUỐC
(Ban hành theo Quyết định số 462/QĐ-QLD ngày 17/09/2020)
BAN SOẠN THẢO
1. Ông Vũ Tuấn Cường, Cục trưởng Cục Quản lý Dược - Bộ Y tế, Trưởng Ban soạn thảo;
2. Ông Tạ Mạnh Hùng, Phó Cục trưởng Cục Quản lý Dược - Bộ Y tế, Phó Trưởng Ban soạn thảo;
3. Ông Nguyễn Thanh Bình, Chủ tịch Hội đồng trường, Trường Đại học Dược Hà Nội, Phó Trưởng Ban;
4. Ông Cao Hưng Thái, Phó Cục trưởng Cục Quản lý Khám chữa bệnh - Bộ Y tế, Thành viên;
5. Bà Đinh Thị Thu Thủy, Phó Vụ trưởng Vụ Pháp chế - Bộ Y tế, Thành viên;
6. Bà Lục Thị Thu Hằng, Giám đốc Trung tâm dược điển, Thành viên;
7. Ông Nguyễn Văn Khải, Trưởng phòng Nghiệp vụ Dược, Sở Y tế thành phố Hà Nội, Thành viên;
8. Ông Lê Ngọc Danh, Phó trưởng Phòng Nghiệp vụ dược, Sở Y tế thành phố Hồ Chí Minh, Thành viên;
9. Bà Trịnh Thị Lê Trâm, Trưởng ban Tư vấn, phản biện, giám định xã hội, Tổng hội Y học Việt Nam, Thành viên;
10.Ông Nguyễn Vân Đình, Phó Chủ tịch Hội Dược học Việt Nam, Thành viên;
11.Ông Phan Công Chiến, Trưởng phòng Quản lý Kinh doanh Dược - Bộ Y tế, Thành viên;
12. Bà Nguyễn Minh Hoài, Phó trưởng phòng Quản lý Kinh doanh Dược - Bộ Y tế, Thành viên;
TỔ BIÊN TẬP XÂY DỰNG
1. Bà Nguyễn Minh Hoài, Phó trưởng phòng Quản lý Kinh doanh Dược - Bộ Y tế, Tổ trưởng;
2. Bà Lê Kim Dung, Chuyên viên Cục Quản lý Khám chữa bệnh - Bô Y tế, Thành viên;
3. Bà Trần Thị Xuân Hằng Chuyên viên Vụ Pháp chế- Bộ Y tế, Thành viên;
4. Ông Đỗ Xuân Thắng, Trưởng phòng Vật tư và Trang thiết bị, Trường Đại học Dược Hà Nội, Thành viên;
5. Bà Trần Thị Lan Anh, Giảng viên Bộ môn Quản lý và Kinh tế dược, Trường Đại học Dược Hà Nội, Thành viên;
6. Bà Nguyễn Thị Phương Thúy, Giảng viên Bộ môn Quản lý và Kinh tế dược, Trường Đại học Dược Hà Nội, Thành viên;
7. Bà Phan Thị Tố Như, Giảng viên Bộ môn Y học cơ sở, Trường Đại học Dược Hà Nội, Thành viên;
8. Ông Nguyễn Hoàng Anh, Giám đốc Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc, Trường Đại học Dược Hà Nội, Thành viên;
9. Bà Lê Hoàng Nhã, Chuyên viên phòng Nghiệp vụ Dược, Sở Y tế Tp. Hồ Chí Minh, Thành viên;
10. Bà Bùi Thanh Nguyệt, Chuyên viên phòng Quản lý Dịch vụ Y tế, Sở Y tế Tp. Hồ Chí Minh, Thành viên;
11. Ông Bùi Văn Xuân, Phó Trưởng phòng Quản lý HNYDTN, Sở Y tế Tp. Hà Nội, Thành viên;
12. Bà Lê Thị Thu Hiền, Cán bộ Trung tâm Dược điển- Dược thư Việt Nam, Thành viên;
13. Bà Đặng Thị Mỹ Hạnh, Cán bộ Tổng hội Y học Việt Nam, Thành viên;
14. Bà Lê Thị Minh Chính, UVBCH Hội Dược học Việt Nam, Thành viên
15. Ông Nguyễn Huy Ngọc, Chuyên gia Phòng Quản lý Kinh doanh Dược, Cục Quản lý Dược- Bộ Y tế ,Thành viên;
16. Bà Hoàng Phương Thảo, Chuyên gia phòng Quản lý Kinh doanh Dược, Cục Quản lý Dược - Bộ Y tế, Thành viên;
17. Ông Đỗ Minh Hùng, Chuyên viên Phòng Pháp chế- Thanh tra, Cục Quản lý Dược- Bộ Y tế, Thành viên;
18. Bà Trần Thị Thu Phương, Chuyên viên Phòng Quản lý Chất lượng thuốc, Cục Quản lý Dược - Bộ Y tế, Thành viên;
19. Bà Đặng Thị Huệ Minh, Chuyên viên phòng Quản lý Kinh doanh Dược, Cục Quản lý Dược- Bộ Y tế, Thư ký.
LỜI NÓI ĐẦU
Giai đoạn 2016-2020 đã chứng kiến nhiều đổi mới trong hệ thống quản lý Dược với việc ban hành Luật Dược sửa đổi năm 2016 và các văn bản quy phạm pháp luật khác liên quan. Trước yêu cầu đặt ra, cuốn tài liệu Sổ tay thực hành tại cơ sở bán lẻ thuốc được ra đời nhằm hướng dẫn cụ thể việc thực hiện các hoạt động tại cơ sở bán lẻ thuốc theo quy định hiện hành và nâng cao kỹ năng thực hành của người bán lẻ thuốc.
Cấu trúc của cuốn sổ tay thực hành tại cơ sở bán lẻ thuốc bao gồm 5 chương.
Chương 1. Vai trò của cơ sở bán lẻ thuốc và một số nguyên tắc trong thực hành dược cộng đồng
Chương 2. Kỹ năng thực hành cho người bán lẻ thuốc
Chương 3. Hướng dẫn tư vấn đối với một số triệu chứng bệnh/bệnh thường gặp tại cộng đồng
Chương 4. Hệ thống hóa một số văn bản quy phạm pháp luật liên quan hoạt động của cơ sở bán lẻ thuốc tại Việt Nam
Chương 5. Hướng dẫn quy trình thao tác chuẩn áp dụng tại cơ sở bán lẻ thuốc
Đây sẽ là tài liệu hữu ích đối với người bán lẻ thuốc tại các cơ sở bán lẻ thuốc để nâng cao chất lượng dịch vụ dược và triển khai các hoạt động tại cơ sở bán lẻ thuốc một cách hiệu quả, thống nhất, hướng tới đảm bảo cung ứng, sử dụng thuốc hợp lý, an toàn.
Thay mặt Cục Quản lý Dược, tôi xin chân thành cảm ơn các thành viên trong Ban soạn thảo cuốn Sổ tay thực hành dành cho người bán lẻ thuốc tại cơ sở bán lẻ thuốc, đặc biệt là các thành viên trong Tổ biên tập, các cán bộ của Cục Quản lý Dược, Vụ Pháp chế, Cục Quản lý Khám chữa bệnh và Trường Đại học Dược Hà Nội, Trung tâm Quốc gia về Thông tin thuốc và theo dõi phản ứng có hại của thuốc, Sở Y tế Tp.Hồ Chí Minh, Sở Y tế Tp.Hà Nội, Hội Dược học Việt Nam, Hội Y học Việt Nam, Trung tâm Dược điển-Dược thư Việt Nam. Với sự nỗ lực của các đồng nghiệp trong Ban soạn thảo, Tổ biên tập, cùng với những ý kiến góp ý của các chuyên gia, các Sở Y tế tỉnh/thành phố trên cả nước, các đồng nghiệp từ nhiều đơn vị khác nhau trong ngành Y tế cũng như các đơn vị liên quan đã góp phần quan trọng trong việc hoàn thiện cuốn tài liệu này.
Tuy đã dày công xây dựng nhưng lần đầu tiên ban hành cuốn tài liệu Sổ tay thực hành tại cơ sở bán lẻ thuốc khó tránh khỏi thiếu sót. Chúng tôi rất mong nhận được các ý kiến đóng góp để lần soạn thảo sau được hoàn thiện hơn. Mọi ý kiến đóng góp xin gửi về Ban biên soạn Cục Quản lý Dược.
Xin trân trọng cảm ơn.
|
| Vũ Tuấn Cường |
MỤC LỤC
LỜI NÓI ĐẦU
DANH MỤC CÁC KÝ HIỆU, CÁC CHỮ VIẾT TẮT
GIẢI THÍCH MỘT SỐ THUẬT NGỮ
CHƯƠNG 1. VAI TRÒ CỦA CƠ SỞ BÁN LẺ THUỐC VÀ
NGUYÊN TẮC ĐẠO ĐỨC HÀNH NGHỀ DƯỢC
1.1. Vai trò của cơ sở bán lẻ thuốc
1.2. Nguyên tắc đạo đức hành nghề dược tại Việt Nam
CHƯƠNG 2. KỸ NĂNG THỰC HÀNH CHO NGƯỜI BÁN LẺ THUỐC
2.1. Vai trò kỹ năng giao tiếp trong thực hành tại CSBLT
2.2. Kỹ năng cơ bản trong giao tiếp thực hành tại CSBLT
2.2.1. Kỹ năng hỏi
2.2.2. Kỹ năng lắng nghe
2.2.3. Kỹ năng phản hồi
2.2.4. Kỹ năng tư vấn/ khuyên
2.3. Kỹ năng giao tiếp với một số đối tượng
2.3.1. Người cao tuổi
2.3.2. Khách hàng khó tính
2.3.3. Khách hàng trầm cảm
CHƯƠNG 3. HƯỚNG DẪN TƯ VẤN ĐỐI VỚI ỘT SỐ TRIỆU CHỨNG BỆNH/BỆNH THƯỜNG GẶP TẠI CỘNG ĐỒNG
A. Ho (Cough)
B. Cảm lạnh (Common Cold)
C. Táo bón (Constipation)
D. Tiêu chảy (Diarrhoea)
CHƯƠNG 4. HỆ THỐNG HÓA MỘT SỐ VĂN BẢN QUY PHẠM PHÁP LUẬT LIÊN QUAN HOẠT ĐỘNG CỦA CƠ SỞ BÁN LẺ THUỐC TẠI VIỆT NAM
4.1. Quyền lợi, trách nhiệm của cơ sở bán lẻ thuốc (Điều 47 Điều 48 Luật dược)
4.2. Quyền lợi nghĩa vụ của người hành nghề dược (Điều 30, 31 Luật dược)
4.3. Hành vi nghiêm cấm (Điều 6- luật dược)
4.4. Một số văn bản quy phạm pháp luật liên quan hoạt động cơ sở bán lẻ thuốc
4.5. Một số yêu cầu trong hoạt động của cơ sở bán lẻ thuốc
4.5.1. Nhân sự ( Điều 18, Luật dược; Thông tư 02/2018/TT-BYT)
4.5.2. Cơ sở vật chất kỹ thuật của cơ sở bán lẻ (Thông tư 02/2018/TT-BYT)
4.5.3. Các hoạt động của cơ sở bán lẻ thuốc
4.6. Một số quy định xử phạt vi phạm hành chính liên quan tại cơ sở bán lẻ thuốc
CHƯƠNG 5. HƯỚNG DẪN QUY TRÌNH THAO TÁC CHUẨN (SOP) ÁP DỤNG TẠI CƠ SỞ BÁN LẺ THUỐC
5.1. Nguyên tắc xây dựng quy trình thao tác chuẩn
5.2. Hướng dẫn nội dung một số quy trình thao tác chuẩn áp dụng tại cơ sở bán lẻ thuốc
A. Quy trình mua thuốc và kiểm soát chất lượng thuốc
B. Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc phải kê đơn
C. Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc không kê đơn
D. Quy trình bảo quản và theo dõi chất lượng thuốc
E. Quy trình quản lý thuốc kiểm soát đặc biệt
E1. Quy trình quản lý thuốc kiểm soát đặc biệt (thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất)
E.2. Quy trình quản lý thuốc kiểm soát đặc biệt (Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực)
PHỤ LỤC
DANH MỤC CÁC KÝ HIỆU, CÁC CHỮ VIẾT TẮT
| STT | Chữ viết tắt | Viết đầy đủ | Giải thích |
| 1 | PTCM | Phụ trách chuyên môn |
|
| 2 | GPP | Good Pharmacy Practice | Thực hành tốt cơ sở bán lẻ thuốc |
| 3 | SOP | Standard Operating Procedures | Quy trình thao tác chuẩn |
| 4 | GN | Gây nghiện |
|
| 5 | HT | Hướng thần |
|
| 6 | TC | Tiền chất |
|
| 7 | ĐĐKKDD | Đủ điều kiện kinh doanh dược |
|
| 8 | TT | Thông tư |
|
| 9 | NĐ | Nghị định |
|
| 10 | CSBLT | Cơ sở bán lẻ thuốc |
|
GIẢI THÍCH THUẬT NGỮ
Hành nghề dược là việc sử dụng trình độ chuyên môn của cá nhân để kinh doanh dược và hoạt động dược lâm sàng (Khoản 36, Điều 2, Luật dược)
Danh mục thuốc không kê đơn là cơ sở để phân loại thuốc không kê đơn và thuốc kê đơn. Các thuốc không thuộc Danh mục thuốc không kê đơn được phân loại là thuốc kê đơn (Khoản 1, Điều 4, TT07/2017/TT-BYT ban hành danh mục thuốc không kê đơn).
Thuốc phải kiểm soát đặc biệt gồm: thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc phóng xạ, đồng vị phóng xạ, thuốc độc, thuốc/dược chất thuộc danh mục bị cấm sử dụng trong một số ngành, lĩnh vực (Khoản 26, Điều 2, Luật dược)
Thực hành tốt cơ sở bán lẻ thuốc là bộ nguyên tắc, tiêu chuẩn trong hành nghề tại cơ sở bán lẻ thuốc nhằm bảo đảm cung ứng, bán lẻ thuốc trực tiếp đến người sử dụng thuốc và khuyến khích việc sử dụng thuốc một cách an toàn và có hiệu quả cho người sử dụng thuốc.
Người bán lẻ thuốc là người phụ trách chuyên môn về dược và nhân viên làm việc tại cơ sở bán lẻ thuốc có bằng cấp chuyên môn được đào tạo về dược phù hợp với loại hình và phạm vi hoạt động của cơ sở.
Phản ứng có hại của thuốc (ADR) là các phản ứng không định trước, gây tác hại cho cơ thể khi sử dụng thuốc ở liều bình thường để điều trị, dự phòng hoặc chẩn đoán.
Chăm sóc dược (pharmaceutical care) là thực hành có trách nhiệm của người dược sỹ trong việc chăm sóc để tối ưu hóa việc sử dụng thuốc và cải thiện sức khỏe, nâng cao chất lượng sống cho người bệnh.
Cơ sở bán lẻ thuốc trong phạm vi tài liệu này được đề cập chỉ bao gồm nhà thuốc và quầy thuốc.
CHƯƠNG 1. VAI TRÒ CỦA CƠ SỞ BÁN LẺ THUỐC VÀ NGUYÊN TẮC ĐẠO ĐỨC HÀNH NGHỀ DƯỢC
1.1. Vai trò của cơ sở bán lẻ thuốc
Tại Việt Nam, hệ thống cơ sở bán lẻ thuốc trong cộng đồng là một trong những nơi đầu tiên người dân dễ dàng tiếp cận khi có vấn đề về sức khỏe. Có thể nói, các cơ sở bán lẻ thuốc trong cộng đồng đóng vai trò quan trọng trong chăm sóc sức khỏe ban đầu cho người dân. Chiến lược phát triển ngành Dược của Tổ chức Y tế thế giới và Liên đoàn Dược phẩm Quốc tế đã chỉ ra xu hướng của hoạt động thực hành dược là hướng tới việc sử dụng thuốc trên người bệnh được an toàn, hợp lý, hiệu quả và kinh tế trong đó thực hành dược trong cộng đồng đóng một vai trò quan trọng.
Dược cộng đồng (Community pharmacy) là hoạt động chăm sóc dược cho người dân thông qua hệ thống các cơ sở bán lẻ thuốc trong cộng đồng, được thực hiện bởi người dược sỹ và nhân viên cơ sở bán lẻ thuốc.
Dược sỹ cộng đồng (Community pharmacists) là người có chuyên môn dược trình độ đại học làm việc tại các cơ sở bán lẻ thuốc với nhiệm vụ cung cấp các thuốc theo đơn của bác sĩ và các thuốc không kê đơn một cách phù hợp. Hoạt động chuyên môn của dược sỹ cộng đồng tại cơ sở bán lẻ thuốc cũng bao gồm việc tư vấn các thông tin về thuốc kê đơn và thuốc không kê đơn cho người bệnh, nhân viên y tế và cộng đồng. Dược sỹ cộng đồng cũng có nhiệm vụ duy trì sự kết nối với các nhân viên y tế khác trong chăm sóc sức khỏe ban đầu cho người dân.
Mục tiêu của hoạt động dược cộng đồng là cung cấp dịch vụ dược có chất lượng từ các cơ sở bán lẻ thuốc và hỗ trợ người dân trong cộng đồng hướng tới sử dụng thuốc an toàn, hợp lý, hiệu quả và kinh tế trong việc phòng và chữa bệnh.
Theo Liên đoàn Dược phẩm Quốc tế (FIP), sứ mệnh của dược cộng đồng là nâng cao hiệu quả sử dụng thuốc và sức khỏe cho cộng đồng bằng việc cung cấp có chất lượng thuốc, các sản phẩm và dịch vụ y tế. Hơn nữa, xu hướng mới của hoạt động chăm sóc dược là việc hỗ trợ, thúc đẩy người bệnh trong cộng đồng tuân thủ điều trị và giảm thiểu các sai sót trong điều trị nhằm hướng tới việc sử dụng thuốc trên người bệnh được an toàn, hợp lý, hiệu quả và kinh tế. Để đảm bảo cải thiện và nâng cao việc sử dụng thuốc có trách nhiệm cho người bệnh cần có sự tham gia tích cực của dược sỹ cộng đồng. Theo đó, dược sỹ, người bán lẻ thuốc cần thể hiện được trách nhiệm của mình trong việc cung ứng thuốc có chất lượng, cùng với sự hướng dẫn và tư vấn phù hợp. Điều đó giúp cho người bệnh tuân thủ điều trị, sử dụng thuốc có trách nhiệm, hướng tới việc sử dụng thuốc hợp lý, an toàn và hiệu quả.
Theo Tổ chức Y tế thế giới (WHO), các hoạt động chuyên môn chính mà dược sỹ cộng đồng đảm nhận bao gồm:
● Xử trí các bệnh, triệu chứng thông thường
Dược sỹ cộng đồng hàng ngày tiếp nhận các yêu cầu của người dân về xử trí các triệu chứng, bệnh thông thường. Trong khả năng cho phép, dược sỹ, người bán lẻ thuốc sẽ cung cấp thuốc không kê đơn và những lời khuyên, hướng dẫn cho người bệnh để xử lý tình huống bệnh và nếu cần thiết có thể chuyển người bệnh tới các cơ sở y tế phù hợp. Trong một số trường hợp, dược sỹ, người bán lẻ thuốc có thể đưa ra lời khuyên về xử trí tình huống bệnh mà không cần dùng thuốc.
● Bán thuốc theo đơn
Dược sỹ cộng đồng có trách nhiệm kiểm tra tính hợp pháp, an toàn và phù hợp của đơn thuốc, kiểm tra thông tin người bệnh, cung cấp đầy đủ và chính xác số lượng thuốc cùng với thông tin hướng dẫn phù hợp để giúp người bệnh sử dụng thuốc được an toàn, hợp lý và hiệu quả. Ở nhiều quốc gia, dược sỹ cộng đồng là người ghi nhận tiền sử dùng thuốc và tiền sử bệnh của người bệnh và do vậy có thể cung cấp các thông tin cần thiết cho người kê đơn.
● Chăm sóc người bệnh
Dược sỹ cộng đồng thu thập thông tin về tiền sử dùng thuốc, đảm bảo người bệnh hiểu và nắm bắt thông tin về chế độ liều điều trị, đường dùng, những lưu ý về thuốc sử dụng, giám sát quá trình đáp ứng điều trị của người bệnh.
● Giám sát và tối ưu hóa việc sử dụng thuốc của người bệnh
Dược sỹ cộng đồng tham gia vào việc giám sát và thúc đẩy người bệnh trong cộng đồng tuân thủ điều trị, sử dụng đúng và đủ thuốc, giảm thiểu các sai sót trong điều trị, đảm bảo tối ưu hóa việc sử dụng thuốc.
● Tham gia vào các chương trình y tế thúc đẩy sức khỏe cộng đồng
Dược sỹ, người bán lẻ thuốc trong cộng đồng tham gia vào các chương trình y tế có liên quan tới thuốc nhằm thúc đẩy việc chăm sóc sức khỏe cộng đồng ở cấp độ địa phương và quốc gia như là: sử dụng thuốc hợp lý an toàn, hạn chế sử dụng thuốc trong quá trình mang thai, kế hoạch hóa gia đình, chương trình phòng chống lao, HIV. Họ cũng tham gia vào việc thúc đẩy phòng bệnh cho cộng đồng như vệ sinh an toàn thực phẩm, tiêm chủng, chương trình phòng chống sốt rét.
Để thực hiện được những vai trò đó, dược sỹ nói riêng và người bán lẻ thuốc nói chung (bao gồm người phụ trách về chuyên môn, nhân viên cơ sở bán lẻ phải đảm bảo được 7 nguyên tắc thực hành dược cơ bản sau (theo Liên đoàn Dược phẩm Quốc tế):
- Nguyên tắc 1: Lấy người bệnh làm trung tâm.
- Nguyên tắc 2: Ra quyết định dựa trên quyền lợi của người bệnh và cộng đồng.
- Nguyên tắc 3: Tôn trọng người bệnh và đồng nghiệp.
- Nguyên tắc 4: Khuyến khích người bệnh và cộng đồng tham gia vào quá trình lựa chọn liệu pháp chăm sóc, điều trị phù hợp.
- Nguyên tắc 5: Không ngừng nâng cao kiến thức, năng lực bản thân.
- Nguyên tắc 6: Trung thực và tin cậy.
- Nguyên tắc 7: Hành nghề một cách có trách nhiệm.
Như vậy, cơ sở bán lẻ thuốc và người bán lẻ thuốc đóng vai trò quan trọng trong chăm sóc sức khoẻ ban đầu cho người dân trong cộng đồng. Cụ thể, người bán lẻ thuốc ngày càng đóng vai trò lớn hơn trong việc nâng cao hiệu quả của việc sử dụng thuốc, cung cấp cho người bệnh những dịch vụ dược chất lượng cao liên quan đến sử dụng thuốc. Có thể nói, hoạt động hành nghề của người bán lẻ thuốc đang chuyển dịch dần từ xu hướng lấy sản phẩm làm trung tâm sang xu hướng lấy người bệnh làm trung tâm.
1.2. Nguyên tắc đạo đức hành nghề dược tại Việt Nam
Theo Thông tư số 08/2021/TT-BYT ngày 25/6/2021 của Bộ trưởng Bộ Y tế ban hành Nguyên tắc đạo đức hành nghề dược, người hành nghề dược phải thực hiện nghiêm túc các nguyên tắc sau:
a. Tuân thủ pháp luật và các quy định có liên quan đến hành nghề dược
- Ngoài việc tuân thủ Hiến pháp, pháp luật thì phải tuân thủ Luật Dược, các văn bản quy định chi tiết thi hành Luật Dược và các văn bản pháp luật có liên quan.
- Phải tuân thủ các quy định của nguyên tắc đạo đức hành nghề dược và Điều lệ của tổ chức xã hội - nghề nghiệp hành nghề dược mà người hành nghề dược là thành viên.
b. Rèn luyện, tu dưỡng bản thân
- Phải luôn rèn luyện kỹ năng giao tiếp, ứng xử, nâng cao phẩm chất đạo đức của người thầy thuốc, lương tâm nghề nghiệp và trách nhiệm với nghề, với người sử dụng thuốc.
- Phải không ngừng học tập nâng cao trình độ chuyên môn, nghiệp vụ; tích cực tham gia các lớp đào tào, bồi dưỡng kiến thức; tích cực nghiên cứu và ứng dụng tiến bộ khoa học - công nghệ, phát huy sáng kiến, cải tiến, đáp ứng tốt các yêu cầu phục vụ công tác chăm sóc sức khỏe nhân dân trong mọi tình huống.
- Phải sẵn sàng vượt qua mọi khó khăn gian khổ vì sự nghiệp chăm sóc và bảo vệ sức khỏe nhân dân.
- Phải tích cực tham gia đấu tranh phòng chống tham nhũng, lãng phí và các tệ nạn xã hội.
c. Trách nhiệm nghề nghiệp
- Có trách nhiệm coi trọng, giữ gìn uy tín nghề nghiệp, không được có hành vi làm tổn hại đến uy tín, danh dự của người hành nghề dược và hình ảnh người cán bộ, công chức, nhân viên y tế.
- Phải nghiêm chỉnh chấp hành những quy định chuyên môn về dược. Không lợi dụng hoặc tạo điều kiện cho người khác lợi dụng nghề nghiệp để mưu cầu lợi ích cá nhân, vi phạm pháp luật.
- Có trách nhiệm hướng dẫn sử dụng thuốc hợp lý, an toàn, hiệu quả và tiết kiệm cho người bệnh và nhân dân; đẩy mạnh hoạt động dược lâm sàng và cảnh giác dược; tích cực, chủ động tuyên truyền kiến thức về chăm sóc và bảo vệ sức khỏe nhân dân, phòng chống dịch bệnh.
- Phải tôn trọng và bảo vệ quyền và lợi ích hợp pháp của người bệnh, người sử dụng thuốc, quan tâm đến những người bệnh được hưởng chính sách xã hội. Bình đẳng, công bằng và không kỳ thị phân biệt đối xử người bệnh, không được có thái độ ban ơn, lạm dụng nghề nghiệp và gây phiền hà cho người bệnh. Phải trung thực khi thanh toán các chi phí cho người bệnh. Không vì lợi ích cá nhân mà giao cho người bệnh thuốc kém chất lượng, thuốc không đúng với yêu cầu và mức độ bệnh.
- Khi bản thân có lỗi trong quá trình hành nghề dược, phải tự giác nhận trách nhiệm về mình và bồi thường thiệt hại theo quy định của pháp luật.
- Phải ứng xử văn minh, luôn có thái độ niềm nở, tận tình, trang phục lịch sự trong hoạt động hành nghề dược.
d. Bảo mật thông tin người bệnh
- Phải tôn trọng những bí mật riêng tư của người bệnh, bí mật liên quan đến bệnh tật người bệnh.
- Thông tin về sức khỏe và đời tư của người bệnh chỉ được phép công bố trong trường hợp được người bệnh đồng ý hoặc các trường hợp khác được pháp luật cho phép.
đ. Quan hệ với đồng nghiệp, tổ chức xã hội - nghề nghiệp của người hành nghề dược
- Phải trung thực, đoàn kết, kính trọng các bậc thầy, hợp tác, tôn trọng đồng nghiệp và lắng nghe ý kiến của đồng nghiệp; bảo vệ danh dự, uy tín của đồng nghiệp.
- Không được có hành vi trái đạo đức, không gây áp lực, đe dọa hoặc thực hiện các hành vi vi phạm pháp luật với đồng nghiệp để giành lợi thế cho mình trong hành nghề, không được thực hiện các hành vi cạnh tranh không lành mạnh khác.
- Có trách nhiệm giám sát và giúp đỡ đồng nghiệp trong hoạt động hành nghề, kiên quyết đấu tranh loại bỏ những hành vi sai trái trong hoạt động kinh doanh dược trên cơ sở tôn trọng đồng nghiệp.
- Có trách nhiệm hướng dẫn, giúp đỡ về chuyên môn, nghiệp vụ đối với đồng nghiệp mới vào nghề.
- Phải tự nguyện tham gia vào các hoạt động nghề nghiệp và hoạt động xã hội khác do Nhà nước, tổ chức xã hội - nghề nghiệp của người hành nghề dược tổ chức hoặc phát động nhằm góp phần vào sự phát triển chung của ngành dược.
e. Quan hệ với người thực hành chuyên môn về dược
- Có trách nhiệm tham gia vào công tác hướng dẫn người thực hành chuyên môn về dược, nêu cao trách nhiệm, tận tâm truyền đạt kiến thức và kinh nghiệm nghề nghiệp đối với người thực hành chuyên môn về dược.
- Không được thực hiện những việc sau:
+ Phân biệt, đối xử mang tính cá nhân đối với những người thực hành chuyên môn về dược;
+ Đòi hỏi lợi ích vật chất, tinh thần từ người thực hành chuyên môn về dược;
+ Lợi dụng tư cách là người hướng dẫn để buộc người thực hành chuyên môn về dược phải làm những việc không thuộc phạm vi tập sự hoặc những hành vi vi phạm pháp luật, trái đạo đức xã hội nhằm đạt được những lợi ích cho mình.
g. Quan hệ với cơ quan, tổ chức, cá nhân khác có liên quan
- Phải chấp hành quyết định của cơ quan nhà nước có thẩm quyền và hợp tác chặt chẽ với các cán bộ, công chức, nhân viên y tế và cán bộ, công chức, nhân viên của cơ quan ban ngành khác bảo đảm cung ứng và hướng dẫn sử dụng thuốc an toàn, hiệu quả trong trường hợp có dịch bệnh nguy hiểm, thiên tai, thảm họa.
- Phải tôn trọng và hợp tác với cơ quan quản lý nhà nước, kiên quyết đấu tranh với các hiện tượng tiêu cực trong hoạt động nghề nghiệp./.
Tài liệu tham khảo
1. Nguyễn Thanh Bình, Đỗ Xuân Thắng (2020), Dược cộng đồng, giáo trình đào tạo dược sỹ đại học, Nhà xuất bản Y học .
2. International Pharmaceutical Federation, the FIP community pharmacy section vision 2020.
3. International Pharmaceutical Federation, Quality care standards in community pharmacy, 2005.
4. Bộ Y tế (2021), Thông tư số 08/2021/TT-BYT Ban hành Nguyên tắc đạo đức hành nghề dược.
CHƯƠNG 2. KỸ NĂNG THỰC HÀNH CHO NGƯỜI BÁN LẺ THUỐC
2.1. Vai trò kỹ năng giao tiếp trong thực hành tại CSBLT
Giao tiếp hiệu quả hỗ trợ rất nhiều trong cuộc sống cũng như trong công việc chuyên môn của dược sỹ - người bán lẻ thuốc. Đây là một trong các kỹ năng thực hành mà người bán lẻ thuốc cần phải rèn luyện để có được và sẽ ngày càng được tích lũy thông qua quá trình hành nghề. Trong giao tiếp với người bệnh, người bán lẻ thuốc cần phải:
- Tìm hiểu về thuốc, tiền sử sử dụng thuốc và những vấn đề y tế liên quan tới người bệnh.
- Cung cấp thông tin và giải thích (giáo dục người bệnh) về liệu pháp điều trị, nguy cơ và thuốc.
- Xác định động lực để tuân thủ điều trị hoặc những điều chỉnh về thói quen và lối sống của người bệnh.
- Giải thích, trao đổi và đưa ra quyết định về phương pháp điều trị và những lựa chọn khác (nếu có).
- Hợp tác và quản lý chế độ điều trị phức tạp (thao tác, tư vấn, kiểm tra).
- Thể hiện sự hỗ trợ và quan tâm.
- Xây dựng sự tin tưởng trong giao tiếp.
Người bán lẻ thuốc phải hiểu được tầm quan trọng của giao tiếp và hiểu được những việc phải làm thì mới giúp nâng cao được chất lượng chăm sóc y tế và hiệu quả của thuốc. Những mong muốn và ưu tiên của người bệnh và nhân viên y tế sẽ có ảnh hưởng tới những ưu tiên và tính hiệu quả của chăm sóc y tế cộng đồng.
Mong muốn của người bệnh khi mua thuốc tại cơ sở bán lẻ là:
- Cảm thấy tin tưởng vào chất lượng thuốc và chất lượng của tư vấn.
- Tương tác có chất lượng với người bán lẻ thuốc.
- Cảm thấy sự riêng tư được tôn trọng.
- Cảm thấy có được sự quan tâm thực sự từ dược sỹ - người bán lẻ thuốc.
- Môi trường thân thiện và thoải mái.
- Người bệnh cảm thấy yên tâm về vấn đề của họ khi giao tiếp với người bán lẻ thuốc.
- Người bán lẻ thuốc giải thích lý do của các câu hỏi đặt ra với người bệnh.
- Thông tin được cung cấp đầy đủ.
Nhiều mong muốn trên của người bệnh có thể giải quyết được nếu người bán lẻ thuốc có kỹ năng giao tiếp tốt.
Mặt khác, nhiều vấn đề nghiêm trọng trong chăm sóc y tế có thể xảy ra có nguyên nhân là do giao tiếp. Một số các vấn đề đó là:
- Thất bại trong xây dựng mối quan hệ với người bệnh.
+ Thiếu sự quyết tâm và thời gian để thuyết phục người bệnh tham gia đầy đủ vào quá trình hiểu và đồng ý về phương pháp điều trị.
+ Tỷ lệ tuân thủ điều trị chưa cao.
+ Tỷ lệ cao người bệnh không hài lòng về hoạt động điều trị của hệ thống và nhân viên y tế.
- Thất bại trong hợp tác.
+ Mâu thuẫn mức độ ưu tiên giữa các nhân viên y tế và giữa nhân viên y tế với nhà quản lý và giữa nhà quản lý tài chính với nhà hoạch định chính sách.
+ Thiếu sự rõ ràng và kết nối trong giao tiếp giữa các nhóm y tế đa ngành, hệ thống hỗ trợ và cộng đồng.
- Thất bại trong thông tin, giáo dục và truyền tải.
+ Thiếu sự truyền đạt, quản lý thông tin hiệu quả.
+ Thiếu hoặc không cung cấp các nguồn thông tin đầy đủ cho người bệnh.
+ Cơ hội giáo dục và cung cấp tài liệu để người bệnh chủ động trong chăm sóc sức khỏe bản thân.
+ Thiếu giáo dục cộng đồng một cách phù hợp về nguy cơ và lợi ích của thuốc, liệu pháp điều trị, những điều không chắc chắn và mong đợi trong điều trị.
+ Ít thấu hiểu về sự phức tạp của câu hỏi y tế và phương pháp khoa học.
+ Mê tín, vấn đề sử dụng thuốc không hợp lý phổ biến ở nhóm người dân.
- Thất bại trong quản lý.
+ Tổ chức, quản lý kém.
+ Thiếu sự rõ ràng và chia sẻ thích hợp về sứ mệnh và mức độ ưu tiên ở cấp quốc gia và khu vực.
Người bán lẻ thuốc giao tiếp hiệu quả trong hoạt động thực hành dược sẽ giúp đảm bảo người bệnh nhận được những lợi ích tốt nhất từ nguồn lực y tế sẵn có mặc dù trong điều kiện bị hạn chế.
2.2 Kỹ năng cơ bản trong giao tiếp thực hành tại CSBLT
Theo cách thức giao tiếp gồm giao tiếp ngôn ngữ và giao tiếp phi ngôn ngữ. Đây là cách phân loại quan trọng mà người bán lẻ thuốc cần hiểu và vận dụng được trong quá trình giao tiếp vì nghiên cứu đã chỉ ra rằng ý nghĩa thông điệp được truyền tải không chỉ phụ thuộc vào ngôn từ mà còn phụ thuộc vào những yếu tố khác (giọng nói, ngôn ngữ cơ thể).
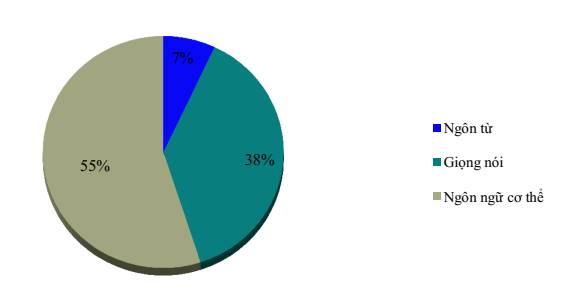
Hình 2.1. Các yếu tố ảnh hưởng đến ý nghĩa thông điệp trong giao tiếp
Trong giao tiếp ngôn ngữ, người bán lẻ thuốc giao tiếp phải chú ý đến âm sắc, âm lượng và âm tốc. Một câu được nói với âm sắc khác nhau sẽ mang những ý nghĩa khác nhau và hiệu quả giao tiếp khác nhau. Ví dụ, câu nói “Vấn đề của anh/ chị là gì” có thể được truyền tải đến người bệnh theo nhiều cách khác nhau, có thể là đồng cảm, thấu hiểu hoặc bực bội, khó chịu… tùy vào âm sắc được sử dụng.. Người bán lẻ thuốc phải chú ý đến âm lượng phù hợp (không nên quá to hoặc quá nhỏ) và âm tốc vừa phải khi giao tiếp, đặc biệt với nhóm đối tượng khách hàng đặc biệt như người cao tuổi.
Cùng với giao tiếp ngôn ngữ, giao tiếp phi ngôn ngữ (non-verbal communication) đóng vai trò rất quan trọng mang lại hiệu quả trong giao tiếp. Giao tiếp phi ngôn ngữ bao gồm: ánh mắt, nét mặt, điệu bộ, cử chỉ, chuyển động cơ thể sẽ chuyển tải những thông điệp giao tiếp không lời tới khách hàng. Hiệu quả có thể tạo ra từ giao tiếp phi ngôn ngữ là vô cùng lớn nếu như người giao tiếp hiểu được nguyên lý và vận dụng một cách thành thục. Trong giao tiếp giữa người bán lẻ và người bệnh, giao tiếp phi ngôn ngữ lại càng quan trọng, đòi hỏi cao khi đối tượng giao tiếp là người bệnh có vấn đề về sức khoẻ và tâm lý lo lắng. Dược sỹ cộng đồng cần vận dụng linh hoạt và mềm mại kỹ năng giao tiếp phi ngôn ngữ để tạo ra sự cảm thông, chia sẻ giúp người bệnh dịu nhẹ sự căng thẳng và tin tưởng vào liệu pháp điều trị. Trong tình huống này, ánh mặt, nét mặt, cử chỉ của người bán lẻ sẽ chuyển tải thông điệp giao tiếp tới người bệnh.
Ấn tượng ban đầu đôi khi rất quan trọng trong giao tiếp.Người bán lẻ thuốc cần tạo ấn tượng ban đầu thân thiện sẽ khiến khách hàng/người bệnh dễ dàng tiếp thu, đồng tình với những điều người bán lẻ thuốc trao đổi. Ngược lại, người bán lẻ thuốc tạo ấn tượng ban đầu không tốt thường khó đạt được sự tin tưởng của người bệnh và bác sĩ. Nếu khách hành nhận được thái độ không thân thiện và không sẵn lòng giúp đỡ của người bán lẻ thuốc, họ có thể sẽ tìm sang cơ sở bán lẻ thuốc khác hoặc thậm chí không tuân thủ theo lời khuyên của người bán lẻ thuốc.
Ngôn ngữ cơ thể là sự truyền tải "vô tình" hoặc "cố tình - có chủ đích" và diễn đạt cảm xúc, thái độ và tâm trạng thông qua nét mặt, ánh mắt, cử chỉ, động tác, tư thế và khoảng cách giao tiếp. Trong giao tiếp tại cơ sở bán lẻ thuốc, khoảng cách được đánh giá là phù hợp để trao đổi với người bệnh là khoảng cách cá nhân từ 0,5 - 1m.
Trong quá trình giao tiếp với người bệnh, khách hàng thì người bán lẻ thuốc phải sử dụng phối hợp các kỹ năng hỏi, kỹ năng lắng nghe, kỹ năng phản hồi và kỹ năng khuyên.
2.2.1. Kỹ năng hỏi
a. Tầm quan trọng của kỹ năng hỏi
Kỹ năng hỏi (Questioning skills) là một trong các kỹ năng giao tiếp quan trọng. Biết cách đặt câu hỏi hợp lý, đúng thời điểm sẽ giúp tạo ra hiệu quả giao tiếp tốt. Vận dụng một cách linh hoạt kỹ năng hỏi và cách đặt câu hỏi sẽ giúp người bán lẻ thuốc khai thác được các thông tin cần thiết từ người bệnh (thông tin liên quan đến bệnh, tiền sử sử dụng thuốc, lối sống của khách hàng…) một cách hiệu quả. Ngoài ra, người bán lẻ thuốc biết cách đặt câu hỏi phù hợp còn giúp mở rộng chủ đề giao tiếp, tăng cơ hội hiểu rộng và sâu hơn các vấn đề có liên quan cần khai thác. Một số dạng câu hỏi còn giúp người bán lẻ thuốc có thể đánh giá, xác minh mức độ chính xác của thông tin nhận được từ khách hàng. Cuối cùng, người bán lẻ thuốc biết vận dụng kỹ năng hỏi phù hợp còn giúp động viên, khuyến khích khách hàng tiếp tục chia sẻ thông tin và duy trì quá trình giao tiếp hai chiều theo hướng tích cực.
b. Các dạng câu hỏi
Câu hỏi mở là dạng câu hỏi có câu trả lời rộng, đa dạng, thường khiến người trả lời cần sử dụng nhiều hơn một từ để trả lời. Dạng câu hỏi này sẽ không đưa ra gợi ý câu trả lời mà khuyến khích người trả lời phải suy nghĩ để đưa ra ý kiến của mình.
Dạng câu hỏi này sẽ giúp người bán lẻ thuốc khai thác được nhiều thông tin và giúp người bệnh cởi mở chia sẻ các thông tin hơn. Tuy nhiên, nhược điểm của dạng câu hỏi này là câu trả lời có thể lan man, không tập trung vào vấn đề chính.
Câu hỏi lựa chọn là dạng câu hỏi đã đưa ra các phương án trả lời và người trả lời chỉ cần lựa chọn đáp án phù hợp với họ. Ví dụ “Chị bị ho có đờm hay không có đờm?”. Câu hỏi lựa chọn sẽ giúp thu hẹp những nghi ngờ của dược sỹ - người bán lẻ thuốc, giúp người bệnh dễ đưa ra câu trả lời hơn và khuyến khích khách hàng chia sẻ thêm những thông tin theo cách của họ. Tuy nhiên, khi sử dụng dạng câu hỏi này cần thận trọng vì nếu không biết đặt câu hỏi đúng cách thì sẽ nhận được câu trả lời theo ý của dược sỹ - người bán lẻ thuốc mong muốn hơn là của khách hàng.
Câu hỏi thăm dò là dạng câu hỏi nhằm khai thác, khám phá thêm những thông tin chưa rõ từ người bệnh. Ví dụ tình huống người bệnh (nữ) bị đau đầu và nói rằng người bệnh dường như có thể biết trước được cơn đau của mình sắp xảy ra. Người bán lẻ có thể sử dụng câu hỏi thăm dò “Chị nói rằng chị dường như có thể biết trước được cơn đau của mình sắp xảy ra, tại sao chị lại nói như vậy?”.
Câu hỏi đóng là dạng câu hỏi chỉ cần trả lời có tính khẳng định hoặc phủ định với các tình huống được đưa ra. Ví dụ khi khai thác thông tin trong tình huống người bệnh bị tiêu chảy, người bán lẻ thuốc muốn đánh giá mức độ mất nước ở trẻ người bán lẻ thuốc có thể hỏi người chăm sóc trẻ câu hỏi “Mắt trẻ có trũng hơn bình thường không?”. Dạng câu hỏi này giúp người bệnh dễ trả lời và phù hợp với đối tượng người bệnh không thích trả lời dài.
Câu hỏi dẫn dắt là dạng câu hỏi mà câu trả lời người hỏi mong chờ đã có trong câu hỏi. Ví dụ tình huống một người bệnh nam nói rằng anh ta bị đau ở vùng bụng, dược sỹ - người bán lẻ thuốc đồng thời cũng biết người bệnh là một người hút thuốc và quá cân. Dược sỹ - người bán lẻ thuốc nghĩ rằng cơn đau là do dạ dày và bắt đầu hỏi những câu hỏi để xác định. Người bán lẻ thuốc hỏi “Sau khi ăn thì anh bị đau như vậy đúng không?”. Người bệnh sẽ trả lời “Đúng” vì người bệnh nhớ bữa chiều ăn nhiều và sau đó thấy đau. Như vậy, với câu trả lời này rất dễ khiến dược sỹ - người bán lẻ thuốc tiếp tục khai thác thông tin về bệnh của người bệnh theo hướng sai. Dược sỹ - người bán lẻ thuốc có thể có xu hướng sử dụng dạng câu hỏi này khi cố gắng giao tiếp với người bệnh hoặc để nhận câu trả lời theo suy đoán của mình. Tuy nhiên, cần cân nhắc khi sử dụng vì nó có thể dẫn dắt theo suy đoán chưa phù hợp.
c. Lưu ý khi thực hiện kỹ năng hỏi
Để có thể thực hiện kỹ năng hỏi tốt ngoài những câu hỏi mang tính chất chuyên môn để khai thác thông tin về bệnh và sử dụng thuốc của người bệnh thì dược sỹ - người bán lẻ thuốc cần phải lưu ý một số vấn đề sau khi thực hiện đặt câu hỏi:
Sử dụng các dạng câu hỏi phù hợp
Mỗi dạng câu hỏi đều có ưu - nhược điểm riêng vì vậy dược sỹ - người bán lẻ thuốc cần phải nắm được các dạng câu hỏi này và vận dụng linh hoạt vào các tình huống giao tiếp. Tuy nhiên, để giúp giảm thời gian của cuộc giao tiếp và để người bệnh có thể nói về các triệu chứng bệnh theo ngôn ngữ của mình thì bất kỳ khi nào có thể và đặc biệt trong giai đoạn đầu của quá trình trao đổi khai thác thông tin về người bệnh nên sử dụng câu hỏi mở. Sau đó sử dụng các dạng câu hỏi khác để xác định hoặc khám phá thêm thông tin.
Đảm bảo người bệnh hiểu ý nghĩa câu hỏi
Nếu người bệnh không hiểu lý do đặt câu hỏi người bệnh sẽ ngại ngùng, bối rối và không muốn chia sẻ thông tin. Nhưng nếu người bệnh hiểu lý do đặt câu hỏi, người bệnh sẽ thoải mái, cởi mở và sẵn sàng chia sẻ thông tin, kể cả những thông tin mang tính cá nhân, nhạy cảm. Vì vậy, một câu hỏi tốt là một câu hỏi rõ ràng và dễ hiểu.
Phù hợp giữa nhịp điệu hỏi và khả năng trả lời của người bệnh
Dược sỹ - người bán lẻ thuốc có kinh nghiệm thường có sẵn một loạt các câu hỏi sử dụng để khai thác thông tin cần thiết từ phía khách hàng. Tuy nhiên, nếu dược sỹ - người bán lẻ thuốc hỏi quá nhanh có thể khiến khách hàng nhầm lẫn và đưa ra câu trả lời không chính xác, không đầy đủ và thậm chí là sai. Vì vậy, trong quá trình hỏi dược sỹ - người bán lẻ thuốc cần phải chú ý đến những biểu hiện ở khách hàng, nếu họ có dấu hiệu bối rối thì cần phải hỏi với tốc độ chậm hơn. Đồng thời, người bán lẻ thuốc có thể hỏi lại một số thông tin đặc biệt trong trường hợp nếu thấy thông tin đó không phù hợp với các thông tin đã được cung cấp trước đó.
Tránh sử dụng câu hỏi dẫn dắt
Tâm lý chung thường không ai muốn thể hiện sự thiếu hiểu biết của mình. Trong một số tình huống khi sử dụng dạng câu hỏi dẫn dắt có thể sẽ nhận được thông tin không chính xác do người bệnh muốn che dấu sự thiếu hiểu biết của mình. Ví dụ tình huống người bệnh đến nhà thuốc mua một thuốc dạng bình xịt định liều. Dược sỹ - người bán lẻ thuốc muốn biết người bệnh đã biết cách sử dụng bình xịt định liều chưa và hỏi: “Cháu đoán bác đã biết lọ thuốc xịt rồi đúng không?”. Khi đó, người bệnh rất có thể sẽ trả lời “Có” trong khi thực tế họ không biết sử dụng dạng thuốc xịt này. Vì khi nghe câu hỏi trên, người bệnh có thể suy diễn ý nghĩa câu hỏi là: “Người bán lẻ thuốc đoán là tôi biết sử dụng lọ thuốc này. Vì chắc lọ thuốc này dễ sử dụng và mọi người đều biết sử dụng vì vậy người bán lẻ thuốc không cần phải nói với tôi. Nếu tôi không biết sử dụng thì thật kém”. Dược sỹ - người bán lẻ thuốc nên hỏi là: “Bác đã biết cách dùng lọ thuốc xịt này chưa?” hoặc tốt hơn là theo cách không thể hiện sự thiếu hiểu biết của người bệnh “Đã có ai hướng dẫn bác cách sử dụng lọ thuốc xịt này chưa?”. Với cách hỏi này thì dường như người bệnh sẽ dễ dàng xác nhận nếu chưa biết cách dùng thuốc. Vì khi đó người bệnh chưa biết cách sử dụng thuốc là do chưa có ai hướng dẫn người bệnh chứ không phải do người bệnh thiếu hiểu biết.
Tránh sử dụng câu hỏi khi câu khẳng định là cần thiết
Tình huống khách hàng nói rằng họ muốn dừng sử dụng thuốc tăng huyết áp. Dược sỹ - người bán lẻ thuốc có thể phản ứng là: “Bác không muốn gặp phải nguy cơ nếu dừng uống thuốc đúng không?”. Tình huống này dược sỹ - người bán lẻ thuốc cần phải tuyên bố với khách hàng rằng: “Nếu bác dừng uống thuốc sẽ có một số nguy cơ”.
2.2.2. Kỹ năng lắng nghe
a. Tầm quan trọng của kỹ năng lắng nghe
Kỹ năng lắng nghe (listening skills) thể hiện thông qua việc lắng nghe chăm chú, nghe tích cực, chủ động, khuyến khích người giao tiếp thông qua sử dụng có hiệu quả ngôn ngữ không lời như ánh mắt, nét mặt, điệu bộ, cử chỉ để khuyến khích người đối diện, người bệnh, khách hàng trao đổi thông tin.
Khi nói đến kỹ năng giao tiếp, người ta thường nghĩ đến kỹ năng nói. Tuy nhiên, kỹ năng lắng nghe cũng quan trọng không kém và có thể khó khăn hơn trong việc rèn luyện. Nhiều nghiên cứu cho thấy hầu hết mọi người không có kỹ năng lắng nghe tốt.
Trong thực hành dược, lắng nghe có thể càng khó thực hiện bởi nhận thức, thái độ của những người tham gia giao tiếp hoặc bởi hạn chế về thời gian. Đặc biệt trong bối cảnh dược sỹ - người bán lẻ thuốc là người bận rộn và thường xuyên tiếp xúc với nhiều khách hàng.
Kỹ năng lắng nghe là chìa khóa của giao tiếp hiệu quả. Ngoài ra, dược sỹ - người bán lẻ thuốc không thể thực hiện được chiến lược lấy người bệnh làm trung tâm nếu thiếu kỹ năng lắng nghe hiệu quả. Hãy nhớ rằng người bệnh là người biết nhiều thông tin về tình trạng sức khỏe của bản thân. Vì vậy, lắng nghe giúp dược sỹ - người bán lẻ thuốc tiếp nhận đầy đủ thông tin, thông điệp từ người bệnh và khuyến khích họ tiếp tục trình bày ý kiến, thể hiện sự tôn trọng, đồng cảm với người nói. Từ những thông tin được lắng nghe một cách đúng và đủ, dược sỹ - người bán lẻ thuốc mới có thể điều chỉnh các thông điệp tiếp theo trong giao tiếp với người bệnh, mới phản hồi phù hợp.
b. Lưu ý khi thực hiện kỹ năng lắng nghe
Sau đây là các thói quen có thể ảnh hưởng đến kỹ năng lắng nghe và biện pháp khắc phục để cải thiện kỹ năng lắng nghe:
Cố gắng làm nhiều việc một lúc: Sự thiếu chú ý sẽ dẫn đến cảm giác như dược sỹ - người bán lẻ thuốc đang thiếu quan tâm đến người bệnh và những gì họ nói. Do đó cần tránh làm những việc khác khi đang giao tiếp với người bệnh.
Kết luận luôn vấn đề trước khi người bệnh truyền tải hết thông điệp của họ: Kết quả là dược sỹ - người bán lẻ thuốc chỉ nghe được một phần những gì được nói ra. Giải pháp trong tình huống này là tập trung lắng nghe đầy đủ thông tin trước khi đưa ra kết luận.
Giao tiếp theo các khuôn mẫu mà người bán lẻ thuốc đã được học hoặc tiếp thu được: Giải pháp là dược sỹ - người bán lẻ thuốc phải phản hồi với những thông tin có được trong giao tiếp chứ không phải với cá nhân, con người.
Giả vờ quan tâm đến những gì đang được thảo luận: để thể hiện dược sỹ - người bán lẻ thuốc đang thực sự chú tâm vào cuộc trao đổi. Tuy nhiên, dược sỹ - người bán lẻ thuốc cần phải cố gắng giao tiếp tốt bằng mắt, điều này sẽ giúp dược sỹ - người bán lẻ thuốc tập trung.
Đánh giá cá nhân dựa trên bề ngoài hoặc tình trạng, biểu hiện: để vượt qua vấn đề này, dược sỹ - người bán lẻ thuốc cần tập trung vào nội dung, các gợi ý phi ngôn ngữ để hiểu những nội dung được truyền tải từ đối tượng giao tiếp.
Lắng nghe không chỉ liên quan đến việc dược sỹ - người bán lẻ thuốc sử dụng trong giao tiếp; Nét mặt, ngôn ngữ cơ thể, giọng điệu của người bệnh có thể đưa ra cho dược sỹ - người bán lẻ thuốc các gợi ý về cảm xúc, suy nghĩ của người bệnh trong quá trình giao tiếp. Do đó, dược sỹ - người bán lẻ thuốc cần kết hợp giữa lắng nghe với quan sát.
Dược sỹ - người bán lẻ thuốc cần kết hợp với ngôn ngữ cơ thể như giao tiếp bằng mắt, tư thế (hướng về phía trước, đứng thẳng...), gật đầu... để thể hiện dược sỹ - người bán lẻ thuốc thực sự đang thoải mái, chân thành và tôn trọng các thông điệp người bệnh truyền tải. Đồng thời, dược sỹ - người bán lẻ thuốc cần phải tránh một số biểu hiện sau trong khi lắng nghe:
- Cãi lại hoặc tranh luận gay gắt với người bệnh.
- Tỏ thái độ sốt ruột, chán nản, cắt ngang lời người bệnh.
- Chỉ nghe những gì mà dược sỹ - người bán lẻ thuốc thích và lưu tâm.
- Để quan điểm riêng của dược sỹ - người bán lẻ thuốc tác động đến việc hiểu vấn đề của người bệnh. Có thái độ định kiến với một số nhóm người bệnh (về tôn giáo, trình độ học vấn, tuổi tác...).
2.2.3. Kỹ năng phản hồi
a. Tầm quan trọng của kỹ năng phản hồi
Kỹ năng phản hồi (responding skills) là khả năng mà dược sỹ - người bán lẻ thuốc sử dụng các kỹ năng về giao tiếp ngôn ngữ và phi ngôn ngữ để chuyển tải hoặc phản hồi thông tin tới đối tượng giao tiếp. Ý nghĩa là thể hiện dược sỹ - người bán lẻ thuốc hiểu và khuyến khích người bệnh giao tiếp hiệu quả hơn. Bằng việc thể hiện tốt kỹ năng nghe và kỹ năng giao tiếp phi ngôn ngữ tốt, dược sỹ - người bán lẻ thuốc đã thể hiện kỹ năng phản hồi phù hợp.
Kỹ năng phản hồi thể hiện kỹ năng “nghe tích cực”, giúp cho cuộc trao đổi tiếp tục và cho khách hàng biết rằng dược sỹ - người bán lẻ thuốc đang tham gia vào cuộc trao đổi và khuyến khích khách hàng chia sẻ thông tin.
b. Các dạng phản hồi
Phản hồi bao gồm phản hồi về nội dung và phản hồi về cảm xúc.
Phản hồi về nội dung
Dược sỹ - người bán lẻ thuốc giao tiếp nhằm tìm kiếm thông tin và đưa ra lời khuyên cho người bệnh vì vậy phản hồi về nội dung là một phần quan trọng của cuộc trao đổi.
Dược sỹ - người bán lẻ thuốc thường cần phải tóm tắt các thông tin nhận được trong quá trình trao đổi với khách hàng. Nếu dược sỹ - người bán lẻ thuốc thực hiện tốt kỹ năng này sẽ làm tăng sự tin tưởng của người bệnh vào khả năng của người bán lẻ thuốc và làm tăng cơ hội người bệnh tuân thủ theo các lời khuyên.
Phản hồi về nội dung thông qua cách tóm tắt lại những thông tin trong quá trình giao tiếp còn giúp dược sỹ - người bán lẻ thuốc kiểm tra lại thông tin, đảm bảo rằng những điều mình nghe được là chính xác. Nếu có thông tin nào không đúng thì khách hàng sẽ phản ứng lại và điều chỉnh.
Phản hồi về cảm xúc
Phản hồi về cảm xúc giúp cho cuộc giao tiếp ở mức độ sâu hơn. Thể hiện không chỉ sự lắng nghe mà còn đồng cảm của người bán lẻ thuốc với người bệnh, giúp người bệnh cảm thấy tin tưởng hơn, muốn chia sẻ hơn và làm cho người bệnh có thể bộc lộ hết cảm xúc, suy nghĩ
b. Lưu ý khi thực hiện kỹ năng phản hồi
Để đảm bảo giao tiếp hiệu quả và có thể khắc phục những rào cản trong quá trình giao tiếp với khách hàng, dược sỹ - người bán lẻ thuốc khi phản hồi cần đảm bảo tiêu chí 5S:
Bảng 2.1. Tiêu chí 5S khi phản hồi với khách hàng
| 5 S | Đầu tiên | 1. Sincere | Chân thành |
| Thứ hai, khi cung cấp thông tin: | 2. Simple 3. Short 4. Specific | Đơn giản Ngắn gọn Cụ thể | |
| Thứ ba, khi kết thúc | 5. Summarise | Tóm tắt |
- Sincere (chân thành)
Thái độ của dược sỹ - người bán lẻ thuốc khi giao tiếp rất quan trọng. Thái độ chân thành, ấm áp và cởi mở của dược sỹ - người bán lẻ thuốc khi trao đổi, tư vấn sẽ ảnh hưởng đến thái độ của người bệnh, làm tăng sự tin cậy và sức thuyết phục với người bệnh.
- Simple (đơn giản)
Chúng ta thường nghĩ rằng nếu dược sỹ - người bán lẻ thuốc sử dụng những từ dài, chuyên môn thì người bệnh sẽ tin tưởng và tôn trọng dược sỹ - người bán lẻ thuốc hơn nhưng đó là một quan điểm sai lầm. Nhiệm vụ của dược sỹ - người bán lẻ thuốc là phải chuyển những thông tin chuyên môn thành hướng dẫn sử dụng thuốc đơn giản cho người bệnh để họ có thể thực hiện theo. Dược sỹ - người bán lẻ thuốc nên sử dụng những ngôn ngữ, câu đơn giản và trực tiếp tránh sử dụng câu phức không cần thiết. Khi dược sỹ - người bán lẻ thuốc sử dụng những từ và câu ngắn trong quá trình giao tiếp thì người bệnh sẽ nhớ thông tin tốt hơn khi sử dụng những câu và từ dài.
- Short (ngắn gọn)
Trong quá trình giao tiếp tại nhà thuốc, dược sỹ - người bán lẻ thuốc thường có nhiều hơn 3 thông tin cần trao đổi với người bệnh và khi số lượng thông tin nhiều hơn 3 thì người bệnh sẽ có xu hướng quên một phần thông tin trao đổi. Chính vì vậy, dược sỹ - người bán lẻ thuốc cần phân loại, cân nhắc trao đổi bằng lời những thông tin gì là quan trọng nhất với từng đối tượng người bệnh, khách hàng. Người bán lẻ thuốc nên sử dụng các biện pháp giao tiếp khác để giúp khách hàng ghi nhớ như viết ra giấy một số thông tin để có thể vượt qua được rào cản này.
- Specific (cụ thể)
Thông tin cụ thể và rõ ý nghĩa sẽ giúp người bệnh không hiểu sai ý nghĩa và nhớ được tốt hơn. Ví dụ tình huống dược sỹ - người bán lẻ thuốc muốn tư vấn cho người bệnh về cách bảo quản lọ thuốc nhỏ mắt. Nếu dược sỹ - người bán lẻ thuốc nói với người bệnh rằng “Khi bác mở lọ thuốc nhỏ mắt này ra, sau một thời gian nó sẽ không còn vô trùng nữa. Vì vậy bác phải nhớ bỏ đi sau 15 ngày mở lọ.” thì người bệnh sẽ nhớ thông tin tốt hơn nếu dược sỹ - người bán lẻ thuốc chỉ nói: “Bác nên bỏ thuốc này đi sau 15 ngày mở lọ”.
- Summarise (tóm tắt)
Khi kết thúc thì dược sỹ - người bán lẻ thuốc cần phải tóm tắt những điều đã nói. Điều này sẽ giúp người bệnh nắm bắt và nhớ được những thông tin quan trọng tốt hơn.
2.2.4. Kỹ năng tư vấn/ khuyên
a. Tầm quan trọng của kỹ năng tư vấn/ khuyên
Trở thành dược sỹ cộng đồng chuyên nghiệp không chỉ đòi hỏi dược sỹ - người bán lẻ thuốc phải am hiểu về thuốc và y tế công cộng mà còn phải biết áp dụng kỹ năng khuyên (advice giving skills) để giúp cho người bệnh hiểu rõ về bệnh và thuốc điều trị và sẵn sàng tuân thủ điều trị và thực hiện các lời khuyên về lối sống lành mạnh. Điều đó sẽ giúp cải thiện kết quả điều trị của người bệnh. Nhiều nghiên cứu đã chỉ ra rằng việc thiếu kiến thức và không hiểu rõ về thuốc ảnh hưởng tiêu cực đến việc sử dụng thuốc ở người bệnh. Do vậy, kỹ năng tư vấn/ khuyên của dược sỹ - người bán lẻ thuốc đóng vai trò rất quan trọng trong việc giúp người bệnh hiểu về thuốc, về bệnh, về chế độ sinh hoạt để từ đó nâng cao hiệu quả của sử dụng thuốc.
b. Nội dung cần tư vấn cho khách hàng
Thông thường, hoạt động tư vấn/khuyên của dược sỹ - người bán lẻ thuốc được thực hiện trong hai bối cảnh: 1/ theo nội dung hỏi của người bệnh; 2/ theo sự chủ động của dược sỹ - người bán lẻ thuốc. Trong trường hợp một, dược sỹ - người bán lẻ thuốc cần phát huy kỹ năng khai thác thông tin và tư vấn tập trung vào thắc mắc, câu hỏi của người bệnh. Trong trường hợp thứ hai, thông qua giao tiếp với người bệnh, dược sỹ - người bán lẻ thuốc phát hiện được những kiến thức còn thiếu hoặc những điều chỉnh cần thực hiện và chủ động trao đổi, tư vấn để giúp người bệnh nâng cao hiệu quả điều trị. Tùy thuộc vào từng trường hợp mà dược sỹ - người bán lẻ thuốc sẽ cung cấp các nội dung tư vấn khác nhau.
Tuy nhiên nhìn chung, khi tiến hành tư vấn về thuốc, dược sỹ - người bán lẻ thuốc cần cung cấp các thông tin sau:
- Tên thuốc (tên generic và tên biệt dược).
- Mô tả thuốc.
- Công dụng của thuốc.
- Đường dùng, dạng thuốc, liều dùng và thời điểm sử dụng.
- Thời gian điều trị: số ngày điều trị và khoảng thời gian điều trị.
- Biện pháp xử trí nếu quên sử dụng thuốc hoặc không dùng đủ liều.
- Điều kiện bảo quản.
- Các chú ý đặc biệt (cách dùng thuốc đặc biệt, liều dùng cách nhật, tương tác thuốc - thuốc, thuốc với đồ uống, thức ăn...).
- Tác dụng không mong muốn của thuốc (ADR) thông thường, cách giảm thiểu và hướng xử trí khi gặp.
- Chi tiết về phác đồ điều trị mới hoặc chế độ điều trị mới.
- Các kỹ thuật, phương pháp để tự giám sát điều trị.
Một trong những vấn đề khi khuyên người bệnh/ tư vấn là dược sỹ - người bán lẻ thuốc ngay lập tức cung cấp các kế hoạch cho điều trị mà quên tìm hiểu nhận thức của người bệnh về thuốc, về tình trạng bệnh dẫn đến có thể cung cấp các thông tin không thực sự cần thiết hoặc thiếu giải thích, cung cấp thiếu các thông tin quan trọng. Vì vậy trước khi tư vấn, dược sỹ - người bán lẻ thuốc phải biết và đánh giá được sẽ phải trao đổi với người bệnh những thông tin gì.
Khi lựa chọn thuốc điều trị cho người bệnh, dược sỹ - người bán lẻ thuốc phải lựa chọn thuốc dựa trên bằng chứng (evidence-based medicines). Thuốc được lựa chọn phải đáp ứng tiêu chí chi phí - hiệu quả. Liều và đường dùng, dạng bào chế của thuốc là phù hợp với người bệnh. Dược sỹ - người bán lẻ thuốc cần phải lưu ý hơn khi lựa chọn thuốc, dạng bào chế cho những nhóm đối tượng đặc biệt như người cao tuổi, trẻ em, phụ nữ có thai, phụ nữ cho con bú… Ngoài ra, dược sỹ - người bán lẻ thuốc cũng cần phải cân nhắc các vấn đề liên quan đến tình trạng bệnh, tài chính và xã hội. Để làm được những điều này dược sỹ - người bán lẻ thuốc cần phải nắm được các hướng dẫn điều trị bệnh đã được công bố đặc biệt là các hướng dẫn điều trị chuẩn được ban hành bởi Bộ Y tế Việt Nam và cập nhật thường xuyên kiến thức. Điều này sẽ giúp cho dược sỹ - người bán lẻ thuốc dễ dàng hơn trong việc lựa chọn thuốc.
Dược sỹ - người bán lẻ thuốc cũng cần phải kiểm tra để đảm bảo liều, tần suất, thời gian, đường dùng là phù hợp với người bệnh. Để làm được điều này, dược sỹ - người bán lẻ thuốc phải có được các thông tin về cân nặng, tuổi, tình trạng bệnh, chức năng gan, thận, các thuốc dùng kèm, thời điểm dùng. Dược sỹ - người bán lẻ thuốc cần cân nhắc để giúp đưa ra chế độ sử dụng thuốc phù hợp nhất với người bệnh giúp giảm thiểu tác dụng không mong muốn.
Dược sỹ - người bán lẻ thuốc cũng nên cung cấp thông tin chi tiết về nhân viên y tế mà người bệnh có thể hỏi thêm thông tin trong quá trình sử dụng thuốc.
b. Lưu ý khi thực hiện kỹ năng tư vấn
Tránh sử dụng các thuật ngữ chuyên môn
Người bệnh hoặc khách hàng thường không hoặc ít có kiến thức chuyên môn về y dược, chính vì vậy những từ ngữ chuyên môn là các từ khó hiểu. Dược sỹ - người bán lẻ thuốc cần tránh sử dụng các từ chuyên môn, nên sử dụng từ ngữ đơn giản dễ hiểu.
Ví dụ tình huống dược sỹ - người bán lẻ thuốc muốn tìm hiểu tác dụng phụ mà người bệnh gặp phải khi sử dụng thuốc thì không nên hỏi là “Khi dùng thuốc này bác có gặp phải ADR nào không ạ”. Từ ADR là một từ ngữ mang tính chất chuyên môn và người bệnh có thể sẽ không hiểu nó có ý nghĩa gì. Trong tình huống này dược sỹ - người bán lẻ thuốc nên hỏi người bệnh là “Khi dùng thuốc này bác có thấy bất cứ biểu hiện gì bất thường không ạ?”.
Dược sỹ - người bán lẻ thuốc cần chú ý các biểu hiện của người bệnh, kiểm tra lại thông tin nếu thấy người bệnh phân vân bằng cách đặt câu hỏi. Khi đặt câu hỏi để tìm hiểu về hiểu biết của người bệnh nên đặt là “Cháu nói có chỗ nào không rõ không ạ?” cách nói này sẽ tốt hơn cách nói “Bác có hiểu những gì cháu nói không?”. Với cách nói thứ nhất sẽ khiến cho khách hàng thoải mái hơn vì những thông tin chưa rõ ở đây là do lỗi của người bán lẻ thuốc.
Đảm bảo người bệnh không quá lo lắng khi được tiến hành tư vấn
Tâm lý của khách hàng khi đến nhà thuốc thường là thiếu bình tĩnh, lo sợ, ngại ngùng hoặc giận dữ… Điều này có thể là bản tính của khách hàng cũng có thể là do ảnh hưởng của bệnh tật hoặc vấn đề cá nhân khác. Một nghiên cứu đã chỉ ra rằng mức độ lo lắng và khả năng ghi nhớ thông tin có mối liên quan.
Nếu dược sỹ - người bán lẻ thuốc thấy khách hàng đang rất lo lắng thì cần lưu ý, nhắc nhở để khách hàng chú ý đến các thông tin trao đổi. Ví dụ tình huống khách hàng nữ đến nhà thuốc mua thuốc hạ sốt cho con và người bán lẻ thuốc thấy khách hàng đang rất lo lắng thì nên nói: “Em biết là chị đang rất lo lắng để có thể về nhà và cho bé uống thuốc. Nhưng việc em hướng dẫn cho chị cách sử dụng đúng thuốc này là rất quan trọng. Chị chú ý lắng nghe nhé.”
Còn nếu dược sỹ - người bán lẻ thuốc thấy người bệnh không lo lắng và có khả năng sẽ không tuân thủ điều trị thì cần phải nhắc nhở để người bệnh lưu ý. “Việc uống những viên thuốc này đủ 5 ngày là rất quan trọng. Nếu anh không uống đủ thời gian thì anh có thể bị mắc lại bệnh viêm phổi. Khi đó điều trị sẽ khó hơn và anh có thể sẽ phải nghỉ việc lâu hơn.”
Số lượng thông tin tư vấn bằng lời phù hợp với một cuộc trao đổi
Khi số lượng thông tin còn ít thì khả năng ghi nhớ hết các thông tin tốt hơn khi số lượng thông tin càng nhiều thì khả năng ghi nhớ thông tin giảm xuống.
Khi số lượng thông tin nhiều hơn 3 thì khách hàng có xu hướng không nhớ được hết các thông tin trao đổi. Vì vậy, dược sỹ - người bán lẻ thuốc phải biết phân tích tình huống để lựa chọn ra những thông tin được đánh giá là quan trọng thông thường là 3 để trao đổi bằng lời với người bệnh. Nếu dược sỹ - người bán lẻ thuốc có nhiều hơn 3 thông tin cần trao đổi thì phải sử dụng các biện pháp khác hỗ trợ giúp người bệnh có thể có được thông tin cần thiết.
Thông tin quan trọng được cung cấp vào những thời điểm phù hợp của giai đoạn tư vấn
Giữa thời điểm trao đổi và thông tin được ghi nhớ có mối liên quan. Một nghiên cứu đánh giá về mối liên quan giữa vị trí, thời điểm cung cấp các thông tin và khả năng ghi nhớ (hình 2.4) cho thấy tại thời điểm đầu và cuối giai đoạn tư vấn khả năng ghi nhớ thông tin là tốt nhất. Chính vì vậy những thông tin quan trọng dược sỹ - người bán lẻ thuốc nên lựa chọn để trao đổi ở đầu hoặc cuối giai đoạn tư vấn với người bệnh. Với những thuốc người bệnh mới sử dụng lần đầu hoặc đơn thuốc mới với người bệnh thì những thông tin được đánh giá là quan trọng cần trao đổi với người bệnh là thông tin về bệnh và thuốc (tác dụng, cách sử dụng, bảo quản). Khi tư vấn sử dụng thuốc với những tình huống người bệnh đã sử dụng thuốc hoặc đơn thuốc nhiều lần, trở nên quen thuộc, dược sỹ - người bán lẻ thuốc cũng cần đánh giá kinh nghiệm, cảm nhận của người bệnh về việc sử dụng thuốc. Những thông tin người bán lẻ thuốc cần trao đổi với người bệnh là: cảm nhận về hiệu quả của phác đồ điều trị, của thuốc; việc kiểm soát các triệu chứng bệnh khi sử dụng thuốc; những tác dụng thực tế gặp phải khi sử dụng thuốc; lý do tại sao người bệnh dừng, thay đổi thuốc hoặc phác đồ điều trị (vấn đề tuân thủ điều trị).
Thông tin cung cấp cần đảm bảo rõ ràng, tránh người bệnh hiểu lầm
Thông tin nếu đưa ra không cụ thể rõ ràng có thể sẽ khiến cho người bệnh hiểu sai dẫn đến những sai sót trong điều trị.
Dược sỹ - người bán lẻ thuốc không thể kiểm soát cách người bệnh hiểu thông tin nhận được. Vì vậy, dược sỹ - người bán lẻ thuốc phải luôn nhắc nhở bản thân về những gì có thể xảy ra và đảm bảo rằng giao tiếp của người bán lẻ thuốc là rõ ràng nhất có thể.
Ngoài ra, trong quá trình tư vấn, dược sỹ - người bán lẻ thuốc phải tôn trọng quan điểm của người bệnh. Người bệnh có những quan điểm riêng về thuốc và tình trạng sức khỏe của họ. Điều này không hẳn dựa trên ‗bằng chứng khoa học‘ nhưng cần được tôn trọng và thấu hiểu. Người bệnh có thể đưa ra các tín hiệu bằng ngôn ngữ hoặc phi ngôn ngữ để thể hiện quan điểm hoặc cảm xúc về vấn đề sức khỏe. Thấu hiểu quan điểm, cảm xúc của người bệnh giúp dược sỹ - người bán lẻ thuốc xây dựng mối quan hệ tốt với người bệnh, khiến họ dễ dàng tuân thủ theo các tư vấn trong sử dụng thuốc và thay đổi lối sống. Ví dụ khi người bệnh bước vào nhà thuốc và chia sẻ với người bán lẻ thuốc rằng họ mới bị chẩn đoán ung thư. Thay vì hỏi ngay về mục đích của việc đến nhà thuốc, dược sỹ - người bán lẻ thuốc có thể trao đổi về cảm xúc của họ hoặc các tác động đến gia đình của họ.
Đánh giá đảm bảo người bệnh nhớ được những thông tin tư vấn
Dược sỹ - người bán lẻ thuốc cần đánh giá xem người bệnh có hiểu những thông tin được cung cấp hay không bằng cách hỏi hoặc yêu cầu người bệnh mô tả lại cách họ sẽ sử dụng thuốc hoặc yêu cầu người bệnh sử dụng thử các thiết bị hỗ trợ điều trị như ống hít/ thuốc dạng xịt. Khi kiểm tra người bệnh có ghi nhớ được các thông tin đã trao đổi, dược sỹ - người bán lẻ thuốc nên áp dụng kỹ thuật "giảng dạy lại" (teach back) hoặc “chỉ cho tôi" (show me) đối với người bệnh. Xác nhận lại xem người bệnh đã nắm được đầy đủ thông tin đã hướng dẫn chưa thông qua kỹ năng phản ánh, nhắc lại và tóm tắt lại thông tin. Ví dụ như "Cháu muốn đảm bảo rằng mọi điều cháu giải thích đều rõ ràng. Nếu bác cần hướng dẫn sử dụng thuốc này cho bác trai, bác sẽ hướng dẫn như thế nào ạ?" Hoặc "Bác có thể cho cháu biết cách dùng của thuốc xịt này không?"
Phối hợp cả ngôn ngữ bằng lời và viết khi tư vấn
Khi lập kế hoạch điều trị cho người bệnh, dược sỹ - người bán lẻ thuốc nên dùng cả ngôn ngữ bằng lời và ngôn ngữ viết (hướng dẫn sử dụng, nhãn thuốc, thông qua các tờ rơi, lập bảng sử dụng thuốc…). Khi giao tiếp với người bệnh bằng ngôn ngữ viết, dược sỹ - người bán lẻ thuốc cần tạo điểm chú ý giúp người bệnh nhớ vị trí sẽ tìm thấy thông tin. Hãy để thông tin về sản phẩm (tờ rơi, tờ hướng dẫn sử dụng) ở vị trí mà cả người bán lẻ thuốc và người bệnh đều có thể nhìn rõ hoặc sử dụng phần thông tin đã viết làm hướng dẫn cho phần tư vấn của người bán lẻ thuốc (chuẩn bị trước, đánh dấu những điểm quan trọng). Đồng thời, dược sỹ - người bán lẻ thuốc cần theo dõi phản hồi của người bệnh trong quá trình trao đổi, tránh biến thông tin người bán lẻ thuốc viết ra là điểm tập trung duy nhất. Một số lưu ý khi sử dụng ngôn ngữ viết trong giao tiếp tại nhà thuốc:
- Sử dụng màu mực tương phản với màu giấy như màu đen hoặc màu xanh trên nền trắng.
- Viết rõ ràng, dễ đọc.
- Tiêu đề nhãn phải cụ thể.
- Ghi thời gian trên nhãn.
- Thông tin đầy đủ, tránh mơ hồ, không rõ ràng.
- Viết thông tin theo mẫu hoặc theo quy định những nội dung bắt buộc đối với thuốc ra lẻ không còn bao bì ngoài đính kèm.
- Ký tên và ghi rõ chức danh (nếu cần).
- Cần có nhãn bổ sung hoặc thông tin thêm trong một số trường hợp đặc biệt.
Phối hợp sử dụng một số biện pháp, kỹ thuật hướng dẫn khi tiến hành tư vấn (nếu có thể)
Khi tiến hành tư vấn nếu có thể dược sỹ - người bán lẻ thuốc nên sử dụng một số biện pháp, kỹ thuật để giúp người bệnh dễ dàng ghi nhớ được cách sử dụng thuốc, đặc biệt trong các tình huống đơn thuốc được đánh giá là phức tạp với người bệnh. Có rất nhiều nguyên nhân khác nhau khiến cho đơn thuốc được đánh giá là sử dụng phức tạp với người bệnh như: (1) Tần suất dùng thuốc nhiều hơn hai lần/ ngày hoặc các thuốc được sử dụng đa dạng vào các thời điểm khác nhau trong ngày. Một số nghiên cứu đã chỉ ra khi tần suất sử dụng thuốc lớn hơn hai lần/ ngày thì người bệnh sẽ có xu hướng tuân thủ điều trị thấp hơn. (2) Các vấn đề liên quan đến dạng bào chế của thuốc như dạng bào chế khó sử dụng hay hướng dẫn sử dụng phức tạp hoặc đơn thuốc có nhiều dạng bào chế khác nhau cũng khiến cho người bệnh cảm thấy khó khăn khi sử dụng thuốc. (3) Ngoài ra những hướng dẫn thêm để đảm bảo người bệnh có thể sử dụng đúng thuốc cũng khiến cho người bệnh có thể lúng túng. Chính vì vậy để đảm bảo hiệu quả điều trị của thuốc, dược sỹ - người bán lẻ thuốc cần phải có những lưu ý, nhắc nhở và tìm kiếm những giải pháp phù hợp với người bệnh.
Với những thuốc có dạng bào chế hoặc cách sử dụng được đánh giá là phức tạp khó khăn với người bệnh thì dược sỹ - người bán lẻ thuốc có thể sử dụng các biện pháp, kỹ thuật như làm mẫu hoặc sử dụng các thiết bị mô phỏng để hướng dẫn người bệnh cách sử dụng. Ngoài ra, việc áp dụng kỹ thuật “teach back” trong tình huống này cũng thường được dược sỹ - người bán lẻ thuốc lựa chọn. Khuyến khích người bệnh thực hành lại ngay trước mặt người bán lẻ thuốc cách sử dụng thuốc sẽ giúp dược sỹ - người bán lẻ thuốc đánh giá xem người bệnh sử dụng thuốc đã đúng chưa và đưa ra những điều chỉnh nếu cần. Hoặc sử dụng phối hợp tờ hướng dẫn sử dụng trong quá trình tư vấn cũng sẽ giúp cho người bệnh sử dụng thuốc dễ dàng hơn, điều này đặc biệt hữu ích trong trường hợp tờ hướng dẫn sử dụng có hình ảnh mô tả các thao tác.
Dược sỹ - người bán lẻ thuốc cũng có thể gợi ý người bệnh hoặc bác sĩ sử dụng chế độ dùng thuốc đơn giản hơn như sử dụng thuốc dạng viên phóng thích chậm để giúp giảm tần suất sử dụng thuốc hay sử dụng sản phẩm kết hợp giúp giảm số lượng thuốc phải sử dụng trong đơn. Nếu có thể nên khuyên người bệnh sử dụng cùng một dạng bào chế, thiết bị để đưa thuốc vào cơ thể.
Bên cạnh đó, dược sỹ - người bán lẻ thuốc cần giúp người bệnh lập một kế hoạch sử dụng thuốc phù hợp với thói quen hàng ngày của họ. Điều này sẽ giúp tạo sự thuận lợi và tăng tuân thủ điều trị ở người bệnh. Với trường hợp đơn thuốc quá phức tạp thì dược sỹ - người bán lẻ thuốc có thể giúp người bệnh lập một bảng sử dụng thuốc phù hợp hoặc tư vấn người bệnh sử dụng các dụng cụ phân chia liều dùng thuốc.
Trong trường hợp cần có những lưu ý thêm với người bệnh, dược sỹ - người bán lẻ thuốc cần phải tìm giải pháp để giúp đơn giản hóa những lời hướng dẫn để người bệnh có thể thực hiện theo. Dược sỹ - người bán lẻ thuốc phải hướng dẫn cụ thể về cách sử dụng thuốc cho người bệnh để người bệnh có thể bẻ hoặc nghiền viên thuốc trước khi sử dụng dễ dàng hơn. Với những thuốc mà cần phải hòa tan thuốc dạng bột vào nước để tạo thành hỗn dịch hoặc nhũ dịch trước khi sử dụng dược sỹ - người bán lẻ thuốc cũng cần phải có những hướng dẫn nhắc nhở. Với những thuốc mà khi sử dụng cho người bệnh phải tính theo cân nặng hoặc tuổi thì dược sỹ - người bán lẻ thuốc cũng cần tính sẵn liều quy về những đơn vị liều đơn giản với người bệnh. Ví dụ như hướng dẫn sử dụng paracetamol thay vì nói liều là 10-15mg/kg dược sỹ - người bán lẻ thuốc nên quy đổi về đơn vị liều là một gói hoặc một viên mỗi lần uống. Với những thuốc sử dụng liều khác nhau hoặc liều cách nhật thì người bán lẻ thuốc nên chuyển cụ thể thành lịch sử dụng thuốc để người bệnh có thể tuân thủ và sử dụng được dễ dàng. Ví dụ thứ 2-4-6 uống một viên, thứ 3-5-7-chủ nhật uống hai viên. Một số thuốc để có tác dụng tốt với người bệnh cần phải uống vào một thời điểm nhất định hoặc để tăng hấp thu cần sử dụng cách xa bữa ăn hoặc khi ăn thì dược sỹ - người bán lẻ thuốc cũng cần phải hướng dẫn để người bệnh biết và tuân thủ theo. Người bán lẻ thuốc cũng cần tư vấn cho người bệnh khi thuốc có tương tác với đồ ăn, thức uống để người bệnh biết và tránh. Hay đơn giản là dược sỹ - người bán lẻ thuốc hướng dẫn người bệnh sử dụng thuốc theo tờ hướng dẫn sử dụng thuốc hoặc lưu ý không cho người bệnh nằm xuống ngay sau khi uống thuốc đặc biệt với những người bệnh phải nằm thường xuyên, không di chuyển được.
Một số trường hợp bệnh người bệnh cần lưu ý khi tư vấn
Trường hợp người bệnh mắc bệnh nặng hoặc ác tính cần tư vấn để giúp người bệnh hiểu rõ về bệnh, lộ trình kiểm tra, điều trị và người bệnh có được tâm lý tốt và thoải mái hơn khi điều trị. Dược sỹ - người bán lẻ thuốc cũng cần tư vấn chi tiết trong trường hợp người bệnh có nhiều bệnh mắc kèm vì với những trường hợp này người bệnh phải sử dụng nhiều thuốc, dễ xảy ra tương tác thuốc.
Trường hợp người bệnh phải sử dụng các thuốc có khoảng điều trị hẹp hoặc khi người bệnh phải dùng nhiều thuốc với nhiều cách sử dụng thuốc khác nhau, dược sỹ - người bán lẻ thuốc phải tư vấn đầy đủ đảm bảo người bệnh có thể sử dụng thành thạo và đúng tất cả các dạng thuốc.
Trường hợp đối tượng sử dụng thuốc là các đối tượng đặc biệt như người cao tuổi, hoặc người bệnh không thể tự sử dụng thuốc (trẻ em, người ốm nặng…) hoặc người bệnh có tiền sử không tuân thủ điều trị, tiền sử không đáp ứng tốt trong điều trị, tiền sử đã từng gặp phản ứng phụ hoặc người nước ngoài, người dân tộc gặp những khó khăn, bất đồng về ngôn ngữ thì dược sỹ - người bán lẻ thuốc cũng cần phải chú ý hơn quá trình tư vấn/ khuyên
2.3. Kỹ năng giao tiếp với một số đối tượng
2.3.1. Người cao tuổi
Tuổi tác ảnh hưởng đến quá trình tiếp thu; khả năng tiếp thu của người cao tuổi thường chậm hơn so với người trẻ tuổi. Do đó, trong giao tiếp với người cao tuổi, dược sỹ - người bán lẻ thuốc nên chia các nội dung trao đổi thành những phần nhỏ để giúp họ dễ nhớ. Nhấn mạnh các điểm chính: “Thông tin này rất quan trọng” giúp cho người bệnh nhớ những điều cần thực hiện và đưa ra hướng dẫn cụ thể, rõ ràng. Có thể sử dụng hình ảnh hoặc trực quan sinh động hỗ trợ trong việc hướng dẫn dùng thuốc. Đồng thời, cần khuyến khích người cao tuổi phản hồi để biết họ có thực sự hiểu thông điệp được truyền tải.
Người cao tuổi thường bị giảm thị lực và thính lực nên trong khi trao đổi thông tin với họ, dược sỹ - người bán lẻ thuốc cần phải có điều chỉnh phù hợp tùy từng đối tượng.
Người cao tuổi có thị lực kém: khi giao tiếp với khách hàng có thị lực kém, giao tiếp bằng lời rất quan trọng và các thông điệp dược sỹ - người bán lẻ thuốc đưa ra cần rõ ràng, cụ thể. Người bán lẻ thuốc có thể cần trao đổi thêm với gia đình và người thân của người bệnh trong trường hợp cần thiết.
Người cao tuổi có thính lực kém:
Thính lực kém là một rào cản lớn trong giao tiếp. Một số dấu hiệu để nhận biết người bị giảm thính lực:
- Giọng nói to bất thường.
- Nghiêng đầu sang một bên hoặc khum tay để lên tai khi nghe.
- Tập trung vào môi người nói.
- Đưa ra những câu trả lời không phù hợp với nội dung hỏi.
- Có những biểu hiện nhầm lẫn.
- Thường yêu cầu người bán lẻ thuốc nói chậm lại hoặc nhắc lại thông tin.
- Không thể giao tiếp khi không thể nhìn vào miệng người bán lẻ thuốc.
- Không thể thực hiện cuộc nói chuyện trong điều kiện có tiếng ồn.
Khi nhận thấy có những dấu hiệu này người bán lẻ thuốc nên hỏi người bệnh xem họ muốn giao tiếp như thế nào. Ngoài ra, trong quá trình giao tiếp dược sỹ - người bán lẻ thuốc cần phải lưu ý một số điều sau:
- Hạn chế các tiếng ồn xung quanh: các âm thanh từ các cuộc nói chuyện khác, các thiết bị điện tử, tiếng ồn từ bên ngoài… khiến cho cuộc trao đổi thông tin giữa dược sỹ - người bán lẻ thuốc và người bệnh thêm khó khăn. Vì vậy hãy cố gắng lựa chọn khu vực yên tĩnh cho cuộc nói chuyện với người bệnh.
- Tập trung chú ý vào người bệnh: nói chuyện trực tiếp và duy trì tốt giao tiếp bằng mắt với người bệnh.
- Nói rõ ràng, rành mạch với tốc độ chậm, sử dụng các câu ngắn, đơn giản và dùng những từ ngữ quen thuộc với người bệnh. Đảm bảo ánh sáng phù hợp trên gương mặt của dược sỹ - người bán lẻ thuốc; không để tay, bút… che mặt, miệng khi đang nói.
- Sử dụng thêm giao tiếp bằng chữ viết để hỗ trợ cho cuộc nói chuyện của người bán lẻ thuốc với người bệnh và có thể trao đổi với người nhà nếu cần thiết.
2.3.2. Khách hàng khó tính
Khi trao đổi thông tin với khách hàng khó tính, người bán lẻ thuốc cần lưu ý một số điều sau để giao tiếp hiệu quả.
Người bán lẻ thuốc có thể áp dụng cách ứng xử quyết đoán, giữ bình tĩnh, chú ý đến ngôn ngữ cơ thể và tránh tranh cãi dù điều khách hàng phản đối có thể vô lý. Nếu dược sỹ - người bán lẻ thuốc nghe thấy khách hàng phản đối về một điều gì, hãy giải thích lại và trả lời ngắn gọn, đúng trọng tâm. Người bán lẻ thuốc hãy tạo cho khách hàng cảm giác nhẹ nhàng và ghi nhận những gì khách hàng phản đối. Tránh sử dụng từ “nhưng” thay vào đó hãy sử dụng từ “và”. Không nên phản đối ngay lập tức và dùng những động từ nhẹ như “Em biết là anh rất lo lắng về cách sử dụng thuốc này và…”.
Người bán lẻ thuốc hãy đưa ra các câu hỏi để khách hàng có thể nói tiếp về sự phản đối của họ và không được chen ngang, ngắt lời khi khách hàng trình bày. Ví dụ như “Anh có thể nói thêm cho em biết về điều gì làm anh không thoải mái…”, “Còn vấn đề gì về loại thuốc này làm anh lo lắng?”. Hãy sử dụng câu hỏi mở “Như thế nào?”, “Điều gì” để tìm hiểu các mối quan tâm của khách hàng, tránh sử dụng câu hỏi “Tại sao” (điều đó khiến khách hàng phải thanh minh) hoặc câu hỏi đóng (hạn chế nội dung trả lời).
Diễn đạt lại để đảm bảo người bán lẻ thuốc hiểu đúng những thông tin khách hàng truyền tải. Dược sỹ - người bán lẻ thuốc cũng có thể nhắc lại cảm giác của họ như “Em cảm thấy anh đang lo lắng về vấn đề này…” để thể hiện sự đồng cảm với người bệnh.
Người bán lẻ thuốc không nên tiết kiệm những lời nói như “vui - xin lỗi - sẵn sàng” trong khi giao tiếp với khách hàng đặc biệt là khách hàng khó tính. Nếu khách hàng chia sẻ những vấn đề lo lắng, những thắc mắc của khách hàng thì dược sỹ - người bán lẻ thuốc nên có phản ứng thể hiện sự động viên khuyến khích khách hàng. Nếu khách hàng phàn nàn với dược sỹ - người bán lẻ thuốc thì người bán lẻ thuốc nên ghi nhận và xin lỗi khách hàng về vấn đề ấy “Em xin lỗi vì đã làm anh cảm thấy không thoải mái”. Người bán lẻ thuốc cũng nên thể hiện sự cam kết sẽ giúp khách hàng giải quyết những vấn đề mà họ gặp phải. Điều này sẽ giúp tạo cảm giác an tâm và hài lòng cho khách hàng hơn “Em chắc chắn sẽ giải quyết vấn đề đó cho anh”.
Người bán lẻ thuốc cũng có thể áp dụng phương pháp 3F‘s (Cảm thấy - ‘feel’, đã cảm thấy ‘felt’, và đã thấy ‘found’) để giúp khách hàng thêm tự tin bản thân có thể vượt qua được những khó khăn trong điều trị. Người bán lẻ thuốc nên tránh sử dụng những câu nhằm mục đích thể hiện sự đồng cảm với người bệnh như “Em biết anh cảm thấy thế nào” nhưng lại khiến tạo cảm giác khó chịu cho người bệnh vì hầu hết mọi người đều sẽ nghĩ “Anh không thể biết được cảm xúc, cảm nghĩ của tôi”.
Tập trung vào những gì dược sỹ - người bán lẻ thuốc có thể làm, không phải những gì dược sỹ - người bán lẻ thuốc không làm được cho người bệnh. Ví dụ như, “Em có thể đưa anh hướng dẫn sử dụng để mang về.” hay “Em sẽ rất vui nếu lần sau anh quay lại nhà thuốc và chia sẻ những vấn đề về điều trị khi sử dụng bình xịt định liều mới”.
Đôi khi khách hàng sẽ cố gắng đánh lạc hướng của dược sỹ - người bán lẻ thuốc để lẩn tránh vấn đề. Để giải quyết tình huống này, dược sỹ - người bán lẻ thuốc có thể sử dụng một số cụm từ như “trước hết, đầu tiên”. Ví dụ “Chúng ta sẽ trao đổi từng vấn đề riêng. Trước hết, em sẽ trao đổi với anh về…..”. Lưu ý giọng nói và tốc độ nói của dược sỹ - người bán lẻ thuốc khi giải thích cho khách hàng. Dược sỹ - người bán lẻ thuốc cũng không nên trình bày tiếp nếu không được sự đồng ý của khách hàng. Sau khi trao đổi dược sỹ - người bán lẻ thuốc nên kiểm tra lại lần nữa để chắc chắn khách hàng đã hiểu đúng. Khi đó người bán lẻ thuốc cũng nên nói theo cách không thể hiện sự thiếu hiểu biết của người bệnh bằng cách nói “Những gì em vừa giải thích có gì không rõ ràng không?” thay vì hỏi “Anh có hiểu những điều em vừa nói không?”. Điều này sẽ khiến cho khách hàng cảm thấy thoải mái hơn khi trả lời “Có”.
2.3.3. Khách hàng trầm cảm
Khoảng 10% người lớn tại các nước phương tây trải qua giai đoạn trầm cảm mỗi năm, tỷ lệ gặp ở nữ giới cao hơn nam giới hai lần. Tại Việt Nam, bệnh trầm cảm đang có xu hướng gia tăng và trẻ hóa. Trong giao tiếp tại nhà thuốc, người bán lẻ thuốc có thể đã gặp nhiều người bệnh có vấn đề về tâm thần với các biểu hiện khác nhau (Bảng 2.2). Do đó, kỹ năng giao tiếp và điều trị cần phù hợp với từng đối tượng người bệnh.
Phân biệt giữa những trường hợp trầm cảm thoáng qua (một người trải qua giai đoạn cảm thấy buồn bã, chán nản nhưng những giai đoạn đó sẽ qua và không cần dùng thuốc điều trị) và trầm cảm kéo dài không phải dễ dàng.
Bảng 2.2. Dấu hiệu của trầm cảm
| - Cảm giác buồn chán, tuyệt vọng, cảm thấy mình vô dụng |
| - Mất hứng thú trong các hoạt động hoặc sở thích hàng ngày |
| - Mất cảm giác ngon miệng hoặc sút cân |
| - Mất nhu cầu tình dục |
| - Mất ngủ |
| - Luôn cảm thấy mệt mỏi |
| - Khó tập trung suy nghĩ |
| - Cảm thấy cuộc sống không có ý nghĩa |
Trong những trường hợp nghiêm trọng, nhiều người bệnh trầm cảm có ý định tự sát. Nhân viên y tế có thể là những người đầu tiên phát hiện hoặc biết được dấu hiệu về ý định tử tự ở người bệnh. Phát hiện sớm những nguy cơ và thực hiện các hành động phù hợp, khẩn cấp là ưu tiên hàng đầu. Trong những trường hợp đó, cần tìm hiểu thông tin và xử lý chuyên nghiệp.
Trầm cảm có thể biểu hiện khác nhau giữa từng người bệnh nên việc hiểu và giao tiếp với người bệnh của nhân viên y tế gặp nhiều khó khăn, bao gồm cả việc xác định và đánh giá tình hình:
- Phát hiện sớm trầm cảm là rất quan trọng.
- Cần có cái nhìn đầy đủ về tình trạng bệnh, mức độ biểu hiện bệnh có thực sự rõ ràng.
- Cần ghi nhớ rằng nhiều biểu hiện (đặc biệt như mất ngủ, đau đầu, đau dạ dày, mệt mỏi, sức khỏe yếu kém nói chung, ứng xử giận dữ…) có thể là biểu hiện của trầm cảm và những triệu chứng này có thể làm trệch hướng nhận biết trạng thái tâm lý hoặc khiến chúng ta tập trung vào tình trạng bệnh.
- Quan tâm nghiêm túc đến quan điểm của người trầm cảm về bản thân họ, về cuộc sống (với thái độ đồng cảm. Không nói với họ rằng mọi việc không quá tệ hoặc bị cuốn vào cảm xúc tiêu cực, bi quan của người trầm cảm.
- Phân biệt giữa buồn bực, tiêu cực thoáng qua và trầm cảm thực sự.
Nhiều người trầm cảm hoặc có bệnh tâm thần thường đổ lỗi cho bản thân mình về hoàn cảnh của họ và không sẵn sàng chia sẻ điều đó với nhân viên y tế hoặc những người xung quanh.
Giao tiếp với người bệnh trầm cảm và gia đình của họ với sự tôn trọng, kiên nhẫn, tình thương như với các người bệnh khác. Trong thực hành, người bán lẻ thuốc cần lưu ý các điều sau:
- Một số người bệnh trầm cảm có thể cần thêm sự hỗ trợ trong việc ghi nhớ và duy trì các cuộc hẹn gặp.
- Người bệnh trầm cảm có thể cảm thấy bối rối, căng thẳng, thậm chí là hoảng loạn khi phải ra khỏi nhà hoặc đến một buổi tư vấn với người bán lẻ thuốc. Người bán lẻ thuốc có thể gợi ý người bệnh liệt kê các câu hỏi hoặc các vấn đề quan tâm trước buổi gặp và/hoặc đi cùng với người thân, bạn bè để cảm thấy yên tâm hơn.
Tài liệu tham khảo
1. Nguyễn Thanh Bình, Đỗ Xuân Thắng (2020), Dược cộng đồng, giáo trình đào tạo dược sỹ đại học, Nhà xuất bản Y học
2. Nguyễn Thanh Bình, Lê Viết Hùng (2011), Kỹ năng giao tiếp và thực hành tốt nhà thuốc, NXB Giáo dục
CHƯƠNG 3. HƯỚNG DẪN TƯ VẤN ĐỐI VỚI MỘT SỐ TRIỆU CHỨNG BỆNH/BỆNH THƯỜNG GẶP TẠI CỘNG ĐỒNG
Người bán lẻ thuốc có vai trò quan trọng trong việc tư vấn xử trí với một số triệu chứng bệnh thường gặp, không phức tạp (bệnh nhẹ) trong cộng đồng. Tại cơ sở bán lẻ thuốc, người bán lẻ thuốc thực hiện hoạt động bán thuốc, tư vấn theo quy trình của cơ sở. Nhằm hỗ trợ người bán lẻ thuốc, chương này hướng dẫn tư vấn đối với một số triệu chứng bệnh nhẹ thường gặp tại cộng đồng. Trong lần ban hành đầu tiên của cuốn tài liệu này, một số triệu chứng bệnh được lựa chọn bao gồm: ho, cảm lạnh, tiêu chảy, táo bón với nội dung được trình bày như sau:
A.Ho (Cough)
1. Đại cương
Ho là cơ chế bảo vệ của cơ thể, có tác dụng làm sạch hoặc thông thoáng đường dẫn khí và đẩy các hạt/chất nhầy ra khỏi cơ thể. Đây là triệu chứng hô hấp phổ biến nhất và là biểu hiện bất thường của đường hô hấp. Ho có thể làm suy nhược sức khỏe của người bệnh, làm giảm chất lượng cuộc sống.
Có nhiều cách phân loại khác nhau về ho. Theo chất tiết bao gồm ho có chất tiết (ho có đờm/dịch); hoặc ho không có chất tiết (ho khan, ho do co thắt, ho do kích ứng họng). Theo thời gian ho được phân loại gồm ho cấp tính (ho kéo dài dưới 3 tuần), ho bán cấp (ho từ 3 đến 8 tuần), ho mạn tính (ho kéo dài>8 tuần).
Trong thực hành nhà thuốc cộng đồng, cần khuyên bệnh nhân đến bác sĩ để thăm khám trong trường hợp ho > 3 tuần (ho bán cấp, ho mạn tính). Trường hợp ho cấp tính thường gặp nhất là do nhiễm virus đường hô hấp trên, chẳng hạn như trong cảm lạnh hoặc cúm. Ho thường tự khỏi trong vòng từ 3 đến 4 tuần.
2. Khai thác thông tin của người bệnh
Người bán thuốc cần khai thác thông tin và đánh giá tình trạng của người bệnh trước khi quyết định xử trí và tư vấn.
2.1. Đặc điểm người bệnh
Cần xem xét:
- Tuổi
- Tình trạng mang thai, cho con bú
- Tiền sử dị ứng hoặc quá mẫn với thuốc (ví dụ đang dùng thuốc ức chế men chuyển)
2.2. Triệu chứng
Ho là triệu chứng của rất nhiều bệnh. Người bán thuốc cần khai thác thông tin về thời gian ho, tính chất ho (ho có đờm/ho không đờm), đặc điểm dịch tiết, thời gian khởi phát ho, tần suất ho, thời điểm xuất hiện ho, tính chu kỳ, tình trạng sốt, tình trạng đường thở (khò khè, khó thở) và các triệu chứng khác kèm theo để phân biệt. Căn cứ thời gian ho của người bệnh để phân loại gồm ho cấp tính (dưới 3 tuần), ho kéo dài (trên 3 tuần).
Ho cấp tính:
Do nhiễm virus: khởi phát đột ngột, có thể có đờm (đờm trong/ trắng) hoặc không có đờm, thường kèm theo các triệu chứng của cảm lạnh (đau họng, hắt hơi, viêm mũi, sốt); Các triệu chứng thường nặng hơn vào buổi tối.
Do dị ứng: thường theo mùa, không có đờm, kèm theo hắt hơi, chảy nước mũi hoặc ngạt mũi và ngứa mắt, ngứa cổ họng.
Do viêm thanh-khí-phế quản: thường xảy ra ở trẻ sơ sinh và trẻ nhỏ; trước đó sẽ có các triệu chứng của cảm lạnh, ho và kèm khó thở, khò khè khi hít thở.
Viêm phổi: Ho khan, đau và có thể kèm theo sốt, khó chịu, khó thở, ớn lạnh, nhức đầu. Ban đầu ho không có đờm nhưng sau đó chuyển thành ho có đờm màu đỏ.
Ho kéo dài (ho bán cấp, mạn tính)
Ho bán cấp thường do nhiễm trùng đường thở, có thể xảy ra sau khi người bệnh bị nhiễm trùng đường hô hấp và dẫn đến ho dai dẳng, không có đờm có thể kéo dài đến 8 tuần. Triệu chứng này thường sẽ tự khỏi và không cần điều trị.
Ho mạn tính có thể do các bệnh lý hoặc do sử dụng thuốc có các tác dụng phụ gây ho (chi tiết xem tại mục 2.3. tiền sử và lối sống)
2.3. Tiền sử và lối sống
- Tiền sử bệnh có thể góp phần gây ra ho mạn tính bao gồm:
Viêm phế quản mạn tính: Thường là do hút thuốc lá, đây là nguyên nhân phổ biến nhất của ho mạn tính.
Hội chứng ho từ đường dẫn khí trên (hội chứng chảy dịch mũi sau): có thể do dị ứng hoặc viêm mũi vận mạch, viêm xoang mạn tính, viêm mũi sau nhiễm trùng, viêm mũi có liên quan thai kỳ. Đặc điểm là ho khi cười hoặc khi nói trong thời gian dài và ho trầm trọng hơn khi nằm, họng thường sạch.
Bệnh hen phế quản: Kèm theo thở khò khè, tức ngực; trầm trọng hơn do lạnh hoặc khi tập thể dục; tăng lên vào ban đêm; tiếp xúc với dị nguyên.
Hội chứng trào ngược dạ dày thực quản: ho tăng lên khi nằm, vào lúc đói. Có triệu chứng ợ chua, đau thượng vị, cảm giác nóng rát sau xương ức chỉ xảy ra ở một số ít người.
Các nguyên nhân khác: bệnh lý (lao, tràn khí màng phổi, giãn phế quản, ung thư phổi, bệnh phổi kẽ, ho gà, suy tim), ho do tâm lý, ho liên quan đến tiền sử dùng thuốc
- Tiền sử dùng thuốc do người bệnh sử dụng các thuốc có tác dụng phụ gây ho như sử dụng các thuốc ức chế men chuyển, chẹn beta giao cảm, các thuốc chống viêm không steroid (NSAIDs).
- Lối sống: tiếp xúc với chất kích ứng hô hấp (ví dụ: khói thuốc lá), hút thuốc lá.
3. Đánh giá tình trạng của người bệnh - trường hợp cần thiết phải đi khám bác sĩ
Cần tư vấn cho người bệnh đi khám bác sĩ khi có một trong các dấu hiệu sau đây:
Ho kéo dài hơn 3 tuần
Đau ngực
Nghi ngờ ho gà hoặc viêm thanh khí phế quản
Thở khò khè và/hoặc khó thở
Đờm đặc, vàng hoặc xanh
Đờm có máu
Đờm có màu gỉ sắt
Đờm sủi bọt và có màu đỏ hồng
Đau ngực khi hít sâu
Nghi ngờ tác dụng không mong muốn của thuốc
Ho tái phát thường xuyên
Ho liên tục về đêm đối với trẻ
Có dấu hiệu suy nhược đối với người cao tuổi
Người bệnh bị giảm cân mà không rõ nguyên nhân
4. Khuyến cáo điều trị
4.1. Mục tiêu điều trị
Ho cấp tính - giảm triệu chứng
Ho cấp tính hầu hết do nhiễm virus, không sử dụng kháng sinh bởi có thể gây nhiều nguy cơ hơn lợi ích của thuốc.
4.2. Các lựa chọn điều trị
Chưa có bằng chứng rõ ràng về hiệu quả điều trị của các thuốc không kê đơn điều trị ho cấp tính.
Không nên sử dụng sản phẩm có chứa đồng thời thuốc giảm ho và thuốc long đờm/tiêu chất nhày.
Thuốc giảm ho: giảm ho khan trong thời gian ngắn với tác dụng giảm phản xạ ho, có vai trò hạn chế trong điều trị ho cấp tính. Không nên sử dụng khi ho có đờm và tránh trường hợp hen phế quản, bệnh mạch vành mạn tính.
Ngoài ra, những biện pháp giảm ho được khuyến cáo như sử dụng siro ho, viên ngậm ho.
Thuốc tiêu chất nhày: làm loãng các dịch tiết, tạo điều kiện thuận lợi cho chất nhày có thể di chuyển dễ dàng và được tống ra khỏi đường hô hấp bởi hệ thống lông chuyển hoặc sự khạc đờm. Các thuốc trong nhóm như: guafenesin, bromhexin acetylcystein, carbocystein, ambroxol.
Thuốc kháng histamin: có thể hữu ích nếu ho đi kèm với chảy dịch mũi sau hoặc viêm mũi dị ứng nhưng cần tránh nếu ho có đờm (nguy cơ tắc nghẽn chất nhầy).
Thuốc thông mũi-giảm nghẹt mũi (thuốc dùng tại chỗ): có thể hữu ích nếu người bệnh ho đi kèm với ngạt mũi, nhưng nếu không có triệu chứng ngạt mũi thì nên tránh sử dụng. Các thuốc cường giao cảm tại chỗ như: naphazolin, oxymetazolin, xylometazolin. Chú ý chống chỉ định sử dụng các thuốc cường giao cảm ở người tăng huyết áp, cường giáp, bệnh mạch vành, đái tháo đường và dùng đồng thời với các chất ức chế imonoamine oxidase.
Tóm tắt một số thuốc điều trị ho được trình bày tại bảng 3.1.
Bảng 3.1. Tóm tắt một số thuốc điều trị ho
| Tên thuốc | Tác dụng phụ thường gặp | Lưu ý tương tác thuốc | Thận trọng khi sử dụng trên bệnh nhân | Khuyến cáo dành cho PNCT và CCB | ||||
| Thuốc tiêu chất nhày | ||||||||
| Guaifenesin | Nôn và buồn nôn | Không | Quá liều có thể dẫn đến tổn thương thận | Sử dụng được cho PNCT. Chưa có dữ liệu với PN CCB | ||||
| Bromhexin | Đau thượng vị, buồn nôn, nôn, tiêu chảy, nhức đầu chóng mặt, ra mồ hôi, ban da, mày đay, nguy cơ ứ dịch tiết phế quản ở người không có khả năng khạc đờm | Không phối hợp với thuốc làm giảm tiết dịch như các thuốc kiểm atropin vì làm giảm tác dụng của bromhexin Không phối hợp với các thuốc chống ho | Tránh phối hợp với thuốc ho vì có nguy cơ ứ đọng đờm ở đường hô hấp (đặc biệt là trẻ em dưới 2 tuổi vì không có khả năng khạc đờm) | Chưa có dữ liệu với PNCT và CCB | ||||
| Acetylcystein | Buồn nôn, nôn; buồn ngủ, nhức đầu, ù tai; viêm miệng, chảy nước mũi nhiều; phản ứng dị ứng (phát ban, mày đay) | Tiền sử loét dạ dày; giám sát chặt chẽ khi dùng thuốc ở người có tiền sử dị ứng vì nguy cơ phát hen. Nếu có nhiều đờm loãng ở phế quản, phải hút ra khi người bệnh giảm khả năng ho Không dùng đồng thời với các thuốc chống ho hoặc thuốc làm giảm bài tiết dịch phế quản. | Chống chỉ định ở trẻ < 2 tuổi với chỉ định tiêu chất nhày | Chưa có dữ liệu với PNCT An toàn cho PN CCB | ||||
| Ambroxol | Ợ nóng, khó tiêu, buồn nôn, nôn, phát ban | Không phối hợp ambroxol với một thuốc giảm ho (như codein) hoặc một thuốc làm gây giảm tiết (như atropine và các thuốc kháng cholinergic khác) | Người có bệnh lý loét đường tiêu hóa, các trường hợp ho ra máu, vì ambroxol có thể làm tan các cục đông fibrin và làm xuất huyết trở lại. Điều trị ambroxol đợt ngắn hạn, nếu không đỡ cần khám lại | Chưa có dữ liệu với PNCT và CCB | ||||
| Thuốc giảm ho - giảm phản xạ ho trong thời gian ngắn (ho khan) | ||||||||
| Codein | Táo bón, buồn ngủ, nôn, đau đầu, khô miệng | Tăng tác dụng buồn ngủ, ức chế thần kinh trung ương khi dùng cùng với rượu, các thuốc giảm đau opioid, thuốc an thần, thuốc ngủ, thuốc chống trầm cảm | Hen phế quản | Tránh sử dụng trong 3 tháng đầu thai kỳ. Có thể sử dụng trong thời gian ngắn cho phụ nữ cho con bú. Gây buồn ngủ và chán ăn ở trẻ em. | ||||
| Dextromethorphan | ||||||||
| Kháng histamin - sử dụng khi ho đi kèm với chảy dịch mũi sau hoặc viêm mũi dị ứng nhưng cần tránh nếu ho có đờm | ||||||||
| Diphenhydramin | Khô miệng, buồn ngủ và táo bón | Tăng tác dụng buồn ngủ khi dùng cùng rượu, giảm đau opioid, thuốc an thần, thuốc ngủ và thuốc chống trầm cảm | Glaucom, phì đại tuyến tiền liệt lành tính. Hạn chế sử dụng cho người cao tuổi và trẻ em dưới 6 tuổi (tăng nhạy cảm với các tác dụng KMM) | Sử dụng được cho PNCT mặc dù 1 số nhà sản xuất khuyên tránh dùng Sử dụng được cho PN CCB vì một lượng thuốc nhỏ vào sữa mẹ. Tuy nhiên, có thể làm giảm lượng sữa và có báo cáo trẻ bú kém hơn. | ||||
| Chất làm dịu | ||||||||
| Mật ong | Không | Không | Không | Có thể sử dụng | ||||
Ghi chú: PNCT - Phụ nữ có thai, PN CCB - Phụ nữ cho con bú
4.3. Điều trị ho ở trẻ em
Nghiên cứu gần đây cho thấy thuốc ho cho trẻ em không tốt hơn giả dược. Chức năng của phản xạ ho là làm sạch chất tiết ra khỏi đường hô hấp và việc giữ lại những chất tiết này có thể gây hại dẫn đến tắc nghẽn đường thở. Đôi khi, trẻ có thể kiệt sức hoặc mất ngủ hoặc nôn trớ nhiều lần do ho. Trong những trường hợp này, việc sử dụng thuốc giảm ho có thể hữu ích. Các hướng dẫn sau nên được tuân thủ:
- Chỉ nên sử dụng thuốc ở bệnh nhân đã được xác định không có dấu hiệu nào cần phải đi khám bác sĩ.
- Không nên sử dụng cho trẻ dưới 2 tuổi thuốc điều trị ho và cảm lạnh có chứa kháng histamin H1 có tác dụng an thần, thuốc giảm ho, thuốc long đờm hoặc thuốc chống sung huyết mũi.
- Nên tránh sử dụng các chế phẩm có chứa long não cho trẻ em do nguy cơ gây tác dụng phụ lên hệ thần kinh trung ương như co giật hoặc suy hô hấp.
- Không nên sử dụng sirô chứa cồn: cồn có thể làm trẻ an thần và ức chế cơn ho.
- Một số sirô ho có thể chứa hàm lượng đường lớn, nếu sử dụng quá nhiều, các sirô này có thể gây tiêu chảy thẩm thấu.
- Không nên cho trẻ sơ sinh bú sữa mẹ hoàn toàn uống sirô: đường trong sirô có thể làm trẻ giảm bú sữa mẹ.
- Mật ong có thể hiệu quả trong điều trị ho ở trẻ em > 1 tuổi. Tránh sử dụng mật ong với trẻ nhỏ hơn 1 tuổi.
5. Cung cấp thông tin và tư vấn
5.1. Cách sử dụng thuốc
Khi một loại thuốc không kê đơn được lựa chọn, người bệnh/khách hàng phải được hướng dẫn cách sử dụng, liều lượng chính xác và lưu ý khi sử dụng.
5.2. Tác dụng không mong muốn của thuốc
Tác dụng không mong muốn của thuốc xem tại bảng 3.1.
5.3. Tư vấn biện pháp không dùng thuốc
- Nghỉ ngơi, giữ ấm họng và cơ thể. Tránh không khí khô, khói thuốc lá, các chất gây kích ứng.
- Uống nhiều nước. Uống ít nhất 2 lít nước (từ 6 đến 9 cốc nước) mỗi ngày.
- Chanh nóng và mật ong (không thích hợp cho trẻ nhỏ dưới 1 tuổi). Thêm nước ép vắt từ nửa quả chanh và một đến hai thìa cà phê mật ong cho vào một cốc nước đun sôi và uống khi còn ấm.
- Làm dịu họng bằng cách súc miệng với nước muối ấm, nhiều lần mỗi ngày
- Ngừng hút thuốc lá, hút thuốc là lý do phổ biến dẫn đến tình trạng ho liên tục
5.4. Tiếp tục theo dõi (Follow-up)
Hầu hết ho có thể tự khỏi
Cần tư vấn người bệnh/khách hàng rõ các thông tin về:
- Thời gian điều trị (sử dụng thuốc/biện pháp)
- Trường hợp cần quay lại nhà thuốc/quầy thuốc hoặc các trường hợp cần tìm kiếm sự chăm sóc y tế, đi khám bác sĩ (xem mục 3.1)
Tài liệu tham khảo
1. Bộ Y tế (2012), Hướng dẫn chẩn đoán và điều trị bệnh hô hấp, ban hành kèm theo Quyết định số 4235/QĐ-BYT ngày 31/12/2012, Hướng dẫn chẩn đoán và điều trị ho kéo dài, trang 11-14
2. Bộ Y tế (2018), Dược thư quốc gia Việt Nam.
3. Bộ Y tế (2017), Dược thư quốc gia Việt Nam dùng cho tuyến cơ sở.
4. Pharmaceutical Society of Australian (2009), Australian Pharmaceutical Formulary and handbook, 21 st edition, Section E, Cough guide, pp 381-383.
5. Pharmaceutical Society of Australian (2020), Australian Pharmaceutical Formulary and handbook, 21 st edition, Section E, Cough guide, pp 381-383.
6. National Institute for Health and Care Excellence (2019), NICE Clinical guidance Cough (acute), https://www.nice.org.uk/guidance/ng120
7. NHS (2020), Cough - NHS (www.nhs.uk)
8. Paul Rutter (2021), Community Pharmacy: Symptoms, Diagnosis and Treatment, Fifth edition, Elsevier, Cough, pp 10-20.
B. Cảm lạnh (Common Cold)
1. Đại cương
Cảm lạnh, với triệu chứng ho đi kèm, là bệnh thường gặp nhất tại cộng đồng. Trẻ em bị cảm lạnh thường xuyên hơn người lớn. Cảm lạnh không có thuốc điều trị đặc hiệu và khoảng 2/3 người bị bệnh có khả năng tự phục hồi trong vòng một tuần. Tuy nhiên, do số ca bệnh rất nhiều nên điều quan trọng là người dược sỹ cần phải hiểu biết về tình trạng có triệu chứng nặng hoặc các triệu chứng gợi ý cúm.
Cảm lạnh là một bệnh nhiễm trùng nhẹ ở mũi và họng (đường hô hấp trên). Cảm lạnh có thể kéo dài khoảng 1 đến 2 tuần, nhưng các triệu chứng thường nhẹ. Cảm lạnh thường gặp do nhiễm virus, dễ lây truyền khi ho hoặc hắt hơi. Ngoài ra, sự lây truyền chủ yếu là do tay tiếp xúc với virus, sau đó chạm vào mũi, miệng và mắt. Các giọt nước rơi ra từ mũi phủ lên các bề mặt như tay nắm cửa và điện thoại. Virus gây cảm lạnh có thể tồn tại trên các bề mặt này trong vài giờ và lây nhiễm cho người khác khi họ chạm vào các bề mặt này. Sự lây truyền do ho và hắt hơi xảy ra, mặc dù nó là một cơ chế thứ cấp. Đây là lý do tại sao vệ sinh tốt (rửa tay thường xuyên và sử dụng khăn giấy dùng một lần) vẫn là nền tảng của việc giảm sự lây lan của cảm lạnh. Cảm lạnh dễ lây nhất trong 1-2 ngày đầu tiên khi bệnh nhân xuất hiện các triệu chứng.
Hơn 200 loại virus khác nhau có thể gây ra các triệu chứng của cảm lạnh, bao gồm rhinovirus (chiếm 30-50% trong tất cả các trường hợp), coronaviruses, parainfluenza virus, vi rút hợp bào hô hấp và adenovirus. Khi tiếp xúc với niêm mạc, virus sẽ xâm nhập vào biểu mô mũi và phế quản, gắn vào các thụ thể và gây tổn thương cho các tế bào có lông. Điều này dẫn đến việc giải phóng các chất trung gian gây viêm, do đó, dẫn đến kích thích các biểu mô ở mũi, tăng khả năng thẩm thấu của thành tế bào mao mạch dẫn đến phù nề, người bệnh nghẹt mũi và hắt hơi. Chất lỏng có thể chảy xuống sau cổ họng, lan truyền virus đến cổ họng và phía trên ngực, gây ho và đau họng.
2. Khai thác thông tin
2.1. Đặc điểm người bệnh
Cần xem xét:
- Tuổi
- Tình trạng mang thai, cho con bú
- Tiền sử dị ứng hoặc quá mẫn với thuốc
2.2. Triệu chứng
Các triệu chứng cảm lạnh xuất hiện dần dần và bao gồm:
- Ngạt mũi hoặc chảy nước mũi
- Đau họng
- Ho
- Đau đầu hoặc đau người
- Hắt hơi
- Sốt
- Giảm hoặc mất vị giác và khứu giác.
Các triệu chứng ở người lớn và trẻ em đều giống nhau. Đôi khi các triệu chứng ở trẻ em kéo dài hơn. Người bệnh thường sử dụng từ "cúm" khi mô tả cảm lạnh thông thường. Tuy nhiên, không dễ phân biệt các triệu chứng giữa cảm lạnh và cúm.
Các bệnh khác có dấu hiệu tương tự cảm lạnh như sau:
Bảng 3.2. Bệnh có triệu chứng tương tự với cảm lạnh
| Bệnh | Đặc điểm đặc trưng |
| Cúm | - Sốt cao (39°C đến 40°C), khởi phát đột ngột - Ớn lạnh - Đổ mồ hôi - Đau cơ nặng |
| Viêm xoang | - Dịch mũi đặc, vàng-xanh - Đau/sưng tấy/áp lực xung quanh mắt, mũi, má, trán. Đau hơn khi ho, hắt hơi và cúi xuống. - Đau nhức hàm trên/răng - Giảm khứu giác và vị giác - Hội chứng hôi miệng - Ù tai - Sốt (gợi ý nhiễm trùng lan đến vùng xoang) |
| Viêm mũi dị ứng | - Ngứa mũi, mắt, miệng - Hắt hơi - Các triệu chứng ở mắt (viêm kết mạc, chảy nước mắt) - Đau đầu - Ho/thở khò khè (thường ở bệnh nhân hen) |
| Viêm phổi | - Đau ngực - Khó thở - Sốt - Ớn lạnh - Nôn hoặc buồn nôn - Lú lẫn/mất định hướng (chủ yếu ở người cao tuổi) |
| Viêm nắp thanh quản | - Khó nuốt - Chảy nước dãi - Thở khò khè - Khó thở - Sốt - Bồn chồn |
| Viêm amidan | - Amidan sưng, đỏ kèm dịch - Sốt - Sưng hạch bạch huyết - Nuốt khó - Giọng nói nghẹt - Hôi miệng - Rối loạn tiêu hóa Ở trẻ nhỏ: - Chảy nước nhãi - Chán ăn. Cáu kỉnh bất thường |
| Viêm tiểu phế quản | - Suy hô hấp - Thở khò khè - Sốt - Hôn mê |
2.3. Tiền sử và lối sống
Yếu tố tiền sử bệnh và lối sống có thể làm tăng nguy cơ và/hoặc mức độ nghiêm trọng của cảm lạnh bao gồm:
- Hút thuốc
- Bệnh mạn tính hoặc suy giảm miễn dịch
- Căng thẳng hoặc mất ngủ
3. Đánh giá tình trạng người bệnh - Trường hợp cần đi khám bác sĩ
Các dấu hiệu cảnh báo, yêu cầu phải khám bác sĩ (xem thêm mục triệu chứng “ho”)
- Sốt > 39°C hoặc ớn lạnh
- Sốt trong 5 ngày hoặc sốt trở lại sau khi đã hết sốt
- Khó thở
- Thở khò khè
- Đau đầu nặng, đau họng, đau xoang hoặc đau cơ
- Mất nước
- Buồn nôn
Các dấu hiệu yêu cầu phải đưa trẻ đi khám bác sĩ bao gồm:
- Sốt > 38°C ở trẻ nhỏ
- Sốt tăng lên hoặc sốt kéo dài > 2 ngày ở trẻ em ở bất kỳ lứa tuổi nào
- Triệu chứng không cải thiện hoặc nặng hơn
- Đau tai
- Khó chịu
- Chán ăn hoặc không thèm ăn
- Phồng thóp
- Buồn ngủ hoặc mệt mỏi
Trường hợp sốt cao, ho, khó thở hoặc mất/giảm khứu giác/vị giác, có thể do coronavirus (covid-19), cần khai báo với cơ quan quản lý theo quy định.
4. Khuyến cáo điều trị
4.1. Mục tiêu điều trị
- Giảm nhẹ triệu chứng
- Xác định các triệu chứng dai dẳng hoặc bất thường và điều trị nguyên nhân hoặc chuyển khám bác sĩ khi cần thiết.
- Cảm lạnh thông thường hầu hết là do virus, không sử dụng kháng sinh để điều trị và thậm chí có thể gây ra tác dụng không mong muốn.
4.2. Lựa chọn điều trị
- Sử dụng chế phẩm đơn thành phần được khuyến cáo bởi liều dùng linh hoạt hơn và giảm nguy cơ quá liều. Tuy nhiên, chế phẩm 2 thành phần điều trị ho và cảm lạnh giúp tiết kiệm chi phí, tăng tuân thủ điều trị (ví dụ thuốc kết hợp kháng histamin và thông mũi) được xem có hiệu quả với người lớn.
- Chưa có đủ bằng chứng cho việc sử dụng các thuốc hỗ trợ (như vitamin C, thảo dược như echinacea) để phòng ngừa hoặc điều trị cảm lạnh.
- Các thông tin về thuốc lựa chọn điều trị trình bày trong bảng 3.3. Thông tin về điều trị ho xem trong phần hướng dẫn điều trị Ho.
Bảng 3.3. Lựa chọn điều trị cảm lạnh
| Thuốc | Tác dụng không mong muốn | Phụ nữ có thai và cho con bú | Ghi chú |
| Paracetamol hạ sốt; giảm đau từ nhẹ đến trung bình | Tổn thương gan (trường hợp quá liều) | Sử dụng được (loại A) | Lưu ý khi sử dụng với các thuốc phối hợp trong điều trị ho và cảm lạnh vì nguy cơ dùng quá liều khuyến cáo |
| Thuốc chống viêm non-steroid (NSAIDs) - giảm đau hạ sốt | |||
| Ibuprofen Naproxen | Trên tiêu hóa (buồn nôn, khó tiêu, xuất huyết) | - PNCT: loại C, cân nhắc lựa chọn thay thế - PN CCB: an toàn khi sử dụng, nên sử dụng NSAID tác dụng ngắn như ibuprofen hơn naproxen | Không sử dụng đồng thời 2 thuốc NSAID Có thể sử dụng aspirin liều thấp Mất nước làm tăng nguy cơ gặp tác dụng phụ của thuốc (đặc biệt đối với trẻ nhỏ và người cao tuổi) Liên hệ với bác sĩ/dược sỹ nếu có biểu hiện sưng mắt cá chân, khó thở, phân đen, chất nôn màu cà phê |
| Aspirin | Trên tiêu hóa (buồn nôn, khó tiêu) Xuất huyết | PNCT: loại C, cân nhắc lựa chọn thay thế nếu liều dùng > 150 mg/ngày | Uống cùng thức ăn có thể làm giảm tác dụng phụ trên đường tiêu hóa Liên hệ với bác sĩ/dược sỹ nếu có biểu hiện sưng mắt cá chân, khó thở, phân đen, chất nôn màu cà phê |
| Kháng histamin H1- giảm dịch tiết hô hấp, khô miệng | |||
| Chlorpheniramin Brompheniramin Diphenhydramin Promethazin Doxylamin | - Buồn ngủ - Chóng mặt - Lú lẫn - Đau đầu - Nhìn mờ - Táo bón - Khô miệng và/hoặc mắt - Bí tiểu - Kích thích (hiếm gặp), đặc biệt ở trẻ em | - Phụ nữ có thai: có thể sử dụng brompheniramin, chlorpheniramin, diphenhydramin, doxylamin (loại A) - Phụ nữ cho con bú: có thể cân nhắc sử dụng brompheniramin, doxylamin | Lưu ý: - Tránh sử dụng đồng thời với chất ức chế MAO - Tránh sử dụng đồng thời với beta-blockers và thuốc chống trầm cảm ba vòng - Bệnh tăng nhãn áp glaucom góc đóng - Bệnh phì đại tuyến tiền liệt - Không dùng với rượu. Hạn chế sử dụng cho người cao tuổi và trẻ em dưới 6 tuổi (tăng nhạy cảm với các tác dụng không mong muốn) |
| Thuốc chống sung huyết mũi (dạng uống) | |||
| Phenylephrin Pseudoephedrin | - Bồn chồn - Mất ngủ - Run rẩy - Đánh trống ngực | - Phụ nữ có thai: Loại B2, cân nhắc lựa chọn thay thế - Phụ nữ CCB: cân nhắc lựa chọn thay thế | - Ít hiệu quả hơn thuốc chống sung huyết m (intranasal decongestions), nhưng không gây nghẹt mũi tái phát - Chống chỉ định bệnh mạch vành, tăng huyết áp nghiêm trọng hoặc không kiểm soát, đang sử dụng hoặc trong vòng 14 ngày sau khi ngừng các thuốc IMAO. - Người cao tuổi là đối tượng có nguy cơ cao gặp phản ứng có hại của thuốc |
| Thuốc chống sung huyết mũi (chống ngạt mũi), dạng tác dụng tại chỗ | |||
| Oxymetazon Xylometazolin | Kích ứng cục bộ Tăng tiết dịch mũi Tái phát ngạt mũi nếu dùng > 3-5 ngày | Thận trọng khi sử dụng | Không sử dụng ở người bệnh tăng huyết áp, bệnh mạch vành, tiền sử đột quỵ. Thận trọng sử dụng cho trẻ em dưới 15 tuổi (nguy cơ tăng tác dụng không mong muốn liên quan đến co mạch) |
| Khác | |||
| Nước muối dạng xịt - giảm ngạt mũi | Kích ứng mũi | An toàn khi sử dụng |
|
4.3. Điều trị cảm lạnh cho trẻ em
- Trẻ em có tần suất cảm lạnh nhiều hơn người lớn bởi khả năng miễn dịch của trẻ chưa hoàn thiện với nhiều loại vi rút.
- Paracetamol có thể sử dụng để giảm đau và giảm sốt có liên quan dến cảm lạnh ở trẻ
- Aspirin không nên sử dụng trẻ < 16 tuổi do tăng nguy cơ xuất hiện hội chứng Reye
- Nước muối/nước muối dạng xịt có thể sử dụng để giảm tình trạng nghẹt mũi
- Sử dụng các biện pháp không dùng thuốc được khuyến cáo ở mục 5.3.
5. Cung cấp thông tin và tư vấn
5.1. Cách sử dụng thuốc
Xem thông tin của từng sản phẩm để tư vấn cách sử dụng thuốc và lưu ý khi sử dụng cho người bệnh.
5.2. Tác dụng không mong muốn
Xem trong bảng 3.3
- Một số sản phẩm điều trị ho và cảm lạnh trong thành phần có chứa sorbitol, có thể là nguyên nhân gây tiêu chảy thẩm thấu nếu dùng thường xuyên.
- Trẻ sơ sinh và trẻ nhỏ có thể gặp nguy cơ hạ đường huyết do thành phần ethanol có trong một số sản phẩm trị ho và cảm lạnh
5.3. Biện pháp không dùng thuốc
Khuyên người bệnh:
- Nghỉ ngơi
- Uống nhiều nước (nước lọc, nước hoa quả). Nước ấm có thể làm dịu cổ họng và giảm tình trạng táo bón.
- Cần tránh dùng đồ uống có thể gây mất nước như cà phê, rượu, đồ uống chứa cồn, chứa ga.
- Tránh sử dụng, hít phải chất có thể gây kích ứng hô hấp (ví dụ khói thuốc lá, hút thuốc lá).
- Giữ phòng ấm nhưng không quá nóng, nếu độ ẩm quá thấp cần sử dụng máy tạo ẩm phun sương hoặc máy hóa hơi có thể làm ẩm không khí
- Bôi thuốc mỡ để làm dịu vùng da bị khô, nứt nẻ quanh mũi
- Hít hơi nước từ vòi hoa sen đang mở nước nóng để giảm nghẹt mũi, khô hoặc chảy nước mũi (trẻ em cần được giám sát trong quá trình hít hơi nước để giảm nguy cơ bỏng)
- Súc miệng bằng nước ấm, nước muối hoặc ngậm viêm ngậm để làm giảm đau họng và ho.
5.4. Phòng ngừa/Dự phòng
Khuyên người bệnh/người chăm sóc người bệnh:
- Rửa tay thường xuyên, đặc biệt sau khi ho, hắt hơi hoặc sử dụng khăn giấy, và rửa tay trước, sau khi ăn. Rửa tay xà phòng hoặc nước sát khuẩn. Hướng dẫn trẻ tầm quan trọng của việc rửa tay
- Làm sạch bếp, phòng tắm, cửa sổ và đồ chơi của trẻ
- Sử dụng khăn giấy khi hắt hơi và ho, vứt khăn giấy ngay sau khi sử dụng đúng quy định
- Khi không có khăn giấy, nếu ho hoặc hắt hơi sử dụng khủy tay để che, không nên sử dụng tay để che
- Tránh dùng chung đồ uống với người khác
- Tránh tiếp xúc gần với người khác khi bị cảm lạnh, nên đeo khẩu trang
- Nghỉ ngơi ở nhà khi cảm thấy không khỏe.
5.5. Theo dõi
- Cảm lạnh thông thường sẽ thường tự cải thiện và hồi phục sau 7-10 ngày.
- Cung cấp cho người bệnh các thông tin về: khoảng thời gian điều trị, trường hợp cần quay trở lại nhà thuốc hoặc trường hợp cần đi khám bác sĩ.
Tài liệu tham khảo
1. Bộ Y tế (2017), Dược thư quốc gia Việt Nam.
2. Pharmaceutical Society of Australian (2009), Australian Pharmaceutical Formulary and handbook, 21 st edition, Section E, Common Cold guide, pp 381 - 383.
3. Pharmaceutical Society of Australian (2020), Australian Pharmaceutical Formulary and handbook, 25th edition, Section E, Common Cough guide, pp 381- 383.
4. NHS (2020), Common cold - NHS (www.nhs.uk)
5. Paul Rutter (2021), Community Pharmacy: Symptoms, Diagnosis and Treatment, Fifth edition, Elsevier, Common Cold, pp 20-28.
C. Táo bón (Constipation)
1. Đại cương
Bệnh nhân được coi là bị táo bón nếu có ít nhất 2 trong 6 triệu chứng sau:
- Đi ngoài dưới 3 lần một tuần.
- Cảm thấy khó đi ngoài trong ít nhất 25% số lần đi đại tiện.
- Đi ra phân cục và cứng trong ít nhất 25% số lần đi đại tiện.
- Có cảm giác tắc nghẽn hậu môn trực tràng trong ít nhất 25% số lần đi đại tiện.
- Có cảm giác đi không hết phân trong ít nhất 25% số lần đi đại tiện.
- Cần dùng tay để hỗ trợ tống phân ra ngoài trong ít nhất 25% số lần đi đại tiện.
Táo bón thường xảy ra phổ biến đối với trẻ em, người cao tuổi và phụ nữ trong giai đoạn cuối thai kỳ.
2. Khai thác thông tin của người bệnh
2.1. Đặc điểm người bệnh
- Tuổi
- Tình trạng mang thai, cho con bú
- Tiền sử dị ứng hoặc quá mẫn với thuốc
2.2. Triệu chứng của người bệnh
Ngoài những triệu chứng đã nêu ở phần đại cương, táo bón còn có những triệu chứng như đầy hơi, chướng bụng, có cảm giác buốt mót, đau khi đại tiện, đau vùng thắt lưng dưới, tiêu chảy, buồn nôn, nôn, giảm cân không rõ lý do, đi ngoài ra máu. Vì vậy, cần khai thác các thông tin về tình trạng đau khi đi đại tiện, thời điểm xuất hiện triệu chứng cũng như các dấu hiệu khác trên đường tiêu hóa.
Nếu không được điều trị, táo bón có thể dẫn đến tình trạng phân chèn ép trực tràng gây tắc ruột, đại tiện và tiểu tiện không tự chủ, nhiễm trùng đường tiết niệu, nứt hậu môn. Táo bón kéo dài có thể trầm trọng đến mức gây ra bệnh trĩ, xuất huyết trực tràng, rối loạn nhịp tim và trào ngược dạ dày-thực quản. Với trẻ em, táo bón có thể làm trẻ biếng ăn và quấy khóc nhiều hơn.
Bảng 3.4. Một số bệnh lý đường tiêu hóa có thể gây táo bón
| Nguyên nhân | Các triệu chứng |
| Bệnh lý trên đường tiêu hóa | |
| Hội chứng ruột kích thích | • Đau, chướng bụng • Mót đại tiện khẩn cấp • Đi ngoài kèm dịch nhầy. • Táo bón hoặc tiêu chảy, hoặc xen kẽ cả hai |
| Trĩ, nứt hậu môn | • Đi ngoài ra máu • Sưng cục trên hậu môn • Đau hậu môn/ trực tràng |
| Ung thư ruột/Khối u gây tắc nghẽn đường tiêu hóa | • Xuất hiện máu và / hoặc chất nhầy trong phân • Biến đổi bất thường trong tình trạng đại tiện (ví dụ như táo bón hoặc tiêu chảy) • Mệt mỏi, suy nhược, xanh xao |
| Viêm túi thừa (túi hình thành do thoát vị của niêm mạc vào thành ruột kết) | • Đau vùng hạ sườn trái • Biến đổi bất thường trong tình trạng đại tiện Buồn nôn và nôn • Đầy hơi • Chướng bụng |
| Tắc ruột già | • Chướng bụng • Buồn nôn và nôn • Đau bụng quặn thắt • Khó đi đại tiện hoặc trung tiện |
2.3. Lối sống
Nhiều yếu tố trong chế độ vận động và sinh hoạt dẫn đến táo bón, ví dụ như:
- Chế độ ăn uống:
+ Không nạp đủ lượng chất lỏng và chất xơ cần thiết.
+ Sử dụng nhiều trà, cà phê và/hoặc uống nhiều rượu
+ Ăn nhiều chất béo
+ Thiếu vitamin B1.
- Nghề nghiệp và thói quen: Ít hoạt động thể chất (ngồi nhiều, ít vận động), thường xuyên nhịn đại tiện.
- Các vấn đề tâm lý (trầm cảm, lo âu) là một trong những nguyên nhân dẫn đến tình trạng thay đổi thói quen đại tiện, làm giảm phản xạ mót rặng, góp phần dẫn đến táo bón.
- Thay đổi thói quen sinh hoạt hoặc môi trường sống góp phần dẫn tới táo bón.
- Đối với phụ nữ mang thai, táo bón thường xuất hiện trong thai kỳ và thường tự hết trong thời gian ngắn sau khi sinh. Thuốc điều trị táo bón có thể gây hại cho thai nhi, vì vậy cần thận trọng khi tư vấn lựa chọn, sử dụng thuốc cho phụ nữ có thai và phụ nữ cho con bú.
- Người cao tuổi cũng thường xuyên bị táo bón do mất cân bằng chế độ ăn uống, đặc biệt là uống ít nước, ít tập thể dục và sử dụng đồng thời nhiều loại thuốc.
2.4. Tiền sử
Tiền sử bệnh lý
Tiền sử bệnh lý không liên quan đường tiêu hóa có thể là nguyên nhân gây táo bón, bao gồm:
- Bệnh lý toàn thân gây mất nước trong cơ thể, làm phân khô và dẫn đến táo bón: tình trạng nhiễm khuẩn, sốt kéo dài, mất máu do phẫu thuật…
- Bệnh không dung nạp gluten.
- Bệnh lý toàn thân: đái tháo đường, suy giáp, đa xơ cứng, Parkinson, hội chứng ruột kích thích, cường cận giáp, suy giáp.
- Tổn thương ống tiêu hóa: khối u đại-trực tràng, viêm đại tràng mạn tính, trĩ và nứt hậu môn.
- Tổn thương ở ngoài ống tiêu hóa: khối u tử cung, u buồng trứng, u tiền liệt tuyến, u phần tiểu khung,…
- Rối loạn điện giải: tăng canxi máu, hạ kali máu.
- Rối loạn thần kinh: tổn thương tủy sống, chấn thương đầu, đột quỵ, bệnh Hirschsprung, bệnh Parkinson
- Các bệnh mô liên kết: xơ cứng bì, lupus.
- Tổn thương cơ sàn chậu sau khi chuyển dạ.
Tiền sử dùng thuốc
Các loại thuốc có thể gây táo bón bao gồm:
- Thuốc chẹn kênh calcium (ví dụ: verapamil)
- Thuốc chứa thành phần kim loại: Calcium, sắt, thuốc kháng acid có chứa nhôm hoặc canxi
- Thuốc giảm đau opioid
- Một số thuốc chống co giật (carbamazepine, phenytoin, pregabalin)
- Thuốc chống trầm cảm (thuốc chống trầm cảm ba vòng, một số chất ức chế monoamine oxidase).
- Thuốc kháng histamin H1.
- Một số loại thuốc kháng cholinergic được sử dụng trong bệnh Parkinson (benztropin, orphenadrin, benzhexol), tiểu tiện không kiểm soát, bệnh ruột kích thích và bệnh viêm túi thừa
- Các thuốc chống loạn thần (clozapin, olanzapin, risperidon, quetiapin)
- Clonidin
- Thuốc lợi tiểu
- Thuốc cường dopaminergic được sử dụng trong điều trị bệnh Parkinson
- Thuốc đối kháng thụ thể 5-HT3:setron
- Một số alkaloid
3. Đánh giá tình trạng người bệnh - trường hợp cần thiết phải đi khám bác sĩ
Người bệnh cần đi khám bác sĩ khi táo bón kèm theo triệu chứng:
- Táo bón kéo dài hơn 14 ngày mà không xác định được nguyên nhân
- Thay đổi bất thường tình trạng đại tiện, ví dụ táo bón xen kẽ với tiêu chảy
- Phân có máu, chất nhầy, hoặc cả hai.
- Đau bụng dữ dội khi đi ngoài
- Đau bụng kèm nôn và táo bón
- Táo bón liên tục kèm đau bụng và sốt
- Giảm cân không rõ nguyên nhân, mệt mỏi
- Có cảm giác muốn đi ngoài liên tục
- Người bệnh có dấu hiệu lạm dụng thuốc nhuận tràng (ví dụ: người bị rối loạn chế độ ăn uống, sử dụng thuốc nhuận tràng để giảm cân)
Trẻ nhỏ dưới 3 tháng tuổi cần thăm khám bác sĩ để loại trừ các nguyên nhân liên quan đến các bệnh lý đường tiêu hóa.
4. Khuyến cáo điều trị
4.1. Mục tiêu điều trị:
- Phục hồi tần suất đi ngoài bình thường,
- Phục hồi tính chất khuôn phân bình thường (phân mềm, đóng thành khuôn, không đau khi đi ngoài, không són phân)
- Nhu động ruột trở lại bình thường, thoải mái
- Sử dụng ít thuốc nhất trong thời gian ngắn nhất
- Tránh phụ thuộc thuốc nhuận tràng: Hạn chế sử dụng thuốc nhuận tràng kéo dài, nên cân nhắc chế độ dùng ngắt quãng.
- Khi phải điều trị kéo dài cần xác định mục tiêu điều trị đầu tiên là thay đổi lối sống tích cực và lâu dài mới có thể thay đổi cấu trúc phân và số lần đại tiện.
- Ngăn ngừa táo bón tái phát.
4.2.Các lựa chọn điều trị
- Tình trạng táo bón có thể được cải thiện từ việc thay đổi chế độ ăn và sinh hoạt: tăng lượng chất xơ ăn vào, tăng lượng dịch hấp thu và tăng cường vận động
+ Chất xơ: Lượng chất xơ khuyến nghị hàng ngày là 20-30 gram đối với người lớn. Đối với cho trẻ em lượng chất xơ cần bổ sung = tuổi + 5 gram/ngày. Thực phẩm giàu chất xơ không hòa tan (ngũ cốc nguyên hạt, yến mạch, gạo lứt, hạt) và chất xơ hòa tan (ví dụ như, rau, đậu, hoa quả) có hiệu quả cao trong việc phòng ngừa và cải thiện tình trạng táo bón. Hàm lượng chất xơ nên tăng dần để tránh các tác dụng phụ như chướng bụng hoặc đầy hơi. Lợi ích của chế độ ăn uống giàu chất xơ thường thể hiện sau từ ba đến năm ngày, nhưng có thể muồn hơn trong vòng một tháng. Thụt tháo phân nên được xử lý trước khi bắt đầu bổ sung chất xơ.
+ Dịch: Người lớn cần hấp thu 2 lít chất lỏng mỗi ngày (trừ trường hợp chống chỉ định, ví dụ như bệnh nhân mắc bệnh tim mạch hoặc bệnh lý thận).
+ Tăng cường tập thể dục, tránh nằm hoặc ngồi nhiều, xoa bụng kết hợp với đi ngoài đúng giờ, đi ngoài ngay lập tức khi có nhu cầu.
Cùng với những thay đổi về chế độ ăn uống, lối sống và luyện tập các biện pháp hỗ trợ đại tiện (thường xuyên và tích cực) là những bước đầu tiên trong quản lý táo bón, đặc biệt là ở trẻ em. Cố gắng đi ngoài ngay sau khi thức dậy vào buổi sáng hay 30 phút sau khi ăn để tận dụng phản xạ dạ dày-kết tràng. Mát-xa bụng (theo chiều kim đồng hồ) trong khi bị táo bón. Một số khuyến cáo đề xuất cho trẻ dùng nước ép mận khô. Tuy nhiên, nước ép mận khô có chứa chất kích thích ruột tự nhiên và không được khuyến khích khi trẻ ít hơn 9 tháng tuổi, kể cả khi pha loãng.
- Thuốc nhuận tràng chỉ được sử dụng khi các biện pháp thay đổi chế độ ăn và luyện tập không thể thực hiện được hoặc khi các biện pháp này thất bại. Có 4 nhóm thuốc nhuận tràng chính: thuốc nhận tràng làm tăng thể tích phân, thuốc nhuận tràng kích thích, thuốc nhuận tràng thẩm thấu và chất làm mềm phân. Lựa chọn thuốc nhuận tràng (thuốc không kê đơn) phải dựa vào đặc điểm và mong muốn của người bệnh (xem Bảng 3.5). Cần lưu ý đến các tác dụng phụ có thể xảy ra và chi phí điều trị đi kèm.
Bảng 3.5: Thuốc nhuận tràng đường uống
| Thuốc nhuận tràng đường uống | Thời gian có hiệu quả | Khuyến cáo lưu ý |
| Tăng thể tích phân/tạo khối (methylcelulose) | 24 giờ (2-3 ngày cho tác dụng đầy đủ) | Cần làm sạch phân ra khỏi trực tràng trước khi bắt đầu bổ sung chất xơ. Đảm bảo cung cấp đủ nước để tránh tắc ruột. |
| Kích thích (bisacodyl, glycerol,…) | 6 - 12 giờ đường uống), 15 - 60 phút (thuốc đạn), 5 - 15 phút (thuốc thụt/xổ) | Không sử dụng lâu dài trừ khi bị táo bón trong tổn thương cột sống, bệnh thần kinh cơ mạn tính và ở những người dùng opioid. Thuốc kích thích nhu động ruột và có thể gây co thắt cơ bụng. |
| Thẩm thấu (muối magnesi, lactulose, sorbitol, macrogol) | 24-72 giờ (đường uống) 5-30 phút (đường trực tràng) | Sử dụng cho bệnh nhân không đi lại được và bệnh nhân táo bón mạn tính. Hiệu quả nhanh hơn khi uống lúc đói |
| Làm mềm phân (parafin lỏng, dầu lạc) | 12 - 72 giờ | Thiếu bằng chứng về hiệu quả khi điều trị đơn độc đối với táo bón ở người lớn. Được đề xuất sử dụng trong điều trị kết hợp và ở trẻ em. |
Phối kết hợp các thuốc nhuận tràng có thể hiệu quả hơn so với sử dụng đơn độc. Thuốc đạn hoặc thuốc xổ có thể hữu ích cho việc tống phân, tuy nhiên hiện chưa có bằng chứng cho thấy chúng có tác dụng lâu dài đối với táo bón. Thuốc đạn và thuốc xổ có thể được sử dụng khi thuốc nhuận tràng đường uống không có hiệu quả.
Việc lựa chọn sản phẩm phụ thuộc vào vị trí và tính chất của phân. Không nên sử dụng thường xuyên thuốc thụt.
5. Cung cấp thông tin và tư vấn
5.1. Cách sử dụng thuốc
Sau khi lựa chọn một loại thuốc, người mua thuốc phải được hướng dẫn cách sử dụng, liều lượng chính xác và lưu ý khi sử dụng:
Thuốc nhuận tràng tạo khối/tăng thể tích phân: Đảm bảo đủ dịch; tăng dần chất xơ làm giảm các tác dụng phụ như chướng bụng hoặc đầy hơi.
Thuốc nhuận tràng kích thích: Ưu tiên sử dụng trong thời gian ngắn; thường được thực hiện vào ban đêm để giúp đi ngoài vào sáng hôm sau; tăng nguy cơ són phân ở người cao tuổi.
Thuốc nhuận tràng thẩm thấu: Được pha với nhiều nước để tăng hiệu quả thẩm thấu; tác dụng nhanh hơn khi uống lúc đói.
Chất làm mềm phân: Mang theo nhiều nước/chất lỏng để sử dụng kết hợp với các chất khác; tránh dùng paraffin lỏng vào trước khi đi ngủ do nguy cơ hít phải.
5.2. Tác dụng không mong muốn
Bệnh nhân cần biết những tác dụng không mong muốn quan trọng và phổ biến nhất của liệu pháp đã chọn:
Thuốc nhuận tràng tạo khối/tăng thể tích phân: Đầy hơi, chướng bụng và khó chịu ở bụng là phổ biến.
Thuốc nhuận tràng kích thích: Tiêu chảy, mất cân bằng dịch và điện giải (khi sử dụng kéo dài hoặc dùng quá liều), khó chịu ở bụng, chuột rút và buồn nôn xảy ra không thường xuyên.
Thuốc nhuận tràng thẩm thấu: Gây mất cân bằng chất lỏng và chất điện giải khi sử dụng kéo dài hoặc quá liều; gây khó chịu ở bụng, chuột rút, buồn nôn, tiêu chảy và kích ứng trực tràng.
Chất làm mềm phân. Đau quặn bụng, tiêu chảy, buồn nôn và kích ứng trực tràng.
5.3. Theo dõi điều trị
Trường hợp táo bón không phải do dùng thuốc hoặc bệnh mạn tính, nên sử dụng thuốc nhuận tràng trong thời gian ngắn cho đến khi thay đổi chế độ ăn uống và lối sống có hiệu quả.
Cha mẹ của trẻ bị táo bón có thể được khuyên duy trì liều thuốc nhuận tràng hiệu quả nhất cho đến khi đại tiện thường xuyên và sau đó giảm liều từ từ trong những tháng tiếp theo.
Thăm khám bác sĩ nếu các biện pháp đang sử dụng không làm giảm táo bón trong thời gian dự kiến hoặc nếu bệnh nhân gặp các triệu chứng cần chuyển tuyến (xem phần Sự cần thiết phải khám bác sĩ).
Tài liệu tham khảo
1. Bộ Y tế (2015), Quyết định số 3312/QĐ-BYT ngày 7/8/2015 của Bộ Y tế ban hành Hướng dẫn chẩn đoán và điều trị một số bệnh thường gặp ở trẻ em, chương 6, trang 325-330.
2. Bộ Y tế (2017), Dược thư quốc gia Việt Nam.
3. Australian Pharmaceutical Formulary and handbook, 21 st edition, Section E, Constipation guide, pp 375-379.
4. National Institute for Health and Care Excellence (2017), NICE Clinical guidance “Constipation in children and young people: diagnosis and management, https://www.nice.org.uk/guidance/cg99/chapter/1-Guidance#antegrade-colonic- enema-procedure.
5. Paul Rutter (2021), Community Pharmacy: Symptoms, Diagnosis and Treatment, Fifth edition, Elsevier, Constipation, pp 189-196.
6. Schmulson MJ, Drossman DA. What Is New in Rome IV. J Neurogastroenterol Motil. 2017;23(2):151-163. doi:10.5056/jnm16214
D. Tiêu chảy (Diarrhoea)
1. Đại cương
Tiêu chảy là tình trạng đi phân lỏng bất thường từ 3 lần trở lên trong 24 giờ. Lưu ý tính chất lỏng của phân vì nếu đi ngoài nhiều lần mà phân bình thường thì không phải là tiêu chảy. Ví dụ: trẻ được bú mẹ hoàn toàn đi ngoài phân sệt là bình thường.
Có thể phân loại tiêu chảy theo thời gian: tiêu chảy cấp tính (thời gian tiêu chảy kéo dài < 14 ngày) và tiêu chảy kéo dài (thời gian tiêu chảy kéo dài trên 14 ngày và dưới 30 ngày) và tiêu chảy mạn tính (thời gian tiêu chảy kéo dài > 30 ngày).
Khi bị tiêu chảy, những đối tượng đặc biệt như trẻ nhỏ hay người già sẽ có nguy cơ mất nước nhanh, đôi khi có thể dẫn đến tử vong, vì thế cần được lưu ý chăm sóc y tế ngay. Xử trí mất nước do tiêu chảy cấp sử dụng dung dịch bù nước điện giải bằng đường uống được chứng minh là an toàn và hiệu quả trong hầu hết các trường hợp tiêu chảy ở mọi lứa tuổi và mọi căn nguyên .
Nguyên nhân gây tiêu chảy cấp thường gặp là do nhiễm khuẩn (virus, vi khuẩn,ký sinh trùng), ngộ độc thức ăn, lạm dụng thuốc nhuận tràng, loạn khuẩn ruột do dùng kháng sinh. Nguyên nhân gây tiêu chảy mạn tính bao gồm: khối u đại tràng, viêm loét đại trực tràng, lao ruột, hội chứng ruột kích thích, nhiễm độc giáp, suy thượng thận, rối loạn hoạt động thần kinh (sợ hãi, mệt mỏi, xúc cảm).
2. Khai thác thông tin về người bệnh
2.1. Đặc điểm người bệnh
Xem xét:
- Tuổi
- Tình trạng mang thai, cho con bú
- Tiền sử dị ứng hoặc quá mẫn với thuốc
2.2. Các triệu chứng
Trong tiêu chảy, khối lượng phân, số lượng phân và / hoặc tần suất đi ngoài tăng lên. Tuy nhiên, tần suất đi ngoài bình thường có thể dao động trong khoảng từ một lần đến hai lần/ngày ở người lớn và vài lần/ngày ở trẻ nhỏ, vì vậy cần xem xét tần suất đi ngoài bất thường hơn là xem xét số lần đi ngoài mỗi ngày.
Đi ngoài không tự chủ (mất kiểm soát cơ vòng hậu môn không tự chủ dẫn đến thải phân) có thể được bệnh nhân mô tả là tiêu chảy. Vì vậy cần xác định tình trạng tiêu chảy để đảm bảo đánh giá và xử trí thích hợp.
Cần đánh giá mức độ mất nước và rối loạn điện giải (số lần đi ngoài, triệu chứng khác như sốt, nôn), tính chất phân của người bệnh. Mất nước nhẹ (<5%) bao gồm mệt mỏi, chán ăn, buồn nôn và đau đầu nhẹ. Mất nước trung bình (5%-10%) đặc trưng bởi khô miệng, mắt trũng, giảm lượng nước tiểu, khát vừa phải và da giảm đàn hồi (nếp véo da mất chậm từ 1-2 giây). Mất nước nặng (>10%) bao gồm các triệu chứng li bì, mắt trũng, không uống được, nếp véo da mất rất chậm > 2 giây [6].
Tiêu chảy cấp kéo dài dưới 14 ngày và thường do các tác nhân nhiễm trùng, thuốc hoặc độc tố thực phẩm.
Tiêu chảy được coi là mạn tính nếu nó kéo dài hơn 30 ngày hoặc nếu có các đợt tiêu chảy lặp đi lặp lại, mỗi đợt kéo dài dưới 14 ngày. Tiêu chảy mạn tính thường là dấu hiệu của một quá trình viêm nhiễm.
2.3. Tiền sử bệnh và tiền sử dùng thuốc
Tiêu chảy là một triệu chứng không đặc hiệu của một loạt các rối loạn tiêu hóa, bao gồm nhiễm trùng đường tiêu hóa do vi rút, vi khuẩn và ký sinh trùng, phản ứng có hại của thuốc, không dung nạp lactose, hội chứng ruột kích thích, tiêu chảy giả (táo bón khi đi ngoài), bệnh viêm ruột, bệnh ác tính của cơ quan tiêu hóa và một loạt các hội chứng kém hấp thu.
Các loại thuốc có thể gây tiêu chảy bao gồm:
- Acarbose
- Thuốc kháng sinh phổ rộng - đặc biệt là amoxycillin/+clavulanate, erythromycin, clindamycin
- Colchicin
- Tác nhân gây độc tế bào
- Digoxin
- Thực phẩm và thuốc - sorbitol, mannitol, fructose, lactose
- Thuốc nhuận tràng
- Thuốc kháng axit chứa magiê
- Metformin
- NSAID
- Orlistat
- Thuốc ức chế protease, đặc biệt là nelfinavir
- Quinidin.
Uống quá nhiều rượu và lạm dụng thuốc nhuận tràng cũng có thể là nguyên nhân gây tiêu chảy. Tư vấn người bệnh đến thăm khám bác sĩ chuyên khoa phù hợp.
2.4. Yếu tố lối sống
Các tác nhân gây bệnh tiêu chảy thường lây truyền qua đường phân-miệng. Tiêu chảy do virus và vi khuẩn thường phát triển trong vòng một đến ba ngày kể từ ngày tiếp xúc với mầm bệnh, thức ăn hoặc bề mặt bị nhiễm mầm bệnh. Tiêu chảy do ký sinh trùng thường có thời gian tiềm tàng từ 1 đến 5 ngày. Vì vậy, cần khai thác thông tin về thực phẩm người bệnh đã sử dụng trong vài ngày qua, xác định xem có ai khác ăn cùng một loại thức ăn và tình trạng sức khỏe của người đó. Tuy nhiên, nguồn lây nhiễm thường không thể được xác định chính xác.
Các nơi chăm sóc trẻ em (trường mẫu giáo) là nguồn phổ biến của các mầm bệnh tiêu chảy. Những thay đổi trong chế độ ăn uống có thể gây ra do thay đổi chức năng ruột ví dụ như khi đi du lịch.
3. Đánh giá tình trạng người bệnh - trường hợp cần thiết phải đi khám bác sĩ
Người bệnh cần đi khám bác sĩ khi bị tiêu chảy kéo dài hoặc khi tiêu chảy đi kèm với các triệu chứng sau:
- Táo bón xen kẽ với tiêu chảy
- Trong phân có máu, chất nhầy, hoặc cả hai
- Sốt cao
- Căng chướng bụng
- Đau bụng nhiều
- Giảm cân không rõ nguyên nhân
- Mất nước từ trung bình đến nặng.
Tư vấn khám bác sĩ trong các trường hợp sau:
- Trẻ dưới 6 tháng tuổi và người cao tuổi (do tăng nguy cơ mất nước, điện giải)
- Bệnh nhân vừa đi du lịch nước ngoài trở về
- Nghi ngờ nhiễm trùng ngoài đường tiêu hóa
- Bệnh nhân mắc các bệnh mạn tính khác cần được quản lý (ví dụ như bệnh đái tháo đường)
- Nghi ngờ lạm dụng thuốc nhuận tràng (ví dụ như ở một người mắc chứng rối loạn ăn uống).
- Trẻ không cải thiện tình trạng sau 2 ngày điều trị
4. Khuyến cáo điều trị
4.1. Mục tiêu của điều trị
- Xác định nguyên nhân cụ thể và biện pháp điều trị phù hợp
- Giảm các triệu chứng và tái lập tính chất phân bình thường
- Dự phòng mất nước
- Phòng tránh các biến chứng.
4.2. Các lựa chọn điều trị
Điều trị rối loạn cơ bản và bổ sung dịch để khắc phục tình trạng mất nước và mất cân bằng điện giải là mục tiêu chính trong việc kiểm soát tiêu chảy. Giải pháp bù nước bằng đường uống là phương pháp tốt nhất để điều trị mất nước trong tất cả các trường hợp, trừ trường hợp nghiêm trọng.
4.3. Điều trị tiêu chảy ở trẻ em
Cho trẻ uống nhiều dịch hơn bình thường để phòng mất nước:
- Dung dịch chứa muối: oresol, dung dịch có vị mặn như nước cháo muối, súp gà, súp rau
- Dung dịch không chứa muối: nước sạch, nước cơm, nước dừa, nước hoa quả tươi không đường).
Những dung dịch không thích hợp khi bị tiêu chảy gồm loại nước ngọt có đường, trà đường, nước trái cây công nghiệp.
Lượng dịch cần uống:
+ Trẻ từ 6 tháng đến < 2 tuổi : 50 - 100ml lượng dịch cần uống sau mỗi lần đi ngoài và giữa mỗi lần.
+ Trẻ 2 - 10 tuổi : 100 - 200ml sau mỗi lần đi ngoài và giữa mỗi lần.
+ Trẻ >10 tuổi: uống theo nhu cầu
Tiếp tục cho trẻ ăn để phòng suy dinh dưỡng: Tiếp tục cho trẻ ăn theo khẩu phần ăn hàng ngày và tăng dần lên. Trẻ bú mẹ tiếp tục bú mẹ thường xuyên. Trẻ nên tiếp tục ăn và uống sữa thường dùng.
Cho trẻ bổ sung kẽm hàng ngày trong 10-14 ngày (viên 20mg kẽm nguyên tố hoặc dạng hỗn dịch, sirup 5ml chứa 10mg kẽm). Cho trẻ uống càng sớm càng tốt ngay sau khi tiêu chảy bắt đầu. Nên cho trẻ uống kẽm lúc đói. Trẻ >6tháng: (20mg/ngày) hoặc 10ml/ngày trong 10 đến 14 ngày
5. Cung cấp thông tin tư vấn
5.1. Cách sử dụng thuốc
- Xác định đúng mức độ mất nước và lựa chọn biện pháp bù nước phù hợp:
Dung dịch bù nước qua đường uống: Hòa tan oresol trong lượng nước theo hướng dẫn trên nhãn thuốc; chỉ sử dụng nước đun sôi để nguội làm chất pha loãng; uống từ từ và thường xuyên khi các triệu chứng vẫn còn. Cần pha dung dịch oresol hàng ngày, bảo quản sạch sẽ. Không dùng dung dịch đã pha quá 24 giờ. Lưu ý rằng phải dùng một lượng nước chính xác để pha gói ORS. Nếu pha không đủ nước, dung dịch sẽ quá đặc gây nguy hiểm. Nếu pha quá loãng, sẽ không đạt hiệu quả điều trị mong muốn.
- Tùy thuộc nguyên nhân gây tiêu chảy mà lựa chọn các loại thuốc không kê đơn phù hợp và hướng dẫn bệnh nhân cách sử dụng chi tiết. Một số lưu ý khi sử dụng các loại thuốc điều trị triệu chứng tiêu chảy:
+ Bismuth: Không sử dụng bismuth khi tiêu chảy có kèm sốt, có máu hoặc dịch nhầy trong phân.
+ Diosmectit: Không nên sử dụng do trẻ dưới 2 tuổi do có thể tiềm ẩn nguy cơ tích lũy kim loại nặng.
+ Loperamid: điều trị triệu chứng tiêu chảy cấp không có biến chứng ở người lớn, không do nhiễm trùng nhiễm độc hoặc khi đã giải quyết nhiễm trùng nhiễm độc mà vẫn còn tiêu chảy; kết hợp với liệu pháp bù nước; tiêu chảy mạn tính ở người lớn. Không dùng cho trẻ < 12 tuổi.
+ Lactobacillus acidophilus: điều trị tiêu chảy không có biến chứng, đặc biệt do dùng kháng sinh.
5.2. Tác dụng không mong muốn
Bệnh nhân cần biết những tác dụng không mong muốn quan trọng và phổ biến nhất của thuốc và phương án điều trị đã lựa chọn:
- Loperamid: Có thể gây đau bụng, chướng bụng, buồn nôn, nôn mửa và táo bón thường gặp.
- Lactobacillus acidophilus: đầy hơi
5.3. Phòng ngừa
Để giảm nguy cơ truyền mầm bệnh tiêu chảy, cần tăng cường vệ sinh cá nhân, rửa tay thường xuyên, đặc biệt là sau khi đi đại tiện, trước khi chế biến thức ăn và trước khi ăn và xử lý phân (ví dụ như thay tã). Đồng thời cần đảm bảo an toàn thực phẩm và vệ sinh môi trường, bảo vệ nguồn nước và sử dụng nước sạch để sinh hoạt.
Người bị tiêu chảy cần được xử trí phù hợp để ngăn ngừa lây truyền thêm.
Khi đi du lịch nước ngoài, chỉ uống nước đun sôi hoặc đồ uống đóng chai thương mại có uy tín. Chọn thực phẩm tươi, nấu chín kỹ và dùng nóng.
5.4. Theo dõi
Tiếp tục theo dõi các dấu hiệu mất nước trong những trường hợp nghiêm trọng, những dấu hiệu này có thể bao gồm khô miệng, khát nước, mắt trũng sâu, mệt mỏi, thở sâu, mạch nhanh và huyết áp thấp và các triệu chứng khác cho thấy cần phải chuyển đi khám bác sĩ.
Có thể cần xem xét khám bác sĩ nếu các triệu chứng kéo dài hơn 48 giờ ở người lớn và 24 giờ ở trẻ em hoặc người cao tuổi, mặc dù đã sử dụng liệu pháp khuyến cáo.
Tài liệu tham khảo
1. Bộ Y tế (2015), Quyết định số 3312/QĐ-BYT ngày 7/8/2015 của Bộ Y tế ban hành Hướng dẫn chẩn đoán và điều trị một số bệnh thường gặp ở trẻ em, chương 6, trang 316-325.
2. Bộ Y tế (2009), Quyết định số 4121/QĐ-BYT ngày 28/20/2009 của Bộ Y tế ban hành Hướng dẫn xử trí tiêu chảy ở trẻ em.
3. Bộ Y tế (2017), Dược thư quốc gia Việt Nam.
4. Pharmaceutical Society of Australia (2009), Australian Pharmaceutical Formulary and handbook 21 st edition, Section E, Diarrhoe guide, pp 383-385.
5. National Institute for Health and Care Excellence (2017), NICE Clinical guidance, https://pathways.nice.org.uk/pathways/diarrhoea-and-vomiting-in- children#content=view-node%3Anodes-advice-for-parents-and-carers
6. Paul Rutter (2021), Community Pharmacy: Symptoms, Diagnosis and Treatment, Fifth edition, Elsevier, Diarrhoea, pp 182-189.
CHƯƠNG 4. HỆ THỐNG HÓA MỘT SỐ VĂN BẢN QUY PHẠM PHÁP LUẬT LIÊN QUAN HOẠT ĐỘNG CỦA CƠ SỞ BÁN LẺ THUỐC TẠI VIỆT NAM
4.1. Quyền lợi, trách nhiệm của cơ sở bán lẻ thuốc (Điều 47 Điều 48 Luật dược)
4.1.1. Quyền lợi, trách nhiệm của cơ sở bán lẻ là nhà thuốc (Điều 47, Luật dược)
a.Cơ sở bán lẻ là nhà thuốc có các quyền sau đây:
- Thực hiện một, một số hoặc tất cả hoạt động kinh doanh dược nếu đáp ứng đủ điều kiện tương ứng với từng loại hình cơ sở kinh doanh theo quy định của Luật dược;
- Hưởng chính sách ưu đãi khi thực hiện hoạt động kinh doanh dược theo quy định của pháp luật;
- Được thông tin, quảng cáo thuốc theo quy định của pháp luật;
- Tổ chức cơ sở bán lẻ thuốc lưu động tại vùng đồng bào dân tộc thiểu số, miền núi, hải đảo, vùng có điều kiện kinh tế - xã hội đặc biệt khó khăn theo quy định của Chính phủ.
- Mua nguyên liệu làm thuốc để pha chế thuốc theo đơn và bán thuốc này tại cơ sở. Người quản lý chuyên môn về dược của nhà thuốc chịu trách nhiệm quản lý trực tiếp việc pha chế thuốc tại cơ sở;
- Mua thuốc để bán lẻ, trừ vắc xin; trường hợp mua, bán thuốc phải kiểm soát đặc biệt và thuốc thuộc Danh mục thuốc hạn chế bán lẻ thực hiện theo quy định tại Điều 34 của Luật dược
- Tham gia cấp phát thuốc của bảo hiểm, chương trình, dự án y tế khi đáp ứng yêu cầu và điều kiện của bảo hiểm, chương trình, dự án đó;
- Người có Bằng dược sỹ được thay thế thuốc đã kê trong đơn thuốc bằng một thuốc khác có cùng hoạt chất, đường dùng, liều lượng khi có sự đồng ý của người mua và phải chịu trách nhiệm về việc thay đổi thuốc.
b. Cơ sở bán lẻ là nhà thuốc có các trách nhiệm sau đây:
- Phải có Giấy chứng nhận đủ điều kiện kinh doanh dược và chỉ được kinh doanh đúng loại hình cơ sở kinh doanh, phạm vi và địa điểm kinh doanh ghi trong Giấy chứng nhận đủ điều kiện kinh doanh dược;
- Bảo đảm duy trì các điều kiện kinh doanh dược trong quá trình hoạt động kinh doanh theo quy định của Luật dược;
- Thu hồi thuốc, nguyên liệu làm thuốc theo quy định tại Điều 62 của Luật dược;
- Bồi thường thiệt hại cho tổ chức, cá nhân bị thiệt hại do lỗi của cơ sở theo quy định của pháp luật
- Chấp hành quyết định của cơ quan nhà nước có thẩm quyền trong trường hợp bảo đảm cung ứng thuốc, nguyên liệu làm thuốc khi xảy ra dịch bệnh nguy hiểm, thiên tai, thảm họa;
- Báo cáo Bộ Y tế hoặc Sở Y tế và thực hiện các nghĩa vụ theo quy định của pháp luật trong trường hợp tạm dừng hoạt động từ 06 tháng trở lên hoặc chấm dứt hoạt động;
- Thông báo, cập nhật danh sách người có Chứng chỉ hành nghề dược đang hành nghề tại cơ sở đến cơ quan có thẩm quyền theo quy định của Bộ trưởng Bộ Y tế;
- Niêm yết công khai Chứng chỉ hành nghề dược và Giấy chứng nhận đủ điều kiện kinh doanh dược tại cơ sở kinh doanh;
- Báo cáo hằng năm và báo cáo theo yêu cầu của cơ quan quản lý về dược có thẩm quyền;
- Tuân thủ quy định của Bộ Y tế trong việc mua, bán thuốc thuộc Danh mục thuốc hạn chế bán lẻ;
- Niêm yết giá bán lẻ bằng đồng Việt Nam tại nơi giao dịch hoặc nơi bán thuốc của cơ sở kinh doanh dược để thuận tiện cho việc quan sát, nhận biết của khách hàng, cơ quan quản lý có thẩm quyền và tuân thủ các quy định khác về quản lý giá thuốc;
- Lưu giữ chứng từ, tài liệu có liên quan đến từng lô thuốc, nguyên liệu làm thuốc trong thời gian ít nhất là 01 năm kể từ ngày thuốc, nguyên liệu làm thuốc hết hạn dùng;
- Bảo quản thuốc, nguyên liệu làm thuốc theo đúng điều kiện ghi trên nhãn;
- Ghi rõ tên thuốc, hàm lượng, hạn dùng cho người sử dụng trong trường hợp bán lẻ thuốc không đựng trong bao bì ngoài của thuốc; trường hợp không có đơn thuốc đi kèm, phải ghi thêm liều dùng, số lần dùng và cách dùng;
- Chỉ được bán thuốc kê đơn tại cơ sở bán lẻ thuốc khi có đơn thuốc.
- Người chịu trách nhiệm chuyên môn của nhà thuốc phải triển khai hoạt động dược lâm sàng theo nội dung quy định tại các Khoản 2, 3 và 6 Điều 80 của Luật dược, cụ thể như sau:
+ Tư vấn, cung cấp thông tin về thuốc cho người mua, người sử dụng thuốc;
+ Tư vấn, trao đổi với người kê đơn trong trường hợp phát hiện việc kê đơn thuốc không hợp lý;
+ Tham gia theo dõi, giám sát phản ứng có hại của thuốc.
- Bảo đảm điều kiện pha chế thuốc theo quy định của Bộ trưởng Bộ Y tế;
- Không được bán nguyên liệu làm thuốc, trừ dược liệu.
Theo Điều 77 của Luật dược quy định cơ sở bán lẻ thuốc có các trách nhiệm:
+ Tư vấn trong phạm vi chuyên môn cho người sử dụng thuốc về các biện pháp xử lý khi có dấu hiệu bất thường trong quá trình sử dụng thuốc;
+ Thu thập, báo cáo cho cơ quan có thẩm quyền các thông tin về dấu hiệu bất thường trong quá trình sử dụng thuốc.
4.1.2. Quyền lợi, trách nhiệm của cơ sở bán lẻ là quầy thuốc (Điều 48, Luật dược)
a. Cơ sở bán lẻ là quầy thuốc có các quyền sau đây
- Thực hiện một, một số hoặc tất cả hoạt động kinh doanh dược nếu đáp ứng đủ điều kiện tương ứng với từng loại hình cơ sở kinh doanh theo quy định của Luật dược;
- Hưởng chính sách ưu đãi khi thực hiện hoạt động kinh doanh dược theo quy định của pháp luật;
- Được thông tin, quảng cáo thuốc theo quy định của pháp luật;
- Tổ chức cơ sở bán lẻ thuốc lưu động tại vùng đồng bào dân tộc thiểu số, miền núi, hải đảo, vùng có điều kiện kinh tế - xã hội đặc biệt khó khăn theo quy định của Chính phủ.
- Mua và bán lẻ thuốc thuộc Danh mục thuốc thiết yếu và Danh mục thuốc không kê đơn, trừ vắc xin; trường hợp mua, bán thuốc thuộc Danh mục thuốc phải kiểm soát đặc biệt và Danh mục thuốc hạn chế bán lẻ thực hiện theo quy định tại Điều 34 của Luật dược. Đối với quầy thuốc ở vùng đồng bào dân tộc thiểu số, miền núi, hải đảo, vùng có điều kiện kinh tế - xã hội đặc biệt khó khăn thì được bán thêm một số loại thuốc khác theo quy định của Bộ trưởng Bộ Y tế: bán thêm một số thuốc kê đơn không thuộc Danh mục thuốc thiết yếu khi được Sở Y tế có văn bản cho phép (Điều 20, Thông tư số 07/2018/TT-BYT)
- Tham gia cấp phát thuốc của bảo hiểm, chương trình, dự án y tế khi đáp ứng yêu cầu và điều kiện của bảo hiểm, chương trình, dự án đó.
b. Cơ sở bán lẻ là quầy thuốc có các trách nhiệm sau đây
- Phải có Giấy chứng nhận đủ điều kiện kinh doanh dược và chỉ được kinh doanh đúng loại hình cơ sở kinh doanh, phạm vi và địa điểm kinh doanh ghi trong Giấy chứng nhận đủ điều kiện kinh doanh dược;
- Bảo đảm duy trì các điều kiện kinh doanh dược trong quá trình hoạt động kinh doanh theo quy định của Luật dược;
- Thu hồi thuốc, nguyên liệu làm thuốc theo quy định tại Điều 62 của Luật dược;
- Bồi thường thiệt hại cho tổ chức, cá nhân bị thiệt hại do lỗi của cơ sở theo quy định của pháp luật;
- Chấp hành quyết định của cơ quan nhà nước có thẩm quyền trong trường hợp bảo đảm cung ứng thuốc, nguyên liệu làm thuốc khi xảy ra dịch bệnh nguy hiểm, thiên tai, thảm họa;
- Báo cáo Bộ Y tế hoặc Sở Y tế và thực hiện các nghĩa vụ theo quy định của pháp luật trong trường hợp tạm dừng hoạt động từ 06 tháng trở lên hoặc chấm dứt hoạt động;
- Thông báo, cập nhật danh sách người có Chứng chỉ hành nghề dược đang hành nghề tại cơ sở đến cơ quan có thẩm quyền theo quy định của Bộ trưởng Bộ Y tế;
- Niêm yết công khai Chứng chỉ hành nghề dược và Giấy chứng nhận đủ điều kiện kinh doanh dược tại cơ sở kinh doanh;
- Báo cáo hằng năm và báo cáo theo yêu cầu của cơ quan quản lý về dược có thẩm quyền;
- Tuân thủ quy định của Bộ Y tế trong việc mua, bán thuốc thuộc Danh mục thuốc hạn chế bán lẻ;
- Niêm yết giá bán lẻ bằng đồng Việt Nam tại nơi giao dịch hoặc nơi bán thuốc của cơ sở kinh doanh dược để thuận tiện cho việc quan sát, nhận biết của khách hàng, cơ quan quản lý có thẩm quyền và tuân thủ các quy định khác về quản lý giá thuốc;
- Lưu giữ chứng từ, tài liệu có liên quan đến từng lô thuốc, nguyên liệu làm thuốc trong thời gian ít nhất là 01 năm kể từ ngày thuốc, nguyên liệu làm thuốc hết hạn dùng;
- Bảo quản thuốc, nguyên liệu làm thuốc theo đúng điều kiện ghi trên nhãn;
- Ghi rõ tên thuốc, hàm lượng, hạn dùng cho người sử dụng trong trường hợp bán lẻ thuốc không đựng trong bao bì ngoài của thuốc; trường hợp không có đơn thuốc đi kèm, phải ghi thêm liều dùng, số lần dùng và cách dùng;
- Chỉ được bán thuốc kê đơn tại cơ sở bán lẻ thuốc khi có đơn thuốc.
- Không được bán nguyên liệu làm thuốc, trừ dược liệu.
Theo Điều 77 của Luật dược quy định cơ sở bán lẻ thuốc có các trách nhiệm:
+ Tư vấn trong phạm vi chuyên môn cho người sử dụng thuốc về các biện pháp xử lý khi có dấu hiệu bất thường trong quá trình sử dụng thuốc;
+ Thu thập, báo cáo cho cơ quan có thẩm quyền các thông tin về dấu hiệu bất thường trong quá trình sử dụng thuốc
4.2. Quyền lợi nghĩa vụ của người hành nghề dược (Điều 30, 31 Luật dược)
a. Quyền lợi của người hành nghề dược
- Được đào tạo, cập nhật kiến thức, trao đổi thông tin chuyên môn, pháp luật về dược.
- Được cấp Chứng chỉ hành nghề dược khi đáp ứng đủ điều kiện quy định.
- Người chịu trách nhiệm chuyên môn của cơ sở kinh doanh dược được ủy quyền cho người có Chứng chỉ hành nghề dược phù hợp khi vắng mặt để chịu trách nhiệm chuyên môn theo quy định.
- Người chịu trách nhiệm chuyên môn về dược của nhà thuốc được thay thế thuốc đã kê trong đơn thuốc bằng một thuốc khác có cùng hoạt chất, cách dùng, liều lượng khi có sự đồng ý của người mua và phải chịu trách nhiệm về việc thay đổi thuốc.
- Từ chối thực hiện hoạt động chuyên môn trái với quy định của pháp luật hoặc đạo đức nghề nghiệp.
b. Nghĩa vụ của người hành nghề dược
- Tuân thủ đạo đức nghề nghiệp trong hành nghề dược.
- Người chịu trách nhiệm chuyên môn của cơ sở bán lẻ thuốc phải có mặt trong toàn bộ thời gian hoạt động của cơ sở dược, trừ trường hợp ủy quyền khi vắng mặt theo quy định.
- Chỉ chịu trách nhiệm chuyên môn đối với một cơ sở kinh doanh dược và tại một địa điểm kinh doanh dược.
- Hành nghề dược theo đúng phạm vi hoạt động chuyên môn ghi trong Chứng chỉ hành nghề dược và quy định chuyên môn kỹ thuật.
- Chấp hành quyết định của cơ quan nhà nước có thẩm quyền trong trường hợp có dịch bệnh nguy hiểm, thiên tai, thảm họa.
- Hoàn thành chương trình đào tạo, cập nhật kiến thức chuyên môn về dược trong thời hạn 03 năm kể từ ngày được cấp Chứng chỉ hành nghề dược hoặc kể từ ngày có giấy xác nhận hoàn thành chương trình đào tạo, cập nhật kiến thức chuyên môn về dược gần nhất. Thời gian đào tạo, cập nhật kiến thức chuyên môn về dược tối thiểu 8 giờ.
- Thông báo với cơ quan, người có thẩm quyền về hành vi vi phạm pháp luật, đạo đức hành nghề dược của người hành nghề dược khác và phải chịu trách nhiệm về những thông tin đã thông báo.
4.3. Hành vi nghiêm cấm (Điều 6- luật dược)
- Kinh doanh dược mà không có Giấy chứng nhận đủ điều kiện kinh doanh dược hoặc trong thời gian bị đình chỉ hoạt động hoặc trong thời gian bị tước quyền sử dụng Giấy chứng nhận đủ điều kiện kinh doanh dược.
- Kinh doanh dược tại nơi không phải là địa điểm kinh doanh dược đã đăng ký.
- Kinh doanh thuốc, nguyên liệu làm thuốc quy định tại khoản 26 Điều 2 của Luật dược và thuốc, nguyên liệu làm thuốc khác không đúng mục đích hoặc cung cấp không đúng đối tượng mà cơ quan quản lý nhà nước có thẩm quyền cho phép.
- Kinh doanh dược không thuộc phạm vi chuyên môn được ghi trong Giấy chứng nhận đủ điều kiện kinh doanh dược.
- Kinh doanh dược thuộc một trong các trường hợp sau đây:
+ Thuốc giả, nguyên liệu làm thuốc giả;
+ Thuốc, nguyên liệu làm thuốc không đạt tiêu chuẩn chất lượng; thuốc, nguyên liệu làm thuốc đã có thông báo thu hồi của cơ quan nhà nước có thẩm quyền; thuốc, nguyên liệu làm thuốc không rõ nguồn gốc, xuất xứ; thuốc, nguyên liệu làm thuốc đã hết hạn dùng;
+ Thuốc, nguyên liệu làm thuốc thuộc danh mục thuốc, nguyên liệu làm thuốc cấm nhập khẩu, cấm sản xuất;
+ Thuốc thử lâm sàng;
+ Thuốc, nguyên liệu làm thuốc làm mẫu để đăng ký, kiểm nghiệm, nghiên cứu khoa học, tham gia trưng bày tại triển lãm, hội chợ;
+ Thuốc, nguyên liệu làm thuốc chưa được phép lưu hành;
+ Thuốc thuộc chương trình mục tiêu quốc gia, thuốc viện trợ và thuốc khác có quy định không được bán;
+ Bán lẻ thuốc kê đơn mà không có đơn thuốc; bán lẻ vắc xin;
+ Bán thuốc cao hơn giá kê khai, giá niêm yết.
- Làm giả, sửa chữa hồ sơ, giấy tờ, tài liệu, giấy chứng nhận của cơ quan, tổ chức có thẩm quyền và tổ chức, cá nhân trong các hoạt động về dược.
- Thay đổi, sửa chữa hạn dùng của thuốc, trừ trường hợp thay đổi hạn dùng của thuốc quy định tại khoản 3 Điều 61 của Luật dược.
- Hành nghề mà không có Chứng chỉ hành nghề dược hoặc trong thời gian bị tước quyền sử dụng Chứng chỉ hành nghề dược tại vị trí công việc quy định tại Điều 11 của Luật dược.
- Thuê, mượn, cho thuê, cho mượn hoặc cho người khác sử dụng Chứng chỉ hành nghề dược, Giấy chứng nhận đủ điều kiện kinh doanh dược để hành nghề hoặc kinh doanh dược.
- Khuyến mại thuốc trái quy định của pháp luật.
- Lợi dụng việc kê đơn thuốc để trục lợi.
- Sản xuất, pha chế, bán thuốc cổ truyền có kết hợp với dược chất khi chưa được phép của cơ quan quản lý nhà nước có thẩm quyền.
- Cấp phát, bán thuốc đã hết hạn dùng, thuốc bảo quản không đúng quy định ghi trên nhãn thuốc, thuốc đã có thông báo thu hồi của cơ quan nhà nước có thẩm quyền, thuốc không rõ nguồn gốc, xuất xứ cho người sử dụng.
- Thông tin, quảng cáo, tiếp thị, kê đơn, tư vấn, ghi nhãn, hướng dẫn sử dụng có nội dung dùng để phòng bệnh, chữa bệnh, chẩn đoán bệnh, điều trị bệnh, giảm nhẹ bệnh, điều chỉnh chức năng sinh lý cơ thể người đối với sản phẩm không phải là thuốc, trừ trang thiết bị y tế.
4.4. Một số văn bản quy phạm pháp luật liên quan hoạt động cơ sở bán lẻ thuốc
Tổng hợp một số văn bản quy phạm pháp luật liên quan hoạt động của cơ sở bán lẻ thuốc trình bày tại Bảng 4.1.
Bảng 4.1.Danh mục văn bản quy phạm pháp luật liên quan hoạt động của cơ sở bán lẻ thuốc
| TT | Tên văn bản | Nội dung | Thời điểm có hiệu lực |
| 1. | Luật số 105/2016/QH13 ngày 6/4/2016 | Luật dược | 01/01/2017 |
| 2. | Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 | Quy định chi tiết một số điều và biện pháp thi hành luật dược | 01/07/2017 |
| 3. | Nghị định số 155/2018/NĐ-CP ngày 12/11/2018 | Sửa đổi, bổ sung một số quy định liên quan đến điều kiện đầu tư kinh doanh thuộc phạm vi quản lý nhà nước của Bộ Y tế, | 12/11/2018 |
| 4. | Nghị định số 117/2020/NĐ-CP ngày 28/09/2020 | Quy định xử phạt vi phạm hành chính trong lĩnh vực y tế | 15/11/2020 |
| 5. | Thông tư số 07/2017/TT-BYT ngày 03/05/2017 | Ban hành danh mục thuốc không kê đơn | 01/07/2017 |
| 6. | Thông tư số 06/2017/TT-BYT ngày 03/05/2017 | Ban hành danh mục thuốc độc và nguyên liệu độc làm thuốc | 01/07/2017 |
| 7. | Thông tư số 20/2017/TT-BYT ngày 10/05/2017 | Quy định chi tiết một số điều của luật dược và nghị định số 54/2017/NĐ-CP ngày 08 tháng 5 năm 2017 của chính phủ về thuốc và nguyên liệu làm thuốc phải kiểm soát đặc biệt | 01/07/2017 |
| 8. | Thông tư số 52/2017/TT-BYT ngày 29/12/2017 | Quy định về đơn thuốc và việc kê đơn thuốc hóa dược, sinh phẩm trong điều trị ngoại trú | 01/03/2018 |
| 9. | Thông tư số 01/2018/TT-BYT ngày 18/1/2018 | Quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc | 01/06/2018 |
| 10. | Thông tư số 02/2018/TT-BYT ngày 22/01/2018 | Quy định về thực hành tốt cơ sở bán lẻ thuốc | 08/03/2018 |
| 11. | Thông tư số 07/2018/TT-BYT ngày 12/04/2018 | Quy định chi tiết một số điều về kinh doanh dược của luật dược và nghị định số 54/2017/NĐ-CP ngày 08/5/2017 của chính phủ quy định chi tiết một số điều và biện pháp thi hành luật dược | 01/06/2018 |
| 12. | Thông tư số 11/2018/TT-BYT ngày 04/05/2018 | Quy định về chất lượng thuốc, nguyên liệu làm thuốc | 20/06/2018 |
| 13. | Thông tư số 13/2018/TT-BYT ngày 15/05/2018 | Quy định về chất lượng dược liệu, thuốc cổ truyền; | 30/06/2018 |
| 14. | Thông tư số 18/2018/TT-BYT ngày 22/08/2018 | Sửa đổi, bổ sung một số điều của Thông tư số 52/2017/TT-BYT ngày 29 tháng 12 năm 2017 quy định về đơn thuốc và việc kê đơn thuốc hóa dược, sinh phẩm trong điều trị ngoại trú | 15/10/2018 |
| 15. | Thông tư số 44/2018/TT-BYT ngày 22/08/2018 | Quy định về kê đơn thuốc cổ truyền, thuốc dược liệu và kê đơn kết hợp thuốc cổ truyền, thuốc dược liệu với thuốc hóa dược | 01/03/2019 |
| 16. | Thông tư số 19/2018/TT-BYT ngày 30/08/2018 | Ban hành Danh mục thuốc thiết yếu | 15/10/2018 |
| 17. | Thông tư số 03/2020/TT-BYT ngày 22/01/2020 | Sửa đổi, bổ sung một số điều của thông tư số 11/2018/TT-BYT ngày 04 tháng 5 năm 2018 của bộ trưởng bộ y tế quy định về chất lượng thuốc, nguyên liệu làm thuốc | 16/03/2020 |
| 18 | Thông tư số 12/2020/TT-BYT ngày 22/06/2020 | Sửa đổi, bổ sung một số điều của thông tư số 02/2018/TT-BYT ngày 22 tháng 01 năm 2018 của bộ trưởng bộ y tế quy định về thực hành tốt cơ sở bán lẻ thuốc | 06/08/2020 |
| 19 | Thông tư số 29/2020/TT-BYT ngày 31/12/2020 | Sửa đổi, bổ sung và bãi bỏ một số văn bản quy phạm pháp luật do bộ trưởng bộ y tế ban hành liên tịch ban hành | 15/02/2021. Riêng các quy định tại các khoản 5, 6, 7, 8 và 11 Điều 1 Thông tư này có hiệu lực từ ngày 01 tháng 01 năm 2021. |
| 20. | Thông tư số 08/2021/TT-BYT ngày 25/6/2021 | Ban hành Nguyên tắc đạo đức hành nghề dược | 13/08/2021 |
4.5. Một số yêu cầu trong hoạt động của cơ sở bán lẻ thuốc
Hoạt động của cơ sở bán lẻ thuốc phải thực hiện theo quy định dược hiện hành, các tiêu chuẩn được ban hành theo hệ thống văn bản quy phạm pháp luật có liên quan. Trong đó, cơ sở bán lẻ thuốc phải bảo đảm luôn đáp ứng tiêu chuẩn GPP trong suốt quá trình hoạt động, thực hiện các hoạt động bán lẻ thuốc theo đúng phạm vi được cấp phép.
Theo tiêu chuẩn GPP hiện nay, cơ sở bán lẻ thuốc phải đạt các tiêu chuẩn theo 03 nội dung cốt lõi là (i) nhân sự; (ii) cơ sở vật chất, kỹ thuật và (iii) các hoạt động chủ yếu (mua thuốc, bán thuốc, bảo quản thuốc).Dựa trên các quy định ban hành thực hành tốt cơ sở bán lẻ thuốc, để được hoạt động, cơ sở bán lẻ thuốc phải đạt yêu cầu theo các tiêu chí thuộc Danh mục kiểm tra (checklist) với 9 khía cạnh như sau:
Hình 4.1. Nội dung danh mục kiểm tra thực hành tốt cơ sở bán lẻ thuốc Việt Nam
4.5.1. Nhân sự (Điều 18, Luật dược; Thông tư 02/2018/TT-BYT)
4.5.1.1. Quy định nhân sự trong hoạt động bán lẻ thuốc
Người phụ trách chuyên môn của nhà thuốc có bằng tốt nghiệp đại học ngành dược, phải có Chứng chỉ hành nghề dược theo quy định hiện hành. Người chịu trách nhiệm chuyên môn về dược của nhà thuốc có thể đồng thời là người làm công tác dược lâm sàng tại nhà thuốc.
Người phụ trách chuyên môn của quầy thuốc tối thiểu có bằng tốt nghiệp trung cấp ngành dược, phải có Chứng chỉ hành nghề dược theo quy định hiện hành.
Nhà thuốc/quầy thuốc có nguồn nhân lực thích hợp (số lượng, bằng cấp, kinh nghiệm nghề nghiệp) để đáp ứng quy mô hoạt động.
Cơ sở bán lẻ thuốc là nhà thuốc, nhân viên trực tiếp tham gia bán thuốc, giao nhận, bảo quản thuốc, quản lý chất lượng thuốc, pha chế thuốc phải có bằng cấp chuyên môn từ trung cấp dược trở lên và có thời gian thực hành nghề nghiệp phù hợp với công việc được giao. Người trực tiếp pha chế thuốc, người làm công tác dược lâm sàng phải có bằng tốt nghiệp đại học ngành dược.
Cơ sở bán lẻ thuốc là quầy thuốc, nhân viên trực tiếp tham gia bán thuốc, giao nhận, bảo quản thuốc, quản lý chất lượng thuốc phải có bằng cấp chuyên môn từ sơ cấp dược trở lên và có thời gian thực hành nghề nghiệp phù hợp với công việc được giao. Nhân viên cung cấp thông tin cho người mua thuốc độc, thuốc kê đơn phải là người phụ trách chuyên môn hoặc người có văn bằng chuyên môn dược từ trung cấp ngành dược trở lên.
Tất cả các nhân viên không đang trong thời gian bị kỷ luật từ hình thức cảnh cáo trở lên có liên quan đến chuyên môn y, dược.
Nhân viên phải được đào tạo ban đầu và cập nhật về tiêu chuẩn Thực hành tốt bán lẻ thuốc.
Quy định về nhân sự của cơ sở bán lẻ thuốc phải kiểm soát đặc biệt (Điều 44, Nghị định 54/2007/NĐ-CP và Điều 5, Nghị định 155/2018/NĐ-CP)
Đối với cơ sở bán lẻ thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất: Người chịu trách nhiệm bán lẻ thuốc gây nghiện phải là người có bằng tốt nghiệp đại học ngành dược trở lên; Người chịu trách nhiệm bán lẻ thuốc hướng thần, thuốc tiền chất phải là người có bằng tốt nghiệp trung cấp ngành dược trở lên.
Đối với cơ sở bán lẻ thuốc phóng xạ: Người chịu trách nhiệm bán lẻ phải là người có bằng tốt nghiệp trung cấp ngành dược trở lên.
4.5.1.2. Yêu cầu đối với người bán lẻ trong thực hành nghề nghiệp
+ Đối với người làm việc trong cơ sở bán lẻ thuốc:
- Có thái độ hòa nhã, lịch sự khi tiếp xúc với người mua thuốc, bệnh nhân.
- Hướng dẫn, giải thích, cung cấp thông tin và lời khuyên đúng đắn về cách dùng thuốc cho người mua hoặc bệnh nhân và có các tư vấn cần thiết nhằm đảm bảo sử dụng thuốc hợp lý, an toàn và hiệu quả.
- Giữ bí mật các thông tin của người bệnh trong quá trình hành nghề như bệnh tật, các thông tin người bệnh yêu cầu.
- Trang phục áo blu trắng, sạch sẽ, gọn gàng, có đeo biển ghi rõ tên, chức danh.
- Thực hiện đúng các quy chế dược, tự nguyện tuân thủ đạo đức hành nghề dược.
- Tham gia các lớp đào tạo, cập nhật kiến thức chuyên môn và pháp luật y tế.
+ Đối với người quản lý chuyên môn:
- Giám sát hoặc trực tiếp tham gia việc bán các thuốc kê đơn, tư vấn cho người mua.
- Chịu trách nhiệm quản lý trực tiếp việc pha chế thuốc theo đơn tại nhà thuốc.
- Liên hệ với bác sĩ kê đơn trong các trường hợp cần thiết để giải quyết các tình huống xảy ra.
- Kiểm soát chất lượng thuốc mua về, thuốc bảo quản tại nhà thuốc.
- Thường xuyên cập nhật các kiến thức chuyên môn, văn bản quy phạm pháp luật về hành nghề dược và không ngừng nâng cao chất lượng dịch vụ cung ứng thuốc.
- Đào tạo, hướng dẫn các nhân viên tại cơ sở bán lẻ về chuyên môn cũng như đạo đức hành nghề dược.
- Cộng tác với y tế cơ sở và nhân viên y tế cơ sở trên địa bàn dân cư, tham gia cấp phát thuốc bảo hiểm, chương trình, dự án y tế khi đáp ứng yêu cầu, phối hợp cung cấp thuốc thiết yếu, tham gia truyền thông giáo dục cho cộng đồng về các nội dung như: tăng cường chăm sóc sức khỏe bằng biện pháp không dùng thuốc, cách phòng tránh, xử lý các bệnh dịch, chăm sóc sức khỏe ban đầu, các nội dung liên quan đến thuốc và sử dụng thuốc và các hoạt động khác.
- Theo dõi và thông báo cho cơ quan y tế về các tác dụng không mong muốn của thuốc.
- Phải có mặt trong toàn bộ thời gian hoạt động của cơ sở. Trường hợp người quản lý chuyên môn vắng mặt phải ủy quyền bằng văn bản cho người có Chứng chỉ hành nghề dược phù hợp để chịu trách nhiệm chuyên môn theo quy định.
![]() Nếu thời gian vắng mặt trên 30 ngày thì người quản lý chuyên môn sau khi ủy quyền phải có văn bản báo cáo Sở Y tế tỉnh, thành phố trực thuộc Trung ương tại nơi cơ sở đang hoạt động.
Nếu thời gian vắng mặt trên 30 ngày thì người quản lý chuyên môn sau khi ủy quyền phải có văn bản báo cáo Sở Y tế tỉnh, thành phố trực thuộc Trung ương tại nơi cơ sở đang hoạt động.
![]() Nếu thời gian vắng mặt trên 180 ngày thì cơ sở kinh doanh thuốc phải làm thủ tục đề nghị cấp mới Giấy chứng nhận điều kiện kinh doanh dược cho cơ sở bán lẻ thuốc. Cơ sở chỉ được phép hoạt động khi đã được cấp giấy chứng nhận đủ điều kiện kinh doanh mới.
Nếu thời gian vắng mặt trên 180 ngày thì cơ sở kinh doanh thuốc phải làm thủ tục đề nghị cấp mới Giấy chứng nhận điều kiện kinh doanh dược cho cơ sở bán lẻ thuốc. Cơ sở chỉ được phép hoạt động khi đã được cấp giấy chứng nhận đủ điều kiện kinh doanh mới.
+ Các hoạt động khác:
- Phải có hệ thống lưu giữ các thông tin, thông báo về thuốc khiếu nại, thuốc không được phép lưu hành, thuốc phải thu hồi.
- Có thông báo thu hồi cho khách hàng đối với các thuốc thuộc danh mục thuốc kê đơn. Biệt trữ các thuốc thu hồi để chờ xử lý.
- Có hồ sơ ghi rõ về việc khiếu nại và biện pháp giải quyết cho người mua về khiếu nại hoặc thu hồi thuốc.
- Đối với thuốc cần hủy phải chuyển cho cơ sở có chức năng xử lý chất thải để hủy theo quy định.
- Có báo cáo các cấp theo quy định.
4.5.2. Cơ sở vật chất kỹ thuật của cơ sở bán lẻ (Thông tư 02/2018/TT-BYT)
4.5.2.1.Xây dựng và thiết kế
a) Địa điểm cố định, bố trí ở nơi cao ráo, thoáng mát, an toàn, cách xa nguồn ô nhiễm.
b) Khu vực hoạt động của nhà thuốc/quầy thuốc phải tách biệt với các hoạt động khác.
c) Xây dựng chắc chắn, có trần chống bụi, tường và nền nhà dễ làm vệ sinh, đủ ánh sáng cho các hoạt động và tránh nhầm lẫn, không để thuốc bị tác động trực tiếp của ánh sáng mặt trời.
4.5.2.2. Diện tích
a) Diện tích phù hợp với quy mô kinh doanh nhưng tối thiểu là 10m2, phải có khu vực để trưng bày, bảo quản thuốc và khu vực để người mua thuốc tiếp xúc và trao đổi thông tin về việc sử dụng thuốc với người bán lẻ.
b) Phải bố trí thêm khu vực cho những hoạt động khác như:
- Phòng pha chế theo đơn nếu nhà thuốc có tổ chức pha chế theo đơn.
- Khu vực ra lẻ các thuốc không còn bao bì tiếp xúc trực tiếp với thuốc để bán lẻ trực tiếp cho người bệnh.
- Kho bảo quản thuốc riêng (nếu cần).
- Phòng hoặc khu vực tư vấn riêng cho người mua thuốc/bệnh nhân.
c) Trường hợp kinh doanh thêm mỹ phẩm, thực phẩm chức năng, dụng cụ y tế thì phải có khu vực riêng, không bày bán cùng với thuốc và không gây ảnh hưởng đến thuốc; phải có biển hiệu khu vực ghi rõ “Sản phẩm này không phải là thuốc”.
d) Trường hợp nhà thuốc có bố trí phòng pha chế theo đơn hoặc nhà thuốc/quầy thuốc có bố trí phòng ra lẻ thuốc không còn bao bì tiếp xúc trực tiếp với thuốc:
- Phòng phải có trần chống bụi, nền và tường nhà bằng vật liệu dễ vệ lau rửa, khi cần thiết có thể thực hiện công việc tẩy trùng;
- Có chỗ rửa tay, rửa và bảo quản dụng cụ pha chế, bao bì đựng;
- Không được bố trí chỗ ngồi cho người mua thuốc trong khu vực phòng pha chế.
- Nhà thuốc phải có hóa chất, các dụng cụ phục vụ cho pha chế, có thiết bị để tiệt trùng dụng cụ (tủ sấy, nồi hấp), bàn pha chế phải dễ vệ sinh, lau rửa.
4.5.2.3. Thiết bị bảo quản thuốc
a) Có đủ thiết bị để bảo quản thuốc tránh được các ảnh hưởng bất lợi của ánh sáng, nhiệt độ, độ ẩm, sự ô nhiễm, sự xâm nhập của côn trùng, bao gồm:
- Tủ, quầy, giá kệ chắc chắn, trơn nhẵn, dễ vệ sinh, thuận tiện cho bày bán, bảo quản thuốc và đảm bảo thẩm mỹ.
- Có đủ ánh sáng để đảm bảo các thao tác, đảm bảo việc kiểm tra các thông tin trên nhãn thuốc và tránh nhầm lẫn.
- Nhiệt kế, ẩm kế để kiểm soát nhiệt độ, độ ẩm tại cơ sở bán lẻ thuốc. Nhiệt kế, ẩm kế phải được hiệu chuẩn định kỳ theo quy định. Phải trang bị ít nhất 01 thiết bị theo dõi nhiệt độ tự ghi với tần suất ghi phù hợp (thường 01 hoặc 02 lần trong 01 giờ tùy theo mùa).
b) Thiết bị bảo quản thuốc phù hợp với yêu cầu bảo quản ghi trên nhãn thuốc. Điều kiện bảo quản ở nhiệt độ phòng: nhiệt độ không vượt quá 30°C, độ ẩm không vượt quá 75%.
- Có tủ lạnh hoặc phương tiện bảo quản lạnh phù hợp với các thuốc có yêu cầu bảo quản mát (8-15°C), lạnh (2-8°C).
c) Có các dụng cụ ra lẻ và bao bì ra lẻ phù hợp với yêu cầu bảo quản thuốc, bao gồm:
- Trường hợp ra lẻ thuốc mà không còn bao bì tiếp xúc trực tiếp với thuốc phải dùng đồ bao gói kín khí; đủ cứng để bảo vệ thuốc, có nút kín.
- Không dùng các bao bì ra lẻ thuốc có chứa nội dung quảng cáo các thuốc khác để làm túi đựng thuốc.
- Thuốc dùng ngoài, thuốc quản lý đặc biệt cần được đóng trong bao bì phù hợp, dễ phân biệt.
- Thuốc pha chế theo đơn cần được đựng trong bao bì dược dụng để không ảnh hưởng đến chất lượng thuốc và dễ phân biệt với các sản phẩm không phải thuốc - như đồ uống/thức ăn/sản phẩm gia dụng (áp dụng đối với nhà thuốc).
d) Ghi nhãn thuốc:
- Đối với trường hợp thuốc bán lẻ không đựng trong bao bì ngoài của thuốc thì phải ghi rõ: tên thuốc; dạng bào chế; nồng độ, hàm lượng thuốc; trường hợp không có đơn thuốc đi kèm phải ghi thêm liều dùng, số lần dùng và cách dùng.
- Thuốc pha chế theo đơn của nhà thuốc: ngoài việc phải ghi đầy đủ các quy định trên phải ghi thêm ngày pha chế; ngày hết hạn; tên bệnh nhân; tên và địa chỉ cơ sở pha chế thuốc; các cảnh báo an toàn cho trẻ em (nếu có) (áp dụng đối với nhà thuốc).
4.5.2.4. Hồ sơ, sổ sách và tài liệu chuyên môn của cơ sở bán lẻ thuốc
a) Có tài liệu hoặc có phương tiện tra cứu các tài liệu hướng dẫn sử dụng thuốc cập nhật, các quy chế dược hiện hành, các thông báo có liên quan của cơ quan quản lý dược để người bán lẻ có thể tra cứu và sử dụng khi cần.
b) Phải có sổ sách hoặc máy tính để quản lý việc nhập, xuất, tồn trữ, theo dõi số lô, hạn dùng, nguồn gốc của thuốc và các thông tin khác có liên quan, bao gồm:
- Thông tin thuốc: Tên thuốc, số Giấy phép lưu hành/Số Giấy phép nhập khẩu, số lô, hạn dùng, nhà sản xuất, nhà nhập khẩu, điều kiện bảo quản.
- Nguồn gốc thuốc: Cơ sở cung cấp, ngày tháng mua, số lượng.
- Cơ sở vận chuyển, điều kiện bảo quản trong quá trình vận chuyển.
- Số lượng nhập, bán, còn tồn của từng loại thuốc.
- Người mua/bệnh nhân, ngày tháng, số lượng (đối với thuốc gây nghiện, thuốc tiền chất, thuốc hướng thần, thuốc dạng phối hợp có chứa dược chất gây nghiện, dược chất hướng thần, tiền chất).
- Đối với thuốc kê đơn phải thêm người kê đơn và cơ sở hành nghề.
c) Nhà thuốc/quầy thuốc phải có thiết bị và triển khai ứng dụng công nghệ thông tin, thực hiện kết nối mạng, bảo đảm kiểm soát xuất xứ, giá cả, nguồn gốc thuốc mua vào, bán ra. Có cơ chế chuyển thông tin về việc mua bán thuốc, chất lượng thuốc giữa nhà cung cấp với khách hàng cũng như việc chuyển giao thông tin cho cơ quan quản lý liên quan khi được yêu cầu.
d) Hồ sơ hoặc sổ sách phải được lưu trữ ít nhất 1 năm kể từ khi hết hạn dùng của thuốc. Hồ sơ hoặc sổ sách lưu trữ các dữ liệu liên quan đến bệnh nhân có đơn thuốc hoặc các trường hợp đặc biệt (bệnh nhân mạn tính, bệnh nhân cần theo dõi....) đặt tại nơi bảo đảm để có thể tra cứu kịp thời khi cần.
đ) Trường hợp cơ sở có kinh doanh thuốc phải quản lý đặc biệt, phải thực hiện các quy định tại Điều 43 Nghị định 54/2017/NĐ-CP ngày 08/5/2017 và các văn bản khác có liên quan.
Theo Thông tư 20/2017/TT-BYT về hồ sơ sổ sách của nhà thuốc bán lẻ thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất phải lập và ghi chép đầy đủ các loại sau đây:
- Sổ theo dõi xuất, nhập, tồn kho thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất theo mẫu sổ quy định tại Phụ lục VIII kèm theo Thông tư 20/2017/TT-BYT.
- Phiếu xuất kho thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất của nơi cung cấp thuốc.
- Đơn thuốc gây nghiện, thuốc hướng thần lưu tại cơ sở sau khi bán.
- Biên bản nhận thuốc gây nghiện theo mẫu biên bản quy định tại Phụ lục XX kèm theo Thông tư 20/2017/TT-BYT.
- Sổ theo dõi thông tin chi tiết khách hàng theo mẫu sổ quy định tại Phụ lục XXI kèm theo Thông tư 20/2017/TT-BYT.
Với cơ sở bán lẻ thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất phải lập và ghi chép đầy đủ Sổ theo dõi thông tin chi tiết khách hàng theo mẫu sổ quy định tại Phụ lục XXI kèm theo Thông tư 20/2017/TT-BYT.
e) Xây dựng và thực hiện theo các quy trình thao tác chuẩn dưới dạng văn bản cho tất cả các hoạt động chuyên môn để mọi nhân viên áp dụng, tối thiểu phải có các quy trình sau:
- Quy trình mua thuốc và kiểm soát chất lượng.
- Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc phải kê đơn.
- Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc không kê đơn.
- Quy trình bảo quản và theo dõi chất lượng.
- Quy trình giải quyết đối với thuốc bị khiếu nại hoặc thu hồi.
- Quy trình pha chế thuốc theo đơn trong trường hợp có tổ chức pha chế theo đơn.
- Các quy trình khác có liên quan.
4.5.2.5. Quy định về cơ sở vật chất của cơ sở bán lẻ thuốc phải kiểm soát đặc biệt (Điều 43, Nghị định 54/2017/NĐ-CP; Điều 5, Nghị định số 155/2018/NĐ-CP)
- Đối với cơ sở bán lẻ thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất:
+ Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất phải bảo quản trong tủ riêng hoặc ngăn riêng có khóa chắc chắn.
+ Có hệ thống quản lý, theo dõi bằng hồ sơ sổ sách theo quy định của Bộ trưởng Bộ Y tế.
- Đối với cơ sở bán lẻ thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất phải thực hiện việc theo dõi bằng hệ thống phần mềm hoặc hồ sơ, sổ sách theo quy định của Bộ trưởng Bộ Y tế.
- Đối với cơ sở bán lẻ thuốc phóng xạ:
+ Có khu vực riêng để bảo quản thuốc phóng xạ..
+ Có hệ thống quản lý, theo dõi bằng hồ sơ sổ sách theo quy định của Bộ trưởng Bộ Y tế.
- Đối với cơ sở kinh doanh thuốc độc, nguyên liệu độc làm thuốc, thuốc và dược chất trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực phải thực hiện việc theo dõi bằng hệ thống phần mềm hoặc hồ sơ, sổ sách quản lý toàn bộ quá trình xuất, nhập, tồn kho theo quy định của Thông tư 20/2017/TT-BYT
4.5.3. Các hoạt động của cơ sở bán lẻ thuốc
4.5.3.1.Mua thuốc (gồm cả thuốc KSĐB)
a) Nguồn thuốc được mua tại các cơ sở kinh doanh thuốc hợp pháp.
b) Có hồ sơ theo dõi, lựa chọn các nhà cung cấp có uy tín, đảm bảo chất lượng thuốc trong quá trình kinh doanh.
c) Chỉ mua các thuốc được phép lưu hành (thuốc có số đăng ký hoặc thuốc chưa có số đăng ký được phép nhập khẩu). Thuốc mua còn nguyên vẹn và có đầy đủ bao gói của nhà sản xuất, nhãn đúng quy định theo quy chế hiện hành. Có đủ hóa đơn, chứng từ hợp lệ của thuốc mua về.
d) Khi nhập thuốc, người bán lẻ kiểm tra hạn dùng, kiểm tra các thông tin trên nhãn thuốc theo quy chế ghi nhãn, kiểm tra chất lượng (bằng cảm quan, nhất là với các thuốc dễ có biến đổi chất lượng) và có kiểm soát trong suốt quá trình bảo quản.
Đối với thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, thuốc dạng phối hợp có chứa tiền chất: chỉ được mua của cơ sở bán buôn trên địa bàn tỉnh có phạm vi kinh doanh thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, thuốc dạng phối hợp có chứa tiền chất hoặc mua của cơ sở đồng thời có giấy chứng nhận đủ điều kiện kinh doanh dược phạm vi xuất khẩu, nhập khẩu thuốc và bán buôn thuốc.
Đối với thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc phóng xạ, thuốc độc, nguyên liệu độc làm thuốc, thuốc và dược chất trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực của các cơ sở kinh doanh thuốc chỉ được mua ở các công ty được phép kinh doanh thuốc kiểm soát đặc biệt.
Hồ sơ đề nghị mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất gồm các tài liệu sau (Điều 53- Nghị định 54/2017/NĐ-CP; Điều 4 - Nghị định 155/2018/NĐ-CP)
+ 03 bản đơn hàng mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất theo Mẫu số 19 tại Phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP;
+ Văn bản giải thích rõ lý do khi số lượng thuốc đề nghị mua vượt quá 150% so với số lượng sử dụng lần trước.
4.5.3.2. Bảo quản, sắp xếp thuốc
a. Bảo quản thuốc
* Khái niệm: là việc cất giữ bảo đảm an toàn, chất lượng của thuốc, bao gồm cả việc đưa vào sử dụng và duy trì đầy đủ hệ thống hồ sơ tài liệu phục vụ bảo quản, xuất, nhập thuốc tại nơi bảo quản. (Thông tư 36/2018/TT-BYT)
* Các quy định liên quan bảo quản thuốc tại cơ sở bán lẻ
- Không được bán thuốc đã hết hạn dùng, thuốc bảo quản không đúng quy định ghi trên nhãn thuốc,
- Kho bảo quản riêng (nếu cần).
- Thuốc phải được bảo quản theo yêu cầu ghi trên nhãn thuốc;
- Các thuốc kê đơn nếu được bày bán và bảo quản tại khu vực riêng có ghi rõ “Thuốc kê đơn” hoặc trong cùng một khu vực phải để riêng các thuốc bán theo đơn.
- Thuốc phải kiểm soát đặc biệt (gây nghiện, hướng tâm thần, và tiền chất) và các thuốc độc hại, nhạy cảm và/hoặc nguy hiểm khác cũng như các thuốc có nguy cơ lạm dụng đặc biệt, gây cháy, nổ (như các chất lỏng và chất rắn dễ bắt lửa, dễ cháy và các loại khí nén) phải được bảo quản ở các khu vực riêng biệt, có các biện pháp bảo đảm an toàn và an ninh theo đúng quy định của pháp luật.
- Thuốc độc, thuốc trong Danh mục thuốc, dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực phải được bảo quản tách biệt, không được để cùng các thuốc khác, phải sắp xếp gọn gàng, tránh nhầm lẫn, dễ quan sát.
* Có các thiết bị bảo quản thuốc theo quy định
b. Sắp xếp thuốc
- Nguyên tắc sắp xếp:
+ Sắp xếp thuốc hóa dược theo tác dụng dược lý.
+ Khu vực riêng cho thuốc kê đơn.
+ Mỹ phẩm, thực phẩm chức năng, thực phẩm bảo vệ sức khỏe, dụng cụ y tế để khu vực riêng, không ảnh hưởng đến thuốc. Có biển hiệu khu vực “Sản phẩm này không phải là thuốc”.
+ Việc sắp xếp đảm bảo sự thuận lợi, tránh gây nhầm lẫn.
+ Sắp xếp theo điều kiện bảo quản ghi trên nhãn.
- Tiến hành phân loại thuốc trước khi sắp xếp:
+ Phân loại thuốc theo điều kiện bảo quản.
+ Phân loại thuốc kê đơn, thuốc không kê đơn.
+ Phân loại thuốc phải kiểm soát đặc biệt.
+ Phân loại thuốc theo tác dụng dược lý.
4.5.4.3. Bán thuốc
a) Các bước cơ bản trong hoạt động bán thuốc, bao gồm:
- Người bán lẻ hỏi người mua những câu hỏi liên quan đến bệnh, đến thuốc mà người mua yêu cầu;
- Người bán lẻ tư vấn thông tin cho người mua về lựa chọn thuốc, cách dùng thuốc, hướng dẫn cách sử dụng thuốc bằng lời nói. Trường hợp không có đơn thuốc kèm theo, Người bán lẻ phải hướng dẫn sử dụng thuốc thêm bằng cách viết tay hoặc đánh máy, in gắn lên đồ bao gói.
- Người bán lẻ cung cấp các thuốc phù hợp, kiểm tra, đối chiếu thuốc bán ra về nhãn thuốc, cảm quan về chất lượng, số lượng, chủng loại thuốc.
- Thuốc được niêm yết giá thuốc đúng quy định và không bán cao hơn giá niêm yết.
b) Các quy định về tư vấn cho người mua, bao gồm:
- Người mua thuốc cần nhận được sự tư vấn đúng đắn, đảm bảo hiệu quả điều trị và phù hợp với nhu cầu, nguyện vọng;
- Người bán lẻ phải xác định rõ trường hợp nào cần có tư vấn của người có chuyên môn phù hợp với loại thuốc cung cấp để tư vấn cho người mua thông tin về thuốc, giá cả và lựa chọn các thuốc không cần kê đơn;
- Đối với người bệnh đòi hỏi phải có chẩn đoán của thầy thuốc mới có thể dùng thuốc, Người bán lẻ cần tư vấn để bệnh nhân tới khám thầy thuốc chuyên khoa thích hợp hoặc bác sĩ điều trị;
- Đối với những người mua thuốc chưa cần thiết phải dùng thuốc, nhân viên bán thuốc cần giải thích rõ cho họ hiểu và tự chăm sóc, tự theo dõi triệu chứng bệnh;
- Không được tiến hành các hoạt động thông tin, quảng cáo thuốc tại nơi bán thuốc trái với quy định về thông tin quảng cáo thuốc; khuyến khích người mua coi thuốc là hàng hóa thông thường và khuyến khích người mua mua thuốc nhiều hơn cần thiết.
c) Bán thuốc theo đơn:
- Khi bán các thuốc theo đơn phải có sự tham gia trực tiếp người bán lẻ có trình độ chuyên môn phù hợp và tuân thủ theo các quy định, quy chế hiện hành của Bộ Y tế về bán thuốc kê đơn.
- Người bán lẻ phải bán theo đúng đơn thuốc. Trường hợp phát hiện đơn thuốc không rõ ràng về tên thuốc, nồng độ, hàm lượng, số lượng, hoặc có sai phạm về pháp lý, chuyên môn hoặc ảnh hưởng đến sức khỏe người bệnh, Người bán lẻ phải thông báo lại cho người kê đơn biết.
- Người bán lẻ giải thích rõ cho người mua và có quyền từ chối bán thuốc theo đơn trong các trường hợp đơn thuốc không hợp lệ, đơn thuốc có sai sót hoặc nghi vấn, đơn thuốc kê không nhằm mục đích chữa bệnh.
- Người bán lẻ là dược sỹ đại học có quyền thay thế thuốc bằng một thuốc khác có cùng hoạt chất, dạng bào chế, cùng liều lượng khi có sự đồng ý của người mua.
- Người bán lẻ hướng dẫn người mua về cách sử dụng thuốc, nhắc nhở người mua thực hiện đúng đơn thuốc.
- Sau khi bán thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất người bán lẻ phải vào sổ, lưu đơn thuốc bản chính.
4.5.4.4. Thuốc khiếu nại hoặc thu hồi
Có tiếp nhận và lưu thông tin hoặc lưu các thông báo về thuốc khiếu nại, thuốc không được phép lưu hành, thuốc phải thu hồi.
Có thu hồi và lập hồ sơ thu hồi theo quy định, Có kiểm kê đối với thuốc khiếu nại, thuốc phải thu hồi .
Có thông báo thu hồi cho khách hàng đối với thuốc thu hồi thuộc danh mục thuốc phải kê đơn..
Có trả lại nơi mua hoặc hủy theo đúng quy định.
Có báo cáo các cấp theo quy định.
Có sổ và có ghi chép theo dõi tác dụng phụ của thuốc do khách hàng phản ánh.
2.4.4.5. Quy định về hủy thuốc phải kiểm soát đặc biệt
- Cơ sở đề nghị hủy thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc có văn bản đề nghị hủy trong đó phải ghi rõ tên thuốc, nguyên liệu làm thuốc, nồng độ hoặc hàm lượng, số lượng, lý do xin hủy, phương pháp hủy.
- Thủ tục cho phép hủy thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc phải thực hiện như sau:
+ Cơ sở đề nghị hủy nộp văn bản trực tiếp hoặc gửi qua đường qua đường bưu điện tại Bộ Y tế đối với cơ sở sản xuất, xuất khẩu, nhập khẩu hoặc tại Sở Y tế nơi cơ sở đó đặt trụ sở đối với các cơ sở kinh doanh dược khác trừ các cơ sở trên; hoặc tại Cục Quân y - Bộ Quốc phòng đối với cơ sở thuộc Bộ Quốc phòng.
+ Sau khi nhận hồ sơ, cơ quan tiếp nhận hồ sơ trả cho cơ sở đề nghị hủy Phiếu tiếp nhận hồ sơ theo Mẫu số 01 tại Phụ lục I ban hành kèm theo Nghị định 54.
+ Trường hợp không có yêu cầu sửa đổi, bổ sung, cơ quan tiếp nhận hồ sơ hủy có công văn cho phép hủy trong thời hạn 20 ngày kể từ ngày ghi trên Phiếu tiếp nhận hồ sơ.
+ Trường hợp có yêu cầu sửa đổi, bổ sung hồ sơ xin hủy, cơ quan tiếp nhận phải có văn bản yêu cầu sửa đổi, bổ sung hồ sơ xin hủy trong thời hạn 20 ngày, kể từ ngày ghi trên Phiếu tiếp nhận hồ sơ.
+ Sau khi cơ sở nộp hồ sơ sửa đổi, bổ sung, cơ quan tiếp nhận hồ sơ trả cho cơ sở Phiếu tiếp nhận hồ sơ sửa đổi, bổ sung theo Mẫu số 01 tại Phụ lục I ban hành kèm theo Nghị định 54. Trường hợp không có yêu cầu sửa đổi, bổ sung hồ sơ, cơ quan tiếp nhận có công văn cho phép hủy theo quy định tại điểm c khoản này. Trường hợp hồ sơ sửa đổi, bổ sung không đáp ứng yêu cầu, cơ quan tiếp nhận có văn bản thông báo cho cơ sở theo quy định tại điểm d khoản này.
- Việc hủy thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc chỉ được thực hiện sau khi có công văn cho phép của Bộ Y tế hoặc Sở Y tế nơi cơ sở đặt trụ sở hoặc của Cục Quân y - Bộ Quốc phòng đối với cơ sở thuộc Bộ Quốc phòng.
- Việc hủy thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc được thực hiện như sau:
+ Người đứng đầu cơ sở thành lập Hội đồng hủy thuốc. Hội đồng có ít nhất 03 người, trong đó phải có 01 đại diện là người phụ trách chuyên môn của cơ sở. Hội đồng hủy thuốc có nhiệm vụ tổ chức việc hủy thuốc, quyết định phương pháp hủy, giám sát việc hủy thuốc của cơ sở;
+ Việc hủy thuốc và nguyên liệu làm thuốc phải có sự chứng kiến của đại diện Sở Y tế trên địa bàn hoặc Cục Quân y - Bộ Quốc phòng và được lập biên bản theo Mẫu số 16 tại Phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP;
+ Trong thời hạn 10 ngày, kể từ ngày kết thúc việc hủy thuốc và nguyên liệu làm thuốc, cơ sở phải gửi báo cáo việc hủy thuốc theo Mẫu số 17 tại Phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP kèm theo biên bản hủy thuốc tới Bộ Y tế hoặc Sở Y tế hoặc Cục Quân y - Bộ Quốc phòng.
- Khi hủy các loại dư phẩm, phế phẩm có chứa dược chất gây nghiện, dược chất hướng thần và tiền chất dùng làm thuốc trong quá trình sản xuất; thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, các loại bao bì đã tiếp xúc trực tiếp với thuốc gây nghiện, thuốc hướng tâm thần, thuốc tiền chất, dược chất gây nghiện, dược chất hướng thần và tiền chất dùng làm thuốc không sử dụng nữa, thuốc độc, nguyên liệu độc làm thuốc, thuốc và dược chất trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực tại các cơ sở kinh doanh thuốc, cơ sở phải tập hợp và hủy theo quy định tại điểm a khoản 4 Điều 48 Nghị định 54/2017/NĐ-CP và lưu hồ sơ hủy tại cơ sở.
4.5.4.6. Quản lý giá thuốc, thông tin thuốc
a. Quản lý giá thuốc
Nguyên tắc quản lý nhà nước về giá thuốc
- Quản lý giá thuốc theo cơ chế thị trường, tôn trọng quyền tự định giá, cạnh tranh về giá của tổ chức, cá nhân kinh doanh thuốc theo quy định của pháp luật.
- Bảo đảm công khai, minh bạch giá thuốc khi lưu hành thuốc trên thị trường.
- Bảo vệ quyền, lợi ích hợp pháp của tổ chức, cá nhân kinh doanh, người tiêu dùng và lợi ích của Nhà nước.
- Thực hiện các biện pháp bình ổn giá và sử dụng các biện pháp khác để quản lý giá thuốc phù hợp với điều kiện phát triển kinh tế - xã hội trong từng thời kỳ.
Các biện pháp quản lý giá thuốc liên quan đến cơ sở bán lẻ thuốc
- Niêm yết giá bán lẻ thuốc bằng đồng Việt Nam tại nơi giao dịch hoặc nơi bán thuốc của cơ sở kinh doanh dược; in, ghi hoặc dán giá bán lẻ trên bao bì chứa đựng thuốc hoặc bao bì ngoài của thuốc; thông báo công khai trên bảng, trên giấy hoặc bằng các hình thức khác.
Việc niêm yết giá bán lẻ thuốc được thực hiện bằng các hình thức in, ghi hoặc dán giá bán lẻ trên bao bì chứa đựng thuốc hoặc bao bì ngoài của thuốc; hoặc thông báo công khai trên bảng, trên giấy hoặc bằng các hình thức khác phù hợp và phải thuận tiện cho việc quan sát, nhận biết của khách hàng, cơ quan nhà nước có thẩm quyền, không che khuất nội dung bắt buộc của nhãn thuốc; (Điều 135, Nghị định 54/2017/NĐ-CP). Các cơ sở bán lẻ thuốc phải thực hiện việc niêm yết giá bán lẻ từng loại thuốc tại cơ sở bán lẻ thuốc. (Điều 135, Nghị định 54/2017/NĐ-CP)
- Thực hiện các biện pháp bình ổn giá thuốc theo quy định của Luật giá đối với thuốc thuộc Danh mục thuốc thiết yếu khi có biến động bất thường về giá hoặc mặt bằng giá biến động ảnh hưởng đến sự ổn định kinh tế - xã hội.
- Quy định thặng số bán lẻ tối đa đối với thuốc bán tại cơ sở bán lẻ thuốc trong khuôn viên cơ sở khám bệnh, chữa bệnh.
Các hành vi không được làm liên quan đến giá thuốc
- Bán thuốc cao hơn giá kê khai, giá niêm yết.
- Khuyến mại thuốc trái quy định của pháp luật: Hàng hóa, dịch vụ được khuyến mại không bao gồm rượu, xổ số, thuốc lá, sữa thay thế sữa mẹ, thuốc chữa bệnh cho người kể cả các loại thuốc đã được phép lưu thông theo quy định của Bộ Y tế (trừ trường hợp khuyến mại cho thương nhân kinh doanh thuốc) (Điều 5 - Nghị định 81/2018/NĐ-CP)
b. Thông tin thuốc
Thông tin thuốc là việc thu thập, cung cấp các thông tin có liên quan đến thuốc bao gồm chỉ định, chống chỉ định, liều dùng, cách dùng, phản ứng có hại của thuốc và các thông tin khác liên quan đến chất lượng, an toàn, hiệu quả của thuốc do các cơ sở có trách nhiệm thông tin thuốc thực hiện nhằm đáp ứng yêu cầu thông tin của cơ quan quản lý nhà nước về dược, tổ chức, cá nhân đang trực tiếp hành nghề y, dược hoặc của người sử dụng thuốc.
Nội dung và trách nhiệm thông tin thuốc của cơ sở bán lẻ
- Thông tin thuốc nhằm mục đích hướng dẫn sử dụng thuốc hợp lý, an toàn, hiệu quả cho người hành nghề khám bệnh, chữa bệnh và người sử dụng thuốc.
- Thông tin thuốc phải cập nhật, rõ ràng, đầy đủ, chính xác dựa trên bằng chứng, dễ hiểu, phù hợp với đối tượng được cung cấp thông tin.
- Thông tin cho người sử dụng thuốc bao gồm tên thuốc, công dụng, chỉ định, chống chỉ định, liều dùng, cách dùng và những vấn đề cần lưu ý trong quá trình sử dụng thuốc;
- Cơ sở bán lẻ thuốc có trách nhiệm cung cấp thông tin thuốc phù hợp với thông tin theo các tài liệu sau:
+ Dược thư Quốc gia Việt Nam.
+ Tờ hướng dẫn sử dụng thuốc đã được Bộ Y tế phê duyệt.
+ Tài liệu, hướng dẫn chuyên môn có liên quan đến thuốc do Bộ Y tế ban hành hoặc công nhận.
- Cơ sở bán lẻ thuốc có các trách nhiệm sau đây:
+ Tư vấn trong phạm vi chuyên môn cho người sử dụng thuốc về các biện pháp xử lý khi có dấu hiệu bất thường trong quá trình sử dụng thuốc;
+ Thu thập, báo cáo cho cơ quan có thẩm quyền các thông tin về dấu hiệu bất thường trong quá trình sử dụng thuốc.
4.5.4.6. Lưu thông tin và báo cáo
Quy định về chế độ báo cáo của cơ sở kinh doanh thuốc phải kiểm soát đặc biệt (Khoản 4, Điều 47-nghị định 54/2017/NĐ-CP)
Trước ngày 15 tháng 7 và trước ngày 15 tháng 01 hàng năm, cơ sở bán lẻ báo cáo 06 (sáu) tháng và báo cáo năm tương ứng về việc xuất, nhập, tồn kho, sử dụng thuốc phóng xạ, thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất theo Mẫu số 11, 12, 13 tại Phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP và gửi Sở Y tế nơi cơ sở đặt trụ sở.
Trong thời hạn 48 giờ, kể từ khi phát hiện nhầm lẫn, thất thoát thuốc phóng xạ, thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất và nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc, cơ sở bán lẻ lập báo cáo gửi Sở Y tế. Mẫu báo cáo theo Mẫu số 14 tại Phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP của Chính phủ.
4.6. Một số quy định xử phạt vi phạm hành chính liên quan tại cơ sở bán lẻ thuốc
Nghị định 117/2020/NĐ-CP ban hành quy định xử phạt vi phạm hành chính trong lĩnh vực y tế. Trong đó, một số quy định xử phạt hành chính liên quan tại cơ sở bán lẻ thuốc được trình bày tại Bảng 2.2 (Mục 3 Nghị định 117/2020/NĐ-CP của Chính phủ).
Bảng 4.2. Một số quy định xử phạt vi phạm hành chính liên quan tại cơ sở bán lẻ thuốc
|
| Hành vi vi phạm | Phạt tiền | Xử phạt bổ sung |
| Vi phạm các quy định về hành nghề dược (Điều 52, Mục 3 NĐ 117/2020/NĐ-CP) | |||
| 1a | Người chịu trách nhiệm chuyên môn của cơ sở bán lẻ thuốc vắng mặt trong thời gian hoạt động của cơ sở dược, trừ trường hợp ủy quyền khi vắng mặt theo quy định của pháp luật | 3.000.000 đồng đến 5.000.000 đồng |
|
| 1b | b) Không chấp hành quyết định của cơ quan nhà nước có thẩm quyền trong trường hợp có dịch bệnh nguy hiểm, thiên tai, thảm họa | 3.000.000 đồng đến 5.000.000 đồng | Tước quyền sử dụng CCHND và GCNĐĐKKDD trong thời hạn từ 06 tháng đến 09 tháng |
| 1c | Chưa hoàn thành chương trình đào tạo, cập nhật kiến thức chuyên môn về dược trong thời hạn 03 năm, kể từ ngày được cấp chứng chỉ hành nghề dược hoặc kể từ ngày có giấy xác nhận hoàn thành chương trình đào tạo, cập nhật kiến thức chuyên môn về dược gần nhất | 3.000.000 đồng đến 5.000.000 đồng |
|
| 1d | Thay thế thuốc đã kê trong đơn thuốc bằng một thuốc khác có cùng hoạt chất, cách dùng, liều lượng khi chưa có sự đồng ý của người mua | 3.000.000 đồng đến 5.000.000 đồng |
|
| 2a | Giả mạo một trong các giấy tờ trong hồ sơ đề nghị cấp chứng chỉ hành nghề dược | 5.000.000 đồng đến 10.000.000 đồng |
|
| 2b | Hành nghề dược mà không có chứng chỉ hành nghề dược hoặc trong thời gian bị tước quyền sử dụng chứng chỉ hành nghề dược tại vị trí công việc phải có chứng chỉ hành nghề dược theo quy định của pháp luật | 5.000.000 đồng đến 10.000.000 đồng |
|
| 2c | Chịu trách nhiệm chuyên môn từ hai cơ sở kinh doanh dược trở lên hoặc tại hai địa điểm kinh doanh dược trở lên | 5.000.000 đồng đến 10.000.000 đồng | Tước quyền sử dụng chứng chỉ hành nghề dược trong thời hạn từ 01 tháng đến 03 tháng |
| 2d | Hành nghề dược không đúng phạm vi hoạt động chuyên môn ghi trong chứng chỉ hành nghề dược và quy định chuyên môn kỹ thuật | 5.000.000 đồng đến 10.000.000 đồng | |
| 2đ,e | Cơ sở đào tạo, cập nhật kiến thức chuyên môn về dược không đáp ứng điều kiện quy định của pháp luật; Cơ sở tổ chức thi xét cấp chứng chỉ hành nghề dược không đáp ứng điều kiện quy định của pháp luật | 5.000.000 đồng đến 10.000.000 đồng |
|
| 2g | Cho thuê, cho mượn hoặc cho người khác sử dụng chứng chỉ hành nghề dược để hành nghề dược | 5.000.000 đồng đến 10.000.000 đồng |
|
| 3 | Hành vi thuê, mượn chứng chỉ hành nghề dược để hành nghề dược. | 10.000.000 đồng đến 20.000.000 đồng |
|
| Vi phạm quy định về cơ sở kinh doanh dược và điều kiện kinh doanh dược (Điều 53, Mục 3 NĐ 117/2020/NĐ- CP) | |||
| 1a | Cơ sở tổ chức bán lẻ thuốc lưu động không đáp ứng điều kiện theo quy định của pháp luật. | 1.000.000 đồng đến 3.000.000 đồng | Đình chỉ hoạt động kinh doanh có liên quan đến hành vi vi phạm trong thời hạn từ 01 tháng đến 03 tháng |
| 1b | Cơ sở tổ chức bán lẻ thuốc lưu động không thông báo bằng văn bản đến Sở Y tế tại địa phương nơi dự kiến có hoạt động bán lẻ thuốc lưu động trước khi tổ chức bán lẻ thuốc lưu động. | 1.000.000 đồng đến 3.000.000 đồng |
|
| 2 | Hành vi không có biện pháp cách ly hoặc để ở khu vực biệt trữ các thuốc, nguyên liệu làm thuốc sau đây, trừ trường hợp quy định tại điểm đ khoản 4 Điều 59 Nghị định 54/2018/NĐ-CP: Không đạt tiêu chuẩn chất lượng; Đã có thông báo thu hồi của cơ quan nhà nước có thẩm quyền; Đã hết hạn dùng; Không rõ nguồn gốc, xuất xứ. | 15.000.000 đồng đến 20.000.000 đồng |
|
| Vi phạm quy định về giấy chứng nhận đủ điều kiện kinh doanh dược (Điều 54, Mục 3 NĐ 117/2020/NĐ-CP) | |||
| 1a | Làm giả, sửa chữa hồ sơ, giấy tờ, tài liệu, giấy chứng nhận của cơ quan, tổ chức có thẩm quyền và tổ chức, cá nhân trong hồ sơ đề nghị cấp giấy chứng nhận đủ điều kiện kinh doanh dược; | 20.000.000 đồng đến 30.000.000 đồng | Tước quyền sử dụng giấy chứng nhận đủ điều kiện kinh doanh dược trong thời hạn 24 tháng |
| 1b | Thuê, mượn, cho thuê, cho mượn hoặc cho cá nhân, tổ chức khác sử dụng giấy chứng nhận đủ điều kiện kinh doanh dược để kinh doanh dược. | 20.000.000 đồng đến 30.000.000 đồng | |
| Vi phạm quy định về quyền và trách nhiệm của cơ sở kinh doanh dược (Điều 55, Mục 3 NĐ 117/2020/NĐ-CP) | |||
| 1a | Không báo cáo Bộ Y tế hoặc Sở Y tế, không thực hiện các nghĩa vụ theo quy định của pháp luật trong trường hợp tạm dừng hoạt động từ 06 tháng trở lên hoặc chấm dứt hoạt động; | 1.000.000 đồng đến 3.000.000 đồng | Đình chỉ hoạt động kinh doanh có liên quan đến hành vi vi phạm trong thời hạn từ 01 tháng đến 03 tháng |
| 1b | Không thông báo, không cập nhật danh sách người có chứng chỉ hành nghề dược đang hành nghề tại cơ sở đến cơ quan nhà nước có thẩm quyền theo quy định của pháp luật; | 1.000.000 đồng đến 3.000.000 đồng |
|
| 1c | Không thực hiện chế độ báo cáo định kỳ, báo cáo đột xuất hoặc báo cáo theo yêu cầu của cơ quan nhà nước có thẩm quyền về dược theo quy định của pháp luật; | Phạt tiền 1,5 lần đối với vi phạm liên quan đến thuốc, dược chất thuộc danh mục cấm sử dụng trong 1 số ngành, lĩnh vực, thuốc phối hợp có chứa dược chất GN/HT/TC/thuốc phóng xạ Phạt tiền bằng 02 lần với hành vi vi phạm liên quan thuốc GN/HT/TC |
|
| 1d | Không niêm yết giá bán buôn, bán lẻ bằng đồng Việt Nam hoặc niêm yết không đầy đủ, không đúng quy định, không rõ ràng gây nhầm lẫn cho khách hàng tại nơi giao dịch hoặc nơi bán thuốc của cơ sở kinh doanh dược. | 1.000.000 đồng đến 3.000.000 đồng |
|
| 2a | Không niêm yết công khai chứng chỉ hành nghề dược đối với trường hợp phải có chứng chỉ hành nghề dược hoặc giấy chứng nhận đủ điều kiện kinh doanh dược tại cơ sở | 5.000.000 đồng đến 10.000.000 đồng |
|
| 2b | Không bồi thường thiệt hại cho tổ chức, cá nhân bị thiệt hại do lỗi của cơ sở bán lẻ thuốc, dược liệu theo quy định của pháp luật. | từ 5.000.000 đồng đến 10.000.000 đồng |
|
| 3 | Hành vi không bồi thường thiệt hại cho tổ chức, cá nhân bị thiệt hại do lỗi của cơ sở theo quy định của pháp luật, trừ trường hợp quy định ở mục 2b | từ 10.000.000 đồng đến 20.000.000 đồng |
|
| Vi phạm quy định về bán lẻ thuốc dược liệu (Điều 59, Mục 3 NĐ 117/2020/NĐ-CP) | |||
| 1a | Bán dược liệu đã qua sơ chế không bảo đảm tiêu chuẩn chất lượng theo quy định của cơ quan có thẩm quyền; | 1.000.000 đồng đến 3.000.000 đồng |
|
| 1b | Người trực tiếp tham gia bán lẻ thuốc không có bằng cấp chuyên môn theo quy định của pháp luật; | 1.000.000 đồng đến 3.000.000 đồng |
|
| 1c | Không mở sổ hoặc không sử dụng máy tính để quản lý nhập, xuất, tồn trữ, theo dõi số lô, hạn dùng, nguồn gốc của thuốc và thông tin liên quan khác theo quy định của pháp luật; | Phạt tiền 1,5 lần đối với vi phạm liên quan đến thuốc, dược chất thuộc danh mục cấm sử dụng trong 1 số ngành, lĩnh vực, thuốc phối hợp có chứa dược chất GN/HT/TC/thuốc phóng xạ Phạt tiền bằng 02 lần với hành vi vi phạm liên quan thuốc GN/HT/TC |
|
| 1d | Mua, bán thuốc vi phạm chất lượng ở mức độ 3 theo quy định của pháp luật; | 1.000.000 đồng đến 3.000.000 đồng |
|
| 1đ | Không ghi rõ tên thuốc, hàm lượng, hạn dùng cho người sử dụng trong trường hợp bán lẻ thuốc không đựng trong bao bì ngoài của thuốc; trường hợp không có đơn thuốc đi kèm, không ghi thêm liều dùng, số lần dùng và cách dùng; | 1.000.000 đồng đến 3.000.000 đồng |
|
| 1e | Không lưu giữ chứng từ, tài liệu có liên quan đến lô thuốc, nguyên liệu làm thuốc trong thời gian phải lưu giữ theo quy định của pháp luật; | Phạt tiền 1,5 lần đối với vi phạm liên quan đến thuốc, dược chất thuộc danh mục cấm sử dụng trong 1 số ngành, lĩnh vực, thuốc phối hợp có chứa dược chất GN/HT/TC/thuốc phóng xạ Phạt tiền bằng 02 lần với hành vi vi phạm liên quan thuốc GN/HT/TC |
|
| 1g | Không hợp tác hoặc cản trở cơ quan kiểm tra chất lượng lấy mẫu thuốc hoặc nguyên liệu làm thuốc để kiểm tra chất lượng. | 1.000.000 đồng đến 3.000.000 đồng |
|
| 2a | Thay đổi vị trí cơ sở bán lẻ thuốc tại cùng địa điểm kinh doanh hoặc mở rộng cơ sở bán lẻ thuốc hoặc sửa chữa, thay đổi lớn về cấu trúc cơ sở bán lẻ thuốc mà cơ sở bán lẻ thuốc không báo cáo về sự thay đổi kèm theo tài liệu kỹ thuật tương ứng với sự thay đổi theo quy định của pháp luật; | 3.000.000 đồng đến 5.000.000 đồng Phạt tiền 1,5 lần đối với vi phạm liên quan đến thuốc, dược chất thuộc danh mục cấm sử dụng trong 1 số ngành, lĩnh vực, thuốc phối hợp có chứa dược chất GN/HT/TC/thuốc phóng xạ Phạt tiền bằng 02 lần với hành vi vi phạm liên quan thuốc GN/HT/TC | Đình chỉ hoạt động của cơ sở trong thời hạn từ 01 tháng đến 03 tháng |
| 2b | Không có khu vực riêng cho các sản phẩm không phải là thuốc hoặc không có biển hiệu tại khu vực riêng ghi rõ "sản phẩm này không phải là thuốc" đối với trường hợp có kinh doanh thêm mỹ phẩm, thực phẩm chức năng, trang thiết bị y tế theo quy định của pháp luật; | 3.000.000 đồng đến 5.000.000 đồng |
|
| 2c | Mua, bán thuốc vi phạm chất lượng ở mức độ 2 theo quy định của pháp luật. | 3.000.000 đồng đến 5.000.000 đồng |
|
| 3a | Không thu hồi thuốc, dược liệu theo yêu cầu của cơ quan có thẩm quyền; | 5.000.000 đồng đến 10.000.000 đồng |
|
| 3b | Không có phòng riêng để pha chế hoặc không có nơi rửa dụng cụ pha chế đối với cơ sở bán lẻ thuốc có tổ chức pha chế theo đơn; | 5.000.000 đồng đến 10.000.000 đồng |
|
| 3c | Không có kho bảo quản đối với cơ sở bán lẻ thuốc có đăng ký kho bảo quản hoặc bảo quản không đúng điều kiện ghi trên nhãn hoặc không tuân thủ các quy định về thực hành tốt cơ sở bán lẻ thuốc; | 5.000.000 đồng đến 10.000.000 đồng |
|
| 3d | Lưu trữ, bán lẻ thuốc không thuộc phạm vi kinh doanh được ghi trong giấy chứng nhận đủ điều kiện kinh doanh dược; thuốc sử dụng cho chương trình mục tiêu quốc gia; thuốc viện trợ và thuốc khác không được bán theo quy định của pháp luật; | Phạt tiền 1,5 lần đối với vi phạm liên quan đến thuốc, dược chất thuộc danh mục cấm sử dụng trong 1 số ngành, lĩnh vực, thuốc phối hợp có chứa dược chất GN/HT/TC/thuốc phóng xạ Phạt tiền bằng 02 lần với hành vi vi phạm liên quan thuốc GN/HT/TC | Đình chỉ hoạt động của cơ sở trong thời hạn từ 06 tháng đến 09 tháng |
| 3đ | Bán vắc xin hoặc bán thuốc kê đơn khi không có đơn thuốc; | 5.000.000 đồng đến 10.000.000 đồng | Đình chỉ hoạt động của cơ sở trong thời hạn từ 06 tháng đến 09 tháng |
| 3e | Không thực hiện báo cáo việc duy trì đáp ứng thực hành tốt cơ sở bán lẻ thuốc theo quy định của pháp luật; | 5.000.000 đồng đến 10.000.000 đồng |
|
| 3g | Không có thiết bị, không triển khai ứng dụng công nghệ thông tin, không thực hiện kết nối mạng, không bảo đảm kiểm soát xuất xứ, giá cả, nguồn gốc thuốc mua vào, bán ra theo quy định của pháp luật, trừ cơ sở bán lẻ dược liệu; | 5.000.000 đồng đến 10.000.000 đồng | Tước quyền sử dụng giấy chứng nhận đủ điều kiện kinh doanh dược trong thời hạn từ 01 tháng đến 02 tháng đối với hành vi quy định tại các điểm g và h khoản 3 Điều này trong trường hợp tái phạm |
| 3h | Không chuyển thông tin về việc mua bán thuốc, chất lượng thuốc giữa nhà cung cấp với khách hàng; không chuyển thông tin cho cơ quan quản lý liên quan khi được yêu cầu theo quy định của pháp luật, trừ cơ sở bán lẻ dược liệu; | 5.000.000 đồng đến 10.000.000 đồng | Tước quyền sử dụng giấy chứng nhận đủ điều kiện kinh doanh dược trong thời hạn từ 01 tháng đến 02 tháng đối với hành vi quy định tại các điểm g và h khoản 3 Điều này trong trường hợp tái phạm |
| 3i | Chỉ duy trì đáp ứng nguyên tắc, tiêu chuẩn thực hành tốt cơ sở bán lẻ thuốc ở mức độ 3. | 5.000.000 đồng đến 10.000.000 đồng | Đình chỉ hoạt động của cơ sở trong thời hạn từ 06 tháng đến 09 tháng |
| 4a | Mua, bán thuốc thử lâm sàng | 10.000.000 đồng đến 20.000.000 đồng |
|
| 4c | Mua, bán thuốc hóa dược pha chế theo đơn của nhà thuốc khác; | 10.000.000 đồng đến 20.000.000 đồng | Tước quyền sử dụng chứng chỉ hành nghề dược, giấy chứng nhận đủ điều kiện kinh doanh dược trong thời hạn từ 01 tháng đến 03 tháng |
| 4d | Mua, bán thuốc thuộc danh mục thuốc hạn chế bán lẻ khi chưa được phép theo quy định của pháp luật; | 10.000.000 đồng đến 20.000.000 đồng | Tước quyền sử dụng chứng chỉ hành nghề dược, giấy chứng nhận đủ điều kiện kinh doanh dược trong thời hạn từ 01 tháng đến 03 tháng |
| 4đ | Không có biện pháp cách ly hoặc để ở khu vực biệt trữ đối với thuốc, dược liệu thuộc một trong các trường hợp: không đạt tiêu chuẩn chất lượng; đã có thông báo thu hồi của cơ quan nhà nước có thẩm quyền; đã hết hạn dùng; không rõ nguồn gốc, xuất xứ; | 10.000.000 đồng đến 20.000.000 đồng |
|
| 4e | Mua bán thuốc vi phạm chất lượng ở mức độ 1 theo quy định của pháp luật. | 10.000.000 đồng đến 20.000.000 đồng |
|
| 5a | Hành vi mua, bán thuốc, dược liệu mà không có giấy chứng nhận đủ điều kiện kinh doanh dược; | 20.000.000 đồng đến 30.000.000 đồng |
|
| 5b | hành vi mua, bán thuốc, dược liệu Không đúng với địa điểm ghi trên giấy chứng nhận đủ điều kiện kinh doanh dược đã được cấp; | 20.000.000 đồng đến 30.000.000 đồng | Tước quyền sử dụng chứng chỉ hành nghề dược trong thời hạn từ 03 tháng đến 06 tháng |
| 5c | hành vi mua, bán thuốc, dược liệu Trong thời gian bị đình chỉ hoạt động hoặc trong thời gian bị tước quyền sử dụng giấy chứng nhận đủ điều kiện kinh doanh dược. | 20.000.000 đồng đến 30.000.000 đồng | Đình chỉ hoạt động của cơ sở trong thời hạn từ 06 tháng đến 09 tháng |
| 6 | hành vi mua, bán thuốc, dược liệu đã có thông báo thu hồi của cơ quan nhà nước có thẩm quyền; đã hết hạn dùng; không có giấy phép nhập khẩu hoặc không có giấy đăng ký lưu hành, trừ trường hợp thuốc, nguyên liệu làm thuốc không phải đăng ký trước khi lưu hành, theo một trong các mức theo giá trị hàng hóa (từ 1.000.000 đồng đến 50.000.000 đồng) | 20.000.000 đồng đến 30.000.000 đồng | Tước quyền sử dụng chứng chỉ hành nghề dược trong thời hạn từ 03 tháng đến 06 tháng |
| Vi phạm quy định về bao bì, nhãn thuốc, nguyên liệu làm thuốc (Điều 64, Mục 3, NĐ 117/2020/NĐ-CP) | |||
|
| cơ sở kinh doanh dược tẩy xóa, sửa chữa làm thay đổi thông tin về ngày sản xuất, số lô sản xuất thuốc, nguyên liệu làm thuốc ghi trên nhãn gốc; | 10.000.000 đồng đến 20.000.000 đồng |
|
| 3a | Thay đổi, sửa chữa hạn dùng của thuốc ghi trên nhãn; | 20.000.000 đồng đến 30.000.000 đồng |
|
| 3b | Vật liệu bao bì hoặc dạng đóng gói không đáp ứng yêu cầu bảo đảm chất lượng thuốc, nguyên liệu làm thuốc; | 20.000.000 đồng đến 30.000.000 đồng | Đình chỉ hoạt động kinh doanh có liên quan đến hành vi vi phạm trong thời hạn từ 01 tháng đến 03 tháng |
| Vi phạm quy định về thuốc phải kiểm soát đặc biệt (Điều 65, Mục 3, NĐ 117/2020/NĐ-CP) | |||
| 1b | Vận chuyển, giao, nhận thuốc phải kiểm soát đặc biệt không đúng quy định của pháp luật; | 5.000.000 đồng đến 10.000.000 đồng |
|
| 1c | Hủy thuốc phải kiểm soát đặc biệt không đúng quy định của pháp luật. | 5.000.000 đồng đến 10.000.000 đồng |
|
| 1d | Không có đủ điều kiện về nhân sự, cơ sở vật chất để bảo đảm không thất thoát thuốc phải kiểm soát đặc biệt theo quy định của pháp luật; | 5.000.000 đồng đến 10.000.000 đồng | Đình chỉ hoạt động kinh doanh có liên quan đến hành vi vi phạm trong thời hạn từ 01 tháng đến 03 tháng |
| Vi phạm quy định về thông tin thuốc (Điều 67, Mục 3, NĐ 117/2020/NĐ-CP) | |||
| 5a | Thông tin, quảng cáo, tiếp thị, tư vấn, ghi nhãn, hướng dẫn sử dụng thực phẩm, mỹ phẩm và các sản phẩm khác không phải là thuốc có tác dụng để phòng bệnh, chữa bệnh, chẩn đoán, điều trị, giảm nhẹ bệnh, điều chỉnh chức năng sinh lý cơ thể người khiến người tiêu dùng hiểu nhầm các sản phẩm đó là thuốc, trừ trang thiết bị y tế; | 30.000.000 đồng đến 40.000.000 đồng | Đình chỉ hoạt động của cơ sở trong thời hạn từ 03 tháng đến 06 tháng trong trường hợp vi phạm từ 03 lần/năm trở lên; |
CHƯƠNG 5. HƯỚNG DẪN QUY TRÌNH THAO TÁC CHUẨN (SOP) ÁP DỤNG TẠI CƠ SỞ BÁN LẺ THUỐC
5.1. Nguyên tắc xây dựng quy trình thao tác chuẩn
Quy trình thao tác chuẩn (Standard Operating Procedures- SOP) áp dụng tại cơ sở bán lẻ thuốc là tài liệu hướng dẫn chi tiết bằng văn bản các bước cụ thể để thực hiện một công việc. Quy trình thao tác chuẩn được xây dựng trên cơ sở các quy định hiện hành, từ đó thực hiện công việc chính xác, nhất quán nhằm đạt được yêu cầu đã xác định trước và đảm bảo chất lượng công việc tại cơ sở bán lẻ thuốc.
SOP có các nội dung:
- Mục đích: Quy định cách thức thực hiện các thao tác chuẩn trong các hoạt động tại cơ sở bán lẻ thuốc.
- Phạm vi áp dụng: cho một hoạt động cụ thể.
- Đối tượng thực hiện: đối tượng thực hiện cụ thể
- Nội dung: các bước tiến hành cụ thể.
- Tài liệu đính kèm.
- Hình thức lưu trữ.
Một số yêu cầu cơ bản:
- Trang 1: Phần mở đầu: ghi tên cơ sở bán lẻ; tên quy trình; số trang; số và ngày ban hành; tên bộ phận; họ tên người soạn thảo/người kiểm tra/người phê chuẩn.
- Trang 2 trở đi là nội dung chính của quy trình.
- Yêu cầu viết văn mệnh lệnh cách, ngắn gọn, dễ hiểu.
- Các quy trình của cơ sở bán lẻ thuốc phải được kiểm tra và phê chuẩn bởi người quản lý chuyên môn về dược của cơ sở.
- Bản gốc của quy trình phải được lưu trữ trong tài liệu. Một số bản sao của mỗi quy trình được gửi cho bộ phận có liên quan và nếu cần thiết phải đặt một bản sao tại nơi thuận tiện cho nhân viên tham khảo. Sau khi ban hành một quy trình mới phải thu hồi quy trình cũ tương ứng để lưu trữ trong một thời gian tùy theo cơ sở quy định.
- Mỗi quy trình phải được sửa đổi, bổ sung cho cập nhật theo định kỳ. Nếu không cần thay đổi thì người phụ trách chuyên môn phải ghi không cần thay đổi lên bản gốc rồi ký tên và ghi ngày tháng. Khi có sửa đổi bổ sung phải in lại toàn bộ quy trình để ban hành.
5.2. Hướng dẫn nội dung một số quy trình thao tác chuẩn áp dụng tại cơ sở bán lẻ thuốc
Tài liệu tham chiếu (áp dụng khi xây dựng quy trình thao tác chuẩn tại cơ sở bán lẻ thuốc)
- Luật Dược 105/2016/QH13
- NĐ 54/2017/NĐ-CP ngày 08/05/2017 của CP quy định chi tiết một số điều & biện pháp thi hành luật Dược.
- NĐ 155/2018/NĐ-CP ngày 12/11/2018 của CP sửa đổi, bổ sung một số quy định liên quan đến điều kiện đầu tư kinh doanh thuộc phạm vi quản lý nhà nước của Bộ Y tế.
- TT 02/2018/TT-BYT ngày 22/01/2018 của BYT quy định về Thực hành tốt cơ sở bán lẻ thuốc.
- TT 12/2020 /TT-BYT ngày 22/6/2020 quy định sửa đổi, bổ sung một số điều của TT 02/2018/TT-BYT
- TT 06/2017/TT-BYT ngày 03/05/2017 của BYT ban hành danh mục thuốc độc và nguyên liệu độc làm thuốc.
- TT 20/2017/TT-BYT ngày 10/05/2017 của BYT quy định về thuốc và nguyên liệu làm thuốc phải kiểm soát đặc biệt.
- TT 07/2017/TT-BYT ngày 03/05/2017 của BYT quy định về danh mục thuốc không kê đơn
- TT 19/2018/TT-BYT ngày 30/8/2018, Ban hành Danh mục thuốc thiết yếu
- TT 01/2018/TT-BYT ngày 18/01/2018 của BYT quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc.
- TT 11/2018/TT-BYT quy định về chất lượng thuốc, nguyên liệu làm thuốc. TT 03/2020/TT-BYT sửa đổi Thông tư 11/2018/TT-BYT
- TT 13/2018/TT-BYT quy định về chất lượng dược liệu và thuốc y học cổ truyền.
- TT 52/2017/TT-BYT ngày 29/12/2017 của BYT quy định về đơn thuốc và việc kê đơn thuốc hóa dược, sinh phẩm trong điều trị ngoại trú.
- TT 18/2018/TT-BYT ngày 22/8/2018 quy định về sửa đổi, bổ sung một số điều của TT 52/2017/TT-BYT ngày 29/12/2017 quy định về kê đơn thuốc hóa dược, sinh phẩm trong điều trị ngoại trú
- TT 44/2017/TT-BYT ngày 22/8/2018 quy định về kê đơn thuốc cổ truyền, thuốc dược liệu và kê đơn kết hợp thuốc cổ truyền, thuốc dược liệu với thuốc hóa dược.
- TT 43/2014/TT-BYT ngày 24/11/2014 của BYT quy định về quản lý thực phẩm chức năng
- TT 06/2011/TT-BYT ngày 25/01/2011 của BYT quy định quản lý mỹ phẩm
- TT 19/2012/TT-BYT ngày 09/11/2012 của BYT quy định việc công bố hợp quy và công bố phù hợp quy định an toàn thực phẩm.
- Quyết định số 122/QĐ-BYT ngày 11/01/2021 về việc ban hành Hướng dẫn Quốc Gia về Cảnh giác dược
A. Quy trình mua thuốc và kiểm soát chất lượng thuốc
1. Mục đích yêu cầu.
Hướng dẫn mua thuốc và kiểm soát chất lượng thuốc đảm bảo chất lượng, đúng quy định của pháp luật hiện hành, đáp ứng kịp thời, đúng đủ theo nhu cầu và đáp ứng nhu cầu kinh doanh của cơ sở bán lẻ thuốc.
2. Phạm vi áp dụng
Tất cả các loại thuốc hóa dược, thuốc dược liệu, thuốc cổ truyền, sinh phẩm nhập vào cơ sở bán lẻ thuốc.
Ngoài ra, các sản phẩm không phải là thuốc: thực phẩm chức năng, mỹ phẩm, dụng cụ y tế nhập vào cơ sở bán lẻ thuốc.
3. Đối tượng thực hiện.
- Người phụ trách chuyên môn về dược của cơ sở bán lẻ thuốc.
- Nhân viên làm việc tại cơ sở bán lẻ thuốc.
4. Nội dung quy trình.
4.1. Sơ đồ tiến trình.
| Người thực hiện | Trình tự thực hiện | Mô tả |
| Người PTCM Nhân viên | Lập dự trù mua thuốc | 4.2.1 |
| Người PTCM Nhân viên | Giao dịch mua thuốc | 4.2.2 |
| Người PTCM Nhân viên | Kiểm nhập thuốc | 4.2.3 |
| Người PTCM Nhân viên | Niêm yết giá thuốc | 4.2.4 |
| Người PTCM Nhân viên | Sắp xếp, trưng bày đúng khu vực | 4.2.5 |
| Người PTCM Nhân viên | Lưu thông tin (Nhập vào máy tính hoặc ghi chép sổ sách) | 4.2.6 |
4.2. Mô tả quy trình
4.2.1. Lập dự trù mua thuốc
Cơ sở bán lẻ thuốc cần xây dựng mức tồn tối thiểu của từng mặt hàng, khi hàng xuất bán đến mức tồn tối thiểu, phần mềm máy tính sẽ hiển thị yêu cầu đặt hàng.
Kế hoạch mua thuốc bao gồm: kế hoạch định kỳ và kế hoạch đột xuất.
Khi lập kế hoạch mua thuốc phải căn cứ vào: Lượng hàng tồn tại cơ sở bán lẻ thuốc, khả năng tài chính cơ sở bán lẻ thuốc, cơ cấu bệnh tật, nhu cầu thị trường trong kỳ kinh doanh, danh mục thuốc thiết yếu, thuốc được phép lưu hành, phạm vi cơ sở bán lẻ thuốc được phép kinh doanh.
4.2.2. Giao dịch mua thuốc
Lựa chọn nhà cung ứng:
Để lựa chọn nhà cung ứng, cơ sở bán lẻ có thể xây dựng tiêu chí đánh giá, xếp loại và lựa chọn cụ thể. Ví dụ xây dựng bản đánh giá, lựa chọn nhà cung cấp (nếu cần thiết).
Mua thuốc từ các nhà cung ứng có đầy đủ tư cách pháp nhân, có Giấy chứng nhận đủ điều kiện kinh doanh dược.
Ưu tiên lựa chọn các nhà cung ứng:
+ Có uy tín trên thị trường. Chính sách giá cả, chính sách phân phối, phương thức thanh toán phù hợp.
+ Chất lượng dịch vụ: Đáp ứng được yêu cầu bảo quản hàng hóa; Có đủ các điều kiện bảo quản trong quá trình vận chuyển; Thái độ dịch vụ tốt (đáp ứng đơn hàng nhanh, dịch vụ chăm sóc khách hàng chu đáo).
Lập “Danh mục các nhà cung ứng” và hồ sơ theo dõi các nhà cung ứng: Danh mục các mặt hàng cung ứng, thông tin về phạm vi kinh doanh dược của các nhà cung ứng (Giấy chứng nhận đủ điều kiện kinh doanh dược), điện thoại, địa chỉ, người liên hệ (nên sử dụng phần mềm để quản lý)
Các thông tin về sản phẩm do nhà cung cấp giới thiệu cần được tìm hiểu:
+ Thông tin về giấy đăng ký lưu hành thuốc, hoạt chất, nồng độ, dạng bào chế, liều dùng, chỉ định, chống chỉ định, lưu ý khi sử dụng.
+ Nhóm tác dụng dược lý;
+ Tiêu chuẩn chất lượng thuốc;
+ Quy cách đóng gói; Hạn dùng; Điều kiện bảo quản
+ Cơ sở sản xuất; Cơ sở phân phối
+ Giá thuốc
+ Các chương trình bán hàng của nhà cung ứng
+ Nhà cung ứng phải cung cấp giấy đủ điều kiện kinh doanh dược.
+ Thuốc phải được phép lưu hành trên thị trường, có số đăng ký hoặc có số giấy phép nhập khẩu.
+ Có chất lượng đảm bảo: Đã qua kiểm nghiệm, có công bố tiêu chuẩn chất lượng,…
Lập đơn đặt hàng và mua hàng
Lập đơn đặt hàng: Tên sản phẩm, hàm lượng, dạng đóng gói, số lượng, đơn giá, quy cách, nhà phân phối và các ghi chú đặc biệt.
Gửi đơn hàng trực tiếp hoặc điện thoại hoặc đặt hàng qua trình dược viên của các công ty hoặc email, fax.
4.2.3. Kiểm nhập thuốc
Người phụ trách chuyên môn về dược chịu trách nhiệm kiểm tra chất lượng thuốc khi nhập hàng.
a) Kiểm tra tính hợp pháp, nguồn gốc xuất xứ, bao bì của thuốc
- Kiểm tra hóa đơn, chứng từ đầy đủ hợp pháp.
- Kiểm tra bao bì: Nguyên vẹn, sạch sẽ
- Kiểm tra sự thống nhất giữa bao bì ngoài và bao bì trực tiếp
- Kiểm tra thuốc có được phép lưu hành: Có số đăng ký hoặc có số giấy phép nhập khẩu
- Kiểm tra số lô sản xuất, hạn dùng.Yêu cầu còn hạn dùng hoặc theo quy định của Hợp đồng (nếu có)
- Kiểm tra điều kiện bảo quản ghi trên nhãn.
- Kiểm tra chủng loại, tên thuốc, nồng độ/hàm lượng, số lượng theo đơn đặt hàng phải chính xác trên hóa đơn và trên thực tế. Nếu sai lệch, đề nghị chỉnh sửa lại hóa đơn (tạm nhận hàng, chưa nhập) hoặc không nhận đơn hàng này.
b) Kiểm tra chất lượng thuốc bằng cảm quan
Một số lưu ý khi kiểm tra chất lượng thuốc bằng cảm quan như sau:
- Viên nén: Kiểm tra màu sắc, kiểm tra độ ẩm của viên trong lọ hay vỉ bằng cách lắc nhẹ và nghe tiếng kêu, kiểm tra độ toàn vẹn của vỉ bằng mắt thường.
- Viên nang: Kiểm tra tính toàn vẹn của viên, của vỉ (vỉ không bị hở, bị rách, không có bột thuốc trong khoảng trống chứa viên).
- Viên bao: Bề mặt nhẵn, không nứt, không bong mặt, bảo quản trong lọ hoặc vỉ kín, lắc không dính. Đối với viên bao đường không được chảy nước.
- Đối với thuốc cốm : Kiểm tra độ ẩm bằng cách lắc nhẹ
- Đối với dạng thuốc đạn, thuốc trứng: Không chảy nước, bao bì trực tiếp nguyên vẹn.
- Đối với thuốc dạng xi-rô : Thuốc phải trong, không biến chất trong quá trình bảo quản, không lắng cặn lên men, không có đường kết tinh lại.
- Đối với thuốc đóng ống: Màu sắc đồng đều, các thông tin in trên ống phải rõ nét, đầy đủ.
Nếu hàng không đạt yêu cầu: Phải để ở “khu vực hàng chờ xử lý”. Liên hệ với nhà cung ứng để trả hoặc đổi lại.
Nếu thuốc đạt chất lượng, hóa đơn chứng từ phù hợp thì tiến hành nhận hàng, nhập thông tin mua hàng vào máy tính (phần mềm quản lý dữ liệu dược quốc gia) hoặc ghi sổ nhập thuốc.
4.2.4. Niêm yết giá thuốc
Niêm yết giá bán lẻ từng loại thuốc, đầy đủ từng mặt hàng, theo đơn vị đóng gói nhỏ nhất trực tiếp trên bao bì thuốc.
Việc niêm yết giá bán lẻ thuốc có thể được thực hiện bằng hình thức in, ghi hoặc dán giá bán lẻ trên bao bì của thuốc hoặc bao bì ngoài của thuốc; thuận tiện cho việc quan sát, nhận biết của khách hàng, cơ quan nhà nước có thẩm quyền, không che khuất nội dung bắt buộc của nhãn thuốc
Đồng tiền niêm yết giá là đồng Việt Nam (Đã bao gồm các loại thuế, phí và lệ phí (nếu có) của thuốc. Giá niêm yết phải rõ ràng, đầy đủ số tiền.
Đối với cơ sở bán lẻ thuốc trong khuôn viên cơ sở khám bệnh, chữa bệnh giá niêm yết theo quy định về thặng số bán lẻ của cơ sở bán lẻ thuốc trong khuôn viên cơ sở khám bệnh, chữa bệnh tại điều 136 nghị định 54/2017/NĐ-CP.
4.2.5. Sắp xếp trưng bày đúng khu vực:
Theo Quy trình bảo quản và theo dõi chất lượng thuốc
4.2.6. Ghi chép sổ sách hoặc nhập vào máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia)
- Ghi “Sổ nhập thuốc”: ghi đủ các thông tin trong sổ
- Nhập vào phần mền quản lý dữ liệu dược quốc gia đầy đủ thông tin.
4.3. Biểu mẫu áp dụng
Danh mục theo dõi nhà cung ứng
Sổ nhập thuốc
4.4. Hình thức lưu trữ:
SOP này được lưu trong tập hồ sơ “SOP” của cơ sở bán lẻ thuốc..
Lưu trữ hồ sơ sổ sách/thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) ít nhất 01 năm kể từ khi thuốc hết hạn dùng. Riêng đối với thuốc phải kiểm soát đặc biệt lưu trữ hồ sơ, sổ sách ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
TÊN CƠ SỞ
DANH MỤC CÁC NHÀ CUNG ỨNG
| Stt | Tên nhà cung ứng | Địa chỉ | Giấy chứng nhận đủ điều kiện kinh doanh dược | Danh mục thuốc cung ứng | Người liên hệ/số điện thoại, email | Nội dung đánh giá nhà cung cấp |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
TÊN CƠ SỞ
SỔ NHẬP THUỐC
| Ngày /tháng/năm | Tên thuốc, nồng độ/hàm lượng | Số đăng ký/GPNK | Số lô, hạn dùng | Nhà sản xuất/ Nhập khẩu | Cơ sở cung cấp | Số hóa đơn/ chứng từ | Điều kiện bảo quản | Quy cách đóng gói | Số lượng | Đơn vị tính | Đơn giá |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Người phụ trách chuyên môn về dược của cơ sở
B. Quy trình bán thuốc thông tin tư vấn hướng dẫn sử dụng thuốc phải kê đơn
1. Mục đích yêu cầu
Đảm bảo bán thuốc và hướng dẫn sử dụng thuốc phải kê đơn hợp lý, an toàn và đúng quy chế chuyên môn.
2. Phạm vi áp dụng
Các thuốc phải kê đơn
3. Đối tượng thực hiện
- Người phụ trách chuyên môn của cơ sở bán lẻ thuốc.
- Nhân viên làm việc tại cơ sở bán lẻ thuốc. Riêng đối với quầy thuốc, nhân viên có bằng chuyên môn dược từ trung cấp ngành dược trở lên.
4. Nội dung quy trình:
4.1. Sơ đồ tiến trình:
| Đối tượng | Sơ đồ | Mô tả |
| Người PTCM Nhân viên | Tiếp nhận và kiểm tra đơn thuốc | 4.2.1 |
| Người PTCM Nhân viên | Khai thác thông tin và tư vấn | 4.2.2 |
| Người PTCM Nhân viên | Nhập dữ liệu vào máy tính hoặc lưu thông tin về đơn thuốc | 4.2.3 |
| Người PTCM Nhân viên | Lấy thuốc | 4.2.4 |
| Người PTCM Nhân viên | Giao thuốc và hướng dẫn sử dụng | 4.2.5 |
| Người PTCM Nhân viên | Lưu các thông tin | 4.2.6 |
4.2. Mô tả quy trình
4.2.1. Tiếp nhận và kiểm tra đơn thuốc
a) Kiểm tra tính hợp lệ của đơn thuốc:
+ Đơn thuốc hoặc Sổ khám bệnh đúng theo mẫu quy định, ghi đủ, rõ ràng các mục in trong đơn hoặc trong Sổ khám bệnh.
+ Có đủ tên, chữ ký của người kê đơn, địa chỉ, dấu của cơ sở khám, chữa bệnh (ví dụ phòng khám/ bệnh viện)
+ Thời hạn: Đơn thuốc có giá trị mua, lĩnh thuốc trong thời hạn tối đa 05 ngày, kể từ ngày kê đơn thuốc (Theo qui định tại Khoản 1 Điều 11 Thông tư số 52/2017/TT-BYT)
+ Kiểm tra tên, tuổi, địa chỉ bệnh nhân và chẩn đoán bệnh.
+ Kiểm tra ghi tên thuốc theo quy định:
Thuốc có một hoạt chất ghi theo tên chung quốc tế hoặc theo tên chung quốc tế + (tên thương mại)
Thuốc có nhiều hoạt chất hoặc sinh phẩm y tế thì ghi theo tên thương mại
Ghi tên thuốc, nồng độ/hàm lượng, số lượng/thể tích, liều dùng, đường dùng, thời điểm dùng của mỗi loại thuốc. Nếu đơn thuốc có thuốc độc phải ghi thuốc độc trước khi ghi các thuốc khác.
+ Chỉ thực hiện bước tiếp theo khi đơn thuốc hợp lệ.
- Trường hợp phát hiện đơn thuốc không rõ ràng về tên thuốc, nồng độ, hàm lượng, số lượng, hoặc có sai phạm về pháp lý, chuyên môn hoặc ảnh hưởng đến sức khỏe người bệnh, Người bán lẻ phải thông báo lại cho người kê đơn biết.
- Người bán lẻ giải thích rõ cho người mua và có quyền từ chối bán thuốc theo đơn trong các trường hợp đơn thuốc không hợp lệ, đơn thuốc có sai sót hoặc nghi vấn, đơn thuốc kê không nhằm mục đích chữa bệnh.
b) Kiểm tra tính an toàn, hiệu quả và hợp lý về sử dụng thuốc của đơn.
- Kiểm tra: liều dùng, tương tác thuốc, kê trùng hoạt chất... Trường hợp phát hiện đơn thuốc không rõ ràng về tên thuốc, nồng độ, hàm lượng, số lượng, hoặc có sai phạm về pháp lý, chuyên môn hoặc ảnh hưởng đến sức khoẻ người bệnh, phải thông báo lại cho người kê đơn biết.
- Chú ý các đối tượng như trẻ em, người già, phụ nữ có thai, người suy gan, thận.
4.2.2. Khai thác thông tin và tư vấn
Hỏi thêm để nắm rõ tình trạng bệnh lý, hỏi tiền sử dị ứng, các bệnh mắc kèm và các biểu hiện tác dụng phụ của những thuốc bệnh nhân đã dùng.
Hỏi người bệnh có đang dùng loại thuốc, thực phẩm chức năng nào không để tránh tương tác thuốc.
4.2.3. Nhập dữ liệu vào máy tính hoặc lưu thông tin về đơn thuốc
Người bán thuốc nhập dữ liệu vào máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) hoặc ghi sổ sách để lưu thông tin về đơn thuốc
Người bán lẻ phải bán theo đúng đơn thuốc.
Trường hợp không có đúng tên thương mại của thuốc được kê trong đơn, phải thông báo với người mua Người bán lẻ là dược sỹ đại học giới thiệu các loại thuốc khác có cùng hoạt chất, đường dùng, liều lượng kèm theo giá của từng loại để khách hàng tham khảo, và tự chọn loại thuốc phù hợp với khả năng kinh tế của người mua.
Chỉ người phụ trách chuyên môn về dược của nhà thuốc được thay thế thuốc đã kê trong đơn bằng một thuốc khác có cùng hoạt chất, cách dùng, liều lượng khi có sự đồng ý của người mua và phải chịu trách nhiệm về việc thay đổi thuốc.
- Không tiến hành thông tin quảng cáo thuốc tại nơi bán trái với quy định,
- In hoặc viết hóa đơn bán hàng
- Thu tiền theo hóa đơn (Thuốc được niêm yết giá đúng qui định và không bán cao hơn giá niêm yết)
- Trường hợp khách hàng không mua thuốc, hủy hóa đơn bán hàng.
4.2.4. Lấy thuốc
- Lấy thuốc theo nguyên tắc: Hạn dùng ngắn bán trước, hạn dài bán sau. Hàng nhập trước bán trước, nhập sau bán sau. Kiểm tra hạn dùng, số lượng thuốc, kiểm soát chất lượng cảm quan trước khi giao cho khách.Đối với các thuốc không còn bao bì ngoài của thuốc cần đóng vào các bao bì phù hợp, dễ phân biệt.
+ Thuốc dùng ngoài dùng bao bì màu vàng có dòng chữ “Thuốc dùng ngoài”
+ Thuốc phải kiểm soát đặc biệt dùng bao bì màu xanh có dòng chữ “Thuốc phải kiểm soát đặc biệt”
+ Các thuốc còn lại dùng bao bì màu trắng
- Đối với các thuốc không còn bao bì tiếp xúc trực tiếp với thuốc cần ra lẻ tại khu vực ra lẻ và cho vào các bao bì kín khí.
Các bao bì đựng thuốc phải ghi đầy đủ các thông tin trên bao bì: Tên thuốc, nồng độ, hàm lượng, liều dùng, cách dùng, hạn dùng của từng thuốc. - Lưu ý, thuốc bán lẻ không đựng trong bao bì mang tên thuốc khác hoặc chứa nội dung quảng cáo của một thuốc khác.
- Nếu khách không mua hết cả vỉ thuốc thì trước khi cắt vỉ phải cho khách xem hạn dùng của thuốc. Để lại phần vỉ có hạn dùng tại nhà thuốc để theo dõi, kiểm soát hạn dùng. Phần không có hạn dùng giao cho khách nhưng phải ghi rõ hạn dùng của thuốc trên bao bì ra lẻ. Ghi vào đơn thuốc: tên thuốc, số lượng thuốc đã thay thế (nếu có)
4.2.5. Giao thuốc và hướng dẫn sử dụng:
- Giao từng khoản thuốc cho khách hàng
- Hướng dẫn, giải thích cho khách hàng về tác dụng, chỉ định, chống chỉ định, tác dụng không mong muốn, liều lượng và cách dùng thuốc, tương tác thuốc với thức ăn đồ uống (nếu có), bảo quản thuốc
- Các chú ý về bảo quản thuốc và thời hạn từ lúc mở lọ thuốc đối với thuốc dạng lỏng
- Lưu ý khách hàng gọi điện hoặc liên lạc lại với cơ sở nếu có vấn đề gì chưa hiểu rõ hoặc có tác dụng không mong muốn của thuốc
- Nhắc nhở người mua thực hiện đúng đơn thuốc
- Giao hóa đơn và đơn thuốc cho khách.
4.2.6. Lưu các thông tin
- Lưu thông tin về đơn thuốc trong “Sổ theo dõi bệnh nhân” hoặc trong phần mềm kết nối cơ sở dữ liệu dược quốc gia. Ngoài hình thức trên, cơ sở có thể thực hiện lưu đơn bản chính hoặc bản sao hoặc bản chụp đơn thuốc.
- Đối với thuốc dạng phối hợp có chứa hoạt chất gây nghiện hoặc chứa hoạt chất hướng tâm thần/tiền chất dùng làm thuốc sau khi bán phải ghi chép thông tin vào “Sổ theo dõi thông tin chi tiết khách hàng mua thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất” hoặc lưu thông tin cần thiết trong phần mềm kết nối cơ sở dữ liệu dược quốc gia.
4.2.7. Lưu ý
- Trang phục áo blu trắng, sạch sẽ, gọn gàng, có đeo biển ghi rõ tên, chức danh;
- Thực hiện đúng các quy chế dược, tự nguyện tuân thủ đạo đức hành nghề dược;
- Phải luôn có thái độ lịch sự, hòa nhã và tôn trọng khách hàng.
- Những thông tin của khách hàng phải được giữ bí mật.
4.3. Biểu mẫu áp dụng
Sổ theo dõi bệnh nhân
Sổ theo dõi thông tin chi tiết khách hàng mua thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất
4.4. Hình thức lưu trữ
SOP này được lưu trong tập hồ sơ “SOP” của cơ sở bán lẻ thuốc.
Lưu trữ hồ sơ sổ sách/thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) ít nhất 01 năm kể từ khi thuốc hết hạn dùng. Riêng đối với thuốc phải kiểm soát đặc biệt lưu trữ hồ sơ, sổ sách ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
Tên cơ sở
SỔ THEO DÕI BỆNH NHÂN
| STT | Ngày tháng năm | Họ tên người bệnh, tuổi | Địa chỉ của người bệnh | Tên và địa chỉ cơ sở khám bệnh | Họ và tên của người kê đơn thuốc | Chẩn đoán của người kê đơn | Tên thuốc, nồng độ/hàm lượng | Hoạt chất | Đường dùng, liều dùng | Số lượng bán | Ghi chú (Số điện thoại của khách hàng, nếu có) |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
……., ngày tháng năm ….
Người phụ trách chuyên môn về dược của cơ sở
(Ký, ghi rõ họ tên, chức danh, đóng dấu (nếu có)
Tên cơ sở:
Số:
SỔ THEO DI THÔNG TIN CHI TIẾT H CH HÀNG UA THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT GÂY NGHIỆN/ THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT HƯỚNG THẦN/THUỐC DẠNG PHỐI HỢP CHỨA TIỀN CHẤT
| TT | Ngày tháng, năm | Tên thuốc quy cách đóng gói | Hoạt chất nồng độ hàm lượng | Đơn vị tính | Số lượng bán | Tên khách hàng | Địa chỉ của khách hàng | Ghi chú |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
……., ngày tháng năm ….
Người phụ trách chuyên môn về dược của cơ sở
(Ký, ghi rõ họ tên, chức danh, đóng dấu (nếu có)
C. Quy trình bán thuốc thông tin tư vấn hướng dẫn sử dụng thuốc không kê đơn
1. Mục đích yêu cầu
Đảm bảo bán thuốc, giới thiệu và tư vấn sử dụng thuốc bán không kê đơn hợp lý, an toàn và đúng quy chế chuyên môn.
2. Phạm vi áp dụng
Các thuốc không kê đơn
3. Đối tượng thực hiện
Người phụ trách chuyên môn về dược của cơ sở bán lẻ thuốc.
Nhân viên làm việc tại cơ sở bán lẻ thuốc.
4. Nội dung quy trình
4.1. Sơ đồ tiến trình
| Đối tượng | Sơ đồ | Mô tả |
| Người PTCM Nhân viên | Tiếp đón, chào hỏi Khai thác thông tin và trao đổi với khách hàng | 4.2.1 |
| Người PTCM Nhân viên | Tư vấn cho người mua | 4.2.2 |
| Người PTCM Nhân viên | Lấy thuốc | 4.2.3 |
| Người PTCM Nhân viên | Nhập dữ liệu vào máy tính | 4.2.4 |
| Người PTCM Nhân viên | Giao thuốc và hướng dẫn sử dụng | 4.2.5 |
| Người PTCM Nhân viên | Lưu thông tin | 4.2.6 |
4.2. Mô tả quy trình
4.2.1. Tiếp đón chào hỏi và khai thác thông tin trao đổi với khách hàng:
a. Trường hợp khách hàng hỏi mua một loại thuốc cụ thể:
- Nếu thuốc cụ thể khách hàng hỏi mua là thuốc kê đơn thì cần hỏi người mua thuốc có đơn thuốc không? Nếu khách hàng có đơn thuốc, thực hiện theo Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc kê đơn. Không bán thuốc kê đơn khi không có đơn thuốc.
- Nếu thuốc cụ thể khách hàng hỏi mua là thuốc không kê đơn, cần khai thác và trao đổi các thông tin để xác định việc dùng thuốc của người bệnh phù hợp hay không phù hợp.:
+ Thuốc được mua dùng để chữa bệnh/triệu chứng gì?Tình trạng, biểu hiện triệu chứng bệnh của người bệnh? Lưu ý người bán lẻ thuốc cần khai thác thông tin để phân biệt tình trạng bệnh thông thường hoặc mức độ nghiêm trọng cần đi khám để có chẩn đoán của thầy thuốc.
+ Đối tượng dùng thuốc (Giới, tuổi, tình trạng sức khỏe, tiền sử bệnh và bệnh hiện mắc; người bệnh có đang dùng thuốc hoặc sản phẩm nào khác? Hiệu quả? Tác dụng không mong muốn? Tiền sử dị ứng thuốc/thực phẩm)
+ Đã dùng thuốc này lần nào chưa? Hiệu quả?
b. Trường hợp khách hàng hỏi và tư vấn điều trị một số triệu chứng hay bệnh thông thường:
- Cần khai thác các thông tin về người bệnh để phân biệt tình trạng bệnh thông thường hoặc cần đi khám để có chẩn đoán của thầy thuốc mới có thể dùng thuốc
+ Đối tượng dùng thuốc (tuổi, giới, đối tượng có thai? Cho con bú?);
+ Triệu chứng bệnh là gì?
+ Thời gian xuất hiện bệnh?
+ Người bệnh đã dùng những thuốc/biện pháp gì để điều trị bệnh hay triệu chứng đang mắc phải?
+ Người bệnh có đang dùng thuốc hoặc sản phẩm thực phẩm chức năng?
+ Người bệnh có tiền sử bệnh? có đang mắc bệnh gì ?
+ Người bệnh có tiền sử dị ứng thuốc ?
+ Chế độ sinh hoạt?
4.2.2. Tư vấn cho người mua
- Nếu việc sử dụng thuốc của người bệnh chưa đúng hoặc chưa phù hợp: Giải thích, tư vấn và hướng dẫn khách hàng chuyển sang loại thuốc khác đúng và phù hợp. Cung cấp các thông tin cụ thể về thuốc không kê đơn phù hợp với khách hàng để khách hàng lựa chọn.
- Đối với người bệnh đòi hỏi phải có chẩn đoán của thầy thuốc mới có thể dùng thuốc, người bán lẻ cần tư vấn để bệnh nhân tới khám thầy thuốc chuyên khoa thích hợp hoặc bác sĩ điều trị;
- Đối với những người mua thuốc chưa cần thiết phải dùng thuốc, nhân viên bán thuốc cần giải thích rõ cho họ hiểu và tự chăm sóc, tự theo dõi triệu chứng bệnh;
- Trao đổi, đưa ra lời khuyên về chế độ sinh hoạt, dinh dưỡng phù hợp với từng đối tượng, từng triệu chứng bệnh/bệnh cụ thể.
4.2.3. Lấy thuốc
- Lấy thuốc theo nguyên tắc: Hạn dùng ngắn bán trước, hạn dài bán sau. Hàng nhập trước bán trước, nhập sau bán sau. Kiểm tra hạn dùng, số lượng thuốc, kiểm soát chất lượng cảm quan trước khi giao cho khách.
- Đối với các thuốc không còn bao bì ngoài của thuốc cần đóng vào các bao bì phù hợp, dễ phân biệt.
+ Thuốc dùng ngoài dùng bao bì màu vàng có dòng chữ “Thuốc dùng ngoài”
+ Thuốc phải kiểm soát đặc biệt dùng bao bì màu xanh có dòng chữ “Thuốc phải kiểm soát đặc biệt”
+ Các thuốc còn lại dùng bao bì màu trắng
+ Lưu ý, thuốc bán lẻ không đựng trong bao bì mang tên thuốc khác hoặc chứa nội dung quảng cáo của một thuốc khác.
- Đối với các thuốc không còn bao bì tiếp xúc trực tiếp với thuốc phải thực hiện ra lẻ tại khu vực ra lẻ và phải cho vào các bao bì kín khí.
- Ghi đầy đủ các thông tin trên bao bì đựng thuốc: Tên thuốc, dạng bào chế, nồng độ, hàm lượng, liều dùng, cách dùng, hạn dùng của từng thuốc.
Nếu khách không mua hết cả vỉ thuốc thì trước khi cắt vỉ phải cho khách xem hạn dùng của thuốc. Để lại phần vỉ có hạn dùng tại nhà thuốc để theo dõi, kiểm soát hạn dùng. Phần không có hạn dùng giao cho khách nhưng phải ghi rõ hạn dùng của thuốc trên bao bì ra lẻ.
4.2.4. Nhập dữ liệu vào máy tính
- Nhân viên nhập dữ liệu về thuốc đã bán vào máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia)
- In hoặc viết hóa đơn bán hàng
- Thu tiền theo hóa đơn
- Trường hợp khách hàng muốn thay đổi số lượng, điều chỉnh số lượng trong máy tính và in/viết lại hóa đơn.
- Trường hợp khách hàng không mua thuốc, hủy hóa đơn bán hàng.
4.2.5. Giao thuốc và hướng dẫn sử dụng cho khách hàng
- Giao từng khoản cho khách hàng
- Hướng dẫn sử dụng thuốc bằng lời nói và ghi đầy đủ thông tin trên bao bì đựng thuốc (tên thuốc, dạng bào chế, nồng độ, hàm lượng, liều dùng, cách dùng, hạn dùng của từng thuốc).
- Hướng dẫn, giải thích cho khách hàng về:
+ Tác dụng, chỉ định, chống chỉ định, tương tác thuốc, tác dụng không mong muốn,
+ Liều lượng và cách dùng thuốc: uống vào thời điểm nào, các tương tác của thuốc với thức ăn đồ uống,
+ Các chú ý về bảo quản thuốc và thời hạn từ lúc mở lọ thuốc đối với thuốc lỏng
+ Lưu ý khách hàng gọi điện hoặc liên lạc lại với cơ sở nếu có vấn đề gì chưa hiểu rõ hoặc xuất hiện các bất thường, tác dụng phụ, dị ứng thuốc
- Giao hóa đơn và đưa thuốc cho khách.
- Cám ơn khách hàng.
4.2.6. Lưu các thông tin và số liệu.
- Lưu thông tin về thuốc đã bán.
- Đối với thuốc dạng phối hợp có chứa hoạt chất gây nghiện hoặc chứa hoạt chất hướng tâm thần/tiền chất dùng làm thuốc sau khi bán phải ghi chép thông tin vào Sổ theo dõi thông tin chi tiết khách hàng mua thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất hoặc lưu thông tin cần thiết trong phần mềm kết nối cơ sở dữ liệu dược quốc gia.
4.2.7. Lưu ý:
Trang phục áo blu trắng, sạch sẽ, gọn gàng, có đeo biển ghi rõ tên, chức danh;
- Thực hiện đúng các quy chế dược, tự nguyện tuân thủ đạo đức hành nghề dược;
- Phải luôn có thái độ lịch sự, hòa nhã và tôn trọng khách hàng.
- Những thông tin của khách hàng phải được giữ bí mật.
4.3. Biểu mẫu áp dụng
Sổ theo dõi thông tin chi tiết khách hàng mua thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất
4.4. Hình thức lưu trữ
- SOP này được lưu trong tập hồ sơ “SOP” của cơ sở bán lẻ thuốc
- Lưu trữ hồ sơ sổ sách/thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) ít nhất 01 năm kể từ khi thuốc hết hạn dùng. Riêng đối với thuốc phải kiểm soát đặc biệt lưu trữ hồ sơ, sổ sách ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
Tên cơ sở:
Số:
SỔ THEO DÕI THÔNG TIN CHI TIẾT KHÁCH HÀNG MUA THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT GÂY NGHIỆN/ THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT HƯỚNG THẦN/THUỐC DẠNG PHỐI HỢP CHỨA TIỀN CHẤT
| TT | Ngày tháng, năm | Tên thuốc quy cách đóng gói | Hoạt chất nồng độ hàm lượng | Đơn vị tính | Số lượng bán | Tên khách hàng | Địa chỉ của khách hàng | Ghi chú |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
……., ngày tháng năm ….
Người phụ trách chuyên môn về dược của cơ sở
(Ký, ghi rõ họ tên, chức danh, đóng dấu (nếu có)
D. Quy trình bảo quản và theo dõi chất lượng thuốc
1. Mục đích yêu cầu
Đảm bảo bảo quản thuốc đúng quy định, dễ dàng cho việc kiểm tra, theo dõi chất lượng.
2. Phạm vi áp dụng
Các mặt hàng thuốc bán tại cơ sở bán lẻ thuốc
3. Đối tượng thực hiện
- Người phụ trách chuyên môn về dược của cơ sở bán lẻ thuốc
- Nhân viên bán thuốc tại cơ sở bán lẻ thuốc.
4. Nội dung quy trình
4.1. Sơ đồ tiến trình
| Đối tượng | Sơ đồ | Mô tả |
| Người PTCM về dược Nhân viên | Nguyên tắc bảo quản thuốc | 4.2.1 |
| Người PTCM về dược Nhân viên | Sắp xếp thuốc | 4.2.2 |
| Người PTCM về dược | Nguyên tắc theo dõi chất lượng thuốc | 4.2.3 |
| Người PTCM về dược Nhân viên | Kiểm tra chất lượng thuốc | 4.2.4 |
| Người PTCM về dược Nhân viên | Lưu thông tin | 4.2.5 |
4.2. Mô tả quy trình
4.2.1. Nguyên tắc bảo quản
Người PTCM về dược, nhân viên nhà thuốc phải đảm bảo điều kiện của cơ sở bán lẻ thuốc đáp ứng theo yêu cầu của nhà sản xuất được ghi trên bao bì của sản phẩm và đúng quy chế chuyên môn
4.2.2. Sắp xếp thuốc
Nguyên tắc
Sắp xếp theo nguyên tắc FIFO (First In First Out: thuốc nhập trước xuất trước) và FEFO (First Expire First Out: hết hạn dùng trước xuất trước)
Gọn gàng, ngay ngắn, có thẩm mỹ, không xếp lẫn lộn giữa các mặt hàng...
Nhãn hàng (chữ, số, hình ảnh...) trên các bao bì: Quay ra ngoài, thuận chiều nhìn của khách hàng.
Các mặt hàng dễ vỡ như chai, lọ, ống tiêm truyền... không xếp chồng lên nhau
Hàng hóa nhập về nhà thuốc phân loại và sắp xếp theo các thứ tự sau:
+ Phân loại theo từng ngành hàng
- Có khu vực riêng cho các sản phẩm không phải là thuốc: Thực phẩm chức năng, Mỹ phẩm, Dụng cụ y tế.
Lưu ý phân biệt thuốc, mỹ phẩm, thực phẩm chức năng:
+ Thuốc có số đăng ký do Cục quản lý dược Việt Nam cấp thường có ký hiệu: VN..., VD., VS…, QLSP…, GPNK…, …/QLD-KD, QLĐB….
+ Thực phẩm chức năng có số đăng ký do Cục An toàn thực phẩm cấp thường có ký hiệu: (số thứ tự)/ (năm cấp)/ATTP-TNCB và (số thứ tự)/ (năm cấp)/ATTP-XNCB. Ngoài ra thường có thêm dòng chữ “Thực phẩm bổ sung” ; “Thực phẩm bảo vệ sức khỏe”, “Thực phẩm dinh dưỡng y học” “Chú ý: Sản phẩm này không phải là thuốc và không có tác dụng thay thế thuốc chữa bệnh”
Thực phẩm chức năng có số đăng ký do Chi cục An toàn vệ sinh thực phẩm tỉnh, thành phố cấp có ký hiệu: (số thứ tự)/ (năm cấp)/YT + tên viết tắt tỉnh, thành phố -TNCB và (số thứ tự)/ (năm cấp)/YT + tên viết tắt tỉnh, thành phố -XNCB.
+ Mỹ phẩm có số đăng ký (số tiếp nhận phiếu công bố sản phẩm mỹ phẩm) có ký hiệu: (số thứ tự)/ (năm cấp)/CBMP - ký hiệu viết tắt tên tỉnh, thành phố, Ban Quản lý Khu kinh tế hoặc Cục Quản lý dược (QLD)
+ Phân loại thuốc theo mức độ quản lý (thuốc phải kiểm soát đặc biệt, thuốc hạn chế bán lẻ)
- Thuốc gây nghiện, hướng tâm thần/tiền chất phải bảo quản trong tủ riêng hoặc ngăn riêng có khóa chắc chắn
- Thuốc dạng phối hợp có chứa dược chất gây nghiện hoặc chứa dược chất hướng thần/tiền chất dùng làm thuốc để ở khu vực riêng
- Thuốc độc, thuốc thuộc danh mục thuốc cấm sử dụng trong một số ngành lĩnh vực, thuốc hạn chế bán lẻ để ở khu vực riêng
+ Phân loại thuốc theo điều kiên bảo quản
Các điều kiện bảo quản thuốc, nguyên liệu làm thuốc phải tuân thủ theo đúng thông tin trên nhãn đã được phê duyệt hoặc công bố theo quy định.
Trừ khi có các yêu cầu đặc biệt khác (ví dụ: duy trì liên tục việc bảo quản lạnh), chỉ chấp nhận việc bảo quản nằm ngoài quy định trên trong các quãng thời gian ngắn, ví dụ khi vận chuyển cục bộ trong kho.
a) Bảo quản điều kiện thường:
Bảo quản trong môi trường khô (độ ẩm 75%), ở nhiệt độ từ 15-30°C. Trong điều kiện thời tiết khắc nghiệt, tại một số thời điểm trong ngày, nhiệt độ có thể trên 30°C nhưng không vượt quá 32°C và độ ẩm không vượt quá 80%. Phải thoáng khí, tránh ảnh hưởng từ các mùi, các yếu tố gây tạp nhiễm và ánh sáng mạnh.
Nếu trên nhãn không ghi rõ điều kiện bảo quản thì bảo quản ở điều kiện thường.
b) Điều kiện bảo quản đặc biệt: Bao gồm các trường hợp có yêu cầu bảo quản khác với bảo quản ở điều kiện thường.
c) Hướng dẫn về điều kiện bảo quản cụ thể:
Thông tin trên nhãn Yêu cầu về điều kiện bảo quản
“Không bảo quản quá 30 °C” : từ +2 °C đến +30 °C
“Không bảo quản quá 25 °C”: từ +2 °C đến +25 °C
“Không bảo quản quá 15 °C”: từ +2 °C đến +15 °C
“Không bảo quản quá 8 °C”: từ +2 °C đến +8 °C
“Không bảo quản dưới 8 °C”: từ +8 °C đến +25 °C
“Bảo quản lạnh”: từ +2 °C đến +8 °C
“Bảo quản mát”: từ +8 °C đến +15 °C
“Khô”, “Tránh ẩm”: không quá 75% độ ẩm tương đối trong điều kiện bảo quản thường; hoặc với điều kiện được chứa trong bao bì chống thấm đến tận tay người bệnh.
“Tránh ánh sáng”: Bảo quản trong bao bì tránh ánh sáng đến tận tay người bệnh.
+ Phân loại thuốc theo tác dụng dược lý và thuốc kê đơn/thuốc không kê đơn
Tra trong danh mục thuốc không kê đơn. Các thuốc có thành phần hoạt chất, dạng bào chế, nồng độ hàm lượng nằm trong “Danh mục thuốc không kê đơn” là thuốc không kê đơn. Còn lại là thuốc kê đơn.
Thuốc sắp xếp theo nhóm tác dụng dược lý của thuốc. Các nhóm thuốc kê đơn có khu vực riêng, các nhóm thuốc không kê đơn có khu vực riêng. Đối với các nhóm thuốc vừa có thuốc kê đơn và không kê đơn như: thuốc dùng ngoài, thuốc tra mắt, thuốc nhỏ mũi…thì nên bố trí các nhóm này ở khu vực riêng và sắp riêng thuốc kê đơn và không kê đơn ở trong cùng một ngăn tủ.
4.2.3. Nguyên tắc theo dõi chất lượng thuốc
- Thuốc trước khi nhập về cơ sở bán lẻ thuốc (Gồm hàng do cơ sở mua và hàng trả về): phải được kiểm soát 100%, tránh nhập hàng giả, hàng kém chất lượng, hàng không rõ nguồn gốc, xuất xứ.
- Thuốc lưu tại cơ sở bán lẻ thuốc: Định kỳ kiểm soát các thuốc tối thiểu 1 lần/1 quý. Tránh để có hàng bị biến đổi chất lượng, hết hạn sử dụng. Kiểm soát đột xuất đối với các loại thuốc: Khi phát hiện dấu hiệu bất thường về chất lượng thuốc, khi có khiếu nại của bệnh nhân về chất lượng thuốc, kiểm soát đối với thuốc có hạn dùng ngắn
4.2.4. Kiểm tra chất lượng thuốc
- Kiểm tra tính hợp pháp, nguồn gốc, xuất xứ của thuốc:
+ Hóa đơn, chứng từ đầy đủ, hợp pháp theo đúng quy chế, quy định hiện hành.
- Kiểm tra cảm quan chất lượng thuốc:
+ Kiểm tra bao bì: phải còn nguyên vẹn, không móp méo, rách, bẩn.
+ Kiểm tra số lô, hạn dùng, ngày sản xuất.
+ Kiểm tra sự thống nhất giữa bao bì ngoài và bao bì trung gian, bao bì trực tiếp.
+ Kiểm tra chất lượng cảm quan và ghi sổ theo dõi.
+ So sánh với các mô tả về cảm quan của nhà sản xuất (nếu có)
+ Nhãn: đúng quy chế nhãn, đủ thông tin. Hình ảnh, chữ số không bị mờ, nhòe, tránh hàng giả, hàng nhái
4.2.5. Lưu thông tin
- Ghi sổ “Sổ kiểm soát chất lượng thuốc”
+ Nếu Đạt yêu cầu các tiêu chí nêu trên, ghi vào Sổ kiểm soát chất lượng thuốc định kỳ: Nhận xét chất lượng: ĐẠT; Phân loại chất lượng: TỐT
+ Nếu thuốc không đạt yêu cầu một trong các tiêu chí nêu trên: ghi vào Sổ kiểm soát chất lượng thuốc định kỳ: Nhận xét chất lượng: KHÔNG ĐẠT; Phân loại chất lượng: ghi rõ tiêu chí không đạt. (Ví dụ: Thuốc hết hạn dùng: chờ hủy), đồng thời xử lý như sau:
Phải để riêng ở khu biệt trữ, gắn nhãn hàng chờ xử lý.
Báo cáo ngay với người phụ trách chuyên môn về dược của cơ sở
Kiểm tra điều kiện bảo quản của từng loại thuốc: Kiểm tra các yêu cầu về điều kiện bảo quản của nhà sản xuất ghi trên nhãn.
- Nhập vào dữ liệu máy tính những thông tin cần thiết.
Lưu ý: Ghi rõ phần mô tả cảm quan vào cột Nhận xét chất lượng và đánh giá Đạt/Không đạt vào cột phân loại chất lượng. Cột ghi chú: ghi lại những thông tin lưu ý về thuốc, bao gồm cả điều kiện bảo quản đặc biệt, hoặc thuốc có hạn sử dụng còn ngắn.
4.3. Biểu mẫu áp dụng
Sổ kiểm soát chất lượng thuốc định kỳ.
4.4. Hình thức lưu trữ
- SOP này được lưu trong tập hồ sơ “SOP” của cơ sở bán lẻ thuốc
- Lưu trữ hồ sơ sổ sách/thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) ít nhất 01 năm kể từ khi thuốc hết hạn dùng. Riêng đối với thuốc phải kiểm soát đặc biệt lưu trữ hồ sơ, sổ sách ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
Tên cơ sở
SỔ KIỂM SOÁT CHẤT LƯỢNG THUỐC ĐỊNH KỲ
| Ngày kiểm soát | Tên thuốc nồng độ/hàm lượng | Dạng bào chế | Quy cách đóng gói | Số lô | Hạn dùng | Đơn vị tính | Số lượng | Chất lượng nhãn thuốc (đạt/không đạt) | Nhận xét chất lượng (đạt/Không đạt) | Phân loại chất lượng | Ghi chú |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Người phụ trách chuyên môn về dược | Nhân viên theo dõi |
E. Quy trình giải quyết đối với thuốc bị khiếu nại hoặc thu hồi
1. Mục đích yêu cầu:
Hướng dẫn thu hồi khẩn trương, triệt để các thuốc bị thu hồi đã được kết luận là thuốc không đạt tiêu chuẩn chất lượng và thuốc bị khiếu nại,
2. Phạm vi áp dụng:
Thuốc bị thu hồi là thuốc có thông báo thu hồi của các cơ quan quản lý hoặc nhà sản xuất, nhà cung cấp.
Thuốc bị khiếu nại là thuốc do khách hàng khiếu nại, yêu cầu trả lại.
3. Đối tượng thực hiện:
- Người phụ trách chuyên môn về dược của cơ sở bán lẻ thuốc
- Nhân viên bán thuốc tại cơ sở bán lẻ thuốc
4. Nội dung quy trình
4.1. Mô tả tiến trình
| Đối tượng | Sơ đồ | Mô tả |
| Người PTCM về dược Nhân viên | Xử lý thuốc bị thu hồi | 4.2.1 |
| Người PTCM về dược Nhân viên | Xử lý thuốc bị khiếu nại | 4.2.2 |
| Người PTCM về dược Nhân viên | Tổng hợp số liệu, ra quyết định xử lý thuốc thu hồi | 4.2.3 |
| Người PTCM về dược Nhân viên | Lưu hồ sơ | 4.2.4 |
4.2. Mô tả quy trình
4.2.1 Xử lý thuốc bị thu hồi
Sau khi nhận được thông báo thu hồi của Bộ Y tế, Sở Y tế, đơn vị sản xuất/kinh doanh thuốc cần tiến hành ngay:
- Kiểm tra xem nhà thuốc có nhập mặt hàng phải thu hồi hay không. Nếu có nhập thì cần phải:
+ Viết thông báo thu hồi lên bảng thông tin thuốc, ghi đầy đủ tên thuốc, số lô, hạn dùng, nhà sản xuất
+ Ngừng nhập, ngừng bán thuốc phải thu hồi, kiểm tra số lượng thuốc còn lại trong nhà thuốc (bao gồm cả thuốc trong nhà thuốc và thuốc mới mua về chưa kiểm nhập) sau đó đưa toàn bộ số thuốc vào khu vực chờ xử lý
+ Có thông báo thu hồi cho khách hàng đối với thuốc thu hồi thuộc danh mục thuốc phải kê đơn. Thông báo thu hồi trên bảng tin, bằng thư, điện thoại…
+ Nếu có khách trả lại hàng thu hồi, kiểm tra nếu đúng thuốc của cơ sở đã bán ra thì nhận lại thuốc và trả lại tiền hoặc đổi thuốc đảm bảo chất lượng cho khách
+ Ghi Sổ theo dõi thuốc bị đình chỉ lưu hành
+ Liên hệ với công ty, nhà cung ứng để trả lại hàng.
4.2.2. Xử lý thuốc bị khiếu nại
- Chỉ giải quyết đối với những thuốc do cơ sở bán lẻ bán cho khách hàng (căn cứ vào bao bì ra lẻ, đơn thuốc, hóa đơn, sổ theo dõi)
a) Nếu khách hàng trả lại thuốc do bị dị ứng, có biểu hiện tác dụng phụ của thuốc:
+ Hỏi khách về triệu chứng, biểu hiện của tác dụng phụ
+ Hỏi khách hàng về chế độ sinh hoạt, ăn uống để xem có phải nguyên nhân do thuốc hay thức ăn
+ Nếu nghi ngờ/xác định do tác dụng không mong muốn của thuốc (ADR) khuyên ngừng dùng thuốc, hỏi kỹ khách hàng các thông tin về tác dụng không mong muốn của thuốc, giải thích cho khách hàng về các tác dụng phụ do dùng thuốc gây ra đã được ghi trong tờ hướng dẫn sử dụng, ghi sổ theo dõi ADR.
+ Cần thiết khuyên khách hàng đi khám bác sỹ. Tư vấn cho khách hàng lần sau nhớ thông báo cho bác sỹ, người bán thuốc việc dùng các loại thuốc có các tác dụng phụ này
- Nhận lại thuốc và trả tiền cho khách, có thể tư vấn đổi thuốc khác cho khách hàng: Đối với thuốc còn nguyên bao bì trực tiếp sắp xếp vào đúng vị trí trong tủ trưng bày/bảo quản thuốc; trường hợp không còn bao bì trực tiếp để thuốc vào khu vực chờ xử lý, cuối tháng kiểm kê và tiến hành hủy thuốc.
- Để thuốc vào khu vực chờ xử lý, cuối tháng kiểm kê và tiến hành hủy thuốc
- Ghi sổ theo dõi tác dụng phụ của thuốc do khách hàng phản ánh
- Làm báo cáo ADR theo mẫu và gửi về Trung tâm DI&ADR quốc gia hoặc Trung tâm khu vực về Thông tin thuốc và phản ứng có hại của thuốc theo Hướng dẫn quốc gia về cảnh giác dược (QĐ số 122/QĐ-BYT năm 2020). Cụ thể hình thức và nơi gửi báo cáo: có thể chọn một trong các hình thức sau:
+ Báo cáo gửi qua email ([email protected]) hoặc
+ Báo cáo trực tuyến tại trang thông tin http://canhgiacduoc.org.vn hoặc
+ Báo cáo gửi trực tiếp hoặc qua đường bưu điện về địa chỉ: Trung tâm Quốc gia về Thông tin thuốc và Theo dõi phản ứng có hại của thuốc. 13, 15 Lê Thánh Tông, Quận Hoàn Kiếm, Hà Nội
+ Báo cáo gửi qua Fax: +84 4 3933 5642.
+ Báo cáo ADR thông qua phần mềm ứng dụng công nghệ thông tin khi kết nối liên thông cơ sở bán lẻ thuốc.
b) Nếu thuốc bị khiếu nại về chất lượng:
Cần xem xét thuốc kém chất lượng nguyên nhân ở đâu:
- Nếu do khách hàng bảo quản không tốt gây nên kém chất lượng, tư vấn và giải thích cho khách hàng về nguyên nhân và đề nghị khách hàng mua thuốc khác để dùng; hướng dẫn kỹ khách hàng về cách bảo quản thuốc để đảm bảo chất lượng.
- Nếu thuốc kém chất lượng do lỗi của cơ sở, xin lỗi khách hàng, nhận lại hàng và đổi lại hàng hoặc trả lại tiền cho khách. Để thuốc vào khu vực chờ xử lý, cuối tháng kiểm kê và tiến hành hủy thuốc.
- Kiểm soát chất lượng toàn bộ lô thuốc khách hàng khiếu nại và thuốc có nghi ngờ kém chất lượng đang trưng bày, bảo quản tại cơ sở
- Kiểm tra lại điều kiện bảo quản để tìm nguyên nhân thuốc kém chất lượng:
+ Nếu do điều kiện bảo quản của cơ sở thì cần phải có biện pháp khắc phục ngay
+ Nếu thuốc kém chất lượng không phải do lỗi bảo quản của cơ sở: Liên hệ thông báo với công ty/ nhà cung cấp về thuốc kém chất lượng để phối hợp tìm nguyên nhân.
- Báo cáo Trung tâm DI & ADR Quốc Gia các vấn đề liên quan đến chất lượng thuốc về mặt cảm quan, hoặc trường hợp nghi ngờ thuốc giả, được cơ sở phát hiện. Trong trường hợp này, các cơ sở bán lẻ thuốc nên gửi kèm ảnh chụp chi tiết thể hiện vấn đề về chất lượng hoặc nghi ngờ thuốc giả (các ảnh chụp: nhãn thuốc; các mặt của bao bì thể hiện rõ tên nhà sản xuất và số lô; viên thuốc, bột hoặc dung dịch thuốc).
- Ghi Sổ theo dõi khiếu nại của khách hàng
c) Nếu khiếu nại về dịch vụ: nhầm lẫn về giá thuốc, số lượng, chủng loại thuốc:
Kiểm tra lại các thông tin khách hàng khiếu nại, nếu có nhầm lẫn xin lỗi khách hàng và khắc phục sai sót với khách hàng.
4.2.3. Tổng hợp số liệu, ra quyết định xử lý thuốc thu hồi
Nhân viên nhà thuốc:
- Tổng hợp số liệu, làm báo cáo: thuốc bị thu hồi, thuốc không đạt tiêu chuẩn chất lượng do lỗi của cơ sở.
- Báo cáo Người phụ trách chuyên môn về dược của cơ sở
Người PTCM về dược của cơ sở:
- Rà soát và kiểm tra lại thông tin
- Thuốc thu hồi: liên hệ với công ty/nhà cung ứng trả lại hàng.
4.2.4. Lưu hồ sơ thu hồi
Lưu hồ sơ (bản photo) tại nhà thuốc, bao gồm:
- Công văn thu hồi
- Phiếu xác nhận thuốc thu hồi có tại nhà thuốc
- Bản báo cáo tổng kết thu hồi thuốc trả về
- Bản sao: Hóa đơn xuất trả hàng cho đơn vị bán (nếu có), biên bản hủy thuốc (nếu có)
4.2.5. Lưu ý
Theo hướng dẫn quốc gia về cảnh giác dược ,nhiệm vụ cụ thể của các cá nhân tại cơ sở bán lẻ thuốc trong hoạt động Cảnh giác Dược như sau:
Người chịu trách nhiệm chuyên môn của cơ sở bán lẻ thuốc:
- Thực hiện và tổ chức thực hiện việc theo dõi, phát hiện, ghi nhận, và báo cáo ADR theo quy định.
- Hướng dẫn nhân viên nhà thuốc về việc theo dõi, phát hiện, ghi nhận, và báo cáo ADR theo quy định.
- Báo cáo ADR theo quy định.
Nhân viên khác của cơ sở bán lẻ thuốc:
- Ghi nhận phản ánh của người bệnh về các biến cố bất lợi xảy ra trong quá trình sử dụng thuốc hoặc các bất thường liên quan đến chế phẩm thuốc.
- Báo cáo ADR theo quy định.
Các trường hợp cần báo cáo Trung tâm DI & ADR Quốc Gia
- Báo cáo các biến cố bất lợi, bao gồm cả các trường hợp thuốc không có hoặc không đạt hiệu quả điều trị, do người mua thuốc phản ánh theo mẫu báo cáo phản ứng có hại của thuốc.
- Báo cáo các vấn đề liên quan đến chất lượng thuốc về mặt cảm quan, hoặc trường hợp nghi ngờ thuốc giả, được cơ sở phát hiện. Trong trường hợp này, các cơ sở bán lẻ thuốc nên gửi kèm ảnh chụp chi tiết thể hiện vấn đề về chất lượng hoặc nghi ngờ thuốc giả (các ảnh chụp: nhãn thuốc; các mặt của bao bì thể hiện rõ tên nhà sản xuất và số lô; viên thuốc, bột hoặc dung dịch thuốc, …).
4.3. Biểu mẫu áp dụng
- Sổ theo dõi thuốc bị thu hồi, đình chỉ lưu hành
- Báo cáo thu hồi thuốc không đạt chất lượng
- Hồ sơ thu hồi thuốc
- Biên bản hủy thuốc
- Sổ theo dõi xử lý khiếu nại của khách hàng
- Sổ theo dõi tác dụng phụ của thuốc
- Biểu mẫu báo cáo phản ứng có hại của thuốc (tại trang thông tin điện tử http://canhgiacduoc.org.vn)
4.4. Hình thức lưu trữ
SOP này được lưu trong tập hồ sơ “SOP” của cơ sở bán lẻ thuốc.
Lưu trữ hồ sơ sổ sách ít nhất 01 năm kể từ khi thuốc hết hạn dùng. Riêng đối với thuốc phải kiểm soát đặc biệt lưu trữ hồ sơ, sổ sách ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
Tên cơ sở
SỔ THEO DÕI THUỐC BỊ THU HỒI ĐÌNH CHỈ LƯU HÀNH
| Số, ngày tháng của công văn cơ quan ban hành | Thuốc bị thu hồi, đình chỉ lưu hành (Tên thuốc, nồng độ/hàm lượng, số đăng ký) | Số lô, hạn dùng | Công ty sản xuất/nhập khẩu | Số lượng thuốc đã mua | Số lượng thuốc đã bán | Số lượng tồn | Số lượng thuốc thu hồi từ khách hàng | Khách hàng trả lại thuốc (Tên - Địa chỉ) | Người nhận | Xử lý của cơ sở |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Người phụ trách chuyên môn về dược |
| Tên cơ sở | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
| ......., ngày .... tháng .... năm 20... |
BÁO CÁO THU HỒI THUỐC KHÔNG ĐẠT CHẤT LƯỢNG
Kính gửi:…………………...……………
Theo công văn số……………., ngày… tháng… năm… của……………………… về việc thu hồi thuốc:
- Tên thuốc:………………………………………
- Nồng độ, hàm lượng:……………………………….
- Dạng bào chế - quy cách đóng gói: ………………
- Nơi sản xuất:………………………………………..
- Số lô sản xuất:………………………………………
Đơn vị đã tiến hành thu hồi như sau:
| Stt | Nơi tiến hành thu hồi | Tổng số lượng thuốc | Dự kiến biện pháp xử lý | Ghi chú | |
| Bán ra | Thu hồi | ||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Người phụ trách chuyên môn về dược |
| Tên cơ sở | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
| ......., ngày .... tháng .... năm 20... |
HỒ SƠ THU HỒI THUỐC
Chúng tôi gồm (ghi rõ họ tên, chức trách từng thành viên):
1.
2.
3.
thuộc:
…………………………………………………………………………………
được giao nhiệm vụ thu hồi thuốc không đạt chất lượng theo công văn số………………...ngày…tháng…năm…của……………………………..…………
Đã tiến hành thu hồi tại: ……………………………. gồm các nội dung sau:
| Stt | Tên thuốc nồng độ hàm lượng | Đơn vị tính | Số lượng thu hồi | Số lô sản xuất | Đơn vị sản xuất | Ghi chú |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Khách hàng | Các thành viên | Đại diện cơ sở bán lẻ thuốc |
| Tên cơ sở | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
| ......., ngày .... tháng .... năm 20... |
BIÊN BẢN HỦY THUỐC
Thực hiện quyết định số……………., ngày… tháng… năm… của …………………..… về việc hủy thuốc không đạt chất lượng, thuốc quá hạn dùng.
Hôm nay, ngày…… tháng… năm……. tại (tên địa điểm hủy thuốc):
Hội đồng hủy thuốc được thành lập theo quyết định số: …ngày…tháng…năm…... của ………………………. gồm có: (ghi rõ tên, chức danh)
1.
2.
3.
Đã chứng kiến và tiến hành hủy các thuốc sau:
| Stt | Tên thuốc nồng độ, hàm lượng | Số lô | Tên đơn vị sản xuất | Số lượng thuốc hủy theo chứng từ | Số thuốc thực hủy | Chênh lệch (*) | Ghi chú |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(*) Nếu có chênh lệch giữa số thuốc thực hủy và số lượng thuốc hủy theo chứng từ thì phải giải trình lý do.
Phương pháp hủy:
………………………………………………………………………………………
………………………………………………………………………………………
………………………………………………………………………………………
………
Biên bản này lập thành…………bản, mỗi bên giữ 01 bản, gửi báo cáo…….. bản.
| Các thành viên tham gia hủy thuốc | Chủ tịch Hội đồng hủy thuốc |
TÊN CƠ SỞ
SỔ THEO DÕI TÁC DỤNG PHỤ CỦA THUỐC
| Ngày/tháng/năm ghi nhận phản ánh | Họ tên người bệnh, tuổi | Địa chỉ, điện thoại | Các thuốc đã dùng | Dấu hiệu phản ứng | Người nhận thông tin | Hướng xử trí | ||
| Tên thuốc, nồng độ/hàm lượng, nhà sản xuất | Số lô | Hạn dùng | ||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Người phụ trách chuyên môn về dược của cơ sở
- Mẫu báo cáo phản ứng có hại của thuốc (có thể tải mẫu báo cáo hoặc báo cáo trực tuyến tại http://canhgiacduoc.org.vn)


TÊN CƠ SỞ
SỔ THEO DÕI XỬ LÝ KHIẾU NẠI CỦA KHÁCH HÀNG
| Ngày tháng | Họ tên khách hàng | Địa chỉ, Số điện thoại (nếu có) | Nội dung khiếu nại | Người nhận thông tin | Hướng xử trí |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Người phụ trách chuyên môn về dược của cơ sở |
E. Quy trình quản lý thuốc kiểm soát đặc biệt
E1. Quy trình quản lý thuốc kiểm soát đặc biệt (thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất)
1. Mục đích yêu cầu
Quy trình nhằm hướng dẫn việc lập dự trù, mua, bán, tiếp nhận, kiểm soát, bảo quản, báo cáo và hủy các thuốc phải kiểm soát đặc biệt là thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất.
2. Phạm vi áp dụng
Áp dụng cho thuốc phải kiểm soát đặc biệt là thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất được bán lẻ tại nhà thuốc.
3. Đối tượng thực hiện
- Người phụ trách chuyên môn về dược của nhà thuốc
- Nhân viên của nhà thuốc
4. Nội dung quy trình
4.1. Sơ đồ quy trình
| Người thực hiện | Trình tự thực hiện | Diển giải |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Lập đơn hàng mua thuốc phải kiểm soát đặc biệt (thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất), gửi Sở Y tế địa phương chờ phê duyệt | 4.2.1 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Mua tiếp nhận và kiểm soát các thuốc phải kiểm soát đặc biệt (chỉ được mua khi được phê duyệt của Sở Y tế địa phương | 4.2.2 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Bảo quản các thuốc phải kiểm soát đặc biệt | 4.2.3 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Bán các thuốc phải kiểm soát đặc biệt | 4.2.4 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Giao nhận, vận chuyển các thuốc phải kiểm soát đặc biệt | 4.2.5 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Nhận lại thuốc phải kiểm soát đặc biệt là thuốc gây nghiện | 4.2.6 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Hủy (xử lý) các thuốc phải kiểm soát đặc biệt | 4.2.7 |
| Người phụ trách chuyên môn nhà thuốc và nhân viên nhà thuốc | Báo cáo các thuốc phải kiểm soát đặc biệt | 4.2.8 |
4.2. Nội dung quy trình quản lý thuốc phải kiểm soát đặc biệt
4.2.1. Lập đơn hàng mua thuốc phải kiểm soát đặc biệt: là thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Chỉ những nhà thuốc có phạm vi kinh doanh thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất mới được phép lập đơn hàng mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất.
- Lập đơn hàng mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất: Nhà thuốc lập đơn hàng theo mẫu (Mẫu số 19 Phụ lục II Nghị định 155), gửi về Sở Y tế địa phương và chờ được phê duyệt theo đúng quy định. Lưu ý, Nhà thuốc xin duyệt mua thuốc tại một trong các Công ty theo quy định của Sở Y tế địa phương.
4.2.2. Mua, tiếp nhận, kiểm soát các thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Chỉ được tiến hành mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất theo đúng đơn hàng được Sở Y tế địa phương đã phê duyệt.
- Mua thuốc gây nghiện, hướng thần, tiền chất từ Công ty theo phê duyệt của Sở Y tế địa phương.
- Mua, tiếp nhận và kiểm tra 100% thuốc nhập về. Thực hiện theo hướng dẫn của Quy trình mua thuốc và kiểm soát chất lượng;
- Phải có ký nhận đầy đủ vào biên bản giao nhận thuốc kiểm soát đặc biệt.
- Kiểm tra và lưu phiếu xuất kho thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất của nơi cung cấp thuốc;
- Thuốc đã kiểm tra đạt yêu cầu: Ghi sổ theo mẫu số VIII Thông tư 20/2017/TT-BYT ngày 10/5/2017.
4.2.3. Bảo quản các thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Bảo quản hàng nhập theo hướng dẫn của Quy trình bảo quản và theo dõi chất lượng thuốc.
- Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất phải bảo quản trong tủ riêng hoặc ngăn riêng có khóa chắc chắn.
- Ngay sau khi tiếp nhận thuốc có chất lượng đạt yêu cầu, người nhận thuốc chuyển ngay các thuốc này vào nơi bảo quản khu vực riêng biệt, có biện pháp đảm bảo an toàn và an ninh theo quy định.
- Thuốc phải kiểm soát đặc biệt là thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất có chế độ kiểm soát định kỳ hàng tháng, mỗi tháng một lần vào cuối tháng: hình thức kiểm soát 100% số lượng thuốc.
4.2.4. Bán các thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Bán thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất theo đơn thuốc, bảo đảm an toàn cho người sử dụng và đúng quy chế chuyên môn quy định.
- Bán thuốc cơ bản thực hiện theo Quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc phải kê đơn. Kiểm tra tính hợp lệ của đơn thuốc và bán thuốc phải thực hiện theo quy định cấp/bán thuốc đối với thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất được quy định trong TT TT 52/2017/TT-BYT và TT 18/2018/TT-BYT (quy định về đơn thuốc và việc kê đơn thuốc hóa dược, sinh phẩm trong điều trị ngoại trú)
- Người chịu trách nhiệm bán lẻ thuốc gây nghiện phải là người có bằng tốt nghiệp đại học ngành dược trở lên;
- Người chịu trách nhiệm bán lẻ thuốc hướng thần, thuốc tiền chất phải là người có bằng tốt nghiệp trung cấp ngành dược trở lên.
- Lưu Đơn thuốc “N”, Đơn thuốc “H” bản chính tại cơ sở sau khi bán, thời gian lưu 02 năm kể từ khi thuốc hết hạn sử dụng.
- Ghi sổ theo dõi xuất, nhập, tồn kho theo mẫu sổ tại Phụ lục VIII kèm theo Thông tư 20/2017/TT-BYT ngày 10/5/2017.
- Ghi sổ theo dõi thông tin chi tiết khách hàng theo mẫu sổ quy định tại Phụ lục XXI kèm theo Thông tư 20/2017/TT-BYT ngày 10/5/2017
4.2.5. Giao nhận và vận chuyển các thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất.
- Giao nhận, vận chuyển thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, phải là người tốt nghiệp trung cấp dược trở lên.
- Người vận chuyển thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, khi làm nhiệm vụ phải mang theo văn bản giao nhiệm vụ của người đứng đầu cơ sở, giấy tờ tùy thân hợp lệ, hóa đơn bán hàng hoặc phiếu xuất kho.
- Khi tiến hành giao, nhận các thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất, nguyên liệu làm thuốc là dược chất gây nghiện, dược chất hướng thần, tiền chất dùng làm thuốc phải có Biên bản giao nhận theo mẫu quy định tại mẫu số 01 tại Phụ lục II ban hành kèm theo NĐ 54/2017/NĐ-CP ngày 8/7/2017.
- Khi giao, nhận thuốc, người giao, người nhận thuốc phải tiến hành kiểm tra đối chiếu tên thuốc, tên nguyên liệu, nồng độ, hàm lượng, số lượng, số lô sản xuất, hạn dùng, chất lượng thuốc về mặt cảm quan; phải ký và ghi rõ họ tên vào chứng từ xuất kho, nhập kho.
4.2.6. Nhận lại thuốc phải kiểm soát đặc biệt là thuốc gây nghiện khi người bệnh sử dụng không hết:
- Khi người bệnh không sử dụng hoặc sử dụng không hết thuốc gây nghiện: nhà thuốc phải thực hiện nhận lại thuốc và lập biên bản nhận lại thuốc gây nghiện theo mẫu biên bản quy định tại Phụ lục XX kèm theo Thông tư 20/2017/TT-BYT ngày 10/5/2017.
4.2.7. Hủy (xử lý) các thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
Hủy các thuốc gây nghiện, hướng thần, tiền chất được thực hiện theo quy định tại điều 48 và của Nghị định 54/2017/NĐ-CP
- Phải có văn bản đề nghị hủy gửi Sở Y tế địa phương, trong đó phải ghi rõ tên thuốc, nồng độ hoặc hàm lượng, số lượng, lý do xin hủy, phương pháp hủy.
- Việc hủy thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất chỉ được thực hiện sau khi có công văn cho phép của Sở Y tế địa phương
- Khi hủy thuốc phải lập Hội đồng hủy thuốc và lập biên bản hủy thuốc, giám sát việc hủy thuốc
- Thuốc hủy sẻ chuyển cho cơ sở có chức năng xử lý chất thải y tế có hợp đồng với công ty để hủy theo quy định.
- Làm hồ sơ hủy tại cơ sở.
- Sau khi hủy thuốc phải gửi báo cáo việc hủy thuốc cho Sở Y tế địa phương (kèm theo biên bản hủy thuốc).
4.2.8. Báo cáo các Thuốc phải kiểm soát đặc biệt: Thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất.
- Báo cáo định kỳ gửi Sở Y tế nơi cơ sở đặt trụ sở: báo cáo 06 (sáu) tháng và báo cáo năm (trước ngày 15 tháng 7 và trước ngày 15 tháng 01 hàng năm) tương ứng về việc xuất, nhập, tồn kho, sử dụng thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất.
- Mẫu báo cáo định kỳ: theo mẫu số 13 tại phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP
- Báo cáo đột xuất: khi phát hiện nhầm lẫn, thất thoát, người phụ trách chuyên môn về dược của nhà thuốc phải lập báo cáo theo mẫu báo cáo số 14 tại Phụ lục II Nghị định 54/2017/NĐ-CP ngày 8/5/2017 và gửi báo cáo về Sở Y tế địa phương trong vòng 48 giờ kể từ khi phát hiện nhầm lẫn, thất thoát.
4.3. Biểu mẫu áp dụng
- Đơn hàng mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Biên bản giao nhận thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Sổ theo dõi xuất, nhập, tồn kho thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Sổ theo dõi thông tin chi tiết khách hàng mua thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Biên bản nhận lại thuốc gây nghiện
- Báo cáo xuất, nhập, tồn kho, sử dụng thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Báo cáo trong trường hợp thất thoát, nhầm lẫn thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất
- Phiếu xuất kho thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất của nơi cung cấp thuốc
- Cam kết về sử dụng thuốc gây nghiện cho người bệnh
- Giấy xác nhận người bệnh cần tiếp tục điều trị giảm đau bằng thuốc gây nghiện của Trạm y tế xã, phường, thị trấn (nếu có).
4.4. Hình thức lưu trữ:
- Quy trình này được lưu trữ trong tập Hồ sơ quy trình của nhà thuốc
- Lưu trữ hồ sơ, sổ sách và thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) liên quan thuốc phải kiểm soát đặc biệt ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
Tên cơ sở:
Số
ĐƠN HÀNG MUA THUỐC GÂY NGHIỆN, THUỐC HƯỚNG THẦN, THUỐC TIỀN CHẤT
Kính gửi: ………………………………………………………….
| TT | Tên thuốc hoạt chất dạng bào chế nồng độ/hàm lượng, quy cách đóng gói | Đơn vị tính | Phần báo cáo kỳ trước (từ ngày….đến ngày…) | Số lượng mua | Duyệt | Ghi chú | ||||
| Số lượng tồn kho kỳ trước chuyển sang | Số lượng nhập trong kỳ | Tổng số | Số lượng xuất trong kỳ | Tồn kho cuối kỳ | ||||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8)* | (9) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Nơi nhận: | NGƯỜI LẬP BÁO CÁO | ……., ngày...tháng…năm… NGƯỜI ĐẠI DIỆN PHÁP LUẬT/NGƯỜI ĐƯỢC ỦY QUYỀN (Ký, ghi rõ họ tên, chức danh đóng dấu (nếu có)) | Số ……, ngày ..... tháng....năm..... Chấp thuận của cơ quan quản lý: Đơn hàng này gồm....trang.....khoản Được mua tại công ty........ Đơn hàng này có giá trị một năm kể từ ngày ký ban hành CƠ QUAN CHẤP THUẬN (Ký tên, đóng dấu) |
- Đối với các cơ sở kinh doanh thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất: Kèm theo tài liệu ghi rõ tên và địa chỉ khách hàng, số lượng, ngày bán.
- Đơn hàng mua thuốc được làm thành 03 bản (cơ sở lưu 01 bản, nơi bán 01 bản, cơ quan chấp thuận lưu 01 bản).
BIÊN BẢN GIAO NHẬN THUỐC GÂY NGHIỆN, THUỐC HƯỚNG THẦN, THUỐC TIỀN CHẤT
1. Tên cơ sở giao:
- Địa chỉ:
- Người giao:
- Số CMND/Thẻ căn cước/Hộ chiếu/Các giấy tờ tương đương khác:
Nơi cấp: Ngày cấp:
2. Tên cơ sở nhận:
- Địa chỉ:
- Người nhận:
- Số CMND/ Thẻ căn cước/ Hộ chiếu/ Các giấy tờ tương đương khác:
Nơi cấp: Ngày cấp:
3. Danh mục mặt hàng giao nhận:
| TT | Nguyên liệu/Tên thuốc dạng bào chế nồng độ/hàm lượng quy cách đóng gói | Đơn vị tính | Số lượng | Số hóa đơn/số phiếu xuất kho | Số Giấy đăng ký lưu hành/số giấy phép nhập khẩu/Công văn hoặc đơn hàng duyệt mua | Ghi chú |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) |
| 1 |
|
|
|
|
|
|
4. Thời gian giao nhận: (Các) mặt hàng trên được giao, nhận vào...giờ...phút ngày …..tháng .... năm ………..
5. Địa điểm giao nhận (Ghi chi tiết địa chỉ thực tế giao nhận):
6. Cam kết:
Các thuốc đã được giao nhận đầy đủ theo Danh mục mặt hàng ghi tại Biên Bản này.
Biên bản này được hai bên thống nhất và lập thành 02 bản, mỗi bên giữ 01 bản.
| BÊN GIAO | ….1…..ngày tháng năm……. |
1 Địa danh bên nhận đóng trụ sở
SỔ THEO DÕI XUẤT, NHẬP TỒN HO THUỐC GÂY NGHIỆN THUỐC HƯỚNG THẦN THUỐC TIỀN CHẤT
(Bắt đầu sử dụng từ.... đến…..)
Tên thuốc, nồng độ/ hàm lượng: ..........................................................
Đơn vị tính: .................................................................................................................
| Ngày tháng | Nơi xuất nhập | Số chứng từ xuất nhập | Số lượng | Số lô hạn dùng | Ghi chú | ||
| Nhập | Xuất | Còn lại | |||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) |
|
|
|
|
|
|
|
|
|
* Sổ được đánh số trang từ 01 đến hết, và đóng dấu giáp lai
* Mỗi thuốc phải dành một số trang riêng, số trang nhiều hay ít tùy loại thuốc xuất, nhập nhiều hay ít.
SỔ THEO DÕI THÔNG TIN CHI TIẾT KHÁCH HÀNG
(Bắt đầu sử dụng từ.... đến…..)
| Ngày tháng | Số thứ tự | Tên thuốc. Quy cách đóng gói | Hoạt chất, nồng độ/ hàm lượng | Đơn vị tính | Số lượng bán | Tên khách hàng | Địa chỉ | Ghi chú |
| (1) | (2) | (3) | (4) |
| (5) | (6) | (7) | (8) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* Sổ được đánh số trang từ 01 đến hết
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập - Tự do - Hạnh phúc
---------------
BIÊN BẢN NHẬN THUỐC GÂY NGHIỆN
1. Tên người giao:
- Địa chỉ:
- Số CMTND/ Thẻ căn cước/ Hộ chiếu/ Các giấy tờ tương đương khác:
Nơi cấp: Ngày cấp:
2. Tên cơ sở bán lẻ:
- Chủ nhà thuốc:
- Địa chỉ:
3. Danh mục mặt hàng nhận:
| TT | Tên thuốc, dạng bào chế, nồng độ/ hàm lượng quy cách đóng gói | Đơn vị tính | Số lượng | Lý do nhận lại | Ghi chú |
| 1 |
|
|
|
|
|
| 2 |
|
|
|
|
|
4. Thời gian giao nhận: (Các) mặt hàng trên được giao, nhận vào….giờ….phút ngày……tháng…..năm….
5. Địa điểm giao nhận (Ghi chi tiết địa chỉ thực tế giao nhận):
Biên bản này được hai bên thống nhất và lập thành 02 bản, mỗi bên giữ 01 bản.
| BÊN GIAO | …….., ngày tháng năm….. |
Tên cơ sở: .................................................................................................................
Số: .............................................................................................................................
BÁO CÁO XUẤT NHẬP TỒN KHO SỬ DỤNG THUỐC GÂY NGHIỆN, THUỐC HƯỚNG THẦN, THUỐC TIỀN CHẤT
(Từ ngày……... đến ngày.……….)
Kính gửi:………………………………………………….
| TT | Tên thuốc dạng bào chế nồng độ/hàm lượng quy cách đóng gói | Đơn vị tính | Số lượng tồn kho kỳ trước chuyển sang | Số lượng nhập trong kỳ | Tổng số | Số lượng xuất trong kỳ | Số lượng hao hụt | Tồn kho cuối kỳ |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8)* | (9) |
|
|
|
|
|
|
|
|
|
|
|
| ………, ngày tháng năm Đại diện đơn vị ** |
* Số lượng hao hụt bao gồm cả hỏng, vỡ, hết hạn dùng... nếu có, cần báo cáo chi tiết
** Người đại diện pháp luật hoặc người phụ trách chuyên môn được ủy quyền hoặc cấp phó của người đại diện pháp luật được ủy quyền
Tên cơ sở:
Số:
BÁO CÁO TRONG TRƯỜNG HỢP THẤT THOÁT, NHẦm LẪN THUỐC GÂY NGHIỆN, THUỐC HƯỚNG THẦN, THUỐC TIỀN CHẤT
Kính gửi:
| TT | Tên thuốc dạng bào chế nồng độ/hàm lượng quy cách đóng gói | Đơn vị tính | Số lượng thất thoát nhầm lẫn | Lý do | Biện pháp xử lý | Ghi chú |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) |
|
|
|
|
|
|
|
|
|
| ………, ngày tháng năm Đại diện đơn vị * |
* Người đại diện pháp luật hoặc người phụ trách chuyên môn được ủy quyền hoặc cấp phó của người đại diện pháp luật được ủy quyền
E.2. Quy trình quản lý thuốc kiểm soát đặc biệt (Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực)
1. Mục đích yêu cầu
Quy trình nhằm hướng dẫn việc mua, bán, tiếp nhận, kiểm soát, bảo quản, báo cáo và hủy các thuốc phải kiểm soát đặc biệt. Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc, dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực.
2. Phạm vi áp dụng
Áp dụng cho tất cả các thuốc phải kiểm soát đặc biệt được bán lẻ tại nhà thuốc, Cụ thể: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dang phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, Thuốc độc, Thuốc trong danh mục thuốc , dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực.
3. Đối tượng thực hiện
- Người phụ trách chuyên môn về dược
- Nhân viên
4. Nội dung quy trình
4.1. Sơ đồ quy trình
| Người thực hiện | Trình tự thực hiện | Diển giải |
| Người phụ trách chuyên môn và nhân viên | Mua, tiếp nhận và kiểm soát các thuốc phải kiểm soát đặc biệt | 4.2.1 |
| Người phụ trách chuyên môn và nhân viên | Bảo quản các thuốc phải kiểm soát đặc biệt | 4.2.2 |
| Người phụ trách chuyên môn và nhân viên | Bán các thuốc phải kiểm soát đặc biệt | 4.2.3 |
| Người phụ trách chuyên môn và nhân viên | Giao nhận, vận chuyển các thuốc phải kiểm soát đặc biệt | 4.2.4 |
| Người phụ trách chuyên môn và nhân viên | Hủy(xử lý) các thuốc phải kiểm soát đặc biệt | 4.2.5 |
| Người phụ trách chuyên môn và nhân viên | Báo cáo các thuốc phải kiểm soát đặc biệt | 4.2.6 |
4.2. Nội dung quy trình quản lý kinh doanh thuốc phải kiểm soát đặc biệt
4.2.1. Mua, tiếp nhận, kiểm soát các thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực
- Mua tiếp nhận thuốc thực hiện theo hướng dẫn của Quy trình mua thuốc và kiểm soát chất lượng
- Mua thuốc phải kiểm soát đặc biệt: từ công ty dược có giấy phép đủ điều kiện kinh doanh dược theo quy định, có phạm vi kinh doanh thuốc phải kiểm soát đặc biệt (Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực).
- Đối với thuốc dạng phối hợp có chứa tiền chất: nhà thuốc chỉ được mua của cơ sở bán buôn đặt địa điểm kinh doanh trên địa bàn tỉnh (nơi nhà thuốc đặt trụ sở) có phạm vi kinh doanh thuốc gây nghiện, thuốc hướng thần, thuốc tiền chất hoặc mua của cơ sở đồng thời có giấy chứng nhận đủ điều kiện kinh doanh dược phạm vi xuất khẩu, nhập khẩu thuốc và bán buôn thuốc.
- Thuốc được kiểm nhập trước khi đưa vào khu vực riêng biệt và lập biên bản kiểm nhập.
4.2.2. Bảo quản các thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực
- Bảo quản theo hướng dẫn của Quy trình bảo quản và theo dõi chất lượng thuốc
- Ngay sau khi tiếp nhận thuốc đạt yêu cầu, người nhận thuốc chuyển ngay các thuốc này vào nơi bảo quản khu vực riêng biệt, có biện pháp đảm bảo an toàn và an ninh theo quy định.
- Có chế độ kiểm soát định kỳ hàng tháng, mỗi tháng một lần vào cuối tháng: hình thức kiểm soát 100% số lượng thuốc phải kiểm soát đặc biệt (Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực)
4.2.3. Bán các thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực
- Với các thuốc được phân loại là thuốc phải kê đơn thực hiện bán thuốc theo quy định của thuốc kê đơn và hướng dẫn theo quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc phải kê đơn
- Với các thuốc được phân loại là thuốc không kê đơn thực hiện bán thuốc theo quy định của thuốc không kê đơn và hướng dẫn theo quy trình bán thuốc, thông tin, tư vấn hướng dẫn sử dụng thuốc không kê đơn
- Có chế độ sổ sách hoặc sử dụng máy tính (phần mềm kết nối dữ liệu dược quốc gia) theo dõi việc xuất nhập tồn và sổ theo dõi thông tin chi tiết khách hàng mua thuốc phải kiểm soát đặc biệt là thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc dược chất thuộc danh mục chất bị cấm trong một số ngành, lĩnh vực.
4.2.4. Giao nhận và vận chuyển các thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc thuộc dược chất danh mục chất bị cấm trong một số ngành, lĩnh vực.
- Giao nhận, vận chuyển thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc thuộc dược chất danh mục chất bị cấm trong một số ngành, lĩnh vực phải là dược sỹ trung học trở lên.
4.2.5. Hủy (xử lý) các thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc thuộc dược chất danh mục chất bị cấm trong một số ngành, lĩnh vực
- Hủy các thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất, thuốc độc, thuốc trong danh mục thuốc thuộc dược chất danh mục chất bị cấm trong một số ngành, lĩnh vực được thực hiện theo quy định tại điểm a khoản 4 và khoản 7 điều 48 và của Nghị định 54/2017/NĐ-CP của Chính phủ.
- Khi hủy thuốc phải lập Hội đồng hủy thuốc và lập biên bản hủy thuốc, giám sát việc hủy thuốc
- Thuốc hủy sẻ chuyển cho cơ sở có chức năng xử lý chất thải y tế có hợp đồng với công ty để hủy theo quy định.
- Làm hồ sơ hủy tại cơ sở
4.2.6. Báo cáo các Thuốc phải kiểm soát đặc biệt: Thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất.
- Báo cáo gửi Sở Y Tế nơi cơ sở đặt trụ sở: định kỳ báo cáo 06 tháng và báo cáo năm (trước ngày 15 tháng 7 và trước ngày 15 tháng 1 hàng năm) tương ứng về việc xuất, nhập, tồn kho thuốc dạng phối hợp có chứa dược chất gây nghiện, thuốc dạng phối hợp có chứa dược chất hướng thần, thuốc dạng phối hợp có chứa tiền chất.
- Mẫu báo cáo: theo mẫu số 12 tại phụ lục II ban hành kèm theo Nghị định 54/2017/NĐ-CP của Chính phủ.
4.3. Biểu mẫu áp dụng
- Biên bản kiểm nhập thuốc phải kiểm soát đặc biệt: thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất
- Sổ theo dõi xuất, nhập, tồn kho thuốc dạng phối hợp chứa dược chất gây nghiện, thuốc dạng phối hợp chứa dược chất hướng thần, thuốc dạng phối hợp chứa tiền chất, thuốc độc, thuốc và dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành, lĩnh vực
- Sổ theo dõi thông tin chi tiết khách hàng mua thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất
- Báo cáo xuất, nhập tồn, sử dụng thuốc dạng phối hợp chứa dược chất gây nghiện/ thuốc dạng phối hợp chứa dược chất hướng thần/thuốc dạng phối hợp chứa tiền chất
4.4. Hình thức lưu trữ:
- Quy trình này được lưu trữ trong tập Hồ sơ quy trình của cơ sở bán lẻ thuốc
- Lưu trữ hồ sơ, sổ sách/thông tin lưu trữ trên máy tính (phần mềm kết nối cơ sở dữ liệu dược quốc gia) liên quan thuốc phải kiểm soát đặc biệt ít nhất 02 năm kể từ khi thuốc hết hạn dùng.
BIÊN BẢN KIỂM NHẬP THUỐC PHẢI KIỂM SOÁT ĐẶC BIỆT: THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT GÂY NGHIỆN/ THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT HƯỚNG THẦN/THUỐC DẠNG PHỐI HỢP CHỨA TIỀN CHẤT
Hôm nay, hồi …….giờ………ngày…..thánh …….năm…….tại nhà thuốc………..
Hội đồng kiểm nhập gồm: 1………………………………………………………
2………………………………………………………
Đã tiến hành kiểm nhập và kiểm soát chất lượng các mặt hàng sau:
| TT | Tên thuốc, nồng độ, hàm lượng | Đơn vị tính | Số chứng từ | Quy cách đóng gói | Nơi sản xuất | Số kiểm soát (số lượng) | Hạn dùng | Số lượng hóa đơn | Số lượng thực nhập | Nhận xét cảm quan | Ghi chú |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tổng số mặt hàng đó kiểm nhập:……………………………………………..
Nhận xét và ý kiến đề nghị:……………………………………………………
| Người phụ trách chuyên môn | Nhân viên |
Biểu mẫu:
SỔ THEO DÕI XUẤT, NHẬP, TỒN KHO THUỐC DẠNG PHỐI HỢP CÓ CHỨA DƯỢC CHẤT GÂY NGHIỆN, THUỐC DẠNG PHỐI HỢP CÓ CHỨA DƯỢC CHẤT HƯỚNG THẦN, THUỐC DẠNG PHỐI HỢP CÓ CHỨA TIỀN CHẤT, THUỐC ĐỘC, THUỐC VÀ DƯỢC CHẤT THUỘC DANH MỤC CHẤT BỊ CẤM SỬ DỤNG TRONG MỘT SỐ NGÀNH, LĨNH VỰC
Tên thuốc, nồng độ/ hàm lượng............................................................
Đơn vị tính: .................................................................................................................
Nhà sản xuất: ..............................................................................................................
| Ngày tháng | Nơi nhập | Số chứng từ xuất nhập | Số lượng | Số lô hạn dùng | Ghi chú | ||
| Nhập | Xuất | Còn lại | |||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* Sổ được đánh số trang từ 01 đến hết.
Tên cơ sở:
Số:
SỔ THEO DÕI THÔNG TIN CHI TIẾT KHÁCH HÀNG MUA THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT GÂY NGHIỆN/ THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT HƯỚNG THẦN/THUỐC DẠNG PHỐI HỢP CHỨA TIỀN CHẤT
| stt | Ngày tháng | Tên thuốc, quy cách đóng gói | Hoạt chất, nồng độ, hàm lượng | Đơn vị tính | Số lượng bán | Tên khách hàng | Địa chỉ | Ghi chú |
| (1) | (2) | (3) | (4) |
| (5) | (6) | (7) | (8) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ……., ngày tháng năm |
Tên cơ sở:
Số
BÁO CÁO XUẤT, NHẬP TỒN, SỬ DỤNG THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT GÂY NGHIỆN/ THUỐC DẠNG PHỐI HỢP CHỨA DƯỢC CHẤT HƯỚNG THẦN/THUỐC DẠNG PHỐI HỢP CHỨA TIỀN CHẤT
Kính gửi: ………………………………………………………….
| STT | Tên thuốc, dạng bào chế quy cách đóng gói | Thành phần nồng độ hàm lượng | Tên dược chất GN/TH/TC hàm lượng có trong 1 đơn vị đã chia liều hoặc chưa chia liều | Số giấy phép nhập khẩu | Đơn vị tính | Số lượng tồn kho kỳ trước chuyển sang | Số lượng nhập trong kỳ | Tổng số | Số lượng xuất trong kỳ | Tồn kho cuối kỳ | Số lượng hao hụt |
| (1) | (2) |
|
|
| (3) | (4) | (5) |
| (6) | (7) | (8) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Số lượng hao hụt bao gồm cả hỏng, vở hết hạn dùng…. Nếu có cần báo cáo chi tiết Chú ý: số lượng báo cáo phải được cập nhật ngày trước thời gian lập đơn hàng đề nghị Báo cáo phải kèm theo danh sách chi tiết tên, địa chỉ khách hàng theo từng lần xuất hàng
|
|
|
………, ngày tháng năm
Người đại diện trước pháp luật/ Người được ủy quyền
(Ký, ghi rõ họ tên, chức danh, đóng dấu (nếu có)
PHỤ LỤC
| TT | Số phụ lục | Nội dung |
| 1. | PL1 | Danh mục thuốc không kê đơn |
| 2. | PL2 | Danh mục thuốc hạn chế bán lẻ |
| 3. | PL3 | Danh mục thuốc độc và nguyên liệu độc làm thuốc |
| 4 | PL4 | Danh mục thuốc dược chất thuộc danh mục chất bị cấm sử dụng trong một số ngành lĩnh vực |
| 5 | PL5 | Danh mục dược chất gây nghiện |
| 6 | PL6 | Danh mục dược chất hướng thần |
| 7 | PL7 | Danh mục tiền chất dùng làm thuốc |
| 8 | PL8 | Bảng giới hạn nồng độ hàm lượng dược chất gây nghiện trong thuốc dạng phối hợp |
| 9 | PL9 | Bảng giới hạn nồng độ hàm lượng dược chất hướng thần trong thuốc dạng |
| 10 | PL10 | Bảng giới hạn nồng độ hàm lượng tiền chất dùng làm thuốc trong thuốc dạng |
PHỤ LỤC 1
DANH MỤC THUỐC KHÔNG KÊ ĐƠN
(Ban hành kèm theo Thông tư số: 07/2017/TT-BYT ngày 03 tháng 5 năm 2017 của Bộ trưởng Bộ Y tế)
I. DANH MỤC THUỐC HÓA DƯỢC VÀ SINH PHẨM KHÔNG KÊ ĐƠN
| TT | Thành phần hoạt chất | Đường dùng, dạng bào chế, giới hạn hàm lượng, nồng độ | Các quy định cụ thể khác |
| 1 | Acetylcystein | Uống: các dạng |
|
| 2 | Acetylleucin | Uống: các dạng |
|
| 3 | Acid acetylsalicylic (Aspirin) dạng đơn thành phần hoặc phối hợp với Vitamin C và/hoặc Acid citric và/hoặc Natri bicarbonat và/hoặc Natri salicylat | Uống: các dạng | Với chỉ định giảm đau, hạ sốt, chống viêm |
| 4 | Acid alginic (Natri Alginat) đơn thành phần hay phối hợp với các hợp chất của nhôm, magnesisi | Uống: các dạng |
|
| 5 | Acid amin đơn thành phần hoặc phối hợp (bao gồm cả dạng phối hợp với các Vitamin) | Uống: các dạng | Với chỉ định bổ sung acid amin, vitamin cho cơ thể |
| 6 | Acid aminobenzoic (Acid para aminobenzoic) | Uống: các dạng |
|
| 7 | Acid benzoic đơn thành phần hoặc phối hợp | Dùng ngoài Uống: viên ngậm |
|
| 8 | Acid boric đơn thành phần hoặc phối hợp | Dùng ngoài Thuốc tra mắt |
|
| 9 | Acid citric phối hợp với các muối natri, kali | Uống: các dạng |
|
| 10 | Acid cromoglicic và các dạng muối cromoglicat | Thuốc tra mắt, tra mũi với giới hạn nồng độ tính theo acid cromoglicic ≤ 2% |
|
| 11 | Acid dimecrotic | Uống: các dạng |
|
| 12 | Acid folic đơn thành phần hoặc phối hợp với sắt và/hoặc các Vitamin nhóm B, khoáng chất, sorbitol | Uống: các dạng | Với chỉ định chống thiếu máu, bổ sung dinh dưỡng |
| 13 | Acid glycyrrhizinic (Glycyrrhizinat) phối hợp với một số hoạt chất khác như Chlorpheniramin maleat, DL-methylephedrin, Cafein... | Uống: các dạng, bao gồm cả dạng viên ngậm Dùng ngoài |
|
| 14 | Acid lactic đơn thành phần hoặc phối hợp | Dùng ngoài |
|
| 15 | Acid mefenamic | Uống: các dạng |
|
| 16 | Acid salicylic đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài (phối hợp Lactic acid; Lưu huỳnh kết tủa...) | Dùng ngoài |
|
| 17 | Acyclovir | Dùng ngoài: thuốc bôi ngoài da với nồng độ Acyclovir ≤ 5% |
|
| 18 | Albendazol | Uống: các dạng | Với chỉ định trị giun |
| 19 | Alcol diclorobenzyl dạng phối hợp trong các thành phẩm viên ngậm | Uống: viên ngậm |
|
| 20 | Alcol polyvinyl | Dùng ngoài |
|
| 21 | Alimemazin tartrat (Trimeprazin tartrat) | Uống: các dạng |
|
| 22 | Allantoin dạng phối hợp trong các thành phẩm dùng ngoài, thuốc đặt hậu môn (Cao cepae fluid; ...) | Dùng ngoài Thuốc đặt hậu môn |
|
| 23 | Allatoin phối hợp với các Vitamin và/hoặc Chondroitin | Thuốc tra mắt |
|
| 24 | Almagat | Uống: các dạng |
|
| 25 | Ambroxol đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng với giới hạn hoạt chất như sau: - Đã chia liều Ambroxol clorhydrat ≤ 30mg/đơn vị - Chưa chia liều: Ambroxol clorhydrat ≤ 0,8% |
|
| 26 | Amylase dạng đơn thành phần hoặc phối hợp với Protease và/hoặc Lipase và/hoặc Cellulase | Uống: các dạng |
|
| 27 | Amylmetacresol dạng phối hợp trong các thành phẩm viên ngậm (như với các tinh dầu, Bacitracin...) | Uống: viên ngậm |
|
| 28 | Argyron | Thuốc tra mắt Dùng ngoài |
|
| 29 | Aspartam | Uống: các dạng |
|
| 30 | Aspartat đơn thành phần hoặc phối hợp | Uống: các dạng |
|
| 31 | Attapulgit | Uống: các dạng |
|
| 32 | Azelastin | Thuốc tra mắt, tra mũi |
|
| 33 | Bạc Sulphadiazin | Dùng ngoài |
|
| 34 | Bacitracin phối hợp với một số hoạt chất khác trong các thành phẩm viên ngậm (phối hợp với Neomycin sulfat; Amylocain; Tixocortol...) | Uống: viên ngậm |
|
| 35 | Beclomethason dipropionat | Thuốc tra mũi: dạng khí dung với giới hạn liều dùng tối đa 1 ngày ≤ 400 mcg, đóng gói ≤ 200 liều (tính theo hoạt chất không có muối) |
|
| 36 | Benzalkonium phối hợp trong các thành phẩm dùng ngoài (với Cholin; acid salicylic; Nystatin; Diiodohydroxyquin ...), trong các thành phẩm viên ngậm (với Tyrothricin, Bacitracin, tinh dầu...) | Dùng ngoài Viên ngậm |
|
| 37 | Benzocain dạng phối hợp | Dùng ngoài: các dạng với giới hạn Benzocain ≤ 10%; Viên đặt hậu môn Uống: viên ngậm |
|
| 38 | Benzoyl peroxid đơn thành phần hoặc phối hợp với Iod và/hoặc lưu huỳnh | Dùng ngoài: các dạng với giới hạn nồng độ ≤ 10% |
|
| 39 | Benzydamin Hydrochlorid đơn thành phần hoặc phối hợp | Dùng ngoài: kem bôi niêm mạc miệng, nước xúc miệng, thuốc xịt họng Uống: viên ngậm |
|
| 40 | Benzydamin salicylat đơn thành phần hoặc phối hợp | Dùng ngoài |
|
| 41 | Benzyl benzoat phối hợp trong các thành phẩm dùng ngoài (với các tinh dầu, Cồn Isopropyl...) | Dùng ngoài: các dạng Miếng dán |
|
| 42 | Berberin | Uống: các dạng |
|
| 43 | Biclotymol đơn thành phần hoặc phối hợp với Enoxolon và/hoặc Phenylephrin hydrochlorid và/hoặc Clorpheniramin maleat và/hoặc tinh dầu | Dùng ngoài Thuốc tra mũi Uống: viên ngậm |
|
| 44 | Bifonazol đơn thành phần hoặc phối hợp với Urea | Dùng ngoài |
|
| 45 | Bisacodyl | Uống: các dạng đã chia liều với hàm lượng ≤ 10mg/đơn vị |
|
| 46 | Bismuth dạng muối | Uống: các dạng | Chỉ định điều trị chứng ợ nóng |
| 47 | Boldine | Uống: các dạng |
|
| 48 | Bromhexin Hydrochlorid đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng với giới hạn Bromhexin Hydrochlorid như sau: - Đã chia liều ≤ 8mg/đơn vị; - Chưa chia liều ≤ 0,8% Thuốc đặt hậu môn |
|
| 49 | Bromelain đơn thành phần hoặc phối hợp với Trypsin | Uống: các dạng |
|
| 50 | Brompheniramin maleat đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng |
|
| 51 | Budesonid | Thuốc tra mũi: dạng khí dung, ống hít, thuốc bột để hít với giới hạn liều dùng tối đa 1 ngày ≤ 400mcg, đóng gói ≤ 200 liều |
|
| 52 | Bufexamac đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài, thuốc đặt hậu môn (với Titan Dioxid, Bismuth, Subgallat, Lidocain...) | Dùng ngoài Thuốc đặt hậu môn |
|
| 53 | Butoconazol | Dùng ngoài |
|
| 54 | Cafein phối hợp với các hoạt chất có trong danh mục này | Uống: các dạng |
|
| 55 | Calamin đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài | Dùng ngoài |
|
| 56 | Calci (bao gồm các dạng hợp chất) thuốc đơn thành phần hoặc phối hợp với Vitamin D (trừ Calcitriol) và/hoặc các Vitamin và/hoặc Ipriflavon | Uống: các dạng | Với chỉ định bổ sung calci cho cơ thể |
| 57 | Carbinoxamin đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau (với Pseudoephedrin hydrochlorid và/hoặc Bromhexin và/hoặc Paracetamol) | Dạng uống | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 58 | Carbocystein | Uống: các dạng |
|
| 59 | Carbomer | Dùng ngoài Thuốc tra mắt |
|
| 60 | Catalase đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài (với Neomycin) | Dùng ngoài |
|
| 61 | Cetirizin dihydrochlorid | Uống: các dạng |
|
| 62 | Cetrimid phối hợp với một số hoạt chất khác trong các thành phẩm dùng ngoài (Lidocain, Kẽm, Calamin, Aminacrine, tinh dầu...) | Dùng ngoài |
|
| 63 | Cetrimonium phối hợp trong các thành phẩm dùng ngoài, viên ngậm (phối hợp với Lidocain; Tyrothricin, tinh dầu...) | Dùng ngoài Uống: viên ngậm |
|
| 64 | Chitosan (Polyglusam) | Dùng ngoài |
|
| 65 | Cholin đơn thành phần hoặc phối hợp các acid amin, Vitamin trong các thành phẩm dạng uống; phối hợp với acid Salicylic, Benzalkonium... trong các thành phẩm dùng ngoài | Uống: các dạng Dùng ngoài |
|
| 66 | Chondroitin đơn thành phần hoặc phối hợp với Glucosamin và/hoặc dầu cá và/hoặc các Vitamin và/hoặc các acid amin | Uống: các dạng |
|
| 67 | Chondroitin đơn thành phần hoặc phối hợp Borneol và, hoặc các Vitamin | Thuốc tra mắt Dùng ngoài |
|
| 68 | Ciclopirox olamin | Dùng ngoài |
|
| 69 | Cimetidin | Uống: dạng chia liều với giới hạn hàm lượng Cimetidin ≤ 200mg/đơn vị | Chỉ định điều trị chứng ợ nóng |
| 70 | Cinarizin | Uống: các dạng |
|
| 71 | Cinchocain phối hợp trong các thành phẩm dùng ngoài, thuốc đặt hậu môn (như với Hydrocortison, Neomycin, Esculin...) | Dùng ngoài Thuốc đặt hậu môn |
|
| 72 | Citrullin | Uống: các dạng |
|
| 73 | Clobetason butyrat | Dùng ngoài |
|
| 74 | Clorhexidin | Dùng ngoài |
|
| 75 | Clorophyl | Uống: các dạng |
|
| 76 | Clorpheniramin maleat đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng. Dạng đơn thành phần đã chia liều: Clorpheniramin maleat ≤ 4mg/đơn vị. |
|
| 77 | Clorpheniramin maleat phối hợp Chondroitin và/hoặc các Vitamin | Thuốc tra mắt |
|
| 78 | Clotrimazol | Dùng ngoài: các dạng với giới hạn nồng độ ≤ 3% Viên đặt âm đạo |
|
| 79 | Codein phối hợp với các hoạt chất có trong danh mục này với chỉ định chữa ho, hạ nhiệt, giảm đau | Uống: các dạng. với giới hạn hàm lượng Codein (tính theo dạng base) như sau: - Dạng chia liều ≤ 12mg/đơn vị; - Dạng chưa chia liều ≤ 2,5% | Thành phẩm chứa Codein được bán không cần đơn với số lượng tối đa cho 10 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 80 | Coenzym Q10 đơn thành phần hoặc phối hợp với các Vitamin | Uống: các dạng |
|
| 81 | Crotamiton | Dùng ngoài |
|
| 82 | Dequalinium đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài, viên ngậm (Tyrothricin; Hydrocortison; acid Glycyrrhetinic; Lidocain...) | Dùng ngoài Viên đặt âm đạo Uống: viên ngậm |
|
| 83 | Desloratadin | Uống: các dạng với giới hạn hàm lượng ≤ 5mg/đơn vị chia liều Hoặc uống với liều tối đa 5mg/ngày |
|
| 84 | Dexbrompheniramin maleat đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng |
|
| 85 | Dexclorpheniramin maleat đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng |
|
| 86 | Dexpanthenol | Thuốc tra mắt Dùng ngoài |
|
| 87 | Diclofenac đơn thành phần hoặc phối hợp với Methyl salicylat; các chất thuộc nhóm tinh dầu... | Dùng ngoài Thuốc tra mắt (dạng đơn thành phần) |
|
| 88 | Dicyclomin | Uống: các dạng |
|
| 89 | Diethylphtalat (DEP) | Dùng ngoài |
|
| 90 | Dimenhydrinat | Uống: các dạng |
|
| 91 | Dimethicon (Dimethylpolysiloxan) đơn thành phần hoặc phối hợp với Guaiazulen | Uống: các dạng |
|
| 92 | Dimethicon phối hợp trong các thành phẩm dùng ngoài (với Kẽm; Calamin; Cetrimid...) | Dùng ngoài |
|
| 93 | Dimethinden | Uống: các dạng Dùng ngoài |
|
| 94 | Dinatri Inosin monophosphat | Thuốc tra mắt |
|
| 95 | Diosmectit (Dioctahedral smectit) | Uống: các dạng |
|
| 96 | Diosmin phối hợp Hesperidin và/hoặc một số cao dược liệu chứa Flavonoid | Uống: các dạng |
|
| 97 | Diphenhydramin hydrochlorid hoặc monocitrat | Uống: các dạng với giới hạn hàm lượng (tính theo dạng base) như sau: - Đã chia liều ≤ 50mg/đơn vị; - Chưa chia liều: ≤ 2,5% |
|
| 98 | Đồng sulfat | Dùng ngoài |
|
| 99 | Doxylamin phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau (với Paracetamol, Pseudoephedrin Hydrochlorid, các hoạt chất khác có trong danh mục thuốc không kê đơn) | Uống: các dạng | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 100 | Econazol đơn thành phần hoặc phối hợp với Hydrocortison | Dùng ngoài, giới hạn nồng độ Hydrocortison tính theo dạng base ≤ 0,05% |
|
| 101 | Enoxolon đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài, viên ngậm | Dùng ngoài: thuốc bôi ngoài da, kem bôi niêm mạc miệng, nước xúc miệng Uống: viên ngậm |
|
| 102 | Ephedrin Hydrochlorid | Thuốc tra mắt, tra mũi: dung dịch ≤ 1%. Đóng gói ≤ 15ml/đơn vị | Thành phẩm chứa Ephedrin được bán tối đa không cần đơn với số lượng 3 đơn vị đóng gói nhỏ nhất/lần Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 103 | Eprazinon | Uống: các dạng |
|
| 104 | Esdepallethrin phối hợp trong các thành phẩm dùng ngoài (với Piperonyl, Spregal, tinh dầu, các chất có trong thành phần tinh dầu) | Dùng ngoài |
|
| 105 | Estradiol đơn thành phần và phối hợp Dydrogesteron | Uống: các dạng đã chia liều | * Thuốc chỉ được phê duyệt với chỉ định tránh thai |
| 106 | Ethanol đơn thành phần hoặc phối hợp | Dùng ngoài (cồn sát trùng) Uống: dạng phối hợp |
|
| 107 | Ethylestradiol đơn thành phần | Uống: các dạng đã chia liều | * Thuốc chỉ được phê duyệt với chỉ định tránh thai |
| 108 | Etofenamat | Dùng ngoài |
|
| 109 | Famotidin | Uống: dạng chia liều với giới hạn hàm lượng ≤20mg/đơn vị | Bán không cần đơn tối đa cho 14 ngày sử dụng |
| 110 | Fenticonazol | Dùng ngoài |
|
| 111 | Fexofenadin | Uống: các dạng |
|
| 112 | Flurbiprofen | Viên ngậm Dùng ngoài Thuốc tra mắt |
|
| 113 | Glucosamin đơn thành phần hoặc phối hợp với Chondroitin và/hoặc các Vitamin | Uống: các dạng |
|
| 114 | Glucose hoặc Dextrose đơn thành phần hoặc phối hợp với các muối natri, kali | Uống: các dạng | Với chỉ định bổ sung đường, chất điện giải. |
| 115 | Glycerin đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài, thuốc tra mắt (với Polysorbat 80) | Dùng ngoài Thuốc tra mắt |
|
| 116 | Glycerol phối hợp với dịch chiết dược liệu | Thuốc thụt trực tràng |
|
| 117 | Guaiphenesin đơn thành phần hoặc phối hợp với các hoạt chất có trong danh mục thuốc không kê đơn có tác dụng chữa ho, hạ nhiệt, giảm đau. | Uống: các dạng | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 118 | Hexamidin đơn thành phần hoặc phối hợp (với Cetrimid, Lidocain, Clotrimazol, Catalase) | Dùng ngoài |
|
| 119 | Hexetidin đơn thành phần hoặc phối hợp (với Benzydamin, Cetylpyridinum, Cholin Salicylat, Methyl salicylat, tinh dầu...) | Dùng ngoài: thuốc bôi ngoài da, dung dịch xúc miệng |
|
| 120 | Hydrocortison đơn thành phần hoặc phối hợp (với Miconazol, Econazol, Tioconazol, Neomycin) | Dùng ngoài: các dạng với nồng độ Hydrocortison ≤ 0,5% |
|
| 121 | Hydrogen Peroxid (Oxy già) đơn thành phần hoặc phối hợp Natri Lauryl sulfat và/hoặc tinh dầu... | Dùng ngoài |
|
| 122 | Hydrotalcit | Uống: các dạng |
|
| 123 | Hyoscine (Scopolamin) butylbromid đơn thành phần hoặc phối hợp với Meclizin hydrochlorid | Uống: các dạng, bao gồm viên nhai. Giới hạn hàm lượng đã chia liều ≤ 20mg Miếng dán |
|
| 124 | Hydroxypropyl methylcellulose (Hypromellose, HPMC) đơn thành phần hoặc phối hợp Dextran 70 và/hoặc Carbomer | Thuốc tra mắt: các dạng |
|
| 125 | Ibuprofen | Uống: các dạng với giới hạn hàm lượng như sau: đã chia liều ≤ 400mg/đơn vị. Dùng ngoài |
|
| 126 | Ichthammol | Dùng ngoài |
|
| 127 | Indomethacin | Dùng ngoài Tra mắt dung dịch 0,1% |
|
| 128 | Iod phối hợp Kali Iodid và/hoặc Acid Benzoic và/hoặc Acid Salicylic | Dùng ngoài với nồng độ Iod ≤ 5% |
|
| 129 | Isoconazol | Dùng ngoài |
|
| 130 | Isopropyl Methylphenol | Dùng ngoài |
|
| 131 | Kẽm oxid, Kẽm pyrithion, Kẽm Gluconat, Kẽm undecylenat đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài | Dùng ngoài |
|
| 132 | Kẽm sulfat | Dùng ngoài Thuốc tra mắt |
|
| 133 | Ketoconazol đơn thành phần hoặc phối hợp với Kẽm Pirythion và/hoặc Hydrocortison và/hoặc Trolamin | Dùng ngoài: các dạng với nồng độ Ketoconazol ≤ 2% |
|
| 134 | Ketoprofen | Dùng ngoài |
|
| 135 | Lactitol | Uống: các dạng |
|
| 136 | Lactoserum atomisate | Dùng ngoài |
|
| 137 | Lactulose | Uống: các dạng |
|
| 138 | L-Carnitin dạng đơn thành phần hoặc phối hợp với các vitamin | Uống: các dạng |
|
| 139 | Levocetirizin | Uống: các dạng |
|
| 140 | Levonorgestrel đơn thành phần hoặc phối hợp với Ethylestradiol | Uống: các dạng | * Thuốc chỉ được phê duyệt với chỉ định tránh thai |
| 141 | Lidocain đơn thành phần hoặc phối hợp | Dùng ngoài |
|
| 142 | Lindan (Benhexachlor, 666, Gamma-BHC) đơn thành phần hoặc phối hợp với Lidocain | Dùng ngoài với nồng độ Lindan ≤ 1% |
|
| 143 | Loperamid | Uống: các dạng với giới hạn hàm lượng đã chia liều Loperamid ≤ 2mg |
|
| 144 | Loratadin đơn thành phần hoặc phối hợp Pseudoephedrin Hydrochlorid và /hoặc Paracetamol | Uống: các dạng với giới hạn hàm lượng như sau (tính theo dạng base): - Đã chia liều: Loratadin ≤ 10mg/đơn vị; - Chưa chia liều: Loratadin ≤ 0,1% | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 145 | Loxoprofen | Uống: các dạng |
|
| 146 | Macrogol | Uống: các dạng Thuốc thụt trực tràng |
|
| 147 | Magaldrat đơn thành phần hoặc phối hợp với các hợp chất Nhôm, Magnesi, Acid Alginic (hay dạng muối Alginat). | Uống: các dạng |
|
| 148 | Magnesi bao gồm các dạng muối, hợp chất của magnesi | Uống: các dạng | Với các chỉ định bổ sung magnesi cho cơ thể, trung hòa acid dịch vị, nhuận tràng. |
| 149 | Mangiferin | Dùng ngoài |
|
| 150 | Mebendazol | Uống: các dạng, với giới hạn hàm lượng như sau: - Dạng chia liều ≤ 500mg/đơn vị - Chưa chia liều ≤ 2% |
|
| 151 | Mebeverin | Uống: dạng chia liều ≤ 200mg/đơn vị |
|
| 152 | Men nấm (cellulase fongique) | Uống: các dạng |
|
| 153 | Men tiêu hóa dạng đơn thành phần hoặc phối hợp bao gồm phối hợp với các vitamin | Uống: các dạng |
|
| 154 | Menthol phối hợp với một số hoạt chất khác như hỗn hợp tinh dầu, Methyl Salycilat.... | Uống: các dạng Dùng ngoài: các dạng |
|
| 155 | Mequinol | Dùng ngoài |
|
| 156 | Mequitazin | Uống: các dạng Dùng ngoài |
|
| 157 | Mercurocrom (Thuốc đỏ) | Dùng ngoài với quy cách đóng gói ≤ 30ml | Bán không đơn mỗi lần không quá 2 đơn vị đóng gói |
| 158 | Methyl salicylat phối hợp trong các thành phẩm viên ngậm, dùng ngoài (phối hợp với tinh dầu...) | Dùng ngoài Miếng dán Viên ngậm |
|
| 159 | Metronidazol | Dùng ngoài |
|
| 160 | Miconazol | Dùng ngoài Thuốc bôi âm đạo ≤ 2% |
|
| 161 | Miconazole phối hợp với Hydrocortison | Dùng ngoài Thuốc bôi âm đạo Miconazol ≤2%; Hydrocortison ≤0,05% |
|
| 162 | Minoxidil | Dùng ngoài: các dạng nồng độ ≤5% |
|
| 163 | Mometasone | Thuốc tra mũi: ≤ 50 mcg/lần xịt với quy cách đóng gói ≤ 200 liều/hộp; Dùng ngoài. |
|
| 164 | Mupirocin | Dùng ngoài |
|
| 165 | Myrtol đơn thành phần hoặc phối hợp trong các thành phẩm viên ngậm | Uống: các dạng Dùng ngoài |
|
| 166 | Naphazolin đơn thành phần hoặc phối hợp trong thành phẩm thuốc mũi như Diphenylhydramin và/hoặc Procain | Thuốc tra mũi với nồng độ Naphazolin ≤ 0,05% |
|
| 167 | Naphazolin phối hợp trong thành phẩm thuốc tra mắt (Pheniramin; Vitamin glycyrhizinat, Dexpanthenol...) | Thuốc tra mắt: các dạng với nồng độ Naphazolin ≤ 0,1%, |
|
| 168 | Naproxen | Uống: các dạng đã chia liều với giới hạn hàm lượng ≤ 275mg/đơn vị |
|
| 169 | Natri benzoat đơn thành phần hoặc phối hợp | Uống: các dạng |
|
| 170 | Natri bicacbonat đơn thành phần hoặc phối hợp | Uống: các dạng |
|
| 171 | Natri carbonat đơn thành phần hoặc phối hợp | Uống: các dạng |
|
| 172 | Natri Carboxymethylcellulose (Na CMC) | Thuốc tra mắt |
|
| 173 | Natri clorid đơn thành phần hoặc phối hợp với các muối Kali Citrat, Natri citrat... | Uống: các dạng Dùng ngoài Thuốc tra mắt, tra mũi với nồng độ 0,9% |
|
| 174 | Natri Docusat | Uống: các dạng |
|
| 175 | Natri Fluorid dạng phối hợp | Dùng ngoài: đánh răng, súc miệng |
|
| 176 | Natri Hyaluronat (Acid Hyaluronic) | Dùng ngoài Dung dịch nhỏ mắt với nồng độ ≤ 0,1% |
|
| 177 | Natri Monofluorophosphat | Dùng ngoài, bao gồm các dạng làm sạch khoang miệng, niêm mạc |
|
| 178 | Natri Salicylat dạng phối hợp | Uống: dạng phối hợp trong các viên ngậm Dùng ngoài |
|
| 179 | Neomycin sulfat phối hợp trong các thành phẩm viên ngậm (Kẽm; Bacitracin; Amylocain...), các thành phẩm dùng ngoài | Uống: viên ngậm Dùng ngoài |
|
| 180 | Nguyên tố vi lượng: crôm, đồng, kali, magnesi, mangan, kẽm, …dạng đơn thành phần hoặc phối hợp, bao gồm cả các dạng phối hợp với các Vitamin. | Uống: các dạng | Với chỉ định bổ sung khoáng chất cho cơ thể. |
| 181 | Nhôm, magnesi, calci và các hợp chất của nhôm, magnesi, calci dạng đơn thành phần hoặc phối hợp | Uống: các dạng | Với chỉ định trung hòa acid dịch vị, chữa loét dạ dày, hành tá tràng. |
| 182 | Nonahydrated Natri Sulfid + Saccharomyces Cerevisiae | Uống: các dạng Dùng ngoài |
|
| 183 | Noscarpin | Uống: các dạng |
|
| 184 | Nystatin đơn thành phần hoặc phối hợp | Dùng ngoài |
|
| 185 | Omeprazol | Uống: dạng đã chia liều với hàm lượng ≤ 10mg/đơn vị | Với chỉ định ợ nóng. Chỉ được bán tối đa 1 lần không có đơn với số lượng cho 14 ngày sử dụng và liều mỗi ngày ≤ 20mg |
| 186 | Orlistat | Uống: các dạng |
|
| 187 | Ossein hydroxy apatit | Uống: các dạng |
|
| 188 | Oxeladin | Uống: các dạng |
|
| 189 | Oxomemazin | Uống: các dạng |
|
| 190 | Oxymetazolin | Thuốc tra mũi với nồng độ ≤ 0,5% |
|
| 191 | Pancreatin đơn thành phần hoặc phối hợp với Simethicon và/hoặc các men tiêu hóa và/hoặc các Vitamin nhóm B và/hoặc Azintamid | Uống: các dạng | . |
| 192 | Panthenol | Dùng ngoài Thuốc tra mắt |
|
| 193 | Paracetamol đơn thành phần | Uống: các dạng Thuốc đặt hậu môn | Dạng phối hợp quy định cụ thể trong danh mục |
| 194 | Paracetamol phối hợp với các hoạt chất có trong Danh mục này có tác dụng chữa ho, hạ nhiệt, giảm đau, chống dị ứng | Uống: các dạng | Thành phẩm phối hợp có chứa các hoạt chất có quy định giới hạn hàm lượng, số lượng bán lẻ tối đa 1 lần, ghi số bán lẻ thì phải thực hiện theo quy định cụ thể đối với các hoạt chất đó |
| 195 | Pentoxyverin | Uống: các dạng |
|
| 196 | Phenylephrin Hydrochlorid | Thuốc tra mắt, nhỏ mũi nồng độ ≤ 1% |
|
| 197 | Phenylephrin Hydrochlorid phối hợp trong các thành phẩm dùng ngoài (như Petrolatum sperti yellow; Mineral oil light; Shark liver oil...) | Dùng ngoài |
|
| 198 | Phenylephrin Hydrochlorid phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau | Uống: các dạng Thuốc đặt hậu môn |
|
| 199 | Phospholipid | Uống: các dạng |
|
| 200 | Picloxydin | Thuốc tra mắt |
|
| 201 | Piroxicam | Dùng ngoài: các dạng với nồng độ ≤ 1% |
|
| 202 | Policresulen (Metacresolsulphonic acid-formaldehyd) | Dùng ngoài Thuốc đặt trực tràng |
|
| 203 | Polyethylen glycol 400 đơn thành phần hoặc phối hợp với Propylen glycol | Thuốc tra mắt | . |
| 204 | Polysacharid | Uống: các dạng |
|
| 205 | Polytar dạng đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài (như Kẽm Pyrithion...) | Dùng ngoài |
|
| 206 | Povidon Iodin | Dùng ngoài: các dạng (bao gồm dung dịch súc miệng với nồng độ ≤ 1%). Thuốc tra mắt |
|
| 207 | Promethazin Hydrochlorid đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau (với Carbocystein; Paracetamol...) | Uống: các dạng với giới hạn hàm lượng, nồng độ Promethazin như sau (tính theo dạng base): - Đã chia liều ≤ 12,5mg/ đơn vị; - Chưa chia liều ≤ 0,1% Dùng ngoài: nồng độ ≤ 2% |
|
| 208 | Pseudoephedrin Hydrochlorid phối hợp với Cetirizin | Uống: các dạng với giới hạn Pseudoephedrin như sau (tính theo dạng base): - Dạng chia liều ≤ 120mg/đơn vị; - Dạng chưa chia liều ≤ 0,5% | Thành phẩm chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 209 | Pseudoephedrin Hydrochlorid phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau, chống dị ứng | Uống: các dạng với giới hạn Pseudoephedrin như sau (tính theo dạng base): - Dạng chia liều ≤120mg/ đơn vị; - Dạng chưa chia liều ≤ 0,5% | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 210 | Pyrantel | Uống: các dạng | Chỉ định trị giun |
| 211 | Ranitidin | Uống: các dạng đã chia liều ≤ 75mg | Bán tối đa không có đơn cho 15 ngày sử dụng. Chỉ định điều trị chứng ợ nóng |
| 212 | Rutin đơn thành phần hoặc phối hợp với Vitamin C và/hoặc các cao, dịch chiết từ dược liệu | Uống: các dạng |
|
| 213 | Saccharomyces boulardic | Uống: các dạng |
|
| 214 | Saccharomyces cerevisiae với Trihydrat Magnesi Sulfat | Uống: các dạng |
|
| 215 | Sắt dạng hợp chất đơn thành phần hoặc phối hợp trong các thành phẩm chứa vitamin, khoáng chất | Uống: các dạng | Với chỉ định bổ sung sắt cho cơ thể. |
| 216 | Selen hữu cơ dạng phối hợp trong các thành phẩm chứa Vitamin, khoáng chất | Uống: các dạng với giới hạn hàm lượng như sau: - Dạng đã chia liều Selen ≤ 50mcg/ đơn vị |
|
| 217 | Selen sulfid | Dùng ngoài |
|
| 218 | Silymarin đơn thành phần hoặc phối hợp với các Vitamin và/hoặc các cao, dịch chiết từ dược liệu. | Uống: các dạng |
|
| 219 | Simethicon đơn thành phần hoặc phối hợp với Pancreatin và/hoặc Acid Desoxycholic và/hoặc các Vitamin nhóm B và/hoặc các men tiêu hóa | Uống: các dạng |
|
| 220 | Simethicon phối hợp với các hợp chất nhôm, magnesi, và/hoặc Dicyclomin và/hoặc than hoạt | Uống: các dạng |
|
| 221 | Sorbitol đơn thành phần hoặc phối hợp | Uống: các dạng |
|
| 222 | Sterculia (gum sterculia) | Uống: các dạng Thuốc thụt trực tràng |
|
| 223 | Sucralfat | Uống: các dạng |
|
| 224 | Sulbutiamin | Uống: các dạng |
|
| 225 | Sulfogaiacol (hoặc Sulfoguaiacol) đơn thành phần hoặc phối hợp trong các thành phẩm hạ nhiệt, giảm đau, chống ho | Uống: các dạng |
|
| 226 | Terbinafin | Dùng ngoài: các dạng với nồng độ ≤ 1% |
|
| 227 | Terpin đơn thành phần hoặc phối hợp với Codein | Uống: các dạng. Dạng phối hợp Codein (tính theo dạng base) giới hạn hàm lượng như sau: - Dạng chia liều ≤ 12mg/đơn vị; - Dạng chưa chia liều ≤ 2,5% | Thành phẩm chứa Codein được bán không cần đơn với số lượng tối đa cho 10 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 228 | Tetrahydrozolin | Thuốc tra mũi |
|
| 229 | Than hoạt đơn thành phần hoặc phối hợp với Simethicon | Uống: các dạng |
|
| 230 | Tinh dầu (bao gồm nhóm các chất Menthol, Pinen, Camphor, Cineol, Fenchone, Borneol, Anethol, Eucalyptol...) | Uống: các dạng Dùng ngoài: thuốc bôi ngoài da Nước súc miệng, thuốc bôi niêm mạc miệng |
|
| 231 | Tioconazol đơn thành phần hoặc phối hợp với Hydrocortison | Dùng ngoài: các dạng với nồng độ như sau: - Tioconazol ≤ 1,00% - Hydrocortison ≤ 0,05% |
|
| 232 | Tolnaftat | Dùng ngoài |
|
| 233 | Triclosan đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài | Dùng ngoài |
|
| 234 | Triprolidin đơn thành phần hoặc phối hợp trong các thành phẩm thuốc ho, hạ nhiệt, giảm đau. | Uống: các dạng | Tất cả các thuốc thành phẩm có chứa Pseudoephedrin được bán không cần đơn với số lượng tối đa cho 15 ngày sử dụng. Cơ sở bán lẻ phải theo dõi tên, địa chỉ người mua trong sổ bán lẻ. |
| 235 | Trolamin đơn thành phần hoặc phối hợp trong các thành phẩm dùng ngoài (với Triclosan và/hoặc Tyrothricin) | Dùng ngoài |
|
| 236 | Tyrothricin đơn thành phần hoặc phối hợp (với Benzalkonium, Benzocain, Formaldehyd, Trolamin, tinh dầu, các thành phần trong tinh dầu) | Uống: viên ngậm Dùng ngoài: dung dịch súc miệng, xịt miệng, bôi ngoài da |
|
| 237 | Urea đơn thành phần hoặc phối hợp với Vitamin E và/hoặc Bifonazol và/hoặc các dược liệu không thuộc Danh mục dược liệu độc do Bộ trưởng Bộ Y tế ban hành | Dùng ngoài |
|
| 238 | Vitamin A và tiền Vitamin A (Betacaroten) dạng đơn thành phân và phối hợp với các vitamin | Uống: các dạng với giới hạn hàm lượng Vitamin A < 5000 IU/đơn vị Dùng ngoài Thuốc tra mắt |
|
| 239 | Vitamin dạng đơn thành phần (trừ Vitamin D dạng đơn thành phần) hoặc dạng phối hợp các Vitamin, khoáng chất, Acid Amin, các Acid béo, Taurin, Lutein, Zeaxanthin | Uống: các dạng Dùng ngoài Các phối hợp dạng uống có chứa Vitamin A thực hiện giới hạn hàm lượng như sau: Vitamin A ≤ 5000 IU/đơn vị chia liều | Với tác dụng bổ sung Vitamin, khoáng chất và dinh dưỡng |
| 240 | Vitamin nhóm B, Vitamin PP đơn thành phần hoặc phối hợp | Thuốc tra mắt |
|
| 241 | Vi khuẩn có lợi cho đường tiêu hóa: Bacillus claussi, Bacillus subtilis, Lactobacillus acidophilus dạng đơn thành phần hoặc phối hợp, bao gồm cả dạng phối hợp với các vitamin | Uống: các dạng |
|
| 242 | Xanh Methylen | Dùng ngoài |
|
| 243 | Xylometazolin đơn thành phần hoặc phối hợp với Benzalkonium. | Thuốc tra mũi với giới hạn nồng độ Xylometazolin ≤ 1% |
|
* Đối với các thuốc có chỉ định tránh thai thuộc Danh mục này, người bán lẻ thuốc là dược sỹ đại học hoặc người chịu trách nhiệm chuyên môn về dược của cơ sở bán lẻ thuốc có trách nhiệm cung cấp và tư vấn các thông tin liên quan đến thuốc, bao gồm: tên thuốc, công dụng, chỉ định, chống chỉ định, liều dùng, cách dùng và những vấn đề cần lưu ý trong quá trình sử dụng thuốc trước khi cấp phát hoặc bán cho người sử dụng.
II. QUY ĐỊNH THUỐC DƯỢC LIỆU, THUỐC CỔ TRUYỀN (TRỪ VỊ THUỐC CỔ TRUYỀN) KHÔNG KÊ ĐƠN
Thuốc dược liệu, thuốc cổ truyền (trừ vị thuốc cổ truyền) đáp ứng đồng thời các tiêu chí sau được phân loại là thuốc không kê đơn:
1. Trong thành phần không chứa dược liệu thuộc Danh mục dược liệu độc do Bộ trưởng Bộ Y tế ban hành.
2. Không được có một trong các chỉ định sau:
a) Hỗ trợ điều trị hoặc điều trị bệnh ung thư, khối u;
b) Điều trị bệnh tim mạch, huyết áp;
c) Điều trị bệnh về gan, mật hoặc tụy (trừ chỉ định: bổ gan);
d) Điều trị Parkinson;
đ) Điều trị virus;
e) Điều trị nấm (trừ thuốc dùng ngoài);
g) Điều trị lao;
h) Điều trị sốt rét;
i) Điều trị bệnh gút;
k) Điều trị hen;
l) Điều trị bệnh về nội tiết;
m) Điều trị bệnh hoặc rối loạn về máu;
n) Điều trị bệnh hoặc rối loạn về miễn dịch;
o) Điều trị các bệnh về thận và sinh dục - tiết niệu (trừ chỉ định: bổ thận, tráng dương);
p) Điều trị bệnh nhiễm khuẩn (trừ chỉ định dùng tại chỗ để điều trị nhiễm khuẩn ngoài da);
q) Điều trị mất ngủ kinh niên, mạn tính;
r) Điều trị bệnh về tâm lý - tâm thần;
s) Điều trị tình trạng nghiện, hỗ trợ điều trị tình trạng nghiện (bao gồm cả hỗ trợ điều trị cắt cơn nghiện);
t) Đình chỉ thai kỳ;
u) Điều trị các bệnh dịch nguy hiểm, mới nổi theo quy định của Bộ trưởng Bộ Y tế.
III. QUY ĐỊNH VỊ THUỐC CỔ TRUYỀN KHÔNG KÊ ĐƠN
Vị thuốc cổ truyền được phân loại là không kê đơn nếu vị thuốc này không được sản xuất, chế biến từ dược liệu thuộc Danh mục dược liệu độc do Bộ trưởng Bộ Y tế ban hành./.
PHỤ LỤC 2.
DANH MỤC THUỐC HẠN CHẾ BÁN LẺ
(Ban hành kèm theo Thông tư số 07/2018/TT-BYT ngày 12 tháng 4 năm 2018 của BYT)
| TT | Thành phần hoạt chất | Đường dùng, dạng bào chế, giới hạn hàm lượng, nồng độ | Các quy định cụ thể |
| 1 | Artesunat phối hợp với Amodiaquin hoặc piperaquin hoặc Mefloquin hoặc Pironaridin | Uống: các dạng | Thuốc điều trị sốt rét |
| 2 | Artemether phối hợp với Lumefantrin | Uống: các dạng | Thuốc điều trị sốt rét |
| 3 | Piperaquin phối hợp với Dihydroartemisinin | Uống: các dạng | Thuốc điều trị sốt rét |
| 4 | Isoniazid đơn thành phần hoặc phối hợp với Rifampicin và/hoặc Pyrazinamid | Uống: các dạng | Thuốc điều trị lao |
| 5 | Pyrazinamid đơn thành phần hoặc phối hợp với Rifampicin, Isoniazid | Uống: các dạng | Thuốc điều trị lao |
| 6 | Ethambutol đơn thành phần hoặc phối hợp với Rifampicin, Isoniazid | Uống: các dạng | Thuốc điều trị lao |
| 7 | Streptomycin | Đường tiêm: các dạng | Thuốc điều trị lao |
| 8 | Kanamycin | Đường tiêm: các dạng | Thuốc điều trị lao |
| 9 | Amikacin | Đường tiêm: các dạng | Thuốc điều trị lao |
| 10 | Capreomycin | Đường tiêm: các dạng | Thuốc điều trị lao |
| 11 | Prothionamid | Uống: các dạng | Thuốc điều trị lao |
| 12 | Cycloserin | Uống: các dạng | Thuốc điều trị lao |
| 13 | Para aminosalicylic acid (PAS) | Uống: các dạng | Thuốc điều trị lao |
| 14 | Levofloxacin | Uống: các dạng | Thuốc điều trị lao |
| 15 | Moxifloxacin | Uống: các dạng | Thuốc điều trị lao |
| 16 | Abacavir đơn thành phần hoặc phối hợp với Lamivudin | Uống: các dạng | Thuốc điều trị HIV |
| 17 | Efavirenz đơn thành phần hoặc phối hợp với Tenofovir, Emtricitabin | Uống: các dạng | Thuốc điều trị HIV |
| 18 | Lamivudin đơn thành phần hoặc phối hợp với (Tenofovir, hoặc/và Efavirenz, hoặc/và Zidovudin, hoặc/và Nevirapin) | Uống: các dạng | Thuốc điều trị HIV |
| 19 | Ritonavir đơn thành phần hoặc phối hợp với Lopinavir | Uống: các dạng | Thuốc điều trị HIV |
| 20 | Nevirapine | Uống: các dạng | Thuốc điều trị HIV |
| 21 | Tenofovir | Uống: các dạng | Thuốc điều trị HIV |
| 22 | Zidovudin | Uống: các dạng | Thuốc điều trị HIV |
| 23 | Các thuốc được Bộ Y tế cấp giấy đăng ký lưu hành quản lý đặc biệt trong đó có yêu cầu hạn chế bán lẻ |
|
|
PHỤ LỤC 3.
DANH MỤC THUỐC ĐỘC VÀ NGUYÊN LIỆU ĐỘC LÀM THUỐC
(Ban hành kèm theo Thông tư số: 06/2017/TT-BYT ngày 03 tháng 5 năm 2017 của Bộ trưởng Bộ Y tế)
| TT | Nguyên liệu độc/ Thuốc chứa nguyên liệu độc | Đường dùng, dạng bào chế của thuốc độc |
| 1 | Abirateron | Uống: các dạng |
| 2 | Acid valproic | Uống: các dạng; Tiêm: các dạng |
| 3 | Anastrozol | Uống: các dạng |
| 4 | Arsenic trioxid | Tiêm: các dạng |
| 5 | Atracurium besylat | Tiêm: các dạng |
| 6 | Atropin sulfat | Tiêm: các dạng |
| 7 | Azacitidin | Tiêm: các dạng |
| 8 | Bicalutamid | Uống: các dạng |
| 9 | Bleomycin | Tiêm: các dạng |
| 10 | Bortezomib | Tiêm: các dạng |
| 11 | Botulinum toxin | Tiêm: các dạng |
| 12 | Bupivacain | Tiêm: các dạng |
| 13 | Capecitabin | Uống: các dạng |
| 14 | Carbamazepin | Uống: các dạng |
| 15 | Carboplatin | Tiêm: các dạng |
| 16 | Carmustin | Tiêm: các dạng |
| 17 | Cetrorelix | Tiêm: các dạng |
| 18 | Chlorambucil | Uống: các dạng |
| 19 | Choriogonadotropin alfa | Tiêm: các dạng |
| 20 | Cisplatin | Tiêm: các dạng |
| 21 | Colistin | Tiêm: các dạng |
| 22 | Conjugated Oestrogens | Uống: các dạng |
| 23 | Cyclophosphamid | Uống: các dạng; Tiêm: các dạng |
| 24 | Cyclosporin | Uống: các dạng |
| 25 | Cytarabin | Tiêm: các dạng |
| 26 | Dacarbazine | Tiêm: các dạng |
| 27 | Dactinomycin | Tiêm: các dạng |
| 28 | Daunorubicin | Tiêm: các dạng |
| 29 | Degarelix | Tiêm: các dạng |
| 30 | Desflurane | Khí hóa lỏng |
| 31 | Dexmedetomidin | Tiêm: các dạng |
| 32 | Docetaxel | Tiêm: các dạng |
| 33 | Doxorubicin | Tiêm: các dạng |
| 34 | Entecavir | Uống: các dạng |
| 35 | Epirubicin | Tiêm: các dạng |
| 36 | Erlotinib | Uống: các dạng |
| 37 | Estradiol | Tiêm: các dạng |
| 38 | Etoposide | Uống: các dạng; Tiêm: các dạng |
| 39 | Everolimus | Uống: các dạng |
| 40 | Exemestane | Uống: các dạng |
| 41 | Fludarabine | Tiêm: các dạng |
| 42 | Fluorouracil (5-FU) | Tiêm: các dạng |
| 43 | Flutamide | Uống: các dạng |
| 44 | Fulvestrant | Tiêm: các dạng |
| 45 | Ganciclovir | Tiêm: các dạng |
| 46 | Ganirelix | Tiêm: các dạng |
| 47 | Gefitinib | Uống: các dạng |
| 48 | Gemcitabine | Tiêm: các dạng |
| 49 | Goserelin | Tiêm: các dạng |
| 50 | Halothan | Khí hóa lỏng |
| 51 | Hydroxyurea | Uống: các dạng |
| 52 | Ifosfamide | Tiêm: các dạng |
| 53 | Imatinib | Uống: các dạng |
| 54 | Irinotecan | Tiêm: các dạng |
| 55 | Isofluran | Khí hóa lỏng |
| 56 | Lenalidomide | Uống: các dạng |
| 57 | Letrozole | Uống: các dạng |
| 58 | Leuprorelin (Leuprolide) | Tiêm: các dạng |
| 59 | Levobupivacain | Tiêm: các dạng |
| 60 | Medroxy progesterone acetate | Tiêm: các dạng |
| 61 | Menotropin | Tiêm: các dạng |
| 62 | Mepivacain | Tiêm: các dạng |
| 63 | Mercaptopurine | Uống: các dạng |
| 64 | Methotrexate | Uống: các dạng; Tiêm: các dạng |
| 65 | Methyltestosteron | Uống: các dạng |
| 66 | Mitomycin C | Tiêm: các dạng |
| 67 | Mitoxantrone | Tiêm: các dạng |
| 68 | Mycophenolate | Uống: các dạng |
| 69 | Neostigmin metylsulfat | Tiêm: các dạng |
| 70 | Nilotinib | Uống: các dạng |
| 71 | Octreotide | Tiêm: các dạng |
| 72 | Oxaliplatin | Tiêm: các dạng |
| 73 | Oxcarbazepine | Uống: các dạng |
| 74 | Oxytocin | Tiêm: các dạng |
| 75 | Paclitaxel | Tiêm: các dạng |
| 76 | Pamidronat disodium | Uống: các dạng; Tiêm: các dạng |
| 77 | Pancuronium bromid | Tiêm: các dạng |
| 78 | Pazopanib | Uống: các dạng |
| 79 | Pemetrexed | Tiêm: các dạng |
| 80 | Pipecuronium bromid | Tiêm: các dạng |
| 81 | Procain hydroclorid | Tiêm: các dạng |
| 82 | Progesterone | Tiêm: các dạng |
| 83 | Propofol | Tiêm: các dạng |
| 84 | Pyridostigmin bromid | Tiêm: các dạng |
| 85 | Ribavirin | Uống: các dạng; Tiêm: các dạng |
| 86 | Rocuronium bromide | Tiêm: các dạng |
| 87 | Ropivacaine | Tiêm: các dạng |
| 88 | Sevofluran | Khí hóa lỏng |
| 89 | Sirolimus | Uống: các dạng |
| 90 | Sorafenib | Uống: các dạng |
| 91 | Sunitinib | Uống: các dạng |
| 92 | Suxamethonium clorid | Tiêm: các dạng |
| 93 | Tacrolimus | Uống: các dạng; Tiêm: các dạng |
| 94 | Talniflumat | Uống: các dạng |
| 95 | Tamoxifen | Uống: các dạng |
| 96 | Temozolomide | Uống: các dạng |
| 97 | Testosterone | Uống: các dạng; Tiêm: các dạng |
| 98 | Thalidomide | Uống: các dạng |
| 99 | Thiopental | Tiêm: các dạng |
| 100 | Thiotepa | Tiêm: các dạng |
| 101 | Thymosin alpha I | Tiêm: các dạng |
| 102 | Topotecan | Uống: các dạng; Tiêm: các dạng |
| 103 | Triptorelin | Tiêm: các dạng |
| 104 | Tritenoin (All-Trans Retinoic Acid) | Uống: các dạng |
| 105 | Valganciclovir | Uống: các dạng |
| 106 | Vecuronium bromide | Tiêm: các dạng |
| 107 | Vinblastine | Tiêm: các dạng |
| 108 | Vincristin | Tiêm: các dạng |
| 109 | Vinorelbine | Tiêm: các dạng |
| 110 | Zidovudine | Uống: các dạng |
| 111 | Ziprasidone | Uống: các dạng |
* Danh mục này bao gồm cả các muối của các chất ghi trong Bảng này, khi các muối đó có thể hình thành và tồn tại./.
PHỤ LỤC 4.
DANH MỤC THUỐC DƯỢC CHẤT THUỘC DANH MỤC CHẤT BỊ CẤM SỬ DỤNG TRONG MỘT SỐ NGÀNH LĨNH VỰC
(Kèm theo Thông tư số: 20/2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| TT | Dược chất |
| 1 | 19 Nor-testosterone (tên gọi khác là Nandrolone) |
| 2 | Amifloxacin |
| 3 | Aristolochia |
| 4 | Azathioprine |
| 5 | Bacitracin Zn |
| 6 | Balofloxacin |
| 7 | Benznidazole |
| 8 | Besifloxacin |
| 9 | Bleomycin |
| 10 | Carbuterol |
| 11 | Chloramphenicol |
| 12 | Chloroform |
| 13 | Chlorpromazine |
| 14 | Ciprofloxacin |
| 15 | Colchicine |
| 16 | Dalbavancin |
| 17 | Dapsone |
| 18 | Diethylstilbestrol (DES) |
| 19 | Enoxacin |
| 20 | Fenoterol |
| 21 | Fleroxacin |
| 22 | Furazidin |
| 23 | Furazolidon |
| 24 | Garenoxacin |
| 25 | Gatifloxacin |
| 26 | Gemifloxacin |
| 27 | Isoxsuprine |
| 28 | Levofloxacin |
| 29 | Lomefloxacin |
| 30 | Methyl-testosterone |
| 31 | Metronidazole |
| 32 | Moxifloxacin |
| 33 | Nadifloxacin |
| 34 | Nifuratel |
| 35 | Nifuroxime |
| 36 | Nifurtimox |
| 37 | Nifurtoinol |
| 38 | Nimorazole |
| 39 | Nitrofurantoin |
| 40 | Nitrofurazone |
| 41 | Norfloxacin |
| 42 | Norvancomycin |
| 43 | Ofloxacin |
| 44 | Oritavancin |
| 45 | Ornidazole |
| 46 | Pazufloxacin |
| 47 | Pefloxacin |
| 48 | Prulifloxacin |
| 49 | Ramoplanin |
| 50 | Rufloxacin |
| 51 | Salbutamol |
| 52 | Secnidazole |
| 53 | Sitafloxacin |
| 54 | Sparfloxacin |
| 55 | Teicoplanin |
| 56 | Terbutaline |
| 57 | Tinidazole |
| 58 | Tosufloxacin |
| 59 | Trovafloxacin |
| 60 | Vancomycin |
*Áp dụng trong các ngành, lĩnh vực sản xuất, kinh doanh thủy sản, thú y, chăn nuôi gia súc, gia cầm tại Việt Nam.
PHỤ LỤC 5.
DANH MỤC DƯỢC CHẤT GÂY NGHIỆN
(Kèm theo Thông tư số: 20/2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| T | TÊN QUỐC TẾ | TÊN KHOA HỌC |
| 1 | ACETYLDIHYDROCODEIN | (5 α, 6 α) - 4,5 - epoxy - 3 - methoxy - 17 methyl - morphinan - 6 - yl - acetat |
| 2 | ALFENTANIL | N - [1 - [2 - (4 - ethyl - 4,5 - dihydro - 5 - oxo - 1 H - tetrazol - 1 - yl) ethyl] - 4 - (methoxymethyl) - 4 - piperidinyl] - N - Phenylpropanamide |
| 3 | ALPHAPRODINE | α - 1,3 - dimethyl - 4 - phenyl - 4 - propionoxypiperidine |
| 4 | ANILERIDINE | 1 - para-aminophenethyl - 4 - phenylpiperidine - 4 - carboxylic acid ethyl ester) |
| 5 | BEZITRAMIDE | (1 - (3 - cyano - 3, 3 - diphenylpropyl) - 4 (2 - oxo - 3 - propionyl - 1 - benzimidazolinyl) - piperidine) |
| 6 | BUTORPHANOL | (-) - 17 - (cyclobutylmethyl) morphinan - 3,14 diol |
| 7 | CIRAMADOL | (-) - 2 - (α - Dimethylamino - 3 - hydroxybenzyl) Cyclohexanol |
| 8 | COCAINE | Methyl ester của benzoylecgonine |
| 9 | CODEINE | (3 - methylmorphine) |
| 10 | DEXTROMORAMIDE | ((+) - 4 [2 - methyl - 4 - oxo -3,3 - diphnyl - 4 (1 - pyrrolidinyl) - butyl] - morpholine) |
| 11 | DEZOCIN | (-)- 13 β- Amino- 5,6,7,8,9,10,11 α, 12 octahydro- 5α- methyl-5, 11- methanobenzo- cyclodecen-3- ol |
| 12 | DIFENOXIN | (1- (3 cyano- 3,3- Diphenylpropyl)- 4- Phenylisonipecotic acid |
| 13 | DIHYDROCODEIN | 6- hydroxy- 3- methoxy-N- methyl-4,5-epoxy- morphinan |
| 14 | DIPHENOXYLATE | 1-(3-cyano-3,3-diphenylpropyl)-4- phenylpiperidine-4-carboxylic acid ethyl ester |
| 15 | DIPIPANONE | 4,4- Diphenyl-6- Piperidino-3- heptanone. |
| 16 | DROTEBANOL | (3,4- Dimethoxy- 17- Methyl morphinan-6 β, 14 diol) |
| 17 | ETHYL MORPHIN | 3- Ethylmorphine |
| 18 | FENTANYL | (1- Phenethyl-4-N- Propionylanilinopiperidine) |
| 19 | HYDROMORPHONE | (Dihydromorphinone) |
| 20 | KETOBEMIDON | (4- meta- hydroxyphenyl-1- methyl-4- propionylpiperidine) |
| 21 | LEVOMETHADON | (3- Heptanone, 6- (dimethylamino)-4,4- Diphenyl, (R) |
| 22 | LEVORPHANOL | ((-)- 3- hydroxy- N- methylmorphinan) |
| 23 | MEPTAZINOL | (3(3- Ethyl-1- methylperhydroazepin-3- yl) phenol |
| 24 | METHADONE | (6- dimethylamino- 4,4- diphenyl-3- heptanone) |
| 25 | MORPHINE | Morphinan-3,6 diol, 7,8-didehydro- 4,5- epoxy- 17 methyl - (5 α, 6 α) |
| 26 | MYROPHINE | MyristylBenzylmorphine |
| 27 | NALBUPHIN | 17- Cyclobutylmethyl- 7,8- dihydro- 14- hydroxy- 17- normorphine |
| 28 | NICOCODINE | Morphinan- 6- ol, 7,8- Dihydrro- 4,5- epoxy- 3- methoxy- 17- methyl- 3- pyridin mecarboxxylate (ester), (5α, 6α) |
| 29 | NICODICODINE | 6- Nicotinyldihydrocodeine |
| 30 | NICOMORPHINE | 3,6- Dinicotinylmorphine) |
| 31 | NORCODEINE | N- Dimethylcodein |
| 32 | OXYCODONE | (14- hydroxydihydrocodeinone) |
| 33 | OXYMORPHONE | (14- hydroxydihydromorphinone) |
| 34 | PETHIDINE | (1- methyl-4- phenylpiperidine-4- carboxylic acid ethyl ester) |
| 35 | PHENAZOCINE | (2’- Hydroxy-5,9- Dimethyl-2- Phenethyl-6,7- Benzomorphan) |
| 36 | PHOLCODIN | (Morpholinylethylmorphine) |
| 37 | PIRITRAMIDE | (1-(3- cyano-3,3- diphenylpropyl-4-(1- piperidino)- piperidine- 4- carboxylic acid amide) |
| 38 | PROPIRAM | (N- (1- Methyl- 2 piperidinoethyl- N- 2- pyridyl Propionamide) |
| 39 | REMIFENTANIL | 1-(2-methoxy carbonylethyl)-4- (phenylpropionylamino)piperidine-4- carboxylic acid methyl ester |
| 40 | SUFENTANIL | (N-[4- (methoxymethyl)-1- [2- (2- thienyl)- ethyl]-4- piperidyl]- propionanilide) |
| 41 | THEBACON | (Acetyldihydrocodeinone) |
| 42 | TONAZOCIN MESYLAT | (±)-1-[(2R*,6S*,11S*)- 1,2,3,4,5,6- hexahydro- 8- hydroxy- 3,6,11- trimethyl- 2,6- methano-3- Benzazocin- 11- yl]-3-one-methanesulphonate |
| 43 | TRAMADOL | (±)- Trans- 2- Dimethylaminomethyl-1- (3- methoxy phenyl) cyclohexan-1-ol |
Danh mục này bao gồm:
- Đồng phân của các chất trên nếu nó tồn tại dưới dạng tên của một chất hóa học cụ thể.
- Các ester và ether của các chất trên nếu chúng tồn tại trừ trường hợp chúng xuất hiện ở các danh mục khác.
- Muối của các chất trên, bao gồm cả các muối của ester, ether và những đồng phân của các chất trên nếu tồn tại.
PHỤ LỤC 6
DANH MỤC DƯỢC CHẤT HƯỚNG THẦN
(Kèm theo Thông tư số: 20 /2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| TT | TÊN QUỐC TẾ | TÊN THÔNG DỤNG KHÁC | TÊN KHOA HỌC |
| 1 | ALLOBARBITAL |
| 5,5-diallylbarbituric acid |
| 2 | ALPRAZOLAM |
| 8- chloro -1- methy -6- phenyl - 4H -s- triazolo [4,3-a] [1,4] benzodiazepine |
| 3 | AMFEPRAMONE | Diethylpropion | 2-(diethylamino) propiophenone |
| 4 | AMINOREX |
| 2- amino-5- phenyl- 2-oxazoline |
| 5 | AMOBARBITAL |
| 5 -ethyl-5 -isopentylbarbituric acid |
| 6 | BARBITAL |
| 5,5-diethylbarbituric acid |
| 7 | BENZFETAMINE | Benzphetamine | N-benzyl-N, α- dimethylphenethylamine |
| 8 | BROMAZEPAM |
| 7-bromo-1,3-dihydro-5-(2- pyridyl)-2H-1,4-benzodiazepine-one |
| 9 | BROTIZOLAM |
| 2- bromo-4-(o-chlorophenyl)-9 methyl-6H-thieno(3,2-f)-s- triazolo(4,3- α)(1,4) diazepine |
| 10 | BUPRENORPHINE |
| 21 -cyclopropyl-7-a[(S)-1 - hydroxy-1,2,2-trimethylpropyl]- 6,14-endo-ethano-6,7,8,14- tetrahydro oripavine |
| 11 | BUTALBITAL |
| 5-allyl-5-isobutylbarbituric acid |
| 12 | BUTOBARBITAL |
| 5-butyl-5- ethylbarbituric acid |
| 13 | CAMAZEPAM |
| 7-chloro-1,3-dihydro-3-hydroxy- 1 -methyl-5-phenyl-2H-1,4- benzodiazepin-2-one dimethylcarbamate (ester) |
| 14 | CHLODIAZEPOXID |
| 7-chloro-2-(methylamino)-5- phenyl-3H-1,4-benzodiazepine- 4-oxide |
| 15 | CATHINE | (+)-norpseudo- ephedrine | (+)-(R)-α-[(R)-1- aminoethyl]benzyl alcohol |
| 16 | CLOBAZAM |
| 7-chloro-1 -methyl-5-phenyl-1H-1,5-benzodiazepin-2,4 (3H,5H) dione |
| 17 | CLONAZEPAM |
| 5- (o-chlorophenyl)-1,3-dihydro- 7- nitro- 2H -1,4 - benzodiazepine-2 -one |
| 18 | CLORAZEPATE |
| 7- chloro - 2,3 - dihydro - 2 - oxo -5-phenyl-1H-1,4- benzodiazepine -3-carbocilic acid |
| 19 | CLOTIAZEPAM |
| 5-(o-chlorophenyl)-7-ethyl-1,3 dihydro-1 methyl-2H- thieno[2,3e]-1,4 -diazepin -2- one |
| 20 | CLOXAZOLAM |
| 10-chloro-11b-(o- chlorophenyl)2,3,7,11b- tetrahydrooxazolo- [3,2-d] [1,4]benzodiazepin-6(5H) -one |
| 21 | DELORAZEPAM |
| 7-chloro-5- (o-chlorophenyl)-1,3 dihydro-2H-1,4 benzodiazepin-2 - one |
| 22 | DIAZEPAM |
| 7-chloro-1,3-dihydro-1 -methyl- 5-phenyl-2H-1,4 benzodiazepin- 2 - one |
| 23 | ESTAZOLAM |
| 8-chloro-6-phenyl-4H-s-triazolo[4,3-α] [1,4]benzodiazepin |
| 24 | ETHCHLORVYNOL |
| 1 - chloro -3- ethyl -1- penten -4 - yn -3-ol |
| 25 | ETHINAMATE |
| 1- ethynylcyclohexanol carbamate |
| 26 | ETHYLLOFLAZEPATE |
| ethyl -7- chloro -5- (0- fluorophenyl) -2,3 - dihydro -2 - oxo -1H-1,4 -benzodiazepine -3- carboxylate |
| 27 | ETILAMFETAMINE | N-ethylamphetamine | N-ethyl-α-methylphenethylamine |
| 28 | FENCAMFAMIN |
| N- ethyl-3- phenyl-2- norbornanamine |
| 29 | FENPROPOREX |
| (±) -3- [(α- methylphenethyl) amino] propionitrile |
| 30 | FLUDIAZEPAM |
| 7-chloro -5- (o-fluorophenyl) - 1,3-dihydro -1- methyl- 2H - 1,4- benzodiazepin -2- one |
| 31 | FLUNITRAZEPAM |
| 5-(o-fluorophenyl) -1,3 -dihydro- 1- methyl -7- nitro-2H-1,4 benzodiazepin -2- one |
| 32 | FLURAZEPAM |
| 7-chloro-1-[2- (diethylamino)ethyl] -5-(o- fluorophenyl)-1,3-dihydro-2H- 1,4-benzodiazepin -2 - one |
| 33 | GLUTETHIMID |
| 2-ethyl-2-phenylglutarimide |
| 34 | HALAZEPAM |
| 7-chloro-1,3- dihydro -5- phenyl- 1-(2,2,2 -trifluoroethyl)-2H-1,4- benzodiazepin -2 - one |
| 35 | HALOXAZOLAM |
| 10-bromo-11b -(o-fluorophenyl)- 2,3,7,11b tetrahydrooxazolo [3,2-d] [1,4] benzodiazepin -6 (5H) -one |
| 36 | KETAZOLAM |
| 11-chloro -8,12b - (dihydro - 2,8 - dimethyl - 12b - phenyl - 4H - [1,3] oxazino[3,2-d] [l,4] benzodiazepin-4,7 (6H)-dione |
| 37 | KETAMIN |
| (±) -2- (2-Clorophenyl)-2- methylaminocyclohexanone. |
| 38 | LEFETAMIN | SPA | (-)-N,N-dimethyl-1,2- diphenylethylamine |
| 39 | LISDEXAMFETAMINE |
| (2S)-2,6-diamino-N-[(1S)-1- methyl-2-phenylethyl] hexanamide dimethanesulfonate |
| 40 | LOPRAZOLAM |
| 6-(o-chlorophenyl)-2,4-dihydro- 2-[(4-methyl-1 -piperazinyl) methylene] -8-nitro- 1H-imidazol[1,2-α] [1,4] benzodiazepin -1 -one |
| 41 | LORAZEPAM |
| 7-chloro-5-(o-chlorophenyl)-1,3- dihydro-3-hydroxy-2H-1,4 benzodiazepin -2 - one |
| 42 | LORMETAZEPAM |
| 7-chloro-5-(o-chlorophenyl)-1,3- dihydro-3-hydroxy-1-methyl- 2H-1,4 benzodiazepin -2 - one |
| 43 | MAZINDOL |
| 5-(p-chlorophenyl)- 2,5-dihydro-3H-imidazo[2,1-a] isoindol-5-ol |
| 44 | MEDAZEPAM |
| 7-chloro-2,3-dihydro-1-methyl- 5-phenyl-1H-1,4 benzodiazepine |
| 45 | MEFENOREX |
| N-(3- chloropropyl)- α - methylphenethylamine |
| 46 | MEPROBAMAT |
| 2-methyl-2-propyl - 1,3- propanediol, dicarbamate |
| 47 | MESOCARB |
| 3- (α methylphenethyl)- N- (phenylcarbamoyl) sydnone imine |
| 48 | METHYLPHENIDATE |
| Methyl α -phenyl-2- piperidineacetate |
| 49 | METHYLPHENO-BARBITAL |
| 5-ethyl-1 -methyl -5- phenylbarbituric acid |
| 50 | METHYPRYLON |
| 3,3 diethyl-5- methyl-2,4 piperydine- dione |
| 51 | MIDAZOLAM |
| 8- chloro- -6- (o-fluorophenyl) - 1-methyl-4H-imidazol[1,5-a] [1,4] benzodiazepine |
| 52 | NIMETAZEPAM |
| 1,3 dihydro -1- methyl-7-nitro-5- phenyl-2H-1,4 benzodiazepin-2- one |
| 53 | NITRAZEPAM |
| 1,3 dihydro -7-nitro-5-phenyl- 2H-1,4 benzodiazepin-2-one |
| 54 | NORDAZEPAM |
| 7-chloro- 1,3 dihydro-5- phenyl- 2H-1,4 benzodiazepin-2-one |
| 55 | OXAZEPAM |
| 7-chloro- 1,3 dihydro- 3 hydroxy-5- phenyl-2H-1,4 benzodiazepin- 2-one |
| 56 | OXAZOLAM |
| 10-chloro--2,3,7,11b- tetrahydro- 2-methyl-11b- phenyloxazolo[3,2-d] [1,4] benzodiazepin-6(5H) -one |
| 57 | PENTAZOCIN |
| (2R*,6R*,11R*)-1,2,3,4,5,6- hexahydro-6,11-dimethyl-3-(3- methyl-2-butenyl)-2,6-methano- 3-benzazocin-8-ol |
| 58 | PENTOBARBITAL |
| 5-ethyl-5-(1-methylbutyl) barbituric acid |
| 59 | PHENDIMETRAZIN |
| (+)-(2S,3S)-3,4-dimethyl-2-phenylmorpholine |
| 60 | PHENOBARBITAL |
| 5-ethyl-5-phenylbarbituric acid |
| 61 | PHENTERMIN |
| α,α- dimethylphenethylamine |
| 62 | PINAZEPAM |
| 7-chloro-1,3-dihydro-5-phenyl-1-(2-propynyl)-2H-1,4- benzodiazepin-2-one |
| 63 | PRAZEPAM |
| 7-chloro -1- (cyclopylmethyl) - 1,3 - dihydro -5- phenyl -2H- 1,4-benzodiazepin-2-one |
| 64 | PYROVALERONE |
| 4’-methyl-2-(1-pyrrolidinyl) valerophenone |
| 65 | SECBUTABARBITAL |
| 5-sec-butyl-5-ethylbarbituric acid |
| 66 | TEMAZEPAM |
| 7- chloro - 1,3 - dihydro -3- hydroxy-1 -methyl-5-phenyl - 2H- 1,4-benzodiazepin -2- one |
| 67 | TETRAZEPAM |
| 7-chloro-5-(1 -cyclohexen-1 -yl)- 1,3 dihydro-1 -methy1-2H-1,4 benzodiazepin -2- one |
| 68 | TRIAZOLAM |
| 8-chloro-6-(o-chlorophenyl)-1 - methyl-4H-s-triazolo[4,3-α] [1,4] benzodiazepin |
| 69 | VINYLBITAL |
| 5-(1-methylbutyl)-5- vinylbarbituric acid |
| 70 | ZOLPIDEM |
| N,N,6- trimethyl-2-p- tolylimidazol [1,2-α] pyridine- 3- acetamide |
Danh mục này bao gồm các muối của các chất ghi trong Bảng này, khi các muối đó có thể hình thành và tồn tại.
PHỤ LỤC 7
DANH MỤC TIỀN CHẤT DÙNG LÀM THUỐC
(Kèm theo Thông tư số: 20 /2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| TT | TÊN QUỐC TẾ | TÊN KHOA HỌC |
| 1 | EPHEDRINE | ([R-(R*, S*)]--[1- (methylamino)ethyl]- Benzenemethanol |
| 2 | N-ETHYLEPHEDRIN | 1 -Ethylephedrin |
| 3 | N-METHYLEPHEDRIN/ METHYLEPHEDRIN/ | (1R, 2S)-2- (dimethylamino)-1 - phenyl- propanol |
| 4 | PSEUDOEPHEDRINE | [S-(R*,R*)]--[1- (methylamino)ethyl]- Benzenemethanol |
| 5 | ERGOMETRINE | Ergoline-8-carboxamide,9,10- didehydro-N-(2-hydroxy-1 - methylethyl)-6-methy- [8 β(s)]. |
| 6 | ERGOTAMINE | Ergotaman-3’, 6’, 18 ’-trione, 12’- hydroxy-2 ’ -methyl- 5’ - (phenylmethyl)-(5) |
| 7 | N-ETHYLPSEUDOEPHEDRIN | Ethyl methyl amino - phenyl - propane - 1 - ol |
| 8 | N-METHYLPSEUDOEPHEDRIN | Dimethylamino - phenyl - propane - 1 - ol |
Danh mục này bao gồm các muối của các chất ghi trong Bảng này, khi các muối đó có thể hình thành và tồn tại.
PHỤ LỤC 8
BẢNG GIỚI HẠN NỒNG ĐỘ, HÀM LƯỢNG DƯỢC CHẤT GÂY NGHIỆN TRONG THUỐC DẠNG PHỐI HỢP
(Kèm theo Thông tư số: 20/2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| TT | TÊN DƯỢC CHẤT GÂY NGHIỆN | HÀM LƯỢNG DƯỢC CHẤT TÍNH THEO DẠNG BAZƠ TRONG MỘT ĐƠN VỊ SẢN PHẨM ĐÃ CHIA LIỀU | NỒNG ĐỘ DƯỢC CHẤT TÍNH THEO DẠNG BAZƠ TRONG SẢN PHẨM CHƯA CHIA LIỀU |
| 1 | ACETYLDIHYDROCODEIN | 100 | 2,5 |
| 2 | COCAINE |
| 0,1 |
| 3 | CODEINE | 100 | 2,5 |
| 4 | DIFENOXIN | Không quá 0,5 mg Difenoxin và với ít nhất 0,025 mg Atropin Sulfat trong một đơn vị sản phẩm đã chia liều. |
|
| 5 | DIPHENOXYLATE | Không quá 2,5 mg Difenoxylat và với ít nhất 0,025 mg Atropin Sulfat trong một đơn vị sản phẩm đã chia liều. |
|
| 6 | DIHYDROCODEIN | 100 | 2,5 |
| 7 | ETHYL MORPHIN | 100 | 2,5 |
| 8 | NICODICODIN | 100 | 2,5 |
| 9 | NORCODEIN | 100 | 2,5 |
| 10 | PHOLCODIN | 100 | 2,5 |
| 11 | PROPIRAM | 100 | 2,5 |
| 12 | MORPHINE |
| 0,2 morphin tính theo morphin base tinh khiết |
| 13 | TRAMADOL | 37,5 |
|
PHỤ LỤC 9
BẢNG GIỚI HẠN NỒNG ĐỘ, HÀM LƯỢNG DƯỢC CHẤT HƯỚNG THẦN TRONG THUỐC DẠNG PHỐI HỢP
(Kèm theo Thông tư số: 20/2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| STT | TÊN DƯỢC CHẤT HƯỚNG THẦN | HÀM LƯỢNG TỐI ĐA CÓ TRONG MỘT ĐƠN VỊ ĐÃ CHIA LIỀU (mg) |
| 1 | ALLOBARBITAL | 10 |
| 2 | ALPRAZOLAM | 0,25 |
| 3 | AMOBARBITAL | 10 |
| 4 | BARBITAL | 10 |
| 5 | BROMAZEPAM | 1 |
| 6 | BROTIZOLAM | 0,25 |
| 7 | BUTOBARBITAL | 10 |
| 8 | CAMAZEPAM | 5 |
| 9 | CHLODIAZEPOXID | 5 |
| 10 | CLOBAZAM | 5 |
| 11 | CLONAZEPAM | 0,5 |
| 12 | CLORAZEPAT | 10 |
| 13 | CLOTIAZEPAM | 5 |
| 14 | DIAZEPAM | 5 |
| 15 | ESTAZOLAM | 0,5 |
| 16 | FLUDIAZEPAM | 0,5 |
| 17 | FLUNITRAZEPAM | 0,5 |
| 18 | FLURAZEPAM | 5 |
| 19 | HALAZEPAM | 5 |
| 20 | KETAZOLAM | 5 |
| 21 | LOPRAZOLAM | 0,25 |
| 22 | LORAZEPAM | 0,5 |
| 23 | LORMETAZEPAM | 0,25 |
| 24 | MEPROBAMAT | 100 |
| 25 | MEDAZEPAM | 5 |
| 26 | METHYLPHENOBARBITAL | 10 |
| 27 | MIDAZOLAM | 5 |
| 28 | NITRAZEPAM | 5 |
| 29 | NORDRAZEPAM | 0,25 |
| 30 | OXAZEPAM | 10 |
| 31 | PARAZEPAM | 5 |
| 32 | PENTOBARBITAL | 10 |
| 33 | PHENOBARBITAL | 25 |
| 34 | SECBUTABARBITAL | 10 |
| 35 | TEMAZEPAM | 25 |
| 36 | TETRAZEPAM | 5 |
| 37 | VINYLBITAL | 10 |
| 38 | CLOXAZOLAM | 1 |
| 39 | DELORAZEPAM | 0,25 |
| 40 | ETHYLCLOFLAZEPAT | 0,25 |
| 41 | NIMETAZEPAM | 0,25 |
| 42 | OXAZOLAM | 5 |
| 43 | PINAZEPAM | 1 |
PHỤ LỤC 10
BẢNG GIỚI HẠN NỒNG ĐỘ, HÀM LƯỢNG TIỀN CHẤT DÙNG LÀM THUỐC TRONG THUỐC DẠNG PHỐI HỢP
(Kèm theo Thông tư số: 20/2017/TT-BYT ngày 10 tháng 05 năm 2017 của Bộ trưởng Bộ Y tế)
| STT | TÊN TIỀN CHẤT DÙNG LÀM THUỐC | HÀ LƯỢNG TỐI ĐA CÓ TRONG MỘT ĐƠN VỊ ĐÃ CHIA LIỀU (mg) | NỒNG ĐỘ TỐI ĐA CÓ TRONG MỘT ĐƠN VỊ CHƯA CHIA LIỀU |
| 1 | EPHEDRINE | 50 | 1,5% |
| 2 | ERGOMETRINE | 0,125 |
|
| 3 | N-ETHYLEPHEDRIN | 12,5 |
|
| 4 | N-METHYLEPHEDRIN/ METHYLEPHEDRIN/ DL-METHYLEPHEDRIN | 31,1 | 0,0625% |
| 5 | ERGOTAMINE | 01 |
|
| 6 | PSEUDOEPHEDRINE | 120 | 0,5% |
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Quyết định 696/QĐ-QLD PDF (Bản có dấu đỏ)
Quyết định 696/QĐ-QLD PDF (Bản có dấu đỏ) Quyết định 696/QĐ-QLD DOC (Bản Word)
Quyết định 696/QĐ-QLD DOC (Bản Word)