- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn TCVN 13653:2023 Nhiên liệu sinh học rắn - Xác định nhiệt lượng
| Số hiệu: | TCVN 13653:2023 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Nông nghiệp-Lâm nghiệp |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
18/07/2023 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 13653:2023
Tiêu chuẩn quốc gia TCVN 13653:2023 về xác định nhiệt lượng của nhiên liệu sinh học rắn
Ngày 18/07/2023, Bộ Khoa học và Công nghệ đã công bố Tiêu chuẩn quốc gia TCVN 13653:2023, quy định về phương pháp xác định giá trị nhiệt lượng toàn phần của nhiên liệu sinh học rắn, tương đương với ISO 18125:2017. Tiêu chuẩn này có hiệu lực ngay lập tức.
Tiêu chuẩn này áp dụng cho việc xác định giá trị nhiệt lượng của các loại nhiên liệu sinh học rắn, như viên nén gỗ, bằng cách sử dụng bom nhiệt lượng ở thể tích không đổi và nhiệt độ chuẩn 25 °C. Kết quả cho thấy giá trị nhiệt lượng toàn phần của mẫu phân tích với toàn bộ nước ngưng lại giữ ở dạng lỏng.
Phương pháp xác định nhiệt lượng
Tiêu chuẩn quy định phương pháp xác định nhiệt lượng bằng cách cháy mẫu nhiên liệu sinh học rắn trong bom nhiệt lượng với oxy ở áp suất thấp. Nhiệt độ tăng do quá trình cháy sẽ được đo để tính toán giá trị nhiệt lượng toàn phần. Quy trình này cũng được hướng dẫn chi tiết trong các phụ lục của tiêu chuẩn với các nguyên tắc và thông số cần tuân thủ.
Các phụ lục kèm theo
Có sáu phụ lục trong tiêu chuẩn này, trong đó có các danh mục kiểm tra quy trình hiệu chuẩn và phép thử nhiên liệu với các loại nhiệt lượng kế. Phụ lục D đưa ra danh sách các bước cần thực hiện để hiệu chuẩn và kiểm tra nhiệt lượng kế, đảm bảo độ chính xác trong việc xác định giá trị nhiệt lượng.
Thiết bị và dụng cụ
Tiêu chuẩn cũng mô tả chi tiết về thiết bị, dụng cụ cần thiết để đo nhiệt lượng, bao gồm bom nhiệt lượng, cảm biến nhiệt độ, và bộ khuấy. Các yêu cầu về thiết bị được định rõ nhằm đảm bảo độ chính xác cho kết quả thử nghiệm.
Chuẩn bị mẫu thử
Mẫu thử để xác định nhiệt lượng phải được chuẩn bị theo các quy định của tiêu chuẩn. Các mẫu cần được lấy đúng cách, lưu trữ trong điều kiện niêm phong và được xử lý không làm ảnh hưởng đến hàm lượng nước và thành phần hóa học của chúng.
Tiêu chuẩn TCVN 13653:2023 không chỉ giúp tăng cường chất lượng đo lường trong lĩnh vực nhiên liệu sinh học mà còn hỗ trợ các tổ chức, doanh nghiệp trong việc sản xuất, kiểm tra và sử dụng nhiên liệu sinh học đạt tiêu chuẩn chất lượng.
Tải tiêu chuẩn Việt Nam TCVN 13653:2023
TIÊU CHUẨN QUỐC GIA
TCVN 13653:2023
ISO 18125:2017
NHIÊN LIỆU SINH HỌC RẮN - XÁC ĐỊNH NHIỆT LƯỢNG
Solid biofuels - Determination of calorific value
Lời nói đầu
TCVN 13653:2023 hoàn toàn tương đương với ISO 18125:2017.
TCVN 13653:2023 do Viện Khoa học Lâm nghiệp Việt Nam biên soạn, Bộ Nông nghiệp và Phát triển nông thôn đề nghị, Tổng Cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
NHIÊN LIỆU SINH HỌC RẮN - XÁC ĐỊNH NHIỆT LƯỢNG
Solid biofuels - Determination of calorific value
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp xác định giá trị nhiệt lượng toàn phần của nhiên liệu sinh học rắn (viên nén gỗ) ở thể tích không đổi và tại nhiệt độ chuẩn 25 °C trong bom nhiệt lượng kế được hiệu chỉnh bằng sự đốt cháy axit benzonic.
Kết quả thu được là giá trị nhiệt lượng toàn phần của mẫu phân tích ở thể tích không đổi, với toàn bộ lượng nước của sản phẩm đốt cháy được ngưng lại như nước lỏng. Trong thực tế, nhiên liệu sinh học được đốt ở áp suất không đổi và lượng nước không ngưng được (được thoát ra dưới dạng bay hơi cùng với chất khí) hoặc ngưng được. Trong cả hai điều kiện, nhiệt hữu hiệu của sự cháy là giá trị tỏa nhiệt thực của nhiên liệu trong điều kiện áp suất không đổi. Giá trị nhiệt lượng thực tại thể tích không đổi cũng được sử dụng; tiêu chuẩn đưa ra công thức để tính cả hai giá trị này.
Các nguyên tắc chung và quy trình để hiệu chuẩn và các phép thử nhiên liệu sinh học được trình bày trong nội dung chính của tiêu chuẩn. Những vấn đề liên quan đến việc sử dụng loại dụng cụ cụ thể đo nhiệt lượng được mô tả trong các Phụ lục A đến Phụ lục C. Phụ lục D gồm các danh mục kiểm tra quy trình hiệu chuẩn và các phép thử nhiên liệu sử dụng các loại nhiệt lượng kế quy định. Phụ lục E đưa ra một số ví dụ để minh họa các tính nhiệt năng.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau đây là cần thiết để áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
ISO 651, Solid - stem calorimeter thermometers (Nhiệt kế nhiệt lượng thân cứng)
TCVN 11555 (ISO 652), Nhiệt kế thang đo kín để đo nhiệt lượng
ISO 1770, Solid-stem general purpose thermometers (Nhiệt kế thân cứng sử dụng chung)
TCVN 11557 (ISO 1771), Nhiệt kế thang đo kín để sử dụng chung
ISO 14780, Solid biofuels - Sample preparation (Nhiên liệu sinh học rắn - Chuẩn bị mẫu)
ISO 16559, Solid biofuels - Terminology, definitions and descriptions (Nhiên liệu sinh học rắn - Thuật ngữ định nghĩa và mô tả)
ISO 18134-1, Solid biofuels - Determination of moisture content - oven dry method, Part 1: Total moisture - Reference method (Nhiên liệu sinh học rắn - Xác định độ ẩm - Phương pháp sấy khô kiệt, Phần 1: Độ ẩm toàn phần - Phương pháp tham chiếu)
ISO 18134-2, Solid biofuels - Determination of moisture content - oven dry method, Part 2: Total moisture - Simplified method (Nhiên liệu sinh học rắn - Xác định độ ẩm - Phương pháp sấy khô kiệt, Phần 2: Độ ẩm toàn phần - Phương pháp đơn giản hóa)
ISO 18134-3, Solid biofuels - Determination of moisture content - Oven dry method - Part 3: Moisture in general analysis sample (Nhiên liệu sinh học rắn - Xác định độ ẩm - Phương pháp sấy khô kiệt - Phần 3: Độ ẩm trong mẫu phân tích chung)
ISO 18135, Solid biofuels - Sampling (Nhiên liệu sinh học rắn - Lấy mẫu).
3 Thuật ngữ và định nghĩa
Tiêu chuẩn này sử dụng một số thuật ngữ và định nghĩa trong ISO 16559 và các thuật ngữ, định nghĩa sau:
3.1
Giá trị nhiệt lượng toàn phần ở thể tích không đổi (gross calorific value at constant volume)
Giá trị năng lượng riêng tuyệt đối của quá trình đốt, tính bằng Jun, đối với đơn vị khối lượng nhiên liệu rắn được đốt cháy với oxy trong bom nhiệt lượng ở các điều kiện quy định.
CHÚ THÍCH 1: Sản phẩm của quá trình đốt cháy thu được giả định bao gồm khí oxy, nitơ, cacbon đioxit và lưu huỳnh đioxit, nước lỏng (tương đương trạng thái hơi) bão hòa với cacbon đioxit dưới các điều kiện của phản ứng trong bom và của tro rắn tại nhiệt độ tham chiếu (3.4).
3.2
Giá trị nhiệt lượng thực ở thể tích không đổi (net calorific value at constant volume)
Giá trị năng lượng riêng tuyệt đối của quá trình đốt, tính bằng Jun, đối với đơn vị khối lượng nhiên liệu sinh học rắn được đốt cháy với oxy dưới điều kiện thể tích không đổi và toàn bộ nước của các sản phẩm phản ứng tồn tại dưới dạng hơi nước (ở trạng thái giả thuyết 0,1 MPa), các sản phẩm khác cũng như đối với giá trị tỏa nhiệt toàn phần, tất cả đều tại nhiệt độ tham chiếu (3.4).
3.3
Giá trị nhiệt lượng thực ở áp suất không đổi (net calorific value at constant pressure)
Giá trị nhiệt lượng riêng (entanpi) tuyệt đối của quá trình cháy, tính bằng Jun, đối với đơn vị khối lượng của nhiên liệu sinh học được đốt cháy trong oxy tại áp suất không đổi trong điều kiện mà toàn bộ nước của các sản phẩm phản ứng tồn tại dạng hơi nước (tại 0,1 MPa), các sản phẩm khác cũng như giá trị tỏa nhiệt toàn phần, tất cả đều ở nhiệt độ tham chiếu (3.4).
3.4
Nhiệt độ tham chiếu (reference temperature)
Nhiệt độ tham chiếu quốc tế dùng cho phép thử nhiệt hóa bằng 25 °C.
CHÚ THÍCH 1: Xem 8.7.
CHÚ THÍCH 2: Giá trị nhiệt lượng của nhiên liệu sinh học ít phụ thuộc vào nhiệt độ [khoảng 1 J/(gxK)].
3.5
Nhiệt dung hữu hiệu của nhiệt lượng kế (effective heat capacity of the calorimeter)
Lượng năng lượng cần thiết để thay đổi đơn vị nhiệt độ của nhiệt lượng kế.
3.6
Tăng nhiệt độ đã hiệu chỉnh (corrected temperature rise)
Nhiệt độ nhiệt lượng kế thay đổi do quá trình bom đốt.
CHÚ THÍCH 1: Nhiệt độ tăng đã hiệu chỉnh là tổng độ tăng nhiệt độ quan sát được đã được hiệu chỉnh cho trao đổi nhiệt và tốc độ khuấy,v v (xem 8.6).
CHÚ THÍCH 2: Sự thay đổi của nhiệt độ có thể được biểu thị bằng các đơn vị đo khác: biến trở platin hoặc nhiệt biến tần suất cộng hưởng của tinh thể thạch anh, v v với điều kiện là quan hệ hàm số được xác định giữa số lượng và sự thay đổi về nhiệt độ. Nhiệt dung hữu hiệu của nhiệt lượng kế có thể biểu thị theo các đơn vị năng lượng trên một đơn vị khác. Các nguyên tắc về độ tuyến tính và tiệm cận trong các điều kiện giữa hiệu chuẩn và các phép thử nhiên liệu được nêu tại 9.3.
CHÚ THÍCH 3: Danh mục các kí hiệu được sử dụng và các định nghĩa về chúng được đưa ra ở Phụ lục F
4 Nguyên tắc của phương pháp
4.1 Giá trị nhiệt lượng toàn phần
Một phần của mẫu phân tích nhiên liệu sinh học rắn đã được cân, cho đốt với oxy ở áp suất cao trong bom nhiệt lượng kế dưới các điều kiện quy định. Nhiệt dung hữu hiệu của nhiệt lượng kế được xác định trong phép thử hiệu chuẩn bằng sự đốt cháy axit benzoic dưới điều kiện tương tự đã nêu trong chứng chỉ. Sự tăng nhiệt độ hiệu chỉnh được thiết lập từ các quan sát nhiệt độ trước, trong và sau phản ứng cháy diễn ra. Khoảng thời gian và tần suất của việc quan sát nhiệt độ phụ thuộc vào loại nhiệt lượng kế được sử dụng. Cho nước vào bom ngay từ ban đầu để tạo pha hơi nước bão hòa trước khi đốt (xem 8.2.1 và 9.2.2), theo cách đó cho phép tất cả lượng nước được hình thành từ hydro và hàm lượng ẩm trong mẫu được xem là dạng nước lỏng.
Giá trị nhiệt lượng toàn phần được tính từ sự tăng nhiệt độ đã hiệu chỉnh và nhiệt dung hữu hiệu của nhiệt lượng kế, có tính đến nhiệt phát ra trong quá trình mồi cháy, và ảnh hưởng của nhiệt hình thành do các phản ứng phụ ví dụ sự hình thành của axit nitric. Hơn nữa, áp dụng việc hiệu chỉnh để giải thích cho sự khác biệt về năng lượng giữa axit sulphuric ở thể lỏng hình thành trong phản ứng bom và khí lưu huỳnh dioxit, đó là sản phẩm phản ứng bắt buộc của lưu huỳnh trong nhiên liệu sinh học. Hiệu suất năng lượng tương ứng giữa axit clohydric ở thể lỏng và thể khí có thể được bỏ qua do giá trị hiệu chỉnh thường thấp đối với nhiên liệu sinh học rắn.
4.2 Giá trị nhiệt lượng thực
Giá trị nhiệt lượng thực tại thể tích không đổi và giá trị nhiệt lượng thực ở áp suất không đổi của nhiên liệu sinh học thu được bằng cách tính từ giá trị nhiệt lượng toàn phần ở thể tích không đổi được xác định trên mẫu phân tích. Việc tính giá trị nhiệt lượng thực ở thể tích không đổi yêu cầu phải biết thông tin về hàm lượng ẩm và hàm lượng hydro của mẫu phân tích. Theo nguyên tắc, để tính giá trị nhiệt lượng thực ở áp suất không đổi cũng yêu cầu thông tin về hàm lượng oxy và hàm lượng nitơ của mẫu phân tích.
5 Hóa chất, thuốc thử
5.1 Oxy
Có áp suất đủ cao để nạp vào bom đến 3 MPa. Độ tinh khiết phân tích không nhỏ hơn 99,5 % thể tích và không có vật liệu dễ cháy.
Oxy được sản xuất bằng quá trình điện phân có thể cho phép tối đa 4 % thể tích là hydro.
5.2 Mồi cháy
5.2.1 Dây đốt, được làm bằng Niken-crom có đường kính từ 0,16 mm đến 0,20 mm, bằng platin có đường kính từ 0,05 mm đến 0,10 mm, hoặc các dây dẫn khác phù hợp có đặc tính dẫn nhiệt tốt cho quá trình đốt.
5.2.2 Mồi cháy bằng bông: làm bằng sợi bông xenlulo trắng hoặc tương đương theo yêu cầu (xem 8.2.1).
5.3 Các chất trợ cháy đã biết tổng nhiệt lượng, thành phần và độ tinh khiết như axit benzonic, n- dodecane, dầu paratin, túi đốt hoặc viên đốt dạng viên có thể được sử dụng.
5.4 Dung dịch chuẩn độ tiêu chuẩn và chất chỉ thị
Chỉ dùng khi phân tích các dung dịch trong bom cuối cùng, theo yêu cầu
5.4.1 Dung dịch bari hydroxit, c[Ba(OH)2] = 0,05 mol/L
5.4.2 Dung dịch natri cacbonat, c(Na2CO3) = 0,05 mol/L
5.4.3 Dung dịch natri hydroxit, c(NaOH) = 0,1 mol/L
5.4.4 Dung dịch axit clohydric, c(HCl) = 0,1 mol/L
5.4.5 Chất chỉ thị methyl màu cam, dung dịch có nồng độ 1 g/l
Hòa tan 0,25 g methyl màu cam và 0,15 g xylene cyanol FF trong 50 ml ethannol 95 % thể tích và pha loãng bằng nước đến 250 ml.
5.4.6 Phenolphthalein, dung dịch 10 g/l.
Hòa tan 2,5 g phenolphthalein trong 250 ml ethanol 95 % thể tích.
5.5 Axit benzoic, chất hóa nhiệt tiêu chuẩn, được cơ quan tiêu chuẩn hóa chứng nhận (hoặc có thể truy xuất nguồn gốc).
Axit benzoic là chất duy nhất được khuyến nghị sử dụng để hiệu chuẩn oxy bom nhiệt lượng. Đối với mục đích kiểm tra độ tin cậy của các phép đo nhiệt lượng, các chất thử ví dụ như n-dodecane được sử dụng. Các chất thử chủ yếu được sử dụng để chứng minh một số đặc tính nhất định của mẫu, ví dụ tốc độ đốt cháy hoặc thành phần hóa học và không gây độ lệch kết quả thử. Các chất thử phải có độ tinh khiết được công nhận và xác định đúng năng lượng trong quá trình đốt.
Axit benzoic được đốt cháy ở dạng viên, thông thường được sử dụng mà không phải sấy khô (Axit benzoic không hút ẩm từ môi trường có độ ẩm tương đối dưới 90 %) hoặc bất cứ xử lý nào khác, theo chứng nhận.
Axit benzoic phải được sử dụng đúng theo các điều kiện chứng nhận quy định; sự thay đổi đáng kể so với các điều kiện chứng nhận phải được tính toán phù hợp theo các hướng được đưa ra trong chứng nhận. Năng lượng của quá trình đốt cháy axit benzoic được xác định thông qua chứng nhận cho các điều kiện sử dụng, được chấp nhận trong cách tính nhiệt dung hữu hiệu của nhiệt lượng kế (xem 9.2).
6 Thiết bị, dụng cụ
6.1 Quy định chung
Nhiệt lượng kế (xem Hình 4.1) bao gồm cụm bom đốt, bình nhiệt lượng kế (có hoặc không có nắp đậy), bộ khuấy, nước, cảm biến nhiệt độ, và dây dẫn có đầu nối bên trong nhiệt lượng kế có thể cần cho sự đốt cháy mẫu hoặc như bộ đo nhiệt độ hoặc các mạch điều khiển. Trong khi đó, nhiệt lượng kế được gắn trong bộ ổn nhiệt. Bằng cách này nhiệt độ bộ ổn nhiệt được kiểm soát, nguyên tắc làm việc của thiết bị được xác định và do đó giám sát đánh giá sự nhiệt độ tăng đã hiệu chỉnh.
Trong các hệ thống áp kế (hệ thống không có chất lỏng), bình nhiệt lượng kế, bộ khuấy, và nước được thay thế bởi một khối kim loại. Bom đốt này tự bản thân nó cấu thành nhiệt lượng kế trong một vài hệ thống áp kế.
Trong các nhiệt lượng kế đốt với mức độ tự động hóa cao, đặc biệt trong việc đánh giá các kết quả, trong một vài trường hợp nhiệt lượng kế không được xác định đúng như nhiệt lượng kế truyền thống và cổ điển. Tuy nhiên, việc sử dụng loại nhiệt lượng kế tự động trong phạm vi của tiêu chuẩn này cùng với các yêu cầu cơ bản cũng đáp ứng những điều kiện hiệu chuẩn, có thể so sánh được giữa việc hiệu chuẩn và phép thử nhiên liệu, tỷ lệ giữa khối lượng mẫu với thể tích bom, áp suất oxy, chất lòng trong bom, nhiệt độ chuẩn của các phép đo và độ chính xác của kết quả đo. Việc chỉ ra một số thông số cụ thể từ các phép thử độc lập là cần thiết. Chi tiết được nêu trong Phụ lục C.
Ở điều kiện phòng (nhiệt độ dao động, sự tuần hoàn của không khí,..) có thể có ảnh hưởng đến độ chụm của việc xác định nhiệt lượng, phải tuân thủ theo hướng dẫn của nhà sản xuất đối với vị trí đặt các thiết bị
Thiết bị thích hợp để xác định giá trị tỏa nhiệt phù hợp với tiêu chuẩn này được nêu trong Điều 6.2 đến 6.8.
6.2 Nhiệt lượng kế có bộ ổn nhiệt
6.2.1 Bom đốt
Bom đốt, có khả năng chịu được áp suất sinh ra trong quá trình đốt. Thiết kế đảm bảo cho phép thu được toàn bộ các sản phẩm dạng lỏng. Vật liệu chế tạo bom phải chịu được ăn mòn do axit sinh ra trong quá trình đốt cháy nhiên liệu sinh học. Thể tích bên trong của bom từ 250 mL đến 350 mL là phù hợp.
CẢNH BÁO: Các bộ phận của bom phải được kiểm tra định kỳ về độ mài mòn vỏ thiết bị và độ ăn mòn, đặc biệt phải chú ý đến tình trạng các đường ren của phần nắp chính. Phải áp dụng các hướng dẫn của nhà sản xuất và các quy chuẩn kỹ thuật về liên quan đến xử lý và sử dụng an toàn của bom. Khi sử dụng nhiều bom có cùng loại thiết kế, thì bắt buộc phải sử dụng riêng từng bom như một thiết bị hoàn chỉnh. Việc thay đổi các bộ phận giữa các bom có thể dẫn đến sự cố nghiêm trọng.
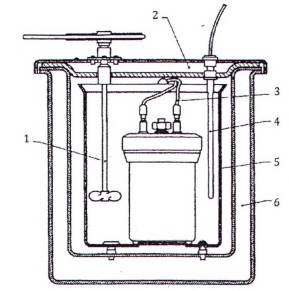
CHÚ DẪN
| 1. Bộ khuấy | 4. Nhiệt kế |
| 2. Nắp bộ ổn nhiệt | 5. Bình nhiệt lượng kế |
| 3. Dây mồi đốt | 6. Bộ ổn nhiệt |
Hình 1 - Nhiệt lượng kế bom đốt loại cổ điển có bộ ổn nhiệt
6.2.2 Bình nhiệt lượng kế
Bình nhiệt lượng kế được chế tạo bằng kim loại, được đánh bóng bên ngoài và có khả năng chứa đủ lượng nước phủ hoàn toàn bề mặt trên của bom trong khi nước được khuấy. Nắp đậy giúp làm giảm sự bay hơi của nước trong nhiệt lượng kế, nhưng không làm chậm quá trình tăng nhiệt độ khi đốt, hoặc làm tăng sự trao đổi nhiệt không xác định với bộ ổn nhiệt và kéo dài chu kỳ chính.
6.2.3 Bộ khuấy làm việc ở tốc độ không đổi. Trục của máy khuấy phải có độ dẫn nhiệt thấp và/hoặc phần phía dưới nắp đậy có khối lượng nhỏ để giảm tối đa sự truyền nhiệt đến hoặc đi từ hệ thống. Điều này là đặc biệt quan trọng khi trục của máy khuấy tiếp xúc trực tiếp với động cơ của máy khuấy. Nếu sử dụng nắp cho bình nhiệt lượng kế thì phần trục này phải ở phía trên nắp.
Tốc độ khuấy nước của nhiệt lượng kế cần đủ lớn để đảm bảo chắc chắn không có các điểm nóng phát sinh do sự thay đổi nhiệt độ nhanh giữa các vùng của nhiệt lượng kế. Tốc độ khuấy của chu kỳ chính có thể phải hạn chế là 10 min hoặc ít hơn (xem Phụ lục A và B).
6.2.4 Bộ ổn nhiệt (túi nước) bao quanh hoàn toàn nhiệt lượng kế với khoảng không khí trống giữa nhiệt lượng kế và bộ ổn nhiệt, xấp xỉ bằng 10 mm.
Khối lượng nước của bộ ổn nhiệt dùng cho mục đích đẳng nhiệt phải đủ lớn để không bị nhiễu nhiệt từ bên ngoài. Trong suốt thời gian thử nghiệm, nhiệt độ phải được kiểm soát trong khoảng ± 0,1 K hoặc chính xác hơn. Bộ ổn nhiệt ổn định nhiệt độ (tĩnh) phải có nhiệt dung đủ lớn để hạn chế sự thay đổi nhiệt độ của nước. Tiêu chuẩn để thỏa mãn yêu cầu của loại túi nước này được nêu trong Phụ lục B.
CHÚ THÍCH 1: Đối với lớp áo cách nhiệt tĩnh bằng kim, những đặc tính phù hợp thông thường được đảm bảo bằng cách làm một vỏ hình khuyên rộng với dung tích ít nhất là 12,5 L nước.
CHÚ THÍCH 2: Nhiệt lượng kế được bọc bởi lớp vật liệu cách, tạo ra hàng rào cản nhiệt được coi là nhiệt lượng kế túi nước tĩnh.
Khi cần bộ ổn nhiệt (túi nước) thì phải đảm bảo nhiệt độ bằng sát với nhiệt độ của nhiệt lượng kế, và cần có khối lượng nhỏ và tốt nhất là có bộ gia nhiệt loại nhúng chìm. Năng lượng được cung cấp với tốc độ vừa đủ để duy trì nhiệt độ của nước trong bộ ổn nhiệt trong khoảng 0,1 K so với nhiệt độ nước của nhiệt lượng kế, sau khi đốt. Khi ở trạng thái ổn định ở 25 °C, nhiệt độ dao động trung bình của nhiệt lượng kế sẽ không vượt quá 0,0005 K/min (xem A 3.2).
6.2.5 Dụng cụ đo nhiệt độ
Dụng cụ đo nhiệt độ có khả năng chỉ thị nhiệt độ với độ phân giải ít nhất là 0,001 K sao cho có thể xác định được những khoảng nhiệt độ từ 2 K đến 3 K với độ chính xác 0,002 K hoặc chính xác hơn. Nhiệt độ tuyệt đối chính xác đến 0,1 K tại nhiệt độ chuẩn của phép đo nhiệt lượng. Dụng cụ đo nhiệt phải là thiết bị đo tuyến tính hoặc tuyến tính hóa để đáp ứng sự thay đổi của nhiệt độ trong khoảng thời gian được sử dụng.
Cách khác là dùng nhiệt kế thủy ngân - thủy tinh truyền thống, các cảm biến nhiệt độ thích hợp là nhiệt kế điện trở platin, nhiệt kế điện trở, nhiệt kế cộng hưởng tinh thể thạch anh,... cùng với các cầu điện trở phù hợp, đầu dò, máy đếm tần số hoặc thiết bị điện tử khác đảm bảo độ chính xác theo yêu cầu. Độ lặp lại tức thời của loại thiết bị này phải là 0,001 K hoặc tốt hơn. Sự sai lệch không lớn hơn 0,05 K trong khoảng thời gian 6 tháng. Đối với cảm biến tuyến tính (trong điều kiện nhiệt độ), sự thay đổi nhiệt độ ít có khả năng gây ra sai lệch trong các phép đo nhiệt lượng so với các cảm biến không tuyến tính.
Nhiệt kế thủy ngân - thủy tinh phải phù hợp với ISO 651, TCVN 11555, ISO 1770 hoặc TCVN 11557. Để đọc nhiệt độ với độ chính xác yêu cầu, cần máy đọc có độ phóng đại 5 lần.
Có thể sử dụng máy rung cơ học để gỗ nhẹ vào nhiệt kế để ngăn cản cột thủy ngân không bị kẹt (xem 8.4). Nếu thiết bị này không có sẵn, phải gõ nhẹ nhiệt kế bằng tay trước khi đọc nhiệt độ.
6.2.6 Mạch đốt
Cung cấp nguồn điện xoay chiều từ 6 V đến 12 V được cấp từ máy hạ áp hoặc trực tiếp từ pin. Cần có đèn báo chỉ dẫn để nhận biết khi đang có điện.
Khi đốt thủ công, núm chuyển đổi đốt là loại lò xo, thường là loại mở được, được định vị sao cho không có nguy hiểm ngược lại đối với người vận hành (xem cảnh báo trong 8.4).
6.3 Chén nung
Chén nung làm bằng silic dioxit, niken-crom, platin hoặc vật liệu tương đương.
Chén nung phải có đường kính từ 15 mm đến 25 mm, đáy phẳng và có chiều sâu khoảng 20 mm. Chén nung silic dioxit phải có chiều dày khoảng 1,5 mm và chén nung kim loại phải có chiều dày khoảng 0,5 mm.
Nếu xuất hiện những vết bẩn do cacbon cháy không hết, sử dụng chén platin nhỏ hoặc dùng chén niken-crom, ví dụ có chiều dày 0,25 mm, đường kính 15 mm và sâu 7 mm.
6.4 Thiết bị phụ trợ đo áp suất
6.4.1 Thiết bị điều chỉnh áp suất, để kiểm tra quá trình nạp oxy vào bom.
6.4.2 Đồng hồ đo áp suất, (ví dụ từ 0 MPa đến 5 MPa) để chỉ ra áp suất trong bom, có vạch chia bằng 0,05 MPa.
6.4.3 Van xả áp hoặc van giảm áp
Van xả áp hoặc van giảm áp hoạt động ở áp suất 3,5 MPa và được lắp vào đường nạp liệu để đề phòng nạp quá đầy bom.
CẢNH BÁO: Thiết bị dùng cho oxy áp lực cao phải được giữ sạch không dính dầu mỡ (mỡ chân không cao được khuyến nghị bởi nhà sản xuất có thể được sử dụng theo hướng dẫn sử dụng thiết bị). Không được thử hoặc hiệu chỉnh đồng hồ áp lực với hydrocacbon dạng lỏng.
6.5 Đồng hồ bấm giây, chỉ rõ bằng phút và giây
6.6. Cân
6.6.1 Cân dùng để cân mẫu
Có vạch chia ít nhất là 0,1 mg; 0,01 mg là thích hợp và nên sử dụng khi khối lượng của mẫu yêu cầu là 0,5 g hoặc nhỏ hơn (xem 8.2.1).
6.6.2 Cân dùng để cản nước của nhiệt lượng kế
Có độ chính xác đến 0,5 g (nếu không thì nước có thể được phân tán vào nhiệt lượng kế theo thể tích với độ chính xác yêu cầu, xem 8.3).
6.7 Bộ ổn nhiệt (tùy chọn), để cân bằng nước trong nhiệt lượng kế trước mỗi phép thử để xác định trước nhiệt độ ban đầu với độ chính xác ± 0,3 K.
6.8 Máy ép viên nén, có khả năng tạo lực là 10 t có thể bằng thủy lực hoặc cơ học và có một khuôn phù hợp để ép viên nén có đường kính khoảng 13 mm và khối lượng là (1,0 ± 0,2) g.
7 Chuẩn bị mẫu thử
Các mẫu để xác định nhiệt lượng phải được lấy phù hợp với ISO 18135 và phải được nhận ở phòng thử trong các hộp kín khí hoặc các bao gói còn niêm phong. Các mẫu nhiên liệu sinh học được sử dụng cho việc xác định nhiệt lượng phải là mẫu phân tích tiêu chuẩn (đã được nghiền để lọt qua rây thử nghiệm có kích thước lỗ là 1,0 mm) được chuẩn bị theo quy trình đưa ra trong ISO 14780. Đối với một số nguyên liệu sinh học rắn cần sàng với kích thước lỗ nhỏ hơn 1,0 mm (0,5 mm hoặc 0,25 mm) để đảm bảo lặp lại cần thiết và nguyên liệu cháy hoàn toàn.
Do nhiên liệu sinh học có khối lượng thể tích thấp, chúng phải được thử nghiệm ở dạng viên nén, khối lượng của một viên nén (1,0 ± 0,2) g được nén với một lực phù hợp để tạo ra mẫu thử rắn chắc không thể vỡ. Ngoài ra, phép thử còn được thực hiện khi phần mẫu thử ở dạng bột được đóng gói trong túi hoặc bao.
Mẫu phân tích tiêu chuẩn có hàm lượng ẩm cân bằng với hàm lượng ẩm phòng thử nghiệm. Độ ẩm phải được xác định đồng thời với việc cân mẫu để xác định nhiệt lượng hoặc mẫu phải được giữ trong hộp kín nhỏ cho đến khi phân tích độ ẩm để cho phép hiệu chỉnh thích hợp độ ẩm trong mẫu phân tích.
Việc xác định độ ẩm (Mad) của mẫu phân tích tiêu chuẩn phải được thực hiện theo phương pháp được chỉ ra trong ISO 18134-3.
Có thể xem sơ đồ xác định nhiệt lượng trong Phụ lục H.
8 Quy trình đo nhiệt lượng
8.1 Quy định chung
Quy trinh xác định nhiệt lượng bao gồm hai phép thử riêng biệt. Đốt cháy chất hiệu chuẩn (axit benzoic) và đốt cháy nhiên liệu sinh học, cả hai được tiến hành trong cùng một điều kiện quy định. Quy trình đo nhiệt lượng cho hai loại phép thử cơ bản là giống nhau. Trong thực tế, để loại bỏ các lỗi hệ thống xảy ta hoàn toàn tương tự, ví dụ sự mất nhiệt không kiểm soát được rò rỉ hoặc không được tính đến khi đánh giá sự gia tăng nhiệt độ hiệu chỉnh θ.
Phép thử bao gồm việc định lượng phản ứng đốt cháy (oxy áp suất cao trong bom nhiệt lượng) đối với những sản phẩm xác định của quá trình đốt cháy và đo sự thay đổi nhiệt độ gây ra do toàn bộ quá trình cháy trong bom.
Những phép đo nhiệt độ là cần thiết để đánh giá tăng nhiệt độ hiệu chỉnh θ được thực hiện trong chu kỳ trước, chu kỳ chính (phản ứng), và chu kỳ sau như mô phỏng trên Hình 2. Đối với nhiệt lượng kế loại đoạn nhiệt, theo nguyên tắc, chu kỳ trước và chu kỳ sau, kéo dài tương ứng với yêu cầu xác định nhiệt độ (đốt) đầu và cuối (xem Phụ lục A). Đối với nhiệt lượng kế đẳng nhiệt và nhiệt lượng kế tĩnh các chu kỳ trước và sau để hình thành tính chất trao đổi nhiệt của nhiệt lượng kế theo yêu cầu, để hiệu chỉnh sự thay đổi nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt trong chu kỳ chính của quá trình đốt. Chu kỳ trước và sau phải kéo dài hơn (xem Phụ lục B).
Lực khuấy phải được duy trì không đổi trong suốt thời gian phép thử để tạo tốc độ khuấy không đổi. Tốc độ khuấy quá mức dẫn đến tăng lực khuấy, gây khó khăn cho việc khuấy đều. Bộ khuấy không chắc chắn có thể gây ra dao động đáng kể về lực khuấy tức thời.
Trong quá trình đốt cháy phần đầu của bom sẽ nóng hơn các phần khác của bom, do đó cần đủ nước khuấy phía trên để duy trì gradien nhiệt độ nhỏ, phù hợp trong phần nước của nhiệt lượng kế, trong khi nhiệt độ của các phần khác tăng nhanh. Đối với hệ thống đo áp kế, thiết kế đặc biệt để xác định khu vực mà các điểm nóng có thể sinh ra (xem Phụ lục C).
Một số loại nhiên liệu sinh học nhất định phản ứng kém có thể để lại cặn dư có chứa một lượng mẫu đáng kể chưa cháy hoặc muội. Bằng cách trộn lẫn những mẫu này với một lượng phụ gia xác định (ví dụ axit benzoic, n-dodecane hoặc dầu parafin), hoặc bằng cách sử dụng túi, bao hình con nhộng hoặc sợi bông, bằng cách loại bỏ nước cất từ bom, hoặc bằng cách sử dụng áp suất nạp oxy thấp hơn, làm tăng thêm khả năng cháy của mẫu, dẫn đến quá trình cháy hết.
Chất trợ cháy phải ổn định về mặt hóa học, tinh khiết và các thành phần hóa học đã biết, có áp suất hơi thấp và tạo năng lượng cháy tốt, với độ chính xác trong khoảng 0,10 % cho từng loại vật liệu sử dụng, số lượng mồi cháy sử dụng phải được hạn chế ở mức tối thiểu cần thiết để đạt được sự cháy hoàn toàn của mẫu. Không được vượt lượng mà cấp một nửa năng lượng toàn phần trong một thí nghiệm. Tỷ lệ tối ưu của mẫu với mồi cháy phụ thuộc vào đặc tính của nhiên liệu và nhu cầu cần phải được xác định bằng thực nghiệm.
Khối lượng của vật liệu phụ phải được xác định chính xác nhất có thể để đóng góp của nó có thể tính toán chính xác, điều này đặc biệt quan trọng khi dầu hydrocacbon được sử dụng do năng lượng riêng trong quá trình đốt chất của nó cao hơn đáng kể so với năng lượng riêng của nhiên liệu sinh học.
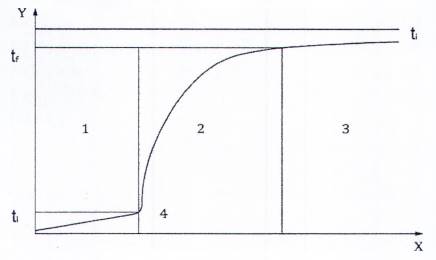
CHÚ DẪN
| X Thời gian | 1 Chu kỳ đầu |
| Y Nhiệt độ | 2 Chu kỳ chính |
| tf Nhiệt độ ở cuối chu kỳ chính | 3 Chu kỳ sau |
| ti Nhiệt độ đánh lửa | 4 Mồi cháy |
| tj Nhiệt độ vỏ (jacket) |
|
Hình 2 - Đường cong quan hệ giữa thời gian - nhiệt độ (nhiệt lượng kế đẳng nhiệt)
8.2 Chuẩn bị bom cho phép đo
8.2.1 Quy trình chung
Cân phần mẫu thử, viên nén hoặc nạp đầy túi đốt hoặc bao dạng viên trong chén nung với độ chính xác đến 0,01 % khối lượng mẫu hoặc tốt hơn. Có nghĩa là đối với thử 1 g mẫu (xem 9.2 và 10.2) cân chính xác đến 0,1 mg. Cân lượng mồi đốt và/hoặc dây đốt với độ chính xác tương đương với cân mẫu thử hoặc giữ khối lượng của mẫu không đổi trong giới hạn quy định đối với tất cả phép thử (xem 9.4 và 9.6.1)
Buộc chặt các dây đốt giữa các điện cực trong bom. Kiểm tra điện trở dây đốt của bom; đối với phần lớn các bom có điện trở không được vượt quá 5 Ω đến 10 Ω, tiến hành đo giữa các đầu nối bên ngoài của phần trên bom, hoặc giữa đầu nối điện cực cách điện và phần trên của bom.
Buộc hoặc gắn chặt mồi đốt vào dây đốt, đặt chén nung vào giá đỡ và cho mồi đốt tiếp xúc với viên nén mẫu dạng viên. Phải đảm bảo vị trí của chén nung được đặt trong bom sẽ đối xứng với thành bom.
Khi dây đốt dẫn điện, có thể chấp nhận áp dụng quy trình khác. Dùng một đoạn dây dài hơn, đủ để tạo một mạch vòng hở, được kết nối đến các điện cực. Sau khi lắp chén nung mạch hở được đưa vào tiếp xúc với viên nén mẫu dạng viên (trong một số trường hợp, quá trình đốt được kiểm soát tốt hơn khi dây được giữ ở một khoảng cách nhỏ phía trên viên nén mẫu), cần cẩn thận để tránh mọi tiếp xúc giữa dây đốt và chén nung, đặc biệt khi chén nung bằng kim loại bởi vì điều này sẽ dẫn đến làm ngắn mạch đánh lửa. Trong điều kiện này mồi đốt không cần thiết. Điện trở dây đốt của bom chỉ tăng lên chỉ một lượng nhỏ. Để biết thêm chi tiết về việc chuẩn bị bom, tham khảo thêm hướng dẫn của nhà sản xuất.
Đổ thêm nước cất vào bom. Lượng nước phải luôn luôn chính xác như nhau đối với cả hiệu chuẩn và xác định, ví dụ 1 mL ± 0,1 mL đối với 1 g mẫu thử (xem 9.2.1 và 9.2.2). Với một số nhiên liệu sinh học (và một số nhiệt lượng kế), việc đốt cháy hoàn toàn có thể đạt được bằng các loại nước cất ra ngoài từ bom hoặc sử dụng chất trợ cháy, trong một số trường hợp, tổng sự hấp thụ của các sản phẩm đốt dạng khí có thể cung cấp việc sử dụng một lượng nước cất lớn hơn (ví dụ 5 mL).
Lắp ráp bom và nạp oxy từ từ cho đến áp suất (3,0 ± 0,2) MPa mà không thay không khí ban đầu hoặc làm đầy bom (với van thoát mở, xem hướng dẫn của nhà sản xuất) với oxy trong 30 s, đóng van từ từ và nạp bom đến áp suất (3,0 ± 0,2) MPa. Cùng một quy trình phải được áp dụng cho cả việc hiệu chuẩn và xác định. Nếu sơ suất nạp oxy vào bom trên mức 3,3 MPa, hủy bỏ phép thử và làm lại từ đầu.
CẢNH BÁO - Không được chạm tay vào bom trong quá trình chiết nạp.
Bom đã sẵn sàng để lắp vào bình nhiệt lượng kế.
8.2.2 Sử dụng chất trợ cháy
Chất trợ cháy dạng lỏng: Sau khi khối lượng của viên nén được xác định, thêm từng giọt chất lỏng trợ cháy vào viên nén đặt trong chén nung (cho phép chất lỏng được hấp thụ) và lượng thêm vào được xác định chính xác bằng cân.
Chất trợ cháy dạng rắn: Sử dụng chất trợ cháy dạng rắn (axit benzoic được khuyến nghị) mà không có túi đốt hoặc viên hình con nhộng không được khuyến nghị (một hỗn hợp đồng nhất của vật liệu mẫu và chất trợ cháy trước khi ép viên thử nghiệm có thể khó mà đạt được).
Túi đốt hoặc viên đốt dạng viên: Viên đốt dạng viên hoặc túi đốt hoặc chén nung dễ cháy với chính xác nhiệt lượng đã biết (gelatin, acetobutyrate hoặc polyethylene) có thể được sử dụng như là chất trợ cháy theo hướng dẫn của nhà sản xuất. Chúng phải được cân chính xác trước khi nạp (xem 8.1). Vật liệu mẫu và chất trợ cháy như là axit benzoic phải được trộn một cách cẩn thận trong túi hoặc bao trước khi thử nghiệm.
8.3 Lắp ráp nhiệt lượng kế
Điều chỉnh nhiệt độ nước của nhiệt lượng kế chính xác đến ± 0,3 K so với nhiệt độ chọn lúc đầu và đổ nước vào bình nhiệt lượng kế với một lượng theo yêu cầu. Trong tất cả các phép thử lượng nước trong bình nhiệt lượng kế phải như nhau, chính xác đến 0,5 g hoặc chính xác hơn (xem 9.6.1). Phải đảm bảo mặt ngoài của bình nhiệt kế khô và sạch trước khi được đặt trong bộ ổn nhiệt. Lắp bom vào bình nhiệt lượng, sau đó đặt bình nhiệt lượng kế (chứa lượng nước điều chỉnh đúng) vào trong bộ ổn nhiệt.
Ngoài ra, hệ thống có thể được vận hành trên cơ sở tổng khối lượng nhiệt lượng kế không đổi (xem 9.6.2). Bom sau đó được đặt trong bình nhiệt lượng kế, trước đó được cân cùng với nước. Tổng khối lượng của bình nhiệt lượng kế, bao gồm bom và nước của nhiệt lượng kế phải như nhau, chính xác đến 0,5 g.
Nhiệt lượng kế đã lắp phải chứa đủ nước để phủ đều lên bề mặt trên của đầu và nắp bom.
CHÚ THÍCH: Cân nước chính xác đến 0,5 g áp dụng khi nhiệt dung hữu hiệu là 10 kJ/K.
Nước làm mát, kiểm soát nhiệt độ, máy khuấy,... được vận hành và điều chỉnh như hướng dẫn trong sổ tay thiết bị. Phải đảm bảo rằng bộ khuấy nhiệt lượng kế hoạt động tốt. Mỗi chu kỳ khoảng 5 min là mức bình thường để nhiệt lượng kế đạt đến trạng thái ổn định trong bộ ổn nhiệt hoặc vỏ bọc mà không phụ thuộc kiểu nhiệt lượng kế. Các tiêu chí về thời điểm đạt được trạng thái ổn định phụ thuộc vào nguyên lý làm việc của nhiệt lượng kế (xem Phụ lục A và B).
8.4 Phản ứng đốt cháy và đo nhiệt độ
Ngay khi nhiệt lượng kế đạt đến trạng thái ổn định, bắt đầu đọc nhiệt độ chính xác đến 0,001 K hoặc chính xác hơn. Các lần đọc thường cách nhau 1 min đủ để thiết lập tốc độ thay đổi nhiệt của chu kỳ trước hoặc kiểm tra chức năng hoạt động chuẩn của hệ thống đoạn nhiệt. Khi sử dụng nhiệt kế thủy ngân để đo nhiệt độ, gõ nhẹ vào nhiệt lượng kế khoảng 10 s trước mỗi lần đọc và cẩn thận để tránh lỗi hiển thị sai.
Vào thời điểm cuối chu kỳ trước khi nhiệt độ ban đầu ti được thiết lập, bắt đầu đốt mồi đốt bằng dây đốt. Giữ công tắc đóng trong khoảng thời gian cần thiết để đốt cháy dây đốt. Thông thường dòng điện tự động ngắt khi dây dẫn bắt đầu cháy hoặc nóng chảy một phần. Miễn là điện trở của mạch đánh lửa của quá trình cháy trong bom được giữ ở giá trị thấp bình thường của nó, năng lượng điện yêu cầu để bắt đầu phản ứng là rất nhỏ nên không cần thiết phải đo và tính toán một cách riêng biệt.
CẢNH BÁO - Không được để bất kỳ bộ phận nào của cơ thể gần nhiệt lượng kế trong quá trình đốt cũng như trong 20 s sau đó.
Tiếp tục đo nhiệt độ trong khoảng thời gian 1 min. Thời gian tương ứng với nhiệt độ ban đầu ti đánh dấu bắt đầu chu kỳ chính. Trong thời gian vài phút đầu sau khi mẫu đã cháy, khi nhiệt độ tăng lên nhanh chóng đọc chính xác đến 0,02 K là thích hợp. Đọc lại nhiệt độ chính xác đến 0,001 K hoặc chính xác hơn ngay sau khi bắt đầu chu kỳ chính, hoặc không chậm hơn 5 min sau khi bắt đầu chu kỳ chính. Đánh giá thời gian của chu kỳ trước, chính và sau, tổng số các số đọc nhiệt độ yêu cầu được nêu ra trong Phụ lục A và B.
8.5 Phân tích sản phẩm của quá trình cháy
Tại thời điểm cuối của chu kỳ sau, khi tất cả các số đọc nhiệt độ yêu cầu được hoàn thành, tháo bom khỏi nhiệt lượng kế, xả áp từ từ (theo hướng dẫn của nhà sản xuất) và tháo bom. Kiểm tra kỹ bên trong bom, chén nung, và bất kỳ chất cặn rắn nào để biết dấu hiệu của sự cháy không hết. Loại bỏ thử nghiệm nếu thấy mẫu chưa cháy hoặc có cặn bồ hóng. Tháo và đo bất kỳ đoạn không cháy của dây đốt.
CHÚ THÍCH: Các dấu hiệu khác của sự cháy không hoàn toàn thể hiện qua sự có mặt của khí carbon monoxide trong bom khí. Xả khí từ từ thông qua một ống dò phù hợp để phát hiện bất kỳ sự tồn tại nào của carbon monoxide và hiển thị mức độ 0,1 mL/L của carbon monoxide trong khí của quá trình cháy từ 300 mL bom tương ứng với sai số khoảng 10 J.
Làm sạch bom bằng nước cất và đổ vào cốc. Đảm bảo rằng mặt dưới của phần đầu bom, các điện cực và phần ngoài của chén nung cũng được rửa sạch.
Trong trường hợp phép thử hiệu chuẩn phân tích bằng axit nitric được hình thành từ hỗn hợp nước rửa bom cũng như bằng sắc ký ion (như nitrat) như được miêu tả trong TCVN 6494-1 (ISO 10304-1) hoặc pha loãng hỗn hợp rửa tới khoảng 50 mL và phân tích axit nitric ví dụ bằng cách chuẩn độ với dung dịch natri hydroxit (5.4.3) đến pH khoảng 5,5 hoặc bằng việc sử dụng dung dịch methyl màu cam (5.4.5) như là một chất chỉ thị.
Khi hiệu chỉnh “lưu huỳnh” và/hoặc axit nitric dựa trên khối lượng thực tế được hình thành trong bom, thì phân tích phần nước rửa bom theo quy trình mô tả trong ba nội dung tiếp theo (phương pháp a đến c) hoặc theo một phương pháp tương đương. Nếu biết lượng lưu huỳnh của nhiên liệu sinh học và lượng axit nitric điều chỉnh thì có thể bỏ qua việc phân tích dung dịch cuối trong bom (xem 10.1)
a) Xác định nitric và axit sulphuric được tạo thành (lần lượt là nitrat và sulfate) bằng sắc ký ion như trong TCVN 6494-1 (ISO 10304-1).
b) Pha loãng nước làm sạch bom đến khoảng 100 mL. Đun sôi nước làm sạch để đuổi khí cacbonic và chuẩn độ bằng dung dịch bari hydroxit (5.4.1), khi dung dịch vẫn nóng sử dụng dung dịch phenolphthalein (5.4.6) làm chất chỉ thị. Cho vào 20,0 mL dung dịch natri cacbonat (5.4.2) lọc dung dịch còn ấm và rửa chất kết tủa bằng nước cất. Khi nguội chuẩn độ dung dịch lọc bằng axit clohydric (5.4.4) sử dụng dung dịch methyl màu cam (5.4.5) đã làm chất chỉ thị, bỏ qua sự thay đổi màu của phenolphthalein.
c) Nếu hàm lượng lưu huỳnh đã được biết, hỗn hợp nước rửa bom đun sôi có thể được chuẩn độ, trong khi vẫn còn nóng với một phương pháp đơn giản hóa sử dụng dung dịch natri hydroxit (5.4.3) và phenolphthalein như chất chỉ thị (5.4.6).
8.6 Tăng nhiệt độ hiệu chỉnh θ
8.6.1 Tăng nhiệt độ quan sát được
Sự tăng nhiệt độ quan sát (tf- ti) là hiệu của nhiệt độ ở cuối chu kỳ chính, tf, và nhiệt độ ban đầu hoặc nhiệt độ cháy ti.
8.6.2 Nhiệt lượng kế đẳng nhiệt và nhiệt lượng kế tĩnh nhiệt
Ngoài sự tăng nhiệt độ gây ra do quá trình đốt cháy trong bom, sự tăng nhiệt độ quan sát bao gồm nhiệt góp từ sự trao đổi nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt và từ cường độ khuấy. Sự bù trừ cho sự trao đổi nhiệt được tạo ra từ hệ số điều chỉnh sự mất nhiệt Δtex bao gồm cả năng lượng khuấy, như trong công thức (1)
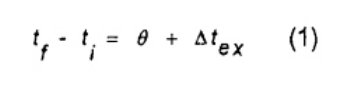
Do đó sự tăng nhiệt độ hiệu chỉnh θ, tính được bằng cách sắp xếp lại công thức (1) thành (2), và do đó công thức (2)
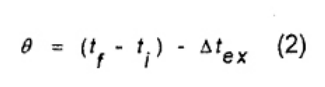
Có nhiều cách để đánh giá Δtex. Quy trình phổ biến nhất được sử dụng là phương pháp Regnault- Pfaundler và phương pháp ngoại suy Dickinson.
CHÚ THÍCH: Phương pháp Regnault - Pfaundler tự động đếm tính các biến động của mối quan hệ giữa nhiệt độ - thời gian đối với các loại mẫu khác nhau và do đó tăng độ tin cậy hơn trong phương pháp còn lại.
Hướng dẫn chi tiết để đánh giá giá trị đối với Δtex và sự tăng nhiệt độ hiệu chỉnh θ đối với nhiệt lượng kế đẳng nhiệt và nhiệt lượng kế tĩnh nhiệt được đưa ra trong Phụ lục B. Công thức kết quả đối với Δtex được tổng hợp trong công thức (3) và (4).
Phương pháp Regnault-Pfaundler (xem B.5.2)
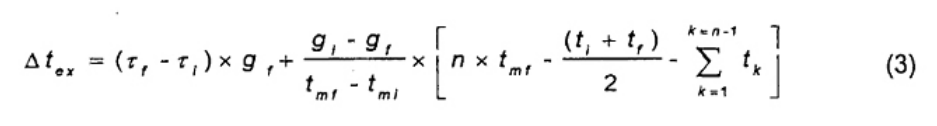
Trong đó
gi là tốc độ trượt ở chu kỳ trước (tốc độ ban đầu), tính bằng K/min;
gf là tốc độ trượt ở chu kỳ sau (tốc độ cuối) tính bằng K/min;
tmi là nhiệt độ trung bình ở chu kỳ trước, tính bằng °C;
tmf là nhiệt độ trung bình ở chu kỳ sau, tính bằng °C;
ti (= t0) nhiệt độ ban đầu của chu kỳ chính, tính bằng °C;
tf (= tn) nhiệt độ ở cuối chu kỳ chính, tính bằng °C;
tk là nhiệt độ đọc liên tiếp, tính bằng °C, được lấy cách nhau 1 min trong chu kỳ chính (t1 nhiệt độ sau khi chu kỳ chính bắt đầu 1 min và tn = tf);
□i là thời gian bắt đầu chu kỳ chính (thời gian đốt), tính bằng min;
□f là thời gian kết thúc chu kỳ chính, tính bằng min;
n là số tổng số lượng khoảng thời gian 1 min trong chu kỳ chính.
Phương pháp ngoại suy Dickinson (xem B.5.3)
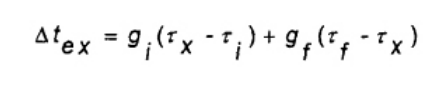 (4)
(4)
Trong đó
□x Thời gian, khi thay đổi nhiệt độ (tx- ti) bằng 0,6 lần thời gian tăng nhiệt độ quan sát (tf- ti), tính bằng min;
gi và gf là tốc độ hạ nhiệt, theo thứ tự tại □i và □f lần lượt. Tính theo phương pháp Regnault-Pfaundler, tính bằng min.
Ngoài ra nhiệt độ còn có thể được biểu thị bằng một số đơn vị tùy chọn (xem 9.6.1)
8.6.3 Nhiệt lượng kế đoạn nhiệt
Trong hệ thống đoạn nhiệt, sự trao đổi nhiệt theo định nghĩa là không đáng kể. Tuy nhiên, trên thực tế thông thường để bù đắp cho năng lượng khuấy bằng sự thay đổi nhiệt độ trong hệ thống kiểm soát đoạn nhiệt (xem Phụ lục A). Sự gia tăng nhiệt độ tăng hiệu chuẩn chính, θ được tính theo công thức (5).
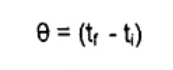 (5)
(5)
Công suất khuấy được biểu thị bằng sự chênh lệch nhiệt độ không đổi xuyên suốt quá trình thử nghiệm và được hiệu chỉnh dễ dàng, nhưng có thể kéo dài toàn bộ chu kỳ quan sát nhiệt độ.
Những hướng dẫn cụ thể để xác định giá trị tăng nhiệt độ hiệu chỉnh θ đối với nhiệt lượng kế đoạn nhiệt được đưa ra trong Phụ lục A.
8.6.4 Hiệu chỉnh nhiệt lượng kế
Khi sử dụng nhiệt kế thủy ngân - thủy tinh, việc hiệu chỉnh được chỉ dẫn trong chứng chỉ với nhiệt kế dùng để quan sát nhiệt độ ban đầu ti và nhiệt độ cuối tf.
8.7 Nhiệt độ chuẩn
Nhiệt độ tại thời điểm cuối của chu kỳ chính, nhiệt độ cuối tf là nhiệt độ chuẩn của mỗi phép thử riêng.
9 Hiệu chuẩn
9.1 Nguyên tắc
Sự đốt cháy axit benzoic được chứng nhận dưới các điều kiện quy định đối với khí cacbonic và nước lỏng đóng vai trò tạo ra sự thay đổi nhiệt độ nhiệt lượng kế của một đơn vị dẫn suất trong những đơn vị năng lượng xác định. Nhiệt lượng kế kiểu đốt cổ điển trong suốt chu kỳ kéo dài có thể được duy trì không đổi về khối lượng (nhiệt dung), dạng hình học và các bề mặt trao đổi nhiệt. Điều này cho phép thực hiện hiệu chuẩn thiết bị theo từng seri riêng, thiết lập nhiệt dung hữu hiệu, tức là hằng số hiệu chuẩn, ε của nhiệt lượng kế.
Hằng số hiệu chuẩn ε không được thay đổi nhiều trong toàn bộ thời gian, có thể có các sửa chữa nhỏ hoặc những thay đổi khác trong hệ thống được tính toán chính xác. Có một số thiết bị đo nhiệt lượng hoàn toàn tự động, tuy nhiên là về mặt vật lý kém chính xác và do vậy yêu cầu hiệu chỉnh thường xuyên, thậm chí hàng ngày đối với một số hệ thống.
Các sai số hệ thống có thể xuất hiện, ví dụ từ sự bay hơi nước của nhiệt lượng kế, từ sự trao đổi nhiệt không kiểm soát dọc theo các đường dẫn và/hoặc sự không hoàn hảo và sự trễ trong hệ thống điều khiển nhiệt độ đoạn nhiệt trong chu kỳ phản ứng. Việc loại bỏ lỗi này phụ thuộc nhiều vào sự tương đồng giữa các phép thử hiệu chỉnh và sự cháy của các phần thử nghiệm với mối quan hệ thời gian - nhiệt độ và sự thay đổi toàn phần về nhiệt độ của nhiệt lượng kế. Những sự biến đổi có hệ thống về khối lượng của axit benzoic được sử dụng trong các phép thử hiệu chuẩn là cách thích hợp để thiết lập các yêu cầu về “độ tương đồng” đối với một hệ thống đo nhiệt lượng cụ thể (xem 9.3).
9.2 Chất hiệu chuẩn
9.2.1 Điều kiện chứng nhận
Giá trị chứng nhận cho năng lượng đốt axit benzoic đối với một quá trình, trong đó khối lượng của mẫu tính bằng gam và lượng nước ban đầu lần lượt bằng ba lần thể tích bom trống tính bằng gam/lít, áp suất oxy ban đầu là 3,0 MPa và nhiệt độ chuẩn là 25 °C. Sản phẩm của quá trình đốt cháy được xác định là khí cacbon dioxit, nước lỏng và một khối lượng tương đương cacbon dioxit hòa tan trong pha lỏng. Các axit nitric hình thành được hiệu chỉnh theo năng lượng của quá trình, trong đó axit bị phân hủy để tạo thành nước lỏng và khí nitơ và oxy. Khi hiệu chuẩn được thực hiện dưới những điều kiện khác nhau, giá trị của chứng chỉ phải được điều chỉnh. Giá trị bằng số để hiệu chỉnh cho những sai lệch này được nêu ra trong chứng chỉ.
9.2.2 Điều kiện hiệu chuẩn
Điều kiện hiệu chuẩn xác định toàn bộ những điều kiện của nhiệt lượng kế để cho các phép xác định nhiên liệu tiếp theo. Đối với bom có thể tích ban đầu 300 mL, thông thường sử dụng 1 g chất hiệu chuẩn và 1 mL nước ban đầu (xem 8.2.1). Đối với bom với thể tích khoảng 200 mL, 0,6 g axit benzoic là thích hợp, lượng nước cần giảm tương ứng (trong cả hiệu chuẩn và xác định).
CHÚ THÍCH 1: Các điều khoản điều chỉnh (theo mỗi g axit benzoic) đối với những thay đổi từ các điều kiện chứng nhận, theo chứng nhận của axit benzoic, đối với áp suất, khối lượng phần thử, khối lượng nước và nhiệt độ tham chiếu ban đầu của phép thử lần lượt là 5 J/MPa, 1,1 J/gl-1, 0,8 J/gl-1 và -1,2 J/K.
CHÚ THÍCH 2: Áp suất ban đầu của oxy và nhiệt độ tham chiếu được duy trì trong khoảng (3,0 ± 0,3) MPa và (25 ± 2) °C lần lượt, những điều kiện chứng nhận gây ra bởi sự sai lệch áp suất và/hoặc những thay đổi nhiệt độ nằm trong khoảng ± 3 J/g thì không cần tính.
CHÚ THÍCH 3: Sự sai lệch đáng kể nhất từ các điều kiện chứng nhận thường gây ra nếu lượng nước lớn hơn, ví dụ 5 ml/g chất hiệu chuẩn được sử dụng. Đối với bom có thể tích 300 mL, nguyên nhân này làm tăng giá trị được chứng nhận là 11 J/g. Nếu sử dụng 1,0 g axit benzoic và 5,0 mL nước trong bom 200 mL, giá trị được chứng nhận tăng lên 20 J/g. Sự thay đổi chủ yếu gây ra bởi sự tăng cacbon dioxit hòa tan trong bom. Nếu không sử dụng nước giá trị chứng nhận giảm 2 J/g.
CHÚ THÍCH 4: Khi tổng nhiệt dung nhiệt lượng kế nhỏ, ví dụ trong các hệ thống đo áp kế, thì cần giảm khối lượng mẫu để giới hạn sự thay đổi nhiệt độ (xem Phụ lục C).
9.3 Phạm vi làm việc có hiệu lực của nhiệt dung hữu hiệu ε
Có thể phải thay đổi lượng chất hiệu chuẩn ít nhất là ± 25 % mà không cần có sự thay đổi đáng kể những giá trị nhiệt dung hữu hiệu. Nếu không thì các giới hạn làm việc đối với giá trị không đổi của ε sẽ được xác định theo tổng nhiệt độ tăng lên đo được. Tất cả các phép đo tiếp theo về giá trị nhiệt dung sẽ được duy trì trong giới hạn này của nhiên liệu sinh học được đo.
Một biểu đồ về các giá trị nhiệt dung hữu hiệu, ε, như một hàm số của khối lượng chất hiệu chuẩn được sử dụng, cho thấy rằng có thể có xu hướng thay đổi đáng kể về nhiệt dung hữu hiệu đối với một nhiệt lượng kế cụ thể. Trong thử nghiệm này, khối lượng chất hiệu chuẩn phải được thay đổi từ 0,7 g đến 1,3 g hoặc một lượng tương đối tương đương và tối thiểu phải thực hiện tám thí nghiệm. Không cần thiết thay đổi khối lượng nước ban đầu trong bom.
Một cách thuận tiện để kiểm tra hệ thống đã được hiệu chuẩn bằng cách đốt cháy, ví dụ 1,0 g mẫu thì phải sử dụng axit benzoic một lượng chưa biết. Giá trị trung bình từ ba lần thực hiện tương ứng trên khối lượng mẫu lần lượt là 0,7 g và 1,3 g được so sánh với giá trị chứng nhận. Thông thường phương pháp này đủ để xác nhận nhiệt dung hữu hiệu có là hằng số trong khoảng nhiệt lượng được sinh ra hay không. Nhìn chung các sai lệch theo chiều hướng có giá trị tỏa nhiệt thấp đối với các mẫu có khối lượng lớn hơn tương đương với việc xác nhận được các giá trị ε theo chiều cao khi lấy ra từ các mẫu lớn. Sử dụng axit benzoic như là một chất thử đặc biệt hữu ích trong việc kiểm tra hiệu suất của hệ thống tự động.
Phạm vi quy định đối với một giá trị ε đã được xác minh phụ thuộc vào sự thay đổi tổng giá trị tỏa nhiệt của nhiên liệu phân tích. Nhìn chung, xu hướng vừa phải đối với ε, ví dụ ± 0,3 % đối với sự tăng nhiệt độ quan sát thay đổi ± 30 % , có thể bù bằng nhiệt dung hữu hiệu ε như là một hàm số của (tf - ti) trong vài phạm vi xác định. Tương tự, nếu sử dụng cảm biến phi tuyến tính, ε có thể được biểu thị như là một hàm (tuyến tính) của (tf - ti), đưa ra các tiêu chí chặt chẽ cũng được thiết lập cho tf và ti được phép thay đổi bao nhiêu.
Độ lệch ε là một giá trị không đổi, như đã giải thích, nguyên nhân do thiết kế của nhiệt lượng kế và/hoặc sai lỗi trong việc kiểm soát nhiệt độ của thiết bị. Đối với cấu tạo đặc biệt, kiểm tra quá trình đặt các điều kiện hiệu chuẩn phải được tiến hành khi thiết bị là mới hoặc đại tu hoặc khi di chuyển đến vị trí khác, và khi có sự thay đổi hệ thống kiểm soát nhiệt độ. Một số hệ thống đoạn nhiệt cần kiểm tra thường xuyên hơn (xem Phụ lục A). Một số nhiệt lượng kế tự động yêu cầu hiệu chuẩn với các quy định bắt buộc về khối lượng mẫu (xem Phụ lục C).
9.4 Các đóng góp phụ
Ngoài năng lượng từ quá trình đốt cháy axit benzoic, còn có các đóng góp từ việc đốt cháy mồi đốt và sự hình thành axit nitric (từ nitơ “không khí” trong pha khí). Sự đóng góp từ mồi đốt được lấy ra từ lượng tham gia vào và năng lượng tương ứng của sự đốt. Bất cứ dây mồi đốt nào không phản ứng phải được tính đến, ví dụ bị trừ đi số lượng ban đầu.
Lượng axit nitric tạo thành được xác định ở dung dịch cuối cùng của bom, ví dụ bằng axit chuẩn độ (xem 8.5).
Trong hầu hết các hệ thống, sự đóng góp từ mồi đốt có thể được giữ gần như giống nhau trong tất cả các phép thử (nhiên liệu và hiệu chuẩn) và do đó có thể được cho một giá trị không đổi. Đối với một loại bom đã có, lượng axit nitric được tạo thành trong các phép thử hiệu chuẩn là có tỷ lệ xấp xỉ với lượng axit benzoic bị đốt cháy.
9.5 Quy trình hiệu chuẩn
Đối với loạt các phép hiệu chuẩn thông thường, sẽ thực hiện năm lần đốt cháy axit benozic đạt yêu cầu. Mẫu được đốt ở dạng viên (xem 5.5). Quá trình đo nhiệt lượng được miêu tả trong điều 8 phải được tuân theo. Các khuyến cáo liên quan khối lượng mẫu và lượng nước ban đầu của bom được nêu trong 9.2.2. Sẽ lợi thế nếu sử dụng chén nung khối lượng nhỏ để đốt axit benzoic. Nhiệt độ ban đầu sẽ được chọn như nhiệt độ chuẩn của phép thử (được xác định là tf; xem 8.7) trong khoảng phạm vi của nhiệt độ chuẩn.
Thiết kế phép thử hiệu chuẩn, dưới dạng áp suất oxy, lượng nước bom, nhiệt độ chuẩn, trong những chu kỳ trước, chính và sau,... Sẽ xác định quy trình cụ thể cho sự cháy nhiên liệu tiếp theo.
Khi nhiệt dung hữu hiệu ε của nhiệt lượng kế có thể không được xem như một hằng số trong phạm vi làm việc yêu cầu nhưng cần biểu thị như một hàm của (tf - ti) (xem 9.3), số lượng phép thử hiệu chuẩn phải được tăng lên tám hoặc nhiều hơn. Khối lượng của mẫu cho các thí nghiệm được chọn những giá trị cho sự thay đổi nhiệt độ trong toàn bộ phạm vi làm việc, với một số phép đo lặp lại xung quanh điểm cuối để xác định độ dốc của ε với mối quan hệ (tf - ti).
9.6 Tính nhiệt dung hữu hiệu cho từng phép thử
9.6.1 Cơ sở khối lượng nước không đổi của nhiệt lượng kế
Đối với các hệ thống trong đó lượng nước trong bình nhiệt lượng kế được duy trì bằng nhau trong tất cả các phép thử, ε được tính theo công thức (6)
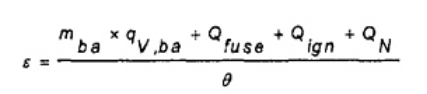 (6)
(6)
Trong đó
mba là khối lượng của axit benzoic (5.5), tính bằng gam;
qv,ba là giá trị nhiệt lượng toàn phần đã được chứng nhận ở thể tích không đổi, cho axit benzoic (xem 9.2.1), tính bằng J/g;
Qfuse là phần đóng góp từ quá trình cháy của mồi cháy, tính bằng Jun;
Qign là phần đóng góp từ sự oxy hóa của dây đốt, tính bằng Jun;
QN là phần đóng góp từ quá trình hình thành axit nitric (từ nước lỏng và khí nitơ và oxy; xem 8.5 và 9.2.1), tính bằng Jun;
θ là nhiệt độ tăng hiệu chuẩn, tính bằng K hoặc đơn vị tùy chọn (xem 3.6 và 8.6).
CHÚ THÍCH: Thông thường ε được biểu thị bằng Jun/K. Khi θ biểu thị theo đơn vị khác, thì ε sẽ được biểu thị bằng J trên đơn vị khác này ví dụ J/Ω.
Phần đóng góp từ quá trình cháy của một dây mồi đốt bông là 17500 J/g và từ dây niken-crom 6000 J/g. Dây platin nóng chảy và rắn lại và không có sự đóng góp thực nào cả.
Trong tất cả các thí nghiệm, khi tổng Qfuse+ Qign là gần như giống nhau, trong khoảng vài Jun, nó có thể được cho là một giá trị không đổi. Không khuyến cáo chung cho việc kết hợp Qfuse + Qign trong giá trị của ε, trừ khi giá trị này nhỏ và sự thay đổi của θ nhỏ hơn ± 20 %.
Đối với sự hình thành của axit nitric từ nước dạng lỏng và khí nitơ và oxy lượng đóng góp là 60
J/mmol.
QN tính bằng Jun, được tính toán từ hàm lượng nitrat tìm thấy w(NO3), tính bằng mg, được xác định bằng sắc tố ion sử dụng công thức (7).
QN = 0,97 x w(NO3) (7)
Hoặc
Từ kết quả chuẩn độ của [c(NaOH) = 0.1 mol/L], tính bằng mL sử dụng công thức QN = 6,0 x ml- (xem 8.5)
9.6.2 Cơ sở tổng khối lượng không đổi của nhiệt lượng kế
Khi hệ thống được hoạt động mà tổng khối lượng của bình nhiệt lượng kế và thiết bị bom được lắp đặt và lượng nước luôn luôn giống nhau, lượng nước bên trong bình có thể thay đổi chút ít, phụ thuộc chủ yếu vào khối lượng của chén nung được sử dụng. Để thuận tiện, xác định ε0 như là nhiệt dung hữu hiệu cho nhiệt lượng kế theo giả thuyết không có chén nung trong bom, được đưa ra theo công thức (8).
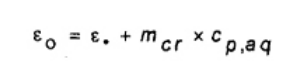 (8)
(8)
Trong đó
ε Bằng ε được xác định trong 9.6.1;
mcr Khối lượng của chén nung được sử dụng trong phép thử hiệu chuẩn (xem chú thích dưới đây), tính bằng gam;
Cp,aq Nhiệt dung riêng của nước, tính bằng J/(g-K), khi giá trị ε tính bằng J/K. Ở nhiệt độ 25 °C, nó bằng 4,18 J/(g·K).
Khi tùy ý sử dụng “đơn vị nhiệt độ”, giá trị của Cp,aq cũng phải được điều chỉnh tương ứng. Mối quan hệ giữa kelvin và đơn vị được sử dụng chỉ cần được biết trong khoảng ± 10 % cho mục đích này.
CHÚ THÍCH: Trong công thức ε0 số hạng thứ hai có nguồn gốc từ:
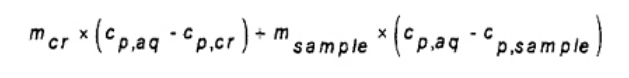
Số hạng thứ hai của biểu thức này có thể được kết hợp trong ε0 mà không làm mất đi độ chính xác, vì giá trị của nó sẽ không thay đổi đáng kể giữa phép thử hiệu chuẩn và phép thử nhiên liệu. Biểu thức này sau đó được rút gọn như công thức (9).
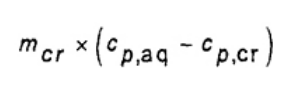 (9)
(9)
Trong hầu hết các trường hợp, có thể rút gọn thành (mcr x cp,aq) cũng như được đưa ra trong công thức đối với ε0. Tuy nhiên, khi sử dụng nhiều loại chén nung, phải tính đến nhiệt dung của chén. Ví dụ như, nếu dùng chén nung platin 10 g cho phép thử hiệu chuẩn và dùng chén nung thạch anh 10 g để đốt cháy nhiên liệu, sai số bằng 6 J/K) được đưa ra nếu cp,cr không được tính đến, tương ứng với 18 J cho sự tăng nhiệt độ khoảng 3 K. Công thức hiệu chuẩn được tính chính xác như công thức (10).
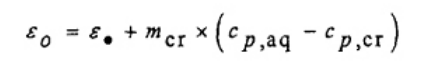 (10)
(10)
Nhiệt dung riêng đối với platin, thạch anh và thép lần lượt là 0,133 J/(g·K), 0,74 J/(g·K) và 0,45 J/(g·K).
9.7 Độ chụm của giá trị trung bình của nhiệt dung hữu hiệu ε
9.7.1 Giá trị không đổi của ε
Tính toán giá trị trung bình số học ε(n) và độ lệch tiêu chuẩn từ các kết quả của các phép thử hiệu chuẩn riêng ε (xem 9.6.1) hoặc εo (xem 9.6.2). Độ lệch tiêu chuẩn không được vượt quá 0,20 %. Tất cả các kết quả từ những đợt hiệu chuẩn cụ thể sẽ bao gồm trong các phép tính; chỉ khi các phép thử với bằng chứng của sự đốt cháy không hoàn toàn sẽ bị loại bỏ.
Nếu yêu cầu độ chụm được đáp ứng, giá trị trung bình số học ε(n) hoặc εo(n) lần lượt được coi là giá trị đối với nhiệt dung hữu hiệu của nhiệt lượng kế.
Nếu không đáp ứng yêu cầu về độ chụm, thì xác định nguyên nhân gây ra kết quả không chính xác và tiến hành các phép thử hiệu chuẩn mới.
9.7.2 ε là hàm số của sự tăng nhiệt độ quan sát được
Khi ε không được cho là không đổi, liệt kê các giá trị của ε (xem 9.6.1) hoặc εo (xem 9.6.2) với các giá trị tương ứng cho sự tăng nhiệt độ quan sát được (tf - ti) đối với Δt đã được xác định rõ. Phù hợp với những kết quả theo đường thẳng bởi sự mất tuyến tính với Δt là sự biến thiên độc lập. Ngoài ra việc tính các hệ số a và b như trong công thức (11).
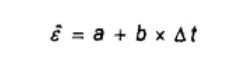 (11)
(11)
Ước lượng sự thay đổi s2 xung quanh đường thẳng sẽ được tính. Để thuận tiện có thể được sử dụng θ thay cho Δt.
Độ lệch chuẩn s không được vượt quá 0,20 %. Chỉ những kết quả từ phép thử với bằng chứng cháy không hoàn toàn sẽ loại bỏ khỏi phép tính.
Nếu yêu cầu độ chụm được đáp ứng, ![]() , như được xác định ở trên được coi là giá trị nhiệt dung hữu hiệu của nhiệt lượng kế sẽ được sử dụng trong phép tính giá trị nhiệt lượng cho nhiên liệu. Dải giá trị làm việc của sự tăng tăng nhiệt độ quan sát được sẽ phải xác định rõ.
, như được xác định ở trên được coi là giá trị nhiệt dung hữu hiệu của nhiệt lượng kế sẽ được sử dụng trong phép tính giá trị nhiệt lượng cho nhiên liệu. Dải giá trị làm việc của sự tăng tăng nhiệt độ quan sát được sẽ phải xác định rõ.
Nếu không được đáp ứng yêu cầu về độ chụm, xác định nguyên nhân gây ra kết quả không chính xác và thực hiện một loạt phép thử hiệu chuẩn mới.
9.8 Xác định lại nhiệt dung hữu hiệu
Khi thay đổi bất cứ phần nào trong hệ thống, nhiệt dung hữu hiệu trung bình phải được xác định lại (xem 9.3). Nhiệt dung hữu hiệu trung bình sẽ được xác định lại trong khoảng thời gian không quá sáu tháng.
CHÚ THÍCH: Đối với một hệ thống mới, nên kiểm tra hiệu chuẩn thường xuyên bằng cách thực hiện một số phép thử hàng tháng sử dụng axit benzoic như là chất thử (xem 9.3).
Khi hệ thống không thay đổi, giá trị trung bình mới của ε phải nằm trong 0,25 % của giá trị trước. Nếu có sự khác biệt lớn hơn 0,25 % quy trình thử phải được kiểm tra, xác minh và tìm nguyên nhân của vấn đề và xử lý.
10 Giá trị nhiệt lượng toàn phần
10.1 Quy định chung
Những điều kiện đo nhiệt lượng đốt cháy nhiên liệu sinh học phải phù hợp với các điều kiện phép thử hiệu chuẩn (xem 8.2.1, 9.2.2 và 9.5). Với quy trình đo nhiệt lượng đã kiểm tra là thỏa mãn, thì xác định sự cháy hoàn toàn của nhiên liệu sinh học là điều quan trọng nhất.
Một số nhiên liệu sinh học có thể là khó để cháy hoàn toàn trong bom và có thể phải được đốt cháy với chất trợ cháy hoặc bằng việc sử dụng túi đốt hoặc viên đốt hình con nhộng, với năng lượng đốt cháy được thiết lập tốt hoặc bởi việc loại bỏ nước cất trong bom (xem Điều 7 và 8.2) hoặc bằng việc giảm áp suất oxy.
Hỗn hợp rửa bom đối với axit sulphuric và axit nitric phải được phân tích, sử dụng quy trình được miêu tả trong 8.5 hoặc theo cách khác, được xem là giá trị không đổi hoặc giá trị mặc định để lưu huỳnh sẽ được sử dụng cho việc hiệu chuẩn (xem 10.3.2 và E.4).
Sự tạo thành axit nitric phụ thuộc vào nhiệt độ đốt cháy và được tăng cường bởi nitơ trong mẫu. Thông thường việc điều chỉnh axit nitric khác nhau đối với sự đốt nhiên liệu và axit benzoic. Nó có thể thay đổi một cách đáng kể cho những loại nhiên liệu sinh học khác nhau. Những biến đổi trong việc hiệu chính axit nitric thường thể hiện rõ trên ranh giới. Khi hàm lượng lưu huỳnh được xác định riêng trên mẫu, việc hiệu chính axit nitric có thể coi như một hằng số tính theo gam của giá trị mẫu. Một cách tương tự sẽ được chấp nhận cho phép thử hiệu chuẩn.
10.2 Đốt cháy
Thực hiện sự đốt kép. Mẫu đại diện lấy từ mẫu phân tích (xem Điều 7) sử dụng viên đốt được nén hoặc viên hình con nhộng. Lấy một lượng sao cho sự tăng nhiệt độ quan sát nằm trong phạm vi của các phép thử hiệu chuẩn. Quy trình đo nhiệt lượng được mô tả trong 8.2.1 đến 8.6 phải được tuân thủ, với các điều kiện như nhau như trong các phép thử hiệu chuẩn.
Thông thường, khối lượng khoảng 1 g mẫu nhiên liệu sinh học là đủ. Nếu sự tăng nhiệt độ quan sát nằm ngoài phạm vi hợp lệ đối với ε, kích thước mẫu của nhiên liệu sinh học phải được điều chỉnh để đáp ứng phạm vi nhiệt độ tăng hợp lệ hoặc việc hiệu chuẩn phải được xác định đối với phạm vi mở rộng của ε (xem 9.3).
10.3 Tính giá trị nhiệt lượng toàn phần
10.3.1 Quy định chung
Sự thay đổi năng lượng cho toàn bộ quá trình của bom được cho trước theo nhiệt dung hữu hiệu ε nhân với sự tăng nhiệt độ hiệu chuẩn θ. Để tính năng lượng của sự đốt cháy mẫu nhiên liệu sinh học, những đóng góp năng lượng từ tất cả các phản ứng phụ phải được trừ đi từ ε x θ (xem 9.4). Khi sử dụng chất trợ cháy được, thường số lượng đóng góp phụ lớn nhất và phải được tính một cách chính xác.
Hơn thế nữa, lưu huỳnh trong mẫu tạo ra axit sulfuric trong bom, trong khi trạng thái yêu cầu của lưu huỳnh đối với giá trị nhiệt lượng của nhiên liệu là khí lưu huỳnh dioxit (xem 4.1). Điều này được tính cho sự phân hủy, ở thể tích không đổi axit sulphuric thể lỏng sang thành thành khí lưu huỳnh dioxit, khí oxy và nước lỏng.
Giá trị nhiệt lượng nhận được đối với nhiên liệu sinh học là giá trị nhiệt lượng toàn phần ở thể tích không đổi.
10.3.2 Cơ sở khối lượng không đổi của nhiệt lượng kế
Tính giá trị nhiệt lượng toàn phần ở điều kiện thể tích không đổi của các mẫu nhiên liệu cho từng phép thử riêng theo công thức (12)
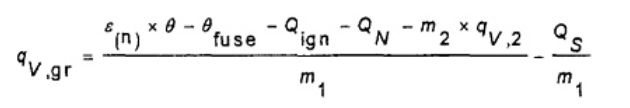 (12)
(12)
Trong đó
qv,gr là giá trị nhiệt lượng toàn phần ở thể tích không đổi của nhiên liệu được phân tích, tính bằng J/g;
ε(n) là giá trị trung bình nhiệt dung hữu hiệu của nhiệt lượng kế được xác định trong hiệu chuẩn (xem 9.6.1), tính bằng Jun/K hoặc thay thế bởi Jun trên đơn vị tùy chọn (xem chú thích 9.6.1);
Qs lấy được do hiệu chỉnh lưu huỳnh từ axit sulphuric loãng thành lưu huỳnh dioxit dạng khí, tính bằng Jun;
m1 là khối lượng mẫu nhiên liệu, tính bằng gam;
m2 là khối lượng của chất trợ cháy nếu có, tính bằng gam;
qv,2 là giá trị nhiệt lượng toàn phần ở thể tích không đổi của chất trợ cháy (nếu có), tính bằng J/g;
θ, Qfuse, Qign và QN được xác định trong 4.9.6.1.
CHÚ THÍCH: Khi không có hiệu chỉnh cho m2, để đảm bảo qv,2 hợp lệ "cân từng gam trong không khí".
Năng lượng yêu cầu để tính sự đóng góp từ mồi đốt, dây đốt, và sự hình thành của axit nitric được đưa ra trong 9.6.1. Nhiệt dung riêng của nước và một số vật liệu của chén nung thông thường được đưa ra trong 9.6.2.
Để tính cho phản ứng khi axit suphuric phân hủy vào trong nước và khí lưu huỳnh dioxit và oxy, hiệu chỉnh bằng 302 J/mmol, tương đương với 9,41 J/mg lưu huỳnh mà lần lượt tương ứng với giá trị Qs/m1 là 94,1 J/g của mẫu cho 1 % lưu huỳnh trong mẫu phân tích như được đưa ra trong công thức.
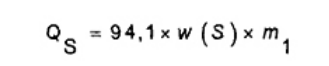 (13)
(13)
Trong đó
w(S) Hàm lượng lưu huỳnh của mẫu (được phân tích), tính bằng phần trăm.
Hàm lượng lưu huỳnh của mẫu phải được xác định hoặc thay thế, một giá trị điển hình hoặc mặc định thể được sử dụng (xem E.4 và Phụ lục G). Nếu hàm lượng lưu huỳnh không được xác định, giá trị sử dụng phải được chỉ ra trong báo cáo thử nghiệm.
Khi sử dụng quy trình phân tích nêu ở 8.5, sự đóng góp từ lưu huỳnh và axit nitric được đưa ra trong công thức (14) đến (19):
a) Xác định bằng sắc ký ion
![]()
![]()
Trong đó
w(SO4) là hàm lượng lưu huỳnh và w(NO3) hàm lượng nitrate, tính bằng mg;
b) Chuẩn độ bằng bari hyđroxit và axit clohydric
![]()
![]()
Trong đó
V1 là thể tích được sử dụng, tính bằng ml của dung dịch bari hydroxit (5.4.1);
V2 là thể tích được sử dụng, tính bằng ml của dung dịch axit clohydric (5.4.4);
c) Chuẩn độ bằng natri hydroxit
Sự hiệu chỉnh đối với axit nitric và axit sulphuric được tính toán sử dụng hiệu chuẩn kết hợp QN,S thay cho QN cùng với một sự hiệu chỉnh bổ sung đối với lưu huỳnh (QS.add.) vào công thức của qv,gr (một phần của QS, cụ thể là 2 x 60 J/mmol được bao gồm trong QN,S; hiệu chỉnh bổ sung cần thiết là 302 - 2 x 60 = 182 J/mmol tương đương với 5,7 J/mg lưu huỳnh trong mẫu).
![]()
![]()
Trong đó
V là thể tích được sử dụng, tính bằng ml của dung dịch natri hydroxit (5.4.3);
w(S) Hàm lượng lưu huỳnh của mẫu (được phân tích), tính bằng phần trăm.
Giá trị điều kiện chứng nhận có thể được sử dụng cho axit benzoic như chất trợ cháy, nếu 1 mL nước được sử dụng từ đầu trong bom. Đối với lượng nước lớn hơn, khuyến cáo điều chỉnh ứng với giá trị mỗi gam phù hợp với lượng nước giới hạn trong chứng chỉ.
Giá trị trung bình của phép xác định được coi là giá trị tỏa nhiệt lượng toàn phần của mẫu nhiên liệu phân tích.
10.3.3 Cơ sở tổng khối lượng không đổi của nhiệt lượng kế
Trong trường hợp này, giá trị trung bình của nhiệt dung hữu hiệu của εo(n) là một trong những giá trị được rút ra từ các kết quả riêng εo (xem 9.6.2) và đại diện cho nhiệt lượng kế không có chén nung. Giá trị của ε hợp lệ cho các phép thử nhiên liệu cụ thể được đưa ra trong công thức (20)
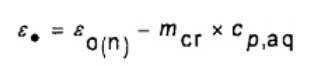 (20)
(20)
Trong đó
mcr là khối lượng của chén nung được sử dụng trong quá trình đốt cháy nhiên liệu, tính bằng g
Các kí hiệu khác được quy định trong 9.6.2
Nếu nhiệt dung của chén nung được tính đến (xem chú thích 9.6.2) khi tính các giá trị εo, (cp,aq- cp,cr) phải được thay thế cho cp,aq để tính ε• .
ε• thay cho ε(n) trong công thức (12) để tính giá trị nhiệt lượng toàn phần ở thể tích không đổi của phần nhiên liệu sinh học thử nghiệm từ các phép thử riêng. Giá trị trung bình của các phép xác định kép được coi là kết quả đối với mẫu phân tích chung của nhiên liệu sinh học.
10.3.4 ε như là hàm số của sự tăng nhiệt độ quan sát được
Khi có yêu cầu nhiệt dung hữu hiệu của nhiệt lượng kế được biểu thị như một hàm số của sự tăng nhiệt độ quan sát (xem 9.3 và 9.7.2) ε(n) trong Công thức (12) và εo(n) và Công thức (20) lần lượt sẽ được thay thế bằng công thức (21).
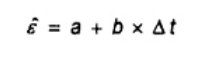 (21)
(21)
Trong đó các hệ số a và b được lấy từ các hiệu chuẩn (xem 9.7.2).
Δt là kí hiệu đối với sự tăng nhiệt độ quan sát (tf- ti), tính bằng °C (K) hoặc sử dụng đơn vị cho phép thử nhiên liệu cụ thể. Để thuận tiện, θ có thể được sử dụng thay thế Δt (xem 9.7.2).
Giá trị trung bình của các phép xác định kép được coi là giá trị kết quả cho các mẫu phân tích chung của nhiên liệu sinh học.
10.4 Biểu thị kết quả
Độ ẩm của mẫu phân tích cụ thể là hiệu số liên quan với việc tính trên các cơ sở khác, được khuyến nghị để tính giá trị nhiệt lượng toàn phần, ở thể tích không đổi cho nhiên liệu sinh học khô, sử dụng Công thức (22).
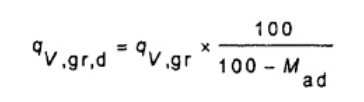 (22)
(22)
Trong đó
qv,gr,d là giá trị nhiệt lượng toàn phần ở thể tích không đổi (không có ẩm), tính bằng J/g;
Mad là độ ẩm của mẫu phân tích chung, tính bằng phần trăm khối lượng;
qv,gr Được xác định theo công thức (12).
Giá trị nhiệt lượng ở thể tích không đổi yêu cầu trên cơ sở về hàm lượng ẩm qv,gr,m được tính theo công thức (23).
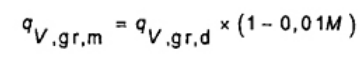 (23)
(23)
Trong đó M là độ ẩm, tính bằng phần trăm khối lượng cho giá trị nhiệt lượng được yêu cầu, thông thường đối với nhiên liệu được lấy mẫu hoặc được đốt cháy (tổng hàm lượng ẩm nhận được Mar) và công thức (24).
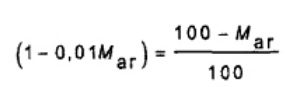 (24)
(24)
Kết quả phải được báo cáo chính xác đến bội số của 10 J/g liên quan đến trạng thái thể tích không đổi, toàn phần (nước lỏng) và cơ sở về hàm lượng ẩm (khô hoặc “mẫu đã lấy” nếu điều này là hợp lý).
Việc xác định độ ẩm (M hoặc Mar) phải được thực hiện theo phương pháp được chỉ ra trong ISO 18134-1 hoặc ISO 18134-2.
10.5 Tính toán cho các cơ sở khác
Đối với việc tính toán các kết quả theo các cơ sở khác tham khảo ISO 16993.
11 Đặc điểm biểu thị độ lặp lại và độ tái lập
11.1 Độ lặp lại
Kết quả của các xác định kép được thực hiện tại cùng một phòng thí nghiệm do cùng một người thao tác, trên cùng một thiết bị, thực hiện trong một khoảng thời gian ngắn trên một mẫu phân tích, không được chênh nhau quá 120 J/g đối với viên nén gỗ và mùn cưa. Đối với tất cả nhiên liệu sinh học rắn khác giới hạn độ lặp lại là 140 J/g.
11.2 Độ tái lập
Kết quả trung bình của các kết quả của các phép xác định kép được thực hiện ở một trong hai phòng thử nghiệm khác nhau, trên các phần mẫu đại diện được lấy từ cùng một mẫu ở chu kỳ cuối của quá trình chuẩn bị mẫu, không được chênh nhau quá 300 J/g đối với viên nén gỗ và mùn cưa. Đối với tất cả nhiên liệu sinh học rắn khác giới hạn độ tái lặp là 400 J/g.
12 Tính giá trị nhiệt lượng thực ở áp suất không đổi
12.1 Quy định chung
Sự khác biệt chính giữa giá trị nhiệt lượng toàn phần và giá trị nhiệt lượng thực có liên quan đến trạng thái vật lý của nước trong các sản phẩm của phản ứng (so sánh các định nghĩa 3.1 đến 3.3). Giá trị nhiệt lượng của nhiên liệu thường được sử dụng nhiều nhất cho mục đích thực tế là giá trị nhiệt lượng thực ở áp suất không đổi đối với nhiên liệu có hàm lượng ẩm xác định. Giá trị này có thể sinh ra từ giá trị nhiệt lượng toàn phần ở thể tích không đổi đối với mẫu khô, với điều kiện là tổng hàm lượng hydro của mẫu ẩm tự nhiên có thể được xác định bằng thử nghiệm hoặc, đối với từng loại nhiên liệu riêng, có sự đánh giá chắc chắn. Ngoài ra, hàm lượng oxy và nitơ của mẫu khô tuyệt đối “thêm” vào pha khí của hệ thống sản phẩm theo nguyên tắc phải được tính đến. Đối với mục đích này nitơ có thể bao gồm oxy.
CHÚ THÍCH: Giá trị nhiệt lượng thực ở thể tích không đổi (xem 3.2) đối với nhiên liệu sinh học có hàm lượng ẩm quy định dễ dàng tính được, ngay khi có số đo của hàm lượng hydro. Trong trường hợp này hàm lượng oxy và nitơ là không quan trọng.
12.2 Các phép tính
Giá trị nhiệt lượng thực ở áp suất không đổi ở các mức độ yêu cầu có thể được tính theo công thức. Để tính toán các cơ sở khác, xem ISO 16993.
Giá trị nhiệt lượng thực ở áp suất không đổi đối với một mẫu khô được tính theo công thức (25).
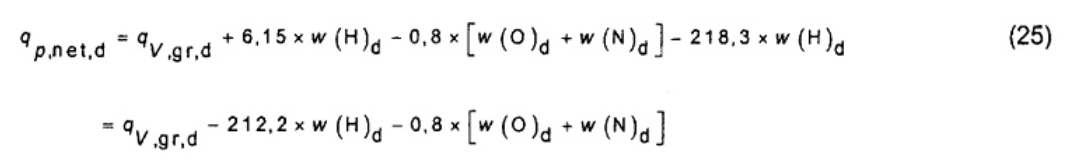
Giá trị nhiệt lượng thực ở áp suất không đổi ở độ ẩm xác định M (ví dụ như đã nhận Mar, sau đó kí hiệu của giá trị nhiệt lượng là qp,net,ar) được tính theo công thức (26)
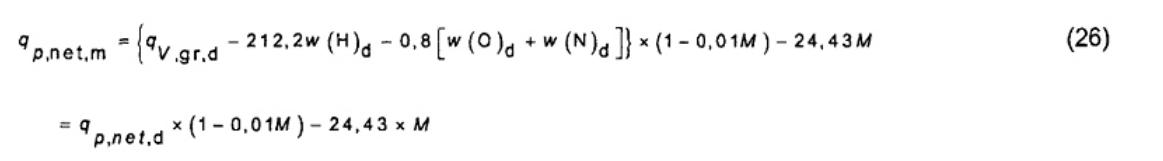
Trong đó
Qp,net,m là giá trị nhiệt lượng thực ở áp suất không đổi, tính bằng J/g của nhiên liệu sinh học với độ ẩm M (thông thường như đã nhận Mar);
qv,gr,d là tổng nhiệt lượng ở thể tích không đổi của nhiên liệu khô (xem 10.4);
w(H)d Hàm lượng hydro, tính bằng phần trăm khối lượng của nhiên liệu sinh học khô (bao gồm hydro từ nước của hydrat hóa cũng như hydro trong nhiên liệu sinh học);
w(O)d Hàm lượng oxy, tính bằng phần trăm khối lượng của nhiên liệu sinh học khô;
w(N)d Hàm lượng nitơ, tính bằng phần trăm khối lượng của nhiên liệu sinh học khô;
M Độ ẩm tính bằng phần trăm khối lượng, được yêu cầu tính toán trên cơ sở khô, M = 0 đối với không khí khô, M = Mad (xem 10.4) trên mẫu được lấy hoặc đã cháy (như đã nhận, ar) cơ sở, M = Mar (tổng hàm lượng ẩm đã nhận).
Lượng nhiệt bay hơi (áp suất không đổi) đối với nước ở 25 °C là 44,01 KJ/mol. Điều này tương đương với 218 J/g cho một phần khối lượng của 1 % hydro trong mẫu nhiên liệu sinh học hoặc 24,43 J/g cho một phần khối lượng của 1 % độ ẩm.
[w(O)d + w(N)d ] có thể được lấy bằng cách trừ đi từ 100 phần trăm của tro, cacbon, hydro và lưu huỳnh.
CHÚ THÍCH: Giá trị nhiệt lượng thực ở thể tích không đổi có thể được tính theo công thức sau.
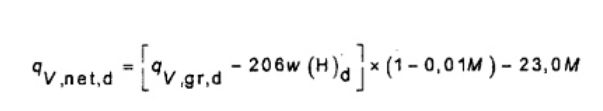
Trong đó qv,net,m giá trị nhiệt lượng thực ở thể tích không đổi, tính bằng J/g của nhiên liệu với độ ẩm M. Các kí hiệu khác như đã được xác định bên trên.
13 Báo cáo thử nghiệm
Báo cáo thử nghiệm phải bao gồm ít nhất các thông tin sau:
a) Nhận biết phòng thí nghiệm thực hiện thử nghiệm và ngày thử nghiệm;
b) Nhận biết của nhiên liệu sinh học và mẫu được thử nghiệm;
c) Viện dẫn tiêu chuẩn này;
d) Kết quả tham chiếu đến trạng thái có hiệu lực đối với giá trị nhiệt lượng, ví dụ với các kí hiệu liên quan:
1) Giá trị nhiệt lượng toàn phần (ở thể tích không đổi) của nhiên liệu sinh học khô (qv,gr,d);
2) Giá trị nhiệt lượng thực (ở áp suất không đổi) của nhiên liệu sinh học khô (qp,net,d);
3) Giá trị nhiệt lượng thực của nhiên liệu sinh học ẩm (như mẫu được lấy hoặc như mẫu nhận được, ar) (qp,net,ar);
e) Giá trị hydro, oxy, nitơ, lưu huỳnh được sử dụng để tính toán giá trị tỏa nhiệt toàn phần và giá trị tỏa nhiệt thực;
f) Nếu giá trị điển hình hoặc mặc định đối với hydro, oxy, nitơ, lưu huỳnh được sử dụng trong tính toán, điều này phải được chỉ ra rõ ràng;
g) Bất kỳ đặc điểm bất thường nào trong quá trình thử nghiệm đều được ghi nhận.
Phụ lục A
(quy định)
Bom nhiệt lượng kế đoạn nhiệt
A.1 Nguyên tắc
Trong thực tế nhiệt lượng kế đoạn nhiệt thực không có sự trao đổi nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt xung quanh (túi nước). Sự trao đổi nhiệt diễn ra ở ranh giới chung, động lực là sự chênh lệch thực về nhiệt độ. Do đó, lý tưởng nhất là toàn bộ bề mặt bên ngoài của nhiệt lượng kế, bao gồm cả nắp phải có nhiệt độ đồng nhất, trong suốt thời gian tiến hành thí nghiệm, nhiệt độ này phải phù hợp với nhiệt độ bên trong của bộ ổn nhiệt và nắp tiếp xúc với nhiệt lượng kế. Không được có bất kỳ sự khác nhau nào về nhiệt độ, tức là không truyền nhiệt, không có dòng nhiệt thực giữa nhiệt lượng kế và bộ ổn nhiệt. Tuy nhiên, vẫn sẽ có sự tăng chậm nhiệt độ của nhiệt lượng kế chủ yếu do công suất bộ khuấy gây ra, với sự tham gia dương hoặc âm do đầu dò nhiệt kế tự nóng lên và sự dẫn nhiệt dọc theo cánh khuấy, dây chì đốt, nhiệt kế.v.v...Để thuận tiện, các nhiệt lượng kế “đoạn nhiệt” thường hoạt động bằng lượng nhiệt nhỏ để cân bằng, ví dụ bù lại, sự thay đổi nhiệt độ tăng lên.
A.2 Nguồn sai số của nhiệt lượng kế thực tế
Trong thực tế khó đạt được các điều kiện đoạn nhiệt thực, đặc biệt là trong thời gian nhiệt độ nhiệt lượng kế tăng nhanh khi đốt cháy mẫu. Thiết kế của bộ ổn nhiệt và phương pháp tiến hành xác định mức độ hiệu quả của nó đối với sự thay đổi nhiệt độ của nhiệt lượng kế và từ đó mở rộng phạm vi trao đổi nhiệt không kiểm soát được.
Khi nhiệt lượng kế không có nắp, những đặc tính trao đổi nhiệt phía trên, phần lớn được xác định bởi bề mặt của nước trong nhiệt lượng kế cùng với bề mặt của phần bom nằm ở trên nước, ví dụ, các bộ phận của bình áp kế nằm trên mặt nước. Với một nhiệt lượng kế “mở” như vậy, luôn có sự bay hơi không kiểm soát của nước nhiệt lượng kế trong chu kỳ chính, gây ra bởi một “tổn thất nhiệt” tương ứng. Mức độ của sai lệch chủ yếu là một hàm của sự trễ nhiệt độ của bộ ổn nhiệt trong chu kỳ chính.
Nếu không có các chú ý đặc biệt trong thiết kế và lắp đặt, thì nắp của nhiệt lượng kế luôn tiếp xúc nhiệt kém với bản thân nhiệt lượng kế đó. Do đó, có thể có sự trễ về nhiệt độ và có thể gây ra rò rỉ nhiệt không kiểm soát được từ bộ ổn nhiệt. Điều này cũng có thể kéo dài thời gian cần thiết để nhiệt lượng kế đạt trạng thái cân bằng nhiệt hoặc trạng thái ổn định. Mặt khác, nắp cũng ngăn chặn sự thất thoát nhiệt thực do bay hơi nước của nhiệt lượng kế vì hơi nước này sẽ ngưng tụ ở bên trong nắp, lưu được năng lượng bay hơi cho nhiệt lượng kế. Trên thực tế, nước ngưng tụ giúp cân bằng nhiệt của nắp với phần còn lại của nhiệt lượng kế.
Để giảm thiểu sự trao đổi nhiệt do chênh lệch nhiệt độ tạm thời mà không thể ngăn ngừa được hoàn toàn, điều quan trọng là phải giữ cho bề mặt bên ngoài của nhiệt lượng kế và “bên trong” bộ ổn nhiệt sạch (đánh bóng) và khô. Nhìn chung, các sai sót và thiếu sót khác nhau hoặc chênh lệch giữa các phép thử hiệu chuẩn và nhiên liệu là nguyên nhân cuối cùng ảnh hưởng đến độ chính xác của kết quả cuối.
A.3 Các điều kiện đoạn nhiệt
A.3.1 Bộ ổn nhiệt
Khi bộ ổn nhiệt được làm nóng bằng cách cho dòng điện trực tiếp qua nước của bộ ổn nhiệt, phải chú ý giữ nồng độ muối (thường là Na2CO3) ở mức quy định để duy trì năng lượng đốt đồng đều trong tất cả các phép thử. Sự giảm nồng độ muối có thể gây cản trở đáng kể tốc độ gia nhiệt, thậm chí cuối cùng dẫn đến khó đạt được điều kiện đoạn nhiệt trong quá trình đốt cháy mẫu.
Kiểm soát đoạn nhiệt không tốt trong nửa đầu của chu kỳ chính rất dễ bị bỏ qua. Không kể đến kiểu gia nhiệt của bộ ổn nhiệt, thì phải kiểm tra định kỳ (hàng tuần) để xác định, ví dụ, thời gian để bộ ổn nhiệt bắt kịp với sự tăng nhanh nhiệt độ của nhiệt lượng kế trong thời gian đốt không bị tăng lên từ từ.
A.3.2 Kiểm soát đoạn nhiệt
Các điều khiển để đạt được các điều kiện đoạn nhiệt phải được điều chỉnh theo quy định trong hướng dẫn sử dụng thiết bị. Đặc biệt, chọn cài đặt mạch liên kết dẫn đến độ lệch nhiệt độ của nhiệt lượng kế bằng không hoặc nhỏ nhất ở nhiệt độ cuối cùng của các phép thử (xem A.5).
CHÚ THÍCH: Cảm biến phi tuyến tính thường được sử dụng trong mạch điều khiển nhiệt độ. Trừ khi hai cảm biến được kết hợp hoàn hảo, không thể có được sự chênh lệch nhiệt độ bằng không trên toàn bộ phạm vi làm việc đã chọn. Sau đó cũng không thể đạt được đầu nhiệt bằng không trên toàn bộ phạm vi với một thiết lập cầu nối. Các cảm biến được kết hợp không hoàn hảo cũng đặt ra những hạn chế đối với sự thay đổi có thể chấp nhận được trong nhiệt độ cuối cùng của các phép thử.
Một nhiệt lượng kế hoạt động tốt, các cài đặt điều khiển đoạn nhiệt thường cần ít hoặc không cần điều chỉnh tạm thời nào. Tuy nhiên, điều này phải được xác minh bằng cách thường xuyên kiểm tra tốc độ thay đổi ở nhiệt độ cuối cùng, ví dụ, bằng cách theo dõi nhiệt độ trong khoảng thời gian từ 5 min đến 10 min vượt quá thời gian bình thường của phép thử. Tốc độ thay đổi từ 0,001 K/min trở lên ở nhiệt độ cuối cùng phải được loại bỏ bằng cách điều chỉnh các cài đặt điều khiển hoặc hiệu chỉnh (xem 6.2.4 và Điều A.5).
A.4 Trạng thái ổn định ban đầu và độ dài của chu kỳ chính
Chu kỳ cân bằng giúp cho các thành phần khác nhau của nhiệt lượng kế đã lắp đạt được nhiệt độ đồng đều. Đồng thời, việc kiểm soát đoạn nhiệt hoạt động để đưa bộ ổn nhiệt về nhiệt độ làm việc , sát với nhiệt độ của nhiệt lượng kế. Đợi một vài phút sau khi kiểm tra hiển thị nhiệt độ của bộ ổn nhiệt và của nhiệt lượng kế là gần bằng nhau trước khi đọc nhiệt độ nhiệt lượng kế tại các khoảng thời gian cách nhau 1 min.
Khi ba lần đọc liên tiếp mang lại cùng một giá trị, trong khoảng 0,001 K hoặc cao hơn, hoặc khi có thay đổi với một lượng (giới hạn) như nhau (tỷ lệ thay đổi không đổi), thì có thể cho mẫu cháy.
CHÚ THÍCH: Khoảng thời gian dự kiến của chu kỳ cân bằng và chu kỳ trước cho phần lớn các hệ thống đoạn nhiệt theo thứ tự từ 8 min đến 10 min. Tuy nhiên, để bất kỳ bộ phận nào của nhiệt lượng kế bị chênh lệch nhiệt độ giữa các phép thử có thể kéo dài thời gian cân bằng nhiệt của nhiệt lượng kế.
Tùy thuộc vào loại mẫu, quá trình đốt cháy trong bom diễn ra trong khoảng từ 10 s đến 25 s. Thời gian cần thiết để tổng lượng nhiệt tỏa ra phân bố đồng đều, tức là để tất cả các bộ phận của nhiệt lượng kế đạt được nhiệt độ đồng đều, chủ yếu là hàm số của cánh khuấy và công suất của bộ khuấy. Chu kỳ chính sẽ bao gồm thời gian cân bằng nhiệt độ nhưng không lâu hơn nhiệt độ cần thiết.
Thời gian của chu kỳ chính được xác định trong một loạt các phép thử hiệu chuẩn trong đó các số đọc nhiệt độ được thực hiện trong khoảng thời gian 1 min kể từ đốt mẫu trong mỗi thí nghiệm. Từ những quan sát này, ghi lại thời gian, tính bằng phút, từ khi đốt cho đến khi đạt được số đọc thứ hai trong ba số đọc liên tiếp không chênh lệch nhau quá 0,001 K. Thời gian xác định lớn nhất của 5 phép thử hiệu chuẩn sẽ xác định độ dài chu kỳ chính. Thời gian này không quá 10 min, các khoảng thời gian được đánh giá từ các phép thử riêng lẻ không được chênh lệch quá 2 min.
Khi thao tác thường có sự thay đổi nhỏ về nhiệt độ cuối của thí nghiệm, yêu cầu về “nhiệt độ không đổi” sẽ thay đổi đến một tốc độ không đổi trong khoảng 0,001 K/min đối với ba khoảng thời gian 1 min liên tiếp.
A.5 Hiệu chỉnh sự thay đổi tại nhiệt độ cuối
Khi bộ điều khiển đoạn nhiệt được đặt về zero tại nhiệt độ cuối cùng, thì sự tăng nhiệt độ hiệu chỉnh sẽ là θ = tf – ti (xem 8.6.3) trong đó ti là nhiệt độ của nhiệt lượng kế tại thời điểm đốt điện tích và tf là nhiệt độ cuối của chu kỳ chính.
Sự thay đổi có giới hạn về nhiệt độ trước khi đốt cháy mẫu không cần tính đến trong các tính toán. Tuy nhiên, sự chênh lệch đáng kể vào cuối và chu kỳ chính phải được tính đến. Nó có thể được coi là một đóng góp không đổi trong hầu hết thời gian chính. Một cách tiếp cận hợp lý là thực hiện hiệu chỉnh bắt đầu 1 min sau khi đốt cháy mẫu. về nguyên tắc, độ lệch phải được xác định cho từng lần chạy. Nhưng trong điều kiện độ lệch cuối cùng đã được thiết lập là không đổi trong khoảng thời gian kéo dài đối với một phạm vi nhiệt độ cuối cùng xác định, thì việc hiệu chỉnh có thể dựa trên tốc độ cố định đó.
CHÚ THÍCH 1: Tốc độ thay đổi nhiệt độ 0,001 K/min không tính đến, với chu kỳ chính khoảng 10 min, sẽ dẫn đến sai số θ trong khoảng 0,01 K. Đối với giá trị ε khoảng 10 kJ/(K, sai số dẫn đến giá trị nhiệt lượng của nhiên liệu sẽ là 100 J/g. Nếu chính xác cùng một sai số từ cùng một nguồn được thực hiện trong các lần hiệu chuẩn và trong tất cả các phép thử nhiên liệu, thì tất nhiên nó sẽ không có ảnh hưởng gì đối với kết quả cuối cùng, ít nhất khi sự sai lệch θ nằm trong khoảng ± 30 %.
Tốc độ thay đổi nhiệt độ cuối cùng gf, tính bằng K/min phải được xác định trong một khoảng thời gian ít nhất bằng một nửa mức hiệu chỉnh được giả định để thực hiện. Đối với một chu kỳ chính là 9 min, điều này đưa ra chu kỳ đánh giá là 4 min.
CHÚ THÍCH 2: Khi tổng thay đổi nhiệt độ của nhiệt lượng kế được biểu thị bằng các đơn vị khác với nhiệt độ (xem 9.6.1), gf là giá trị trên phút tương ứng của đơn vị đó.
Sự tăng nhiệt độ tăng hiệu chỉnh θ, được hiệu chỉnh đối với thay đổi ở nhiệt độ cuối cùng, được tính theo công thức (A.1)
![]()
Trong đó
![]() là khoảng thời gian của chu kỳ chính, tính bằng min;
là khoảng thời gian của chu kỳ chính, tính bằng min;
gf được tính theo công thức (A.2):
![]()
Trong đó tf+a là nhiệt độ a phút sau khi kết thúc chu kỳ chính
Một cách khác để đánh giá gf là độ dốc của đường hồi quy tuyến tính thích hợp của các số đọc nhiệt độ theo thời gian tại các khoảng thời gian 1 min kể từ cuối chu kỳ chính trở đi.
A.6 Cách kiểm tra độ lệch
Đối với nhiệt lượng kế đốt đoạn nhiệt, nguyên nhân chính gây ra sai số hệ thống trong phép đo liên quan đến những khó khăn trong việc duy trì điều kiện đoạn nhiệt trong thời gian thay đổi các bộ phận của nhiệt lượng kế. Nó được biểu thị theo sự tăng giá trị nhiệt dung hữu hiệu với sự tăng của khối lượng mẫu. Các mẫu cháy nhanh, chẳng hạn như dầu parafin, thông thường các lỗi về trọng lượng và dạng mất nhiệt có thể không hủy được giữa hiệu chuẩn và những phép thử nhiên liệu.
Trong hầu hết các nhiệt lượng kế, kiểm tra độ trễ nhiệt độ trong bộ ổn nhiệt như một hàm số của khối lượng và loại mẫu luôn phải thực hiện. Sự thay đổi nhiệt độ của bộ ổn nhiệt khi đốt cháy mẫu được đo trong khoảng 3 min và được thể hiện bằng hàm số của thời gian cùng với các giá trị nhiệt độ thời gian của nhiệt lượng kế. Đối với nhiệt lượng kế đoạn nhiệt, trên thực tế, không cần đọc nhiệt độ của nhiệt lượng kế trong phần đầu tiên chu kỳ chính ngoài mục đích chẩn đoán. Đối với phép kiểm tra sự trễ của bộ ổn nhiệt, cần thực hiện ở các tần suất đủ để biểu diễn đường cong nhiệt độ thời gian.
Không yêu cầu hiệu chuẩn riêng nhiệt kế bộ ổn nhiệt, nhưng phải có thời gian phản tương thích với thời gian của bộ ổn nhiệt của nhiệt lượng kế. Trên biểu đồ, hai “thang đo” nhiệt độ chỉ đơn giản là trùng với thời điểm bắt cháy mẫu. Hai nhiệt độ cần phải sát giới hạn trên, khi hệ thống đang tiến tới trạng thái cân bằng nhiệt. Diện tích giữa hai đường cong là thước đo độ rò rỉ nhiệt tiềm ẩn và sự gia tăng đáng kể của diện tích này là hàm của khối lượng mẫu, tức là của θ, hoặc loại mẫu để so sánh giá trị θ, hiển thị sự rủi ro của lỗi hệ thống trong việc xác định giá trị nhiệt lượng. Khi đó, cẩn thận để hạn chế sự thay đổi nhiệt khi tiến hành phép thử trong phạm vi và mức an toàn.
Phụ lục B
(quy định)
Bom nhiệt lượng kế đẳng nhiệt và vỏ bọc tĩnh nhiệt
B.1 Nguyên tắc
Tính chất đặc trưng của nhiệt lượng kế đẳng nhiệt là lớp vỏ đẳng nhiệt. Nhiệt độ xung quanh bộ ổn nhiệt được giữ không đổi trong suốt quá trình thử nghiệm bằng cách kiểm soát tích cực. Bộ ổn nhiệt của nhiệt lượng vỏ bọc tĩnh có nhiệt dung sao cho ngay cả khi không kiểm soát tích cực, nhiệt độ của nó vẫn gần như không đổi trong các phép đo. Trong cả hai trường hợp, có luồng nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt. Nhiệt lượng kế được bao bọc bằng vật liệu cách nhiệt hoạt động phần lớn như nhiệt lượng kế vỏ tĩnh.
Sự trao đổi nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt diễn ra thông qua các ranh giới chung, động lực là phần đầu nhiệt. Lý tưởng nhất là toàn bộ bề mặt bên ngoài của nhiệt lượng kế, bao gồm cả nắp, phải có nhiệt độ đồng nhất bằng nhiệt độ được đo bằng cảm biến nhiệt độ trong nhiệt lượng kế. Nhiệt độ của thành trong của bộ ổn nhiệt và nắp đối diện với nhiệt lượng kế phải không đổi và đồng nhất trong suốt quá trình phép thử.
Để có thể đánh giá và điều chỉnh sự trao đổi nhiệt thực tế, nhiệt lượng kế được làm mát theo định luật Newton, tức là dòng nhiệt giữa nhiệt lượng kế và bộ ổn nhiệt phải tỷ lệ thuận với chênh lệch nhiệt độ thực tế đối với phạm vi đủ lớn của đầu nhiệt. Đối với máy đo nhiệt lượng, giá trị này được biểu thị là:
![]()
Trong đó
![]() Dòng nhiệt trong nhiệt lượng kế;
Dòng nhiệt trong nhiệt lượng kế;
t Nhiệt độ của vỏ (áo);
(tj-t) Đầu nhiệt;
K Hằng số làm nguội theo định luật Newton.
Trong công thức (B.1) dq (sự thay đổi nhiệt) có thể được thay thế bởi cp dt (nhiệt dung nhân với chênh lệch nhiệt độ). Vì nhiệt dung của nhiệt lượng kế ε có thể được xem như không đổi trên khoảng nhiệt độ của phép thử, công thức trở thành công thức (B.2)
![]()
Trong đó
![]() là tốc độ thay đổi nhiệt độ trong nhiệt lượng kế do dòng nhiệt gây ra;
là tốc độ thay đổi nhiệt độ trong nhiệt lượng kế do dòng nhiệt gây ra;
G là hằng số thường được gọi là hằng số tốc độ riêng;
Pst Cường độ khuấy.
Yêu cầu về tốc độ khuấy nên không đổi trong quá trình thử nghiệm(xem 8.1) để cho ![]() có thể tính theo công thức (B.3):
có thể tính theo công thức (B.3):
![]()
Trong đó
![]() Nhiệt độ mà nhiệt lượng kế cuối cùng sẽ đạt được nếu để chạy trong một khoảng thời gian dài;
Nhiệt độ mà nhiệt lượng kế cuối cùng sẽ đạt được nếu để chạy trong một khoảng thời gian dài;
G và ![]() được đánh giá từ các phép đo thời gian nhiệt độ của các khoảng thời gian đánh giá, chu kỳ trước và sau, tương ứng (xem Hình 2 trong 8.1).
được đánh giá từ các phép đo thời gian nhiệt độ của các khoảng thời gian đánh giá, chu kỳ trước và sau, tương ứng (xem Hình 2 trong 8.1).
Sự đóng góp của trao đổi nhiệt đến toàn bộ sự tăng nhiệt độ quan sát được trong thời kỳ chính thu được bằng tích phân xem công thức (B.4)]:
![]()
Sử dụng số đọc nhiệt độ - thời gian (t, ![]() ) của chu kỳ chính
) của chu kỳ chính
B.2 Nguyên nhân sai số của nhiệt lượng kế thực
Việc chế tạo vỏ đẳng nhiệt của nhiệt lượng kế đẳng nhiệt theo yêu cầu về hằng số và sự đồng đều nhiệt độ là không khó khăn, miễn là chất lỏng trong bộ ổn nhiệt được lưu thông qua nắp bộ ổn nhiệt với tốc độ hợp lý.
Trong nhiệt lượng kế vỏ bọc tĩnh, nhiệt độ bộ ổn nhiệt sẽ ít thay đổi trong quá trình thí nghiệm, với một vài sự khác biệt khi tăng nhiệt độ của nhiệt lượng kế do quá trình đốt mẫu. Công suất nhiệt của bộ ổn nhiệt phải sao cho tốc độ (làm mát) không đổi G là 0,002 0 min-1, sự gia tăng nhiệt độ áo nước nhỏ hơn 0,16 K kể từ thời điểm đốt mẫu đến khi kết thúc chu kỳ sau; đối với hằng số riêng bằng 0,003 0 min-1, sẽ nhỏ hơn 0,11 K. Sự thay đổi nhiệt độ của bộ ổn nhiệt tỷ lệ thuận với đầu đo nhiệt.
Nắp nhiệt lượng kế tiếp xúc nhiệt kém với bộ phận chính của nhiệt lượng kế sẽ bị trễ khi nhiệt độ thay đổi nhanh chu kỳ chính và có thể làm phát sinh sự trao đổi nhiệt không thể đoán trước với bộ ổn nhiệt. Nó cũng có thể kéo dài thời gian cần thiết để nhiệt lượng kế đạt trạng thái cân bằng nhiệt hoặc trạng thái ổn định. Mặt khác, nắp đậy ngăn chặn sự thất thoát nhiệt thực do bay hơi nước của nhiệt lượng kế hơi nước này sẽ ngưng tụ ở bên trong nắp, khôi phục năng lượng bay hơi cho nhiệt lượng kế. Trong thực tế, nước ngưng tụ giúp cân bằng nhiệt của nắp với phần còn lại của nhiệt lượng kế. Việc lựa chọn nhiệt độ của bộ điều chỉnh nhiệt ảnh hưởng đến tổn thất do bay hơi khi nhiệt lượng kế không có nắp.
Các thay đổi về đặc tính trao đổi nhiệt được giảm thiểu bằng cách giữ cho bề mặt bên ngoài của nhiệt lượng kế và “bên trong" của bộ ổn nhiệt sạch (đánh bóng) và khô. Khi đó, hằng số tốc độ riêng G không được thay đổi quá ± 3 % giữa các lần thí nghiệm. Ví dụ, sai lệch lớn hơn có thể là dấu hiệu của sự cố máy khuấy, cần nhấn mạnh rằng các sai số thực sự ảnh hưởng đến độ chính xác của kết quả cuối cùng là các sai số khác nhau hoặc khác nhau giữa các phép thử hiệu chuẩn và nhiên liệu.
B.3 Lựa chọn nhiệt độ vỏ bọc
Thực hiện phép đo nhiệt lượng để chạy bộ ổn nhiệt của nhiệt lượng kế đẳng nhiệt ở nhiệt độ từ 0,2 K đến 0,4 K cao hơn nhiệt độ cuối của nhiệt lượng kế. Bằng cách này, nhiệt lượng kế sẽ là phần lạnh hơn trong suốt quá trình thí nghiệm, do đó giảm thiểu thất thoát do bay hơi. Điều này đặc biệt quan trọng khi nhiệt lượng kế không có nắp.
Cùng nguyên tắc trên áp dụng tương tự với nhiệt lượng kế vỏ bọc tĩnh.
B.4 Chu kỳ đánh giá
B.4.1 Trạng thái ổn định ban đầu và chu kỳ trước
Các bộ phận của nhiệt lượng kế cần ít phút để đạt được nhiệt độ đồng nhất sau khi vận hành bộ khuấy, trước khi thực hiện các phép đọc nhiệt độ cách nhau 1 min. Về nguyên tắc, giai đoạn bắt đầu đánh giá, chu kỳ trước, bắt đầu ngay sau khi nhiệt lượng kế đạt đến trạng thái ổn định về tốc độ thay đổi nhiệt độ. Trong các khoảng thời gian 1 min liên tiếp, tăng nhiệt độ từ từ đến khi chênh lệch không lớn hơn 0,002 K/min hoặc chênh lệch trung bình không được vượt quá 0,001 K/min. Chu kỳ trước bằng 5 min (đọc sáu lần; tăng năm lần) cần phải đủ để thiết lập giá trị bằng ![]() , tốc độ thay đổi nhiệt ban đầu. Để gia tăng nhiệt độ, gi có giá trị dương (> 0).
, tốc độ thay đổi nhiệt ban đầu. Để gia tăng nhiệt độ, gi có giá trị dương (> 0).
CHÚ THÍCH: Nhiệt độ của nhiệt lượng kế, như là một hàm của thời gian nối chung, là một cấp số nhân tiến tới tiệm cận đến ![]() . Tuy nhiên, chu kỳ gian đánh giá từ 10 min trở xuống, độ cong là không đáng kể ngoại trừ trường hợp đầu nhiệt lớn, vượt quá 5 K, kết hợp với giá trị lớn của hằng số tốc độ riêng, lớn hơn 0,005 min-1
. Tuy nhiên, chu kỳ gian đánh giá từ 10 min trở xuống, độ cong là không đáng kể ngoại trừ trường hợp đầu nhiệt lớn, vượt quá 5 K, kết hợp với giá trị lớn của hằng số tốc độ riêng, lớn hơn 0,005 min-1
Ngay khi cháy mồi đốt, đọc nhiệt độ cuối cùng của nhiệt độ của chu kỳ trước (xem 8.4).
B.4.2 Chu kỳ sau và độ dài của chu kỳ chính
Chu kỳ đánh giá cuối cùng (chu kỳ sau) bắt đầu khi tất cả các bộ phận của nhiệt lượng kế đã đạt được nhiệt độ đồng nhất sau khi đốt cháy mẫu, tức là khi nhiệt lượng kế đã đạt đến trạng thái ổn định mới về tốc độ thay đổi nhiệt độ. Thời gian yêu cầu đối với toàn bộ lượng nhiệt thoát ra đồng đều là cơ sở hàm số của bộ khuấy mẫu và công suất bộ khuấy. Khoảng thời gian chu kỳ chính phải được chọn sao cho đảm bảo cân bằng nhiệt độ, nhưng không làm chu kỳ chính kéo dài hơn mức cần thiết.
Chu kỳ chính bắt đầu từ lần đọc nhiệt độ cuối cùng của chu kỳ trước và kết thúc cùng với sự bắt đầu của chu kỳ sau. Chu kỳ chính được xác định trong một loạt các phép thử hiệu chuẩn và tiến hành với tần suất chu kỳ 5 min, độ lệch trung bình của các bước tăng nhiệt độ trong 1 min riêng lẻ không quá 0,001 K/min. Giá trị trung bình của khoảng thời gian chu kỳ chính được xác định từ năm phép thử hiệu chuẩn, lấy chính xác đến một phút, để xác định thời gian của chu kỳ chính. Chu kỳ này sẽ không vượt quá 10 min. Khoảng thời gian được đánh giá từ các phép thử riêng lẻ cũng không được chênh lệch quá 2 min.
Chu kỳ chính phải giống nhau trong quá trình hiệu chuẩn và trong các phép thử nhiên liệu. Khi θ thay đổi trong dải rộng thì thích hợp để xác định thời gian của chu kỳ chính ở những giá trị rộng của, của θ.
Khoảng thời gian của chu kỳ sau phải từ 5 min đến 7 min để thiết lập tốc độ thay đổi nhiệt cuối cùng gf đủ tốt cho việc tính toán hiệu chỉnh đối với trao đổi nhiệt Δtex. Nhiệt độ tăng với thời gian, gf có giá trị dương (> 0).
B.5 Tính sự tăng nhiệt độ hiệu chỉnh θ
B.5.1 Quy định chung
Sự gia tăng nhiệt độ quan sát, tf - ti, là tổng của θ, sự thay đổi nhiệt độ gây ra bởi các quá trình trong bom, và Δtex, sự đóng góp từ sụ trao đổi nhiệt với môi trường xung quanh bộ ổn nhiệt (bao gồm cả sự đóng góp của công suất khuấy). Các số đọc nhiệt độ thời gian được thực hiện trong các chu kỳ trước, chính và sau chứa thông tin cần thiết để đánh giá Δtex, và do đó θ được tính theo công thức (B.5):
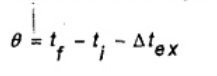 (B.5)
(B.5)
Hiệu suất của chu kỳ đánh giá, được hiển thị trong công thức (B.6) và (B.7):
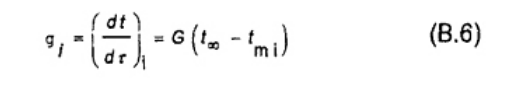
và
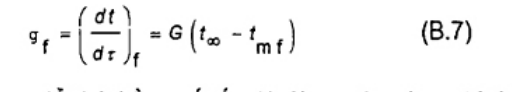
Sử dụng để tính hằng số tốc độ riêng, như được trình bày trong công thức (B.8):

trong đó
gi Tốc độ trượt ở chu kỳ trước (đánh giá ban đầu), tính bằng K/min;
gf Tốc độ trượt ở chu kỳ sau sau (đánh giá sau cùng), tính bằng K/min;
tmf Nhiệt độ trung bình của chu kỳ sau, tính bằng °C;
tmi Nhiệt độ trung bình của chu kỳ trước, tính bằng °C.
Nhiệt độ có thể được biểu thị bằng một số đơn vị khác (xem 9.6.1).
gi và gf tốt nhất là được đánh giá như là độ dốc tuyến tính của bình phương nhỏ nhất phù hợp với giá trị thời gian nhiệt độ của chu kỳ trước và sau tương ứng. Ngoài ra, chúng được coi là giá trị trung bình của mức tăng nhiệt độ trong 1 min trong các chu kỳ đánh giá.
B.5.2 Phương pháp Regnault - Pfaimdler
Việc đọc các giá trị nhiệt độ - thời gian ở chu kỳ chính nên được thực hiện ở các khoảng thời gian bằng nhau (ví dụ 1 min) Δtx nên được tính theo công thức (B.9)
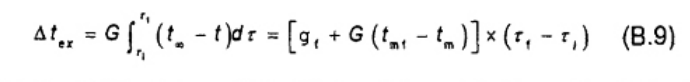
trong đó tm (nhiệt độ trung bình tích hợp) được tính theo công thức (B.10):

trong đó
t0 (= ti) Nhiệt độ ở thời điểm bắt đầu của chu kỳ chính;
t1, t2, ...., tk,…. tn là các số đọc nhiệt độ liên tiếp được thực hiện tại chu kỳ chính, t n (= t f) là giá trị đó ở thời điểm cuối;
![]() và
và ![]() là thời điểm bắt đầu và kết thúc chu kỳ chính.
là thời điểm bắt đầu và kết thúc chu kỳ chính.
B.5.3 Phương pháp ngoại suy Dickinson
Trong phương pháp ngoại suy Dickinson, mục tiêu là tìm ra thời điểm Tx sao cho Công thức (B.11) được giải:
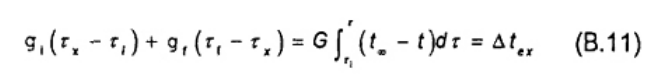
Điều này được thực hiện khi các khu vực bao quanh a và b trong Hình B.1 có kích thước bằng nhau. Nhiệt độ tăng hiệu chỉnh θ trở thành công thức (B.12)
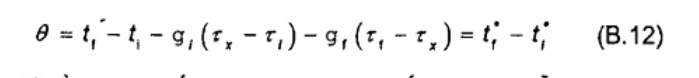
trong đó về nguyên tắc, gi và gf đại diện ctốc độ thay đổi nhiệt ở thời điểm ![]() và
và ![]()
Đối với phản ứng đốt cháy, đường cong nhiệt độ - thời gian gần với hàm số mũ có nghĩa là Tx là thời gian gắn với nhiệt độ, trong đó sự thay đổi nhiệt độ tx - ti là 0,6 lần tăng nhiệt độ tổng (quan sát được)
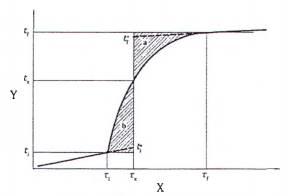
(tf- ti). Đại lượng (Tx - Ti) thay đổi theo đặc tính động học của phản ứng cháy của loại mẫu nghiên cứu.
CHÚ DẪN
X thời gian, ![]()
Y nhiệt độ, t
Hình B.1 - Phương pháp ngoại suy Dickinson
Phụ lục C
(quy định)
Bom nhiệt lượng kế tự động
C.1 Dụng cụ
Trong số các loại bom nhiệt lượng kế hoàn toàn tự động, có những thiết bị đáp ứng tất cả các yêu cầu cơ bản liên quan đến nhiệt lượng kế được xác định rõ về mặt vật lý, cũng như các thiết bị có đặc tính nhiệt phải được mô tả theo kinh nghiệm. Loại thiết bị kiểu cũ thông thường ít đòi hỏi sự tương thích, ví dụ, về lượng nhiệt tỏa ra trong các lần hiệu chuẩn và trong các phép thử nhiên liệu, để thu được những kết quả đáng tin cậy. Ngoài ra, nhiệt dung hữu hiệu ε của nhiệt lượng kế tiêu chuẩn theo một quy tắc duy trì không đổi trong thời gian dài.
Không có lý do cụ thể nào để cho rằng các thiết bị với nhiệt lượng kế tiêu chuẩn không thể đưa ra giá trị nhiệt lượng với độ chính xác yêu cầu, nhưng với điều kiện là độ lặp lại nằm trong một số giới hạn được thiết lập và người sử dụng phải biết và tuân thủ các hạn chế trong việc lựa chọn điều kiện vận hành. Thông thường, nhiệt lượng kế loại này yêu cầu hiệu chuẩn thường xuyên hơn, trong một số trường hợp là hàng ngày khi nó được sử dụng.
Nhiệt lượng kế khí áp (xem 6.1) là phù hợp đối với vận hành tự động, vì chúng không yêu cầu chia từng phần nước của nhiệt lượng kế, do đó cũng loại bỏ sai số do bay hơi. Chúng thường được vận hành như hệ thống đoạn nhiệt hoặc bán đoạn nhiệt nhưng cũng có thể thuộc loại đẳng nhiệt, về đặc điểm, chúng có nhiệt dung nhỏ dẫn đến nhiệt độ nhiệt lượng kế thay đổi lớn, do đó thuận lợi cho việc đo θ với độ phân giải tương đối cao. Ngược lại, các giá trị lớn của θ có xu hướng làm tăng nguy cơ gây ra sai số hệ thống trong các hệ thống an toàn không trở nên trầm trọng hơn do khó khăn trong việc đạt được nhiệt độ bề mặt nhiệt lượng kế đồng nhất trong quá trình đốt cháy mẫu. Biện pháp đối phó là hạn chế khối lượng mẫu, lưu ý rằng đối với các mẫu nhỏ hơn, phải đặc biệt chú ý đến tính đại diện của chúng.
Trong một số trường hợp, những hệ thống nhiệt lượng kế ổn định xác định tốt thì cho phép thao tác kiểu động lực, ví dụ ngay trong một vài phút của chu kỳ chính, có thể dự đoán kết quả cuối cùng của thử nghiệm theo θ mà không làm giảm độ chính xác của kết quả.
C.2 Hiệu chuẩn
Theo nguyên tắc, nhiệt dung hữu hiệu ε phải được xác định như quy định trong Điều 9, cụ thể là tham khảo 9.2, 9.4 và 9.5.
Nhà sản xuất thiết bị có thể quy định các điều kiện của bom (tỷ lệ giữa khối lượng mẫu với thể tích bình, nước bình ban đầu, áp suất oxy) sai lệch đáng kể so với các điều kiện được xác định trong 9.2.1. Khí các điều kiện của bom gây ra sự thay đổi năng lượng đốt cháy của chất hiệu chuẩn (axit benzoic) lớn hơn ± 5 J/g (xem 9.2.2), thì có thể điều chỉnh bất kỳ giá trị đặt trước nào cho axit benzoic, tức là nhập giá trị chính xác cho việc tính toán ε.
Các khuyến cáo để loại trừ lượng nước ban đầu trong bom cần bỏ qua. Tuy nhiên, khối lượng có thể tương đối nhỏ (hoặc thậm chí bằng không) nhưng phải giống nhau cả trong hiệu chuẩn và trong tất cả các phép thử
Nhiệt độ chuẩn của các phép thử (bằng nhiệt độ cuối cùng tf của chu kỳ chính) phải được giữ nguyên, trong khoảng ± 1 K, trong tất cả các phép thử. Nếu cần thiết, có thể được chọn tùy ý trong khoảng ± 10 K từ 25 °C mà không ảnh hưởng đáng kể đến các giá trị khi xác định giá trị nhiệt lượng (xem 3.4). Độ lệch vượt quá ± 5 K so với 25 °C phải được trích dẫn cùng với kết quả thử nghiệm.
CHÚ THÍCH: Theo nguyên tắc các số lượng phụ cho trong 9.6.1, 9.6.2, và 10.3.2 đạt được trạng thái, những phản ứng ở 25°C.
Một số thiết bị dùng để hiệu chuẩn bằng cách sử dụng các mẫu khác nhau bằng khoảng hệ số 2 theo khối lượng. Nếu áp dụng chính xác thì sẽ rất dễ dùng cho các phép đo nhiên liệu tiếp theo. Luôn luôn yêu cầu thiết lập phạm vi làm việc hợp lệ cho nhiệt dung hữu hiệu ε (xem 9.3). Khi phạm vi giới hạn khối lượng của sự mất nhiệt là nhỏ, phải đặc biệt chú ý khi thực hiện tất cả các phép thử trong các giới hạn này.
Đối với những thiết bị mà yêu cầu thường xuyên phải hiệu chuẩn, nhà sản xuất có thể cung cấp những viên axit benzoic có khối lượng thích hợp với giá trị được chỉ định cho năng lượng đốt. Theo quy định, những viên này không đủ tiêu chuẩn làm chất hiệu chuẩn (xem 5.5 và 9.2) nhưng thuận tiện cho việc sử dụng hàng ngày. Một giải pháp thay thế là kiểm tra hiệu chuẩn bằng cách thực hiện một loạt các phép đo trên một mẫu axit benzoic đã được chứng nhận ở những khoảng thời gian đều đặn và sử dụng một lô mẫu mới của nhà sản xuất. Giá trị trung bình từ loạt năm mẫu, với khối lượng mẫu gần như nhau, không được chênh lệch quá ± 50 J/g so với giá trị được chứng nhận, được tính toán lại khi thích hợp cho những điều kiện thực tế bom.
Một số thiết bị yêu cầu điều hòa trước bằng cách đốt cháy một vài mẫu trước khi thực hiện các kết quả ổn định. Hầu hết mọi axit benzoic (dạng viên) hoặc chất hỗ trợ cháy (xem 8.1) đều có thể được sử dụng cho mục đích này. Kết quả từ những lần chạy thử này nên được bỏ qua.
Đốt axit benzoic được chứng nhận là “chưa biết” thường là cách thuận tiện nhất để kiểm tra hoạt động của nhiệt lượng kế (xem 9.3).
C.3 Yêu cầu độ chụm đối với hiệu chuẩn
Các giá trị của ε cho các phép thử hiệu chuẩn riêng phải được in hoặc trình bày sao cho chúng có thể được ghi lại theo phương pháp thủ công (tính bằng J/K hoặc theo các đơn vị tùy chọn cùng với θ trong các đơn vị này). Nói chung, áp dụng các yêu cầu về độ chụm đối với ε, như nêu trong 9.7.
Một số hệ thống bù cho các thay đổi nhiệt độ đáng kể bằng cách sử dụng giá trị trung bình của giá trị trung bình trước đó và giá trị của từ phép thử hiệu chuẩn cuối cùng làm thước đo cho nhiệt dung hữu hiệu. Trong trường hợp này, các giá trị riêng của ε đối với một loạt các phép thử hiệu chuẩn không thể được sử dụng để đánh giá các đặc tính chính xác của phép đo. Thay vào đó, một loạt các phép đo riêng lẻ sử dụng axit benzoic đã được chứng nhận làm mẫu phải được thực hiện trong khoảng thời gian 1 ngày hoặc nhiều nhất là 2 ngày. Đối với năm lần đốt axit benzoic, độ lệch chuẩn không được vượt quá 0,20 %. Giá trị trung bình không được chênh lệch quá ± 50 J/g so với giá trị đã được chứng nhận (xem C.2).
C.4 Sự tương thích của các phép thử hiệu chuẩn và phép thử nhiên liệu
Áp dụng các điều kiện quy định từ 10.1 đến 10.3, cần tính đến sự đóng góp nhiệt từ sự cháy của mồi đốt và/hoặc gần các phản ứng, chẳng hạn như sự hình thành axit nitric, cần được tính đến trong các đánh giá (xem 9.6.1).
Trong các quy trình tính các thiết bị tự động, thông thường không cho phép sử dụng chén nung với khối lượng và vật liệu quá khác nhau.
Trong các hệ thống đo khí áp hoặc các hệ thống hoạt động trên cơ sở khối lượng nước không đổi, các sai lỗi do không tính đến sự chênh lệch nhiệt dung của chén nung được trình bày trong công thức (C.1)
![]()
trong đó
ΔC là sự chênh lệch nhiệt dung (mcr x cp,cr) của chén nung sử dụng trong hiệu chỉnh và sử dụng trong quá trình cháy của nhiên liệu;
m1 là khối lượng của nhiên liệu cháy;
Đối với nhiệt lượng kế làm việc trên cơ sở khối lượng tổng nhiệt lượng kế không đổi, sai số được ước tính bằng cách sử dụng công thức (C.2) (xem 9.6.2):
![]()
Đạt được sự cháy sạch là ưu tiên hàng đầu. Nên tối ưu hóa các điều kiện tổng thể để đạt được điều đó.
C.5 Tài liệu hóa và bản in
Theo nguyên tắc đánh giá, giá trị tỏa nhiệt toàn phần ở thể tích không đổi qv gr đối với mẫu phân tích được đánh giá theo 10.4. Giá trị phải được tính bằng Jun trên gam hoặc một đơn vị khác.
Các thông tin được in ra hoặc được ghi lại trên từng phép thử phải cho phép người dùng xác minh các phép tính bắt đầu từ các giá trị θ, ε, khối lượng mẫu, mồi đốt và bất kỳ chất trợ cháy nào. Các công thức được sử dụng phải được nêu trong sổ tay hoặc trong phụ lục. Các đại lượng phụ được sử dụng trong tính toán phải được nhận biết rõ ràng và có thể thực hiện các thay đổi cần thiết trong chương trình do các thay đổi trong quy trình yêu cầu, bao gồm cả sự thay đổi giá trị bằng số dụng cho năng lượng đốt cháy của các chất hiệu chuẩn trong các phép thử hiệu chuẩn. Các hiệu chỉnh áp dụng cho năng lượng bắt lửa, phản ứng phụ, v.v... phải được nêu rõ.
Nhiệt độ tham chiếu của thử nghiệm phải được xác định chính xác đến 0,2 K.
C.6 Yêu cầu về độ chụm đối với phép thử nhiên liệu
Các yêu cầu chính xác về giới hạn độ lặp lại của các kết quả phép đo kép được nêu trong Điều 11.
Phụ lục D
(tham khảo)
Danh sách kiểm tra đối với thiết kế các phép thử và quy trình đốt cháy
D.1 Quy định chung
Phụ lục này bao gồm các danh sách kiểm tra nhằm điều chỉnh và tiến hành xác định giá trị nhiệt lượng, bao gồm hiệu chuẩn các thiết bị, sử dụng loại nhiệt lượng kế quy định. Các công thức, được đưa ra ở phần nội dung chính của tiêu chuẩn, sẽ được nhắc lại cho rõ ràng.
Các điều kiện thử nghiệm chung, các điều kiện này thông thường được dùng cho tất cả các loại bom nhiệt lượng kế được quy định tại Điều D.2. Điều D.3 bao gồm các thông tin thích hợp áp dụng cho nhiệt lượng kế đoạn nhiệt, Điều D.4 áp dụng cho nhiệt lượng kế đẳng nhiệt và Điều D.5 đề cập đến hệ thống đo nhiệt lượng kế bom tự động hóa cao. Nhiệt lượng kế vỏ bọc tĩnh có thể được coi là hệ thống đẳng nhiệt.
Các số trong ngoặc đơn đề cập đến các Điều hoặc khoản được đưa ra ở phần nội dung chính của tiêu chuẩn hoặc từ Phụ lục A đến Phụ lục C. Quy trình đo nhiệt lượng cơ bản được mô tả trong Điều 8. Quy trình hiệu chuẩn được mô tả trong 9.5 và 9.6. Các quy trình thử nghiệm và tính toán cho quá trình đốt cháy nhiên liệu được quy định trong 10.2 đến 10.4. Thông tin bổ sung cần thiết cho loại nhiệt lượng kế cụ thể được đưa ra trong:
- Phụ lục A và Điều D.3 về nhiệt lượng kế đoạn nhiệt;
- Phụ lục B và Điều D.4 đối với nhiệt lượng kế đẳng nhiệt hoặc vỏ tĩnh nhiệt;
- Phụ lục C và Điều D.5 về các loại nhiệt lượng kế khác.
D.2 Lựa chọn các thông số chung
Điều kiện hiệu chuẩn, cơ sở cho các điều kiện của phép thử nhiên liệu tiếp theo (xem 9.2.2 và 9.3 đối với các yêu cầu hiệu chuẩn chung);
- Thể tích bom, Vbom, được biểu thị bằng lit;
- Khối lượng của axit benzoic mba, tính bằng gam;
- Khối lượng nước bom maq, tính bằng gam; Vaq, tính bằng millilit (ml), có thể thay thế cho maq;
- Áp suất ép ban đầu của oxy p0, tính bằng megapascals (MPa);
- Nhiệt độ tham chiếu tref, tính bằng °C.
Tính toán giá trị của axit benzoic ở điều kiện bom
Sử dụng giá trị này trong các phép tính nhiệt dung hữu hiệu của nhiệt lượng kế, ε. Tham khảo chứng chỉ cụ thể của axit benzoic; xem thêm 9.6.1 và 9.6.2.
Giá trị chứng chỉ của axit benzoic, tính bằng Jun trên gam (xem 9.2.1)
- mba / Vbom, tính bằng gam trên lít, tương đương với 3,0 g/L;
- Vaq / Vbom, tính bằng mililit trên lít, bằng 3,0 m/L;
- ρo, tính bằng megapascal, tương đương với 3,0 MPa;
- tref, tính bằng °C, tương đương với 25 °C; xem 8.7;
- Điều chỉnh đến giá trị chứng nhận, tính bằng Jun trên gram, theo công thức trong chứng chỉ.
Đường cong qv,ba, tính bằng Jun trên gam
Lượng nước của nhiệt lượng kế (xem 8.1 và 8.3; không liên quan đến hệ thống đo khí áp):
Lượng nước của nhiệt lượng kế được xác định bằng các cách sau
a) Cơ sở khối lượng nước không đổi của nhiệt lượng kế, ví dụ khối lượng của nước trong nhiệt lượng kế, tính bằng gam; xem 8.3, 9.6.1 và 10.3.2; Hay cách khác
b) Cơ sở tổng khối lượng của nhiệt lượng kế tổng không đổi, ví dụ khối lượng của (nhiệt lượng kế + nước + bom lắp ráp) tính bằng gam; xem 8.3, 9.6.2 và 10.3.3.
Các thông số bổ sung:
- Dây mồi đốt (dây chì), Iwire, tính bằng centimet, hoặc Qign không đổi, tính bằng Jun; xem 9.4 và 9.6.1
- Mồi cháy , mfuse, tính bằng gam, hoặc Qfuse không đổi, tính bằng Jun; xem 9.4 và 9.6.1.
Phải quyết định cần hoặc không cần xác định hiệu chỉnh, QN đối với axit nitric, bằng cách phân tích đối với từng phép thử riêng hoặc theo giá trị không đổi trên mỗi gam (không nhất thiết phải giống nhau đối với phép thử chất hiệu chuẩn và nhiên liệu) hay giá trị trên mỗi phép thử (xem 9.4 và 10.1).
D.3 Nhiệt lượng kế đoạn nhiệt
D.3.1 Xác định tăng nhiệt độ hiệu chỉnh θ
Thực hiện các điều chỉnh cần thiết để đạt được điều kiện đoạn nhiệt (xem A.3.1 và A.3.2).
Những ước tính nhiệt dung của hệ thống và từ việc lựa chọn khối lượng mẫu, đưa ra dự đoán về độ tăng nhiệt dự kiến Δt nhằm xác định nhiệt độ ban đầu (tref - Δt).
Xác định các điều kiện cho trạng thái ổn định ban đầu (xem A.4).
Tiến hành các phép thử để xác định thời gian của chu kỳ chính (xem A.4, 8.2 đến 8.5 và 9.5).
Từ các phép đo nhiệt độ - thời gian (Tk , tk) đối với thiết bị đốt axit benzoic, tính sự tăng nhiệt độ hiệu chỉnh θ bằng phép thử riêng theo Công thức (D.1); (xem A.5):
θ = tf - ti (D.1)
Đối với sự thay đổi đáng kể (nhưng có giới hạn) ở cuối chu kỳ chính, θ được tính theo công thức (D.2) (xem A.5):
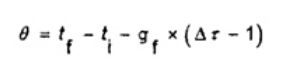 (D.2)
(D.2)
D.3.2 Đánh giá nhiệt dung hữu hiệu ε
Tính toán hiệu dung hữu hiệu ε cho các phép thử riêng.
Đối với phương án thay thế D.2 a), tính ε, trên cơ sở tổng khối lượng nước nhiệt lượng kế không đổi theo công thức (D.3) xem 9.6.1.
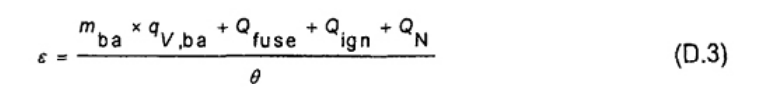
Đối với phương án thay thế D.2 b), tính ε0 , trên cơ sở tổng khối lượng nhiệt lượng kế không đổi theo công thức (D.4) xem 9.6.2.

Trong đó
ε• tương đương với ε xác định ở trên;
mcr là khối lượng của chén nung sử dụng trong phép thử hiệu chuẩn cụ thể; xem chú thích tại 9.6.2.
Tính giá trị trung bình ε(n) hoặc ε0(n), theo thứ tự, và phải đảm bảo yêu cầu về độ chụm đáp; xem 9.7.
Hiệu chuẩn hệ thống và cài đặt các thông số nhiệt lượng chính cho các phép đo đốt mẫu nhiên liệu tiếp theo.
Các đại lượng phụ trợ cần thiết dùng cho các phép tính được nêu trong 9.6.1.
D.3.3 Giá trị nhiệt lượng toàn phần ở thể tích không đổi qv,gr
Tính giá trị nhiệt lượng toàn phần ở thể tích không đổi tiến hành đốt cháy nhiên liệu theo hướng dẫn trong 10.2 và 10.3. θ được tính theo cách giống như đối với hiệu chuẩn.
Bằng cách khác D.2 a), nhiệt lượng kế được vận hành trên cơ sở khối lượng nước không đổi của nhiệt lượng kế, tính nhiệt lượng theo Công thức (D.5); (xem 10.3.2):
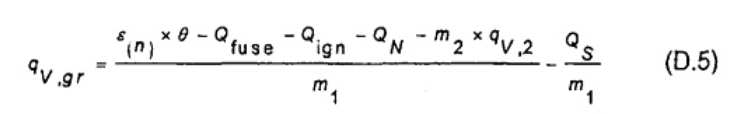
Bằng cách khác D.2 b), nhiệt lượng kế được vận hành trên cơ sở tổng khối lượng nhiệt lượng kế không đổi, tính nhiệt lượng theo Công thức (D.6); (xem 10.3.3):
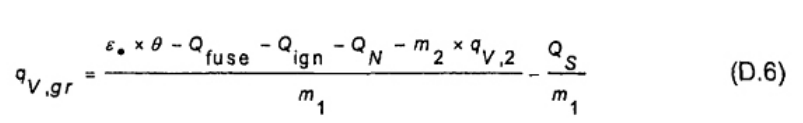
Trong đó
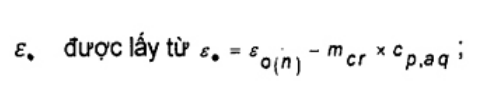
![]() là khối lượng của chén nung trong phép thử cụ thể, tính bằng gam.
là khối lượng của chén nung trong phép thử cụ thể, tính bằng gam.
Luôn luôn sử dụng chén nung phù hợp nhất với các mẫu cụ thể
Các đại lượng phụ trợ cần thiết trong tính toán được nêu trong 9.6.1 và 10.3.2.
D.4 Nhiệt lượng kế Đẳng nhiệt
D.4.1 Xác định nhiệt độ tăng hiệu chỉnh θ
Đặt nhiệt độ của vỏ bình đến giá trị được chọn cho các phép thử (xem B.3).
Ước tính nhiệt dung của hệ thống và từ việc lựa chọn khối lượng mẫu, đưa ra dự đoán về nhiệt độ tăng dự kiến Δt để xác định nhiệt độ ban đầu (tref - Δt).
Điều tra các điều kiện đối với trạng thái ổn định ban đầu và quyết định độ dài của chu kỳ đầu hoặc chu kỳ đánh giá ban đầu (B.4.1).
Thực hiện một loạt phép thử để xác định độ dài của chu kỳ chính (xem B.4.2, 8.2 đến 8.5 và 9.5).
Từ các phép đo nhiệt độ thời gian (Tk, tK) đối với một chuỗi các chất cháy axit benzoic, tính toán mức nhiệt độ tăng hiệu chỉnh θ cho các phép thử riêng lẻ, sử dụng phương pháp Regnault- Pfaundle hoặc phương pháp Dickinson.
Phương pháp Regnault-Ptaundle (xem B.5.1 và B.5.2)
Xác định tốc độ thay đổi nhiệt gi và gf và nhiệt độ trung bình tmi và tmf của các khoảng thời gian định mức và tính hằng số tốc độ riêng G theo Công thức (D.7):
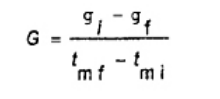 (D.7)
(D.7)
tiếp theo tính tm (giá trị nhiệt độ trung bình) và Δtex (đóng góp từ quá trình trao đổi nhiệt) theo công thức (D.8) và (D.9):

và
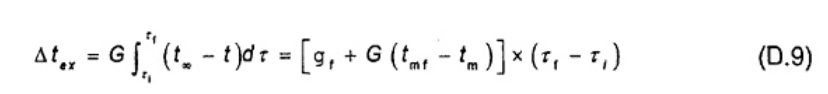
Cuối cùng, tính toán θ sử dụng công thức (D.10)

Phương pháp ngoại suy Dickinson (xem B.5.1 và B.5.3).
Lập đồ thị của các giá trị nhiệt độ - thời gian (Tk, tk) của chu kỳ chính và xác định thời gian cho ti + 0,6 x (tf -ti). Thời gian này được coi là Tx. Xác định tốc độ thay đổi nhiệt, tức là độ dốc của các khoảng thời gian đánh giá, sử dụng công thức (D.11) và (D.12):

tiếp theo tính giá trị θ sử dụng công thức (D.13):
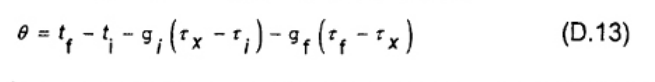
CHÚ THÍCH Thời gian ngoại suy ![]() đối với các phép thử nhiên liệu có khả năng khác với các giá trị hiệu chỉnh
đối với các phép thử nhiên liệu có khả năng khác với các giá trị hiệu chỉnh
D.4.2 Đánh giá nhiệt dung hữu hiệu ε
Tính toán giá trị nhiệt dung hữu hiệu cho các phép thử riêng lẻ sử dụng công thức phù hợp [thay thế D.2 a) hoặc D.2 b)] như đã cho trong D.3.2.
Tính giá trị trung bình ε(n) hoặc ε0(n) tương ứng và đảm bảo rằng các yêu cầu về độ chụm được đáp ứng (xem 9.7).
Hệ thống hiện đã được hiệu chỉnh và các thông số nhiệt lượng chính được thiết lập cho phép đo quá trình đốt cháy tiếp theo trên mẫu nhiên liệu.
D.4.3 Giá trị tỏa nhiệt toàn phần ở thể tích không đổi qv,gr
Thực hiện đốt cháy nhiên liệu theo hướng dẫn trong 10.2 và 10.3. θ được tính giống như cách tính hiệu chuẩn.
Tính nhiệt lượng theo công thức thích hợp [thay thế D.2 a) hoặc D.2 b)] như đã cho trong D.3.3.
D.5 Bom nhiệt lượng kế tự động
Vận hành nhiệt lượng kế theo hướng dẫn tăng nhiệt độ hiệu chỉnh θ mà thông thường được lấy ra tự động từ hệ thống.
Phải đảm bảo sử dụng đúng giá trị năng lượng đốt của chất hiệu chuẩn dưới các điều kiện của bom đã sử dụng (xem D.2) trong việc đánh giá hằng số hiệu chuẩn.
Phải đảm bảo phù hợp với các yêu cầu về độ chụm. Nếu cần, kiểm tra hệ thống bằng cách đốt cháy axit benzoic khi chưa biết. Phải tuân thủ bất kỳ hạn chế nào do nhà sản xuất đặt ra, về lượng mẫu được đốt cháy.
Xác định phạm vi làm việc hợp lệ cho các phép đo tiếp theo.
Kiểm tra các phép tính liên quan đến hiệu chỉnh dây đốt và axit nitric. Trừ khi việc hiệu chỉnh axit sulfuric thành sulfur dioxide đã được hệ thống xử lý, sử dụng giá trị cho trong 10.3.2
Phụ lục E
(tham khảo)
Một ví dụ về các phép tính sử dụng trong tiêu chuẩn này khi dùng bom nhiệt lượng kế tự động để xác định
Ví dụ đã cho dựa trên nhiệt lượng kế đoạn nhiệt. Sự khác biệt giữa các loại nhiệt lượng kế tự động (đoạn nhiệt, đẳng nhiệt hoặc đẳng nhiệt) và các nhà sản xuất dường như đưa ra cả hai nhiệt độ tới hạn (ti và tf) hoặc chỉ tăng nhiệt độ đã hiệu chỉnh θ. Cần chú ý đến xử lý các chỉnh sửa, đặc biệt là Qfuse và Qign (có thể có sự khác biệt nhỏ giữa các nhà sản xuất).
E.1 Giá trị nhiệt lượng toàn phần ở thể tích không đổi
Số liệu hiệu chuẩn được đưa ra trong Bảng E.1.
Bảng E.1. số liệu hiệu chuẩn
| No. | mba g | ti K | tf K | θ K | Qfuse J | Qign J | NaOH ml | QN J | ε K |
| 1 | 1,028 2 | 1,059 | 4,102 | 3,043 | 0 | 21,5 | 6,5 | 39,5 | 8 962 |
| 2 | 1,052 5 | 0,454 | 3,568 | 3,114 | 0 | 21,5 | 5,9 | 35,4 | 8 963 |
| 3 | 1,001 9 | 0,892 | 3,859 | 2,967 | 0 | 21,5 | 6,4 | 38,4 | 8 957 |
| 4 | 1,022 9 | 0,942 | 3,942 | 3,028 | 0 | 21,5 | 5,7 | 34,2 | 8 959 |
| 5 | 1,014 6 | 0,373 | 3,375 | 3,002 | 0 | 21,5 | 6,4 | 38,4 | 8 964 |
Trung bình ε(n) = 8 961
qv, ba = 26 465 J/g
Iwire = 10 cm dây đốt; trong đó 8 cm là đã cháy (Qign = 2,69 J/cm)
Không dây đốt, bông, vv đã được sử dụng.
NaOH, [c = 0,1 mol /]
Tăng nhiệt độ đã hiệu chỉnh θ
Sự khác biệt của nhiệt độ ban đầu và nhiệt độ cuối cùng (ti - tf) hoặc đọc trực tiếp nhiệt độ tăng θ (xem ở trên).
Tính nhiệt dung hữu hiệu ε
Nhiệt dung hữu hiệu ε được tính từ tổng năng lượng thay đổi của quá trình bom tổng thể, ví dụ (1,028 2 x 26 465 + 21,5 + 39,0) chia cho θ (3,043), tức là ε = 8 962 J/ K.
Tính tổng nhiệt lượng qv,ba
Để đốt cháy khoảng 1 g mẫu nhiên liệu sinh học, các thông số của phép thử là
m1 = 1,1924 g Qfuse = 0
Iwire = 8 cm; Qign = 21,5 J
θ = 2,630 K QN,S = 29,4 J
Hiệu chỉnh axit nitric (và một phần hiệu chỉnh axit sunfuric) được xác định bằng cách chuẩn độ với NaOH (phương pháp c) là QN,S.
“Năng lượng cháy” từ mẫu nhiên liệu sinh học được tính từ (ε(n)x θ) trừ đi phần đóng góp từ dây đốt và sự hình thành axit nitric, tức là (21,5 + 29,4) J, chia cho khối lượng của mẫu nhiên liệu sinh học m1.
vì thế
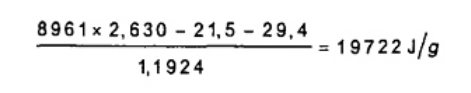
Trong đó ε được sử dụng giống với ε(n)
Hàm lượng lưu huỳnh trong mẫu phân tích nhiên liệu sinh học là 0,02 % khối lượng. Hiệu chỉnh cho phản ứng từ axit sunfuric trong nước thành khí lưu huỳnh đioxit là 0,02 x 57 = 1 J/g (Qs/ m1 = (57 z S x m1)/m1), được trừ cho 19 722 J/g, thu được 19 721 J/g là giá trị nhiệt lượng tổng ở khối lượng không đổi của mẫu phân tích qv,gr
Tổng độ ẩm nhận được (Mar) đối với nhiên liệu sinh học được đề cập là 40,0 % khối lượng; độ ẩm của mẫu phân tích (Mad) là 3,0 % khối lượng. Đối với mẫu khô (cơ bản, chất khô), tổng nhiệt lượng ở thể tích không đổi là.
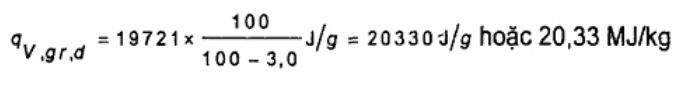
Đối với mẫu nhiên liệu sinh học ban đầu (ẩm), tổng nhiệt lượng ở thể tích không đổi là.
![]()
E.2 Giá trị nhiệt lượng toàn phần ở thể tích không đổi
Nếu nhiên liệu sinh học được đốt cháy trong oxy ở áp suất không đổi, thay vì ở thể tích không đổi trong bom, thể tích của hệ thống sẽ thay đổi. Hydro trong nhiên liệu, phản ứng với oxy ở thể khí để tạo ra nước lỏng, làm giảm thể tích của hệ thống. Khi carbon nhiên liệu sinh học phản ứng với oxy thể khí, một thể tích khí carbon dioxide tương đương được hình thành và do đó không có sự thay đổi về thể tích xảy ra trong quá trình đốt cháy carbon. Oxy và nitơ trong nhiên liệu sinh học đều làm tăng thể tích của pha khí đối với phản ứng cháy có thể được biểu thị bằng
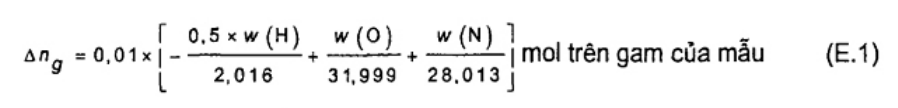
Trong đó w(H), w(O), và w (N) là tổng phần trăm tương ứng của hydrogen, oxygen, và nitrogen, trong chất nhiên liệu sinh học ở trạng thái được chỉ định để chuyển đổi từ giá trị nhiệt lượng thể tích không đổi sang giá trị áp suất không đổi.
Giá trị Δng sẽ được nhân với RT để làm sáng tỏ sự thay đổi thể tích năng lượng liên quan.Trong bối cảnh này là nhiệt độ tham chiếu cho các giá trị nhiệt lượng, tức là 298,15K (25 °C).
Để thuận tiện, các giá trị ở trạng thái khô được sử dụng để biểu thị mối quan hệ giữa nhiệt lượng tổng ở áp suất không đổi và ở thể tích không đổi:
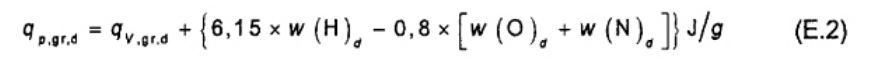
trong đó w(H)d, w(O)d và w(N)d có cùng mức ý nghĩa như trong 12.2. w(H), w(O) và w(N) không chứa bất kỳ sự đóng góp nào từ phần khoáng chất của mẫu nhiên liệu. Tuy vậy, sự không chắc chắn/không đảm bảo được đưa vào bằng cách thay thế w(H)d, w(O)d và w(N)d là không đáng kể. Hệ số cho w(N)d, chặt chẽ, là 0,9 nhưng có thể được coi là bằng với hệ số của oxy vì hệ số như vậy là nhỏ
E.3 Giá trị nhiệt lượng thực
E.3.1 Giá trị nhiệt lượng thực ở thể tích không đổi
Năng lượng của sự bay hơi (thể tích không đổi) đối với nước ở 25 °C là 41,53 kJ/mol. Điều này tương ứng với 206,0 J/g đối với phần khối lượng của 1 % hydro trong mẫu nhiên liệu hoặc 23,05 J/g đối với phần khối lượng là 1 % độ ẩm, tương ứng.
Giá trị nhiệt lượng thực ở thể tích không đổi, qv,net, được suy ra từ giá trị nhiệt lượng toàn phần tương ứng, ví dụ:

trong đó w(N)d là lượng hydrogen, tính bằng % khối lượng, của nhiên liệu khô (xem12.2)
Đối với độ ẩm yêu cầu M (ví dụ tổng độ ẩm nhận được, Mar), giá trị nhiệt lượng thực ở thể tích không đổi được tính theo
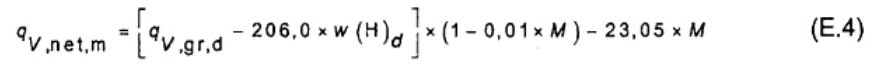
E.3.2 Giá trị nhiệt lượng thực ở áp suất không đổi
Entanpi hóa hơi (áp suất không đổi) đối với nước ở 25 °C là 44,01 kJ/mol. Điều này tương ứng với 218,3 J/g đối với khối lượng của 1 % hydro trong mẫu nhiên liệu hoặc 24,43 J/g đối với khối lượng của 1 % độ ẩm, tương ứng.
Nhiệt lượng thực ở áp suất không đổi đối với mẫu khô có thể được tính từ giá trị đó ở thể tích không đổi theo
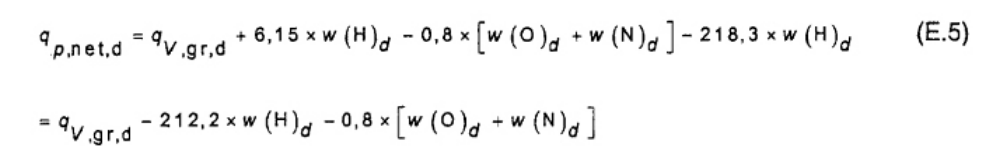
Đối với độ ẩm yêu cầu M (ví dụ: tổng độ ẩm nhận được, Mar), giá trị nhiệt lượng thực ở áp suất không đổi được tính toán từ công thức:
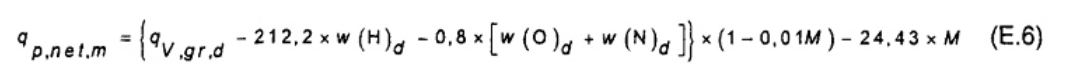
E.4 Sử dụng giá trị mặc định hoặc đặc trưng để tính giá trị nhiệt lượng
a) Nhiên liệu sinh học rắn nguyên chất được xác định rõ ràng và đặc trưng
Đối với nhiên liệu sinh học gốc được xác định rõ ràng các đặc tính, các giá trị đặc trưng với các tài liệu viện dẫn đầy đủ hoặc nếu không có sẵn, các giá trị mặc định cho hydro (H), nitơ (N), oxy (O) và lưu huỳnh (S) có thể được sử dụng thay thế của các giá trị xác định trên các tính toán của giá trị nhiệt lượng tổng và giá trị nhiệt lượng thực.
Các giá trị mặc định trong Phụ lục G được đưa ra trên cơ sở khô, không có tro và phải được chuyển đổi sang chu kỳ yêu cầu trong tài liệu này bằng cách sử dụng các công thức cho trong ISO 16993.
b) Nhiên liệu sinh học và hỗn hợp nhiên liệu sinh học
Đối với nhiên liệu sinh học và hỗn hợp nhiên liệu sinh học khác, việc xác định hydro (H), nitơ (N) oxy (O), lưu huỳnh (S) và tro phải được thực hiện đồng thời với việc xác định nhiệt lượng.
Hàm lượng oxy (O) trên cơ sở khô được tính toán theo ISO 16993.
Hàm lượng clo w (Cl)d và lưu huỳnh w (S)d có thể được bỏ qua trong tính toán hàm lượng oxy vì hàm lượng của chúng thường thấp trong nhiên liệu sinh học rắn và ảnh hưởng không đáng kể đến việc tính toán.
Phụ lục F
(tham khảo)
Danh sách ký hiệu sử dụng trong tiêu chuẩn
| qv,gr | Giá nhiệt lượng toàn phần ở thể tích không đổi của nhiên liệu sinh học được phân tích |
| qv,gr,d | Giá trị nhiệt lượng toàn phần ở thể tích không đổi của nhiên liệu khô |
| qv,gr,m | Giá trị nhiệt lượng toàn phần ở thể tích không đổi của nhiên liệu sinh học có độ ẩm M |
| qp,gr,d | Giá trị nhiệt lượng toàn phần ở áp suất không đổi của nhiên liệu khô) |
| qv,net,m | Giá trị nhiệt lượng thực ở áp suất không đổi của nhiên liệu sinh học có độ ẩm M |
| qp,net | Giá trị nhiệt lượng ở áp suất không đổi |
| qp,net,d | Giá trị nhiệt lượng thực ở áp suất không đổi của nhiên liệu khô |
| qp,net,m | Giá trị nhiệt lượng thực ở áp suất không đổi của nhiên liệu sinh học có độ ẩm M |
| qv,ba | Giá trị nhiệt lượng toàn phần đã được chứng nhận ở thể tích không đổi đối với axit benzoic |
| qv,2 | Giá trị nhiệt lượng toàn phần ở thể tích không đổi của chất trợ cháy |
| Qfuse | Từ quá trình đốt cháy mồi đốt |
| Qign | Từ quá trình oxy hóa của mồi đốt |
| QN | Từ quá trình hình thành axit nitric (từ nước dạng lỏng với oxy và nitơ dạng khí) |
| QS | Hiệu chỉnh lưu huỳnh từ axit sunfuric loãng trong bình áp lực thành khí lưu huỳnh dioxit |
| Q N,S | Hiệu chỉnh kết hợp đối với axit sulphuric và nitric |
| Qs.add | Hiệu chỉnh bổ sung đối với lưu huỳnh được sử dụng với Q N,S |
| M | Độ ẩm của nhiên liệu sinh học cần tính toán |
| Mad | Độ ẩm trong mẫu phân tích chung |
| Mar | Tổng độ ẩm của mẫu nhận được (mẫu được lấy) |
| mba | Khối lượng axit benzoic |
| m1 | Khối lượng của mẫu nhiên liệu sinh học |
| m2 | Khối lượng của chất trợ cháy |
| mcr | Khối lượng của chén nung |
| ε | Nhiệt dung hữu hiệu của nhiệt lượng kế |
| εo | Nhiệt dung hữu hiệu của nhiệt lượng kế giả định không có chén nung trong bom |
| ε• | Nhiệt dung hữu hiệu của nhiệt lượng kế trên cơ sở “tổng khối lượng nhiệt lượng kế” |
| ε(n) | Nhiệt dung hữu hiệu trung bình của nhiệt lượng kế dựa trên phép xác định n của ε |
| εo(n) | Nhiệt dung hữu hiệu trung bình của nhiệt lượng kế dựa trên phép xác định n của ε0 |
|
| Ước số (tương ứng với giá trị "trung bình") của ε từ đường hồi quy tuyến tính của ε dưới dạng hàm của sự tăng nhiệt độ quan sát được (tf- ti) |
| Cp,cr | Nhiệt dung riêng của bình nung |
| Cp,aq | Nhiệt dung riêng của nước |
| θ | Nhiệt độ tăng hiệu chỉnh |
| T | Nhiệt độ tham chiếu để tính nhiệt lượng (T = 298,15 K) |
| t | Nhiệt độ nhiệt lượng kế |
| ti | Nhiệt độ ban đầu ở chu kỳ chính |
| tf | Nhiệt độ cuối của chu kỳ chính = nhiệt độ tham chiếu |
| tf-ti | Sự tăng nhiệt độ quan sát |
| Δtex | Hiệu chỉnh mất nhiệt |
| ti | Nhiệt độ bộ ổn nhiệt |
| ti-t | Chênh nhiệt đầu |
|
| Nhiệt độ tiệm cận của nhiệt lượng kế đẳng tích (ở thời gian "vô hạn") |
| tmi | Nhiệt độ trung bình ở chu kỳ trước |
| tmf | Nhiệt độ trung bình t ở chu kỳ sau |
| tf+a | Nhiệt độ một phút sau khi kết thúc chu kỳ chính |
| tx | Nhiệt độ tại thời điểm |
|
| Thời gian |
|
| Thời gian bắt đầu chu kỳ chính |
|
| Thời gian kết thúc chu kỳ chính |
|
| Thời gian ngoại suy Dickinson |
| R | Hằng số khí (R = 8,314 47 J/mol x K) |
| G | Hằng số tỷ lệ cụ thể |
| g | Tốc độ thay đổi nhiệt (dt/d |
| gi | Tốc độ trượt ở chu kỳ trước |
| gf | Tốc độ trượt ở chu kỳ sau |
| Pst | Công độ khuấy |
| daf | Khô và tro tự do |
| w(A)d | Hàm lượng tro của nhiên liệu sinh học khô |
| w(C)d | Hàm lượng carbon của nhiên liệu sinh học khô |
| w(CI)d | Hàm lượng clo của nhiên liệu sinh học khô |
| w(H)d | Hàm lượng hydro của nhiên liệu sinh học khô (bao gồm hydro từ nước hydrat hóa cũng như hydro trong nhiên liệu sinh học) |
| w(O)d | Hàm lượng oxy của nhiên liệu sinh học khô |
| w(N)d | Hàm lượng nitơ của nhiên liệu sinh học khô |
| w(S)d | Hàm lượng Sulfur của nhiên liệu sinh học khô |
Phụ lục G
(tham khảo)
Giá trị xác định của các loại nhiên liệu sinh học rắn dùng để tính giá trị nhiệt lượng
| Nhiên liệu sinh học rắn, nguồn gốc | Hydrogen (H) phân số khối lượng | Oxygen (0) phân số khối lượng | Nitrogen (N) phân số khối lương | Sulfur (S) phân số khối lượng | |
| Rừng, rừng trồng và gỗ nguyên sinh khác (1.1) | Thân gỗ không vỏ, đầu mẩu và lá (1.1.3.3, 1.1.3.4, 1.2.1.3, 1.2.1.4) | 6.2 | 43 | 0.1 | 0.02 |
| Phế liệu và phụ phẩm chưa xử lý hoá học của ngành công nghiệp chế biến gỗ (1.2.1) | Toàn bộ cây (1.1.1) (1.1.2) | 6.2 | 42 | 0.2 | 0.02 |
| Phế liệu gỗ (1.1.4) | 6.1 | 41 | 0.5 | 0.04 | |
| Vỏ cây (1.1.6, 1.2.1.5) | 6.1 | 40 | 0.4 | 0.1 | |
| Cây bụi chu kỳ ngắn(1.1.1.3, 1.1.2.3) | 6.3 | 44 | 0.5 | 0.05 | |
| Phần thân cây ngũ cốc (2.1.1.2) | Cây lúa mì, rye, lúa mạch(2.1.1.2) | 6.3 | 43 | 0.5 | 0.1 |
| Cây lúa (2.1.1.2) | 6.2 | 44 | 1.0 | 0.1 | |
| Thân cây cỏ (2.1.2.2) | Cây cải dầu (2.1.1.2) | 6.3 | 43 | 0.8 | 0.3 |
| Các loại cỏ (2.1.2.2) | 6.3 | 43 | 1.0 | 0.2 | |
| Các loại hạt và hạt ngũ cốc (2.1.1.3) | Cây lúa mì, lúa mạch (2.1.1.3) | 6.6 | 45 | 2.0 | 0.1 |
| Hột Olive (2.1.2.3; 3.2.1.2) | Hột nguyên và các hột chưa xử lý hóa chất (3.1.2.3, 3.2.1.2) | 6.2 | 42 | 0.2 | 0.02 |
CHÚ THÍCH 1: Các giá trị liệt kê ở trên đã được dữ liệu hóa và chứng nhận trong tiêu chuẩn ISO/TC 238/WG4.
CHÚ THÍCH 2: Các giá trị liệt kê ở trên dựa trên hàm lượng khô, không có tro. ISO 16993 cung cấp các công thức để chuyển đổi sang cơ sở “như đã phân tích” và “khô”.
CHÚ THÍCH 3: Đặc điểm kỹ thuật về nguồn gốc của nhiên liệu sinh học rắn tuân theo ISO 17225-1: 2014, Bảng 1
CHÚ THÍCH 4: Giá trị mặc định đối với hột ô liu chỉ có giá trị nếu hàm lượng tro <1,5 w-% cơ sở khô.
Phụ lục H
(tham khảo)
Sơ đồ xác định giá trị nhiệt lượng thông thường
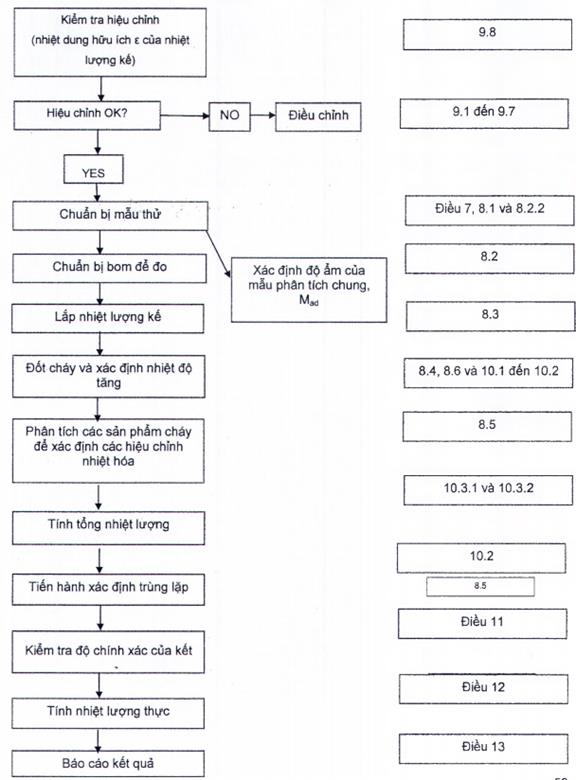
Thư mục tài liệu tham khảo
[1] ISO 1928, Solid mineral fuels - Determination of gross calorific value by the bomb calorimetric method and calculation of net calorific value
[2] ISO 10304-1, Water quality - Determination of dissolved anions by liquyd chromatography of ions - Part 1: Determination of bromide, chloride, fluoride, nitrate, nitrite, phosphate and sulfate
[3] ISO 16948, Solid biofuels - Determination of total content of carbon, hydrogen and nitrogen
[4] ISO 16993, Solid biofuels - Conversion of analytical results from one basis to another
[5] ISO 16994, Solid biofuels - Determination of total content of sulphur and chlorine
[6] ISO 17225-1:2014, Solid biofuels - Fuel specifications and classes - Part 1: General requyrements
[7] ISO 18122, Solid biofuels - Determination of ash content
[8] ISO 18134-1, Solid biofuels - Determination of moisture content - Oven dry method - Part 1: Total moisture - Reference method
[9] ISO 18134-2, Solid biofuels - Determination of moisture content - Oven dry method - Part 2: Total moisture - Simplified method
Mục lục
1 Phạm vi áp dụng
2 Tài liệu viện dẫn
3 Thuật ngữ và định nghĩa
4 Nguyên tắc của phương pháp
5 Hóa chất, thuốc thử
6 Thiết bị, dụng cụ
7 Chuẩn bị mẫu thử
8 Quy trình đo nhiệt lượng
9 Hiệu chuẩn
10 Giá trị nhiệt lượng toàn phần
11 Đặc điểm biểu thị độ lặp lại và độ tái lập
12 Tính giá trị nhiệt lượng thực ở áp suất không đổi
13 Báo cáo thử nghiệm
Phụ lục A (quy định) - Bom nhiệt lượng kế
Phụ lục B (quy định) - Bom nhiệt lượng kế đẳng nhiệt và vỏ bọc tĩnh nhiệt
Phụ lục C (quy định) - Bom nhiệt lượng kế tự động
Phụ lục D (tham khảo) - Danh sách kiểm tra đối với thiết kế các phép thử và quy trình đốt cháy
Phụ lục E (tham khảo) - Một ví dụ về các phép tính sử dụng trong tiêu chuẩn này khi dùng bom nhiệt lượng kế tự động để xác định
Phụ lục F (tham khảo) - Danh sách ký hiệu sử dụng trong tiêu chuẩn
Phụ lục G (tham khảo) - Giá trị xác định của các loại nhiên liệu sinh học rắn dùng để tính giá trị nhiệt lượng
Phụ lục H (tham khảo) - Sơ đồ xác định giá trị nhiệt lượng thông thường
Thư mục tài liệu tham khảo
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 13653:2023 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 13653:2023 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 13653:2023 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 13653:2023 DOC (Bản Word)