- Tổng quan
- Nội dung
- VB gốc
- Tiếng Anh
- Hiệu lực
- VB liên quan
- Lược đồ
-
Nội dung hợp nhất
Tính năng này chỉ có tại LuatVietnam.vn. Nội dung hợp nhất tổng hợp lại tất cả các quy định còn hiệu lực của văn bản gốc và các văn bản sửa đổi, bổ sung, đính chính... trên một trang. Việc hợp nhất văn bản gốc và những văn bản, Thông tư, Nghị định hướng dẫn khác không làm thay đổi thứ tự điều khoản, nội dung.
Khách hàng chỉ cần xem Nội dung hợp nhất là có thể nắm bắt toàn bộ quy định hiện hành đang áp dụng, cho dù văn bản gốc đã qua nhiều lần chỉnh sửa, bổ sung.
- Tải về
Quyết định 344/QĐ-QLD 2024 Quy trình thao tác trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015
| Cơ quan ban hành: | Cục Quản lý Dược |
Số công báo:
Số công báo là mã số ấn phẩm được đăng chính thức trên ấn phẩm thông tin của Nhà nước. Mã số này do Chính phủ thống nhất quản lý.
|
Đang cập nhật |
| Số hiệu: | 344/QĐ-QLD | Ngày đăng công báo: | Đang cập nhật |
| Loại văn bản: | Quyết định | Người ký: | Vũ Tuấn Cường |
| Trích yếu: | Về việc ban hành Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý Nhà nước tại Cục Quản lý Dược | ||
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
30/05/2024 |
Ngày hết hiệu lực:
Ngày hết hiệu lực là ngày, tháng, năm văn bản chính thức không còn hiệu lực (áp dụng).
|
Đang cập nhật |
|
Áp dụng:
Ngày áp dụng là ngày, tháng, năm văn bản chính thức có hiệu lực (áp dụng).
|
Đã biết
|
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
| Lĩnh vực: | Thực phẩm-Dược phẩm | ||
TÓM TẮT QUYẾT ĐỊNH 344/QĐ-QLD
Quyết định 344/QĐ-QLD: Quy trình thao tác chuẩn trong quản lý thuốc đối chứng tại Cục Quản lý Dược
Quyết định 344/QĐ-QLD được ban hành bởi Cục Quản lý Dược thuộc Bộ Y tế ngày 30 tháng 05 năm 2024, có hiệu lực kể từ ngày ký. Quyết định này quy định Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015, áp dụng cho hoạt động quản lý nhà nước tại Cục Quản lý Dược, đặc biệt liên quan đến việc công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học.
Quy trình này hướng tới mục tiêu thống nhất và cải tiến quy trình công bố thuốc đối chứng, từ khâu lựa chọn thuốc tới việc ra quyết định công bố. Nội dung chính của quy trình bao gồm:
- Thống nhất các bước công bố: Quy trình chỉ rõ từng bước trong quy trình công bố thuốc đối chứng, bao gồm từ việc lập danh mục và lựa chọn thuốc đến việc thông qua hội đồng chuyên gia.
- Trách nhiệm rõ ràng: Văn bản quy định rõ trách nhiệm của từng cá nhân và phòng ban liên quan, từ lãnh đạo Cục, phòng Đăng ký thuốc, đến những chuyên viên thực hiện thẩm định hồ sơ.
- Thời gian thực hiện: Mỗi bước trong quy trình đều có thời gian thực hiện cụ thể nhằm đảm bảo tiến độ và chất lượng công việc.
- Hồ sơ và biểu mẫu: Quy trình cũng bao gồm các mẫu hồ sơ và biểu mẫu cụ thể để thuận tiện trong việc triển khai thực hiện và lưu trữ thông tin.
Quyết định này có thể tác động lớn đến các cơ sở sản xuất, các doanh nghiệp dược, và các chuyên viên làm việc trong lĩnh vực quản lý và giám sát thuốc, giúp họ nắm bắt được quy trình công bố và tuân thủ các yêu cầu pháp lý mới nhất.
Nội dung của Quyết định 344/QĐ-QLD sẽ không chỉ đơn thuần là hướng dẫn kỹ thuật mà còn đóng vai trò quan trọng trong việc nâng cao chất lượng quản lý dược phẩm tại Việt Nam, phù hợp với các quy định của pháp luật hiện hành, bao gồm Luật Dược số 105/2016/QH13 và các Thông tư liên quan.
Xem chi tiết Quyết định 344/QĐ-QLD có hiệu lực kể từ ngày 30/05/2024
Tải Quyết định 344/QĐ-QLD
| BỘ Y TẾ | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
| Số: 344/QĐ-QLD | Hà Nội, ngày 30 tháng 05 năm 2024 |
QUYẾT ĐỊNH
Về việc ban hành Quy trình thao tác chuẩn trong
Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015
áp dụng vào hoạt động quản lý nhà nước tại Cục quản lý Dược
________________________
CỤC TRƯỞNG CỤC QUẢN LÝ DƯỢC
Căn cứ Nghị định số 95/2022/NĐ-CP ngày 15/11/2022 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Căn cứ Quyết định số 1969/QĐ-BYT ngày 26/4/2023 của Bộ trưởng Bộ Y tế quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Cục Quản lý Dược thuộc Bộ Y tế;
Căn cứ Quyết định số 388/QĐ-QLD ngày 29/5/2023 của Cục trưởng Cục Quản lý Dược về việc ban hành Quy định chức năng, nhiệm vụ, quyền hạn của Văn phòng và các phòng thuộc Cục Quản lý Dược;
Căn cứ yêu cầu thực tế công tác quản lý của Cục Quản lý Dược;
Theo đề nghị của Chánh Văn phòng Cục.
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này Quy trình thao tác chuẩn trong Hệ thống quản lý chất lượng theo tiêu chuẩn ISO 9001:2015 áp dụng vào hoạt động quản lý nhà nước tại Cục Quản lý Dược, cụ thể:
Quy trình công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học (Mã số QTDK.27.01).
Điều 2. Quyết định này có hiệu lực kể từ ngày ký ban hành.
Điều 3. Các Ông/bà: Lãnh đạo Cục, Lãnh đạo Ban QMS, Chánh Văn phòng, Trưởng các phòng thuộc Cục Quản lý Dược chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: | CỤC TRƯỞNG |
|
CỤC QUẢN LÝ DƯỢC PHÒNG ĐĂNG KÝ THUỐC
QUY TRÌNH CÔNG BỐ DANH MỤC THUỐC ĐỐI CHỨNG DÙNG TRONG THỬ TƯƠNG ĐƯƠNG SINH HỌC
MÃ SỐ: QT.ĐK.27.01
|
|
CỤC QUẢN LÝ DƯỢC | QUY TRÌNH | Mã số: QT.ĐK.27.01 Ngày ban hành: Lần ban hành: 01 Tổng số trang: 10 |
| 1. Người có liên quan phải nghiên cứu và thực hiện đúng các nội dung của quy định này. 2. Nội dung trong quy định này có hiệu lực thi hành như sự chỉ đạo của lãnh đạo Cục Quản lý Dược. 3. Mỗi đơn vị chỉ được phân phối 01 bản (có đóng dấu kiểm soát). Khi các đơn vị có nhu cầu phân phối thêm tài liệu phải đề nghị với Ban QMS để có bản đóng dấu có kiểm soát. File mềm được cung cấp trên mạng nội bộ để chia sẻ thông tin. |
NƠI NHẬN (ghi rõ nơi nhận rồi đánh dấu X ô bên cạnh)
|
| Lãnh đạo Cục |
| Phòng Đăng ký thuốc |
|
| Ban QMS |
| Phòng Quản lý chất lượng thuốc |
|
| Văn phòng Cục |
| Phòng Quản lý giá thuốc |
|
| Phòng Pháp chế Hội nhập |
| Phòng Quản lý mỹ phẩm |
|
| Phòng Quản lý kinh doanh dược |
| Trung tâm Đào tạo và Hỗ trợ doanh nghiệp dược mỹ phẩm |
|
| Văn phòng NRA |
| Văn phòng Hội đồng tư vấn cấp GĐKLH thuốc, nguyên liệu làm thuốc |
1. MỤC ĐÍCH
Quy trình này nhằm thống nhất việc công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học theo quy định tại khoản 4 Điều 6 Thông tư số 07/2022/TT-BYT ngày 05 tháng 9 năm 2022 của Bộ Y tế quy định thuốc phải thử tương đương sinh học và các yêu cầu đối với hồ sơ báo cáo số liệu nghiên cứu tương đương sinh học trong đăng ký lưu hành thuốc tại Việt Nam (sau đây gọi tắt là Thông tư 07).
2. PHẠM VI ÁP DỤNG
Quy trình này áp dụng đối với hoạt động công bố thuốc đối chứng dùng trong thử tương đương sinh học.
3. TÀI LIỆU THAM CHIẾU
- Luật Dược số 105/2016/QH13 ngày 06/4/2016
- Thông tư số 07/2022/TT-BYT ngày 05 tháng 9 năm 2022 của Bộ Y tế quy định thuốc phải thử tương đương sinh học và các yêu cầu đối với hồ sơ báo cáo số liệu nghiên cứu tương đương sinh học trong đăng ký lưu hành thuốc tại Việt Nam.
- Thông tư 08/2022/TT-BYT ngày 05/09/2022 quy định việc đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
4. TRÁCH NHIỆM THỰC HIỆN
- Lãnh đạo phòng ĐKT có trách nhiệm thường xuyên kiểm tra, đôn đốc, tổ chức thực hiện theo đúng quy định tại quy trình này.
- Lãnh đạo Cục, Lãnh đạo phòng ĐKT và chuyên viên có liên quan của phòng ĐKT, Văn phòng Cục có trách nhiệm thực hiện và tuân thủ những quy định trong quy trình này.
- Lãnh đạo các phòng có liên quan trong Cục QLD có trách nhiệm phối hợp, kiểm tra và bảo đảm những quy định trong quy trình này được thực hiện và tuân thủ.
- Phòng Đăng ký thuốc chịu trách nhiệm phối hợp với Văn phòng Hội đồng tư vấn cấp GĐKLH thuốc, nguyên liệu làm thuốc tổ chức họp Hội đồng và xử lý biên bản họp Hội đồng.
5. ĐỊNH NGHĨA VÀ CHỮ VIẾT TẮT
5.1. Thuật ngữ:
- Chuyên viên đầu mối: là chuyên viên được giao nhiệm vụ tổng hợp danh mục thuốc đối chứng đề nghị công bố, dự thảo Quyết định và Phiếu trình Lãnh đạo Cục theo danh sách phân công của Lãnh đạo Cục hoặc Lãnh đạo Phòng.
- Chuyên viên phụ trách: là chuyên viên được giao nhiệm vụ thụ lý hồ sơ đăng ký thuốc trong nước, thuốc nước ngoài theo danh sách phân công của Lãnh đạo Phòng hoặc Lãnh đạo Cục.
- Chuyên gia thẩm định: Là Chuyên gia thẩm định hồ sơ cấp/thay đổi bổ sung giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc tiểu ban tương đương sinh học theo Quyết định về việc ban hành Danh sách chuyên gia của Cục Quản lý Dược.
5.2. Chữ viết tắt:
- HĐ: Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
- Cục QLD: Cục Quản lý Dược
- VPHĐ: Văn phòng Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc;
- BB: Biên bản;
- CVĐM: Chuyên viên đầu mối
- CVPT: Chuyên viên phụ trách
- CGTĐ: Chuyên gia thẩm định (Trong phạm vi quy trình này, chuyên gia thẩm định là các chuyên gia được phân công thẩm định tiểu ban tương đương sinh học theo các quyết định chuyên gia hiện hành).
- P. ĐKT: Phòng Đăng ký thuốc.
- HS: Hồ sơ
- BM: Biểu mẫu.
- ĐKT: Đăng ký thuốc
- SĐK: Số đăng ký
- GĐKLH: Giấy đăng ký lưu hành
- LĐP: Lãnh đạo phòng
- TP: Trưởng phòng
- PTP: Phó Trưởng phòng
- TĐSH: tương đương sinh học.
- HS TĐSH: hồ sơ tương đương sinh học.
6. QUY ĐỊNH CHUNG
6.1. Trách nhiệm của Cục trưởng:
- Xem xét số lượng các thuốc thuộc danh mục công bố phù hợp với nội dung Phiếu trình báo cáo của Phòng Đăng ký thuốc, các Biên bản thẩm định và ý kiến của Phó Cục trưởng phụ trách lĩnh vực tương đương sinh học, ký hoặc ủy quyền Trưởng phòng Đăng ký thuốc ký Danh mục báo cáo Hội đồng tư vấn cấp GĐKLH thuốc, nguyên liệu làm thuốc.
- Xem xét ký hoặc giao Phó Cục trưởng phụ trách lĩnh vực tương đương sinh học ký quyết định công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học sau khi có ý kiến tư vấn của Hội đồng.
6.2. Trách nhiệm của Phó Cục trưởng phụ trách lĩnh vực tương đương sinh học:
- Xem xét danh mục công bố phù hợp với nội dung Phiếu trình báo cáo của Trưởng Phòng Đăng ký thuốc và các Biên bản thẩm định kèm theo.
- Ký quyết định công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học khi được Cục trưởng phân công.
6.3. Trách nhiệm của Trưởng Phòng Đăng ký thuốc:
- Xem xét thông tin thuốc trong Danh mục thuốc đối chứng dùng trong thử tương đương sinh học trên cơ sở đề xuất của Phó trưởng phòng Đăng ký thuốc phù hợp với tài liệu và nội dung dự thảo Phiếu trình báo cáo của Phòng, các Biên bản thẩm định kèm theo.
- Ký công văn gửi VPHĐ Danh mục báo cáo Hội đồng tư vấn cấp GĐKLH thuốc, nguyên liệu làm thuốc khi được Cục trưởng ủy quyền.
- Xem xét ký tắt dự thảo Quyết định công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học.
6.4. Trách nhiệm của Phó trưởng Phòng Đăng ký thuốc (phụ trách công tác thử tương đương sinh học):
- Xem xét và kết luận về việc lựa chọn thuốc đối chứng tại Biên bản thẩm định.
- Xem xét thông tin thuốc trong Danh mục thuốc đối chứng dùng trong thử tương đương sinh học theo đề xuất của Chuyên viên phù hợp với Biên bản lựa chọn thuốc đối chứng.
- Xem xét ký tắt dự thảo Quyết định công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học.
6.5. Trách nhiệm của Chuyên viên đầu mối công bố Danh mục thuốc đối chứng:
- Chuẩn bị mẫu Biên bản lựa chọn thuốc đối chứng, trong đó ghi rõ thông tin thuốc thử cần lựa chọn thuốc đối chứng.
- Gửi Biên bản thẩm định lựa chọn thuốc đối chứng đến các chuyên gia thẩm định hồ sơ tương đương sinh học để lấy ý kiến.
- Chuyển thông tin thuốc đối chứng được lựa chọn đến Chuyên viên phụ trách cơ sở sản xuất thuốc đối chứng để kiểm tra và xác nhận thông tin thuốc đối chứng (trong trường hợp thuốc đối chứng đã được cấp phép lưu hành tại Việt Nam).
- Tổng hợp Danh mục thuốc đối chứng dùng trong thử tương đương sinh học.
- Dự thảo Phiếu trình Lãnh đạo Cục và Quyết định về việc công bố danh mục thuốc có tài liệu chứng minh tương đương sinh học.
6.6. Trách nhiệm của Chuyên viên phụ trách:
- Chuyên viên phụ trách cơ sở sản xuất thuốc đối chứng được các chuyên gia lựa chọn kiểm tra và xác nhận thông tin thuốc đối chứng theo nội dung tại Biểu mẫu Biên bản (trong trường hợp thuốc đối chứng đã được cấp phép lưu hành tại Việt Nam).
6.7. Trách nhiệm của Chuyên gia:
- Chuyên gia phải thẩm định và ghi đầy đủ ý kiến theo các mục trong Biểu mẫu Biên bản thẩm định, ký và ghi rõ họ tên, ngày thẩm định.
7. NỘI DUNG QUY TRÌNH
7.1. Sơ đồ Quy trình công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học: Chi tiết xem trang sau:
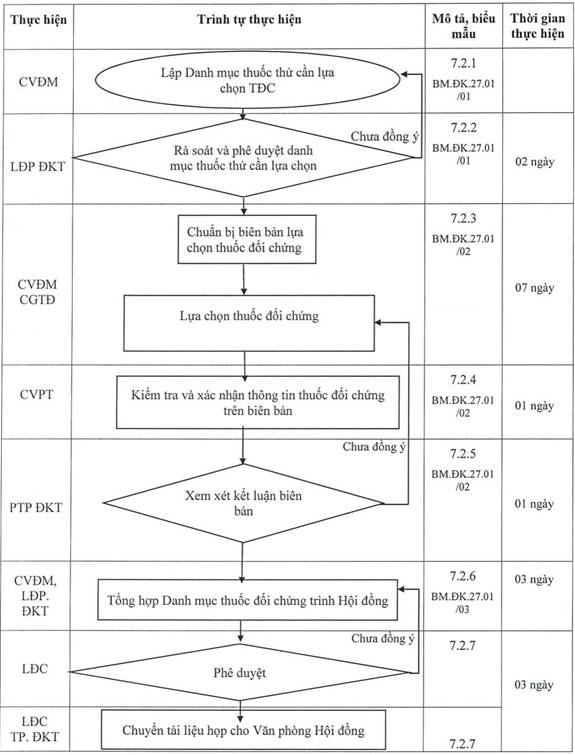
7.2. Mô tả Quy trình
7.2.1. Lập Danh mục thuốc thử cần lựa chọn thuốc đối chứng:
Căn cứ trên Danh mục dược chất chứa trong thuốc generic phải báo cáo dữ liệu nghiên cứu tương đương sinh học khi đăng ký lưu hành thuốc (bao gồm thuốc đơn thành phần, thuốc phối hợp có chứa dược chất phải thử, thuốc có dạng bào chế phải thử), các thuốc có dạng bào chế bắt buộc phải thử hoặc các văn bản đề nghị lựa chọn thuốc đối chứng của các đơn vị, CVĐM lập Danh mục thuốc cần lựa chọn thuốc đối chứng theo biểu mẫu BM.ĐK.27.01/01.
7.2.2. Rà soát, phê duyệt danh mục thuốc thử cần lựa chọn thuốc đối chứng:
Thời gian tối đa thực hiện là 02 ngày làm việc.
- LĐP xem xét rà soát và phê duyệt Danh mục thuốc cần lựa chọn thuốc đối chứng dự kiến đã được lập tại bước 1.
- Trong trường hợp có thuốc bị loại bỏ khỏi danh mục: LĐP phải nêu rõ lý do loại bỏ.
7.2.3. Lựa chọn thuốc đối chứng, rà soát thông tin thuốc đối chứng:
Thời gian tối đa thực hiện là 07 ngày làm việc.
- Căn cứ trên Danh mục thuốc cần lựa chọn thuốc đối chứng đã được LĐP phê duyệt, CVĐM tra cứu và ghi thông tin các thuốc có thể được lựa chọn làm thuốc đối chứng trên biên bản theo biểu mẫu BM.ĐK.27.01/02. Trong trường hợp cần thiết, CVĐM có thể xin ý kiến của các chuyên gia tiểu ban Tương đương sinh học.
7.2.4. CVPT kiểm tra và xác nhận thông tin thuốc đối chứng trên biên bản:
Thời gian tối đa thực hiện là 01 ngày làm việc.
- Sau khi có kết luận về việc lựa chọn thuốc đối chứng, nếu thuốc đối chứng được lựa chọn đã được cấp GĐKLH tại Việt Nam, CVĐM chuyển biên bản cho CVPT kiểm tra và xác nhận thông tin thuốc đối chứng theo nội dung tại Biểu mẫu biên bản BM.ĐK.27.01/02.
Trường hợp CVPT có ý kiến với ý kiến thẩm định của chuyên gia hoặc bổ sung ý kiến, CVPT ghi ý kiến vào nội dung đề xuất trên BB, phần xử lý của Phòng ĐKT.
7.2.5. Phó Trưởng phòng xem xét kết luận biên bản:
Thời gian tối đa thực hiện là 01 ngày làm việc.
- Trên cơ sở các ý kiến chuyên gia thẩm định và chuyên viên, PTP ghi kết luận trên BB: Trình Hội đồng công bố thuốc đối chứng và/hoặc ý kiến khác.
- Trường hợp PTP có ý kiến khác với ý kiến của chuyên gia thẩm định và chuyên viên, PTP ghi ý kiến vào nội dung đề xuất trên BB, phần xử lý của Phòng ĐKT.
- Trường hợp cần trao đổi lại với chuyên gia thẩm định và chuyên viên, PTP ghi rõ ý kiến trên BB để chuyển lại cho chuyên viên và chuyên gia thẩm định.
7.2.6. Tổng hợp danh mục thuốc đối chứng trình Hội đồng:
Thời gian thực hiện tối đa: 03 ngày làm việc.
- CVĐM tổng hợp Danh mục thuốc đối chứng đã được PTP kết luận trình Hội đồng công bố thuốc đối chứng để xin ý kiến Hội đồng (kèm theo nội dung báo cáo cụ thể) theo Biểu mẫu BM.ĐK.27.01/03.
- PTP rà soát, ký tắt trên từng trang của các Danh mục trình Hội đồng. Trường hợp PTP chưa đồng ý, PTP ghi rõ ý kiến vào dự thảo Danh mục để CVĐM và CVPT cùng kiểm tra và báo cáo lại PTP.
- TP rà soát các Danh mục trình Hội đồng và ký Phiếu trình báo cáo Lãnh đạo Cục. Trường hợp đồng ý với dự thảo, TP ký Phiếu trình Lãnh đạo Cục. Trường hợp TP chưa đồng ý, TP ghi rõ ý kiến vào dự thảo danh mục và Phiếu trình để CVĐM và CVPT cùng kiểm tra và báo cáo lại PTP và TP.
7.2.7. Chuyển tài liệu họp cho Văn phòng Hội đồng:
Thời gian thực hiện tối đa: 03 ngày làm việc.
- Phó Cục trưởng phụ trách lĩnh vực tương đương sinh học xem xét Danh mục thuốc đối chứng trình Hội đồng xin ý kiến.
- Cục trưởng xem xét số lượng thuốc thuộc Danh mục thuốc đối chứng trình Hội đồng xin ý kiến.
- Trên cơ sở Danh mục thuốc đối chứng trình Hội đồng do P. ĐKT đề xuất, Cục trưởng xem xét ký hoặc giao Phó Cục trưởng phụ trách lĩnh vực tương đương sinh học hoặc ủy quyền Trưởng Phòng ĐKT ký công văn chuyển Văn phòng Hội đồng Danh mục thuốc đối chứng trình Hội đồng, Biên bản lựa chọn thuốc đối chứng và các tài liệu kèm theo (nếu có).
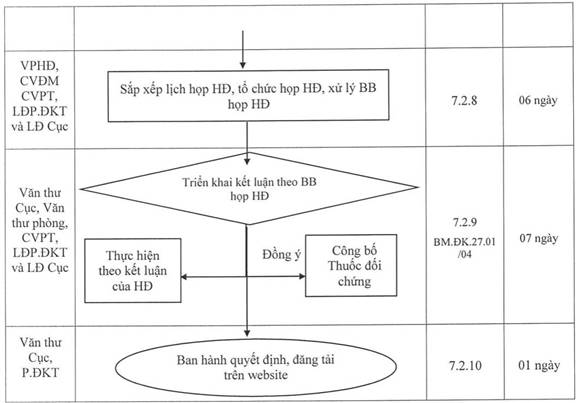
7.2.8. Sắp xếp lịch họp HĐ, tổ chức họp HĐ, xử lý BB họp HĐ
Thời gian thực hiện: Theo Quy chế của Hội đồng, VPHĐ
Người thực hiện: CV được phân công, LĐP. ĐKT, LĐ Cục QLD, VPHĐ
Văn phòng Hội đồng hoàn thiện Biên bản họp Hội đồng và thông báo cho Cục Quản lý Dược để triển khai các bước tiếp theo: Nội dung này thực hiện theo Quy chế về tổ chức, hoạt động của Hội đồng tư vấn cấp giấy ĐKLH thuốc, nguyên liệu làm thuốc.
7.2.9. Triển khai kết luận theo biên bản họp HĐ:
Sau khi nhận được biên bản họp Hội đồng đã có ý kiến kết luận của Chủ tịch Hội đồng từ Văn phòng Hội đồng, Cục Quản lý Dược sẽ tiến hành các bước sau:
7.2.9.1. Đối với các thuốc đối chứng Hội đồng chưa đồng ý công bố:
Thời gian thực hiện: 07 ngày.
Trên cơ sở kết luận của Hội đồng, Cục Quản lý Dược (Phòng ĐKT) thực hiện các bước tiếp theo theo kết luận của Hội đồng.
7.2.9.2. Đối với các thuốc đối chứng Hội đồng đồng ý công bố:
Thời gian thực hiện: 07 ngày.
- CVĐM căn cứ vào thông tin Biên bản họp Hội đồng để trình Lãnh đạo Phòng phụ trách dự thảo Quyết định công bố danh mục thuốc đối chứng dùng trong thử tương đương sinh học (BM.ĐK.27.01/04).
- Lãnh đạo phòng phụ trách xem xét dự thảo quyết định:
+ Trường hợp đồng ý với dự thảo Quyết định: LĐP ký tắt dự thảo Quyết định để trình LĐC xem xét, phê duyệt.
+ Trường hợp chưa đồng ý với dự thảo quyết định: LĐP chuyển lại cho CVĐM phối hợp với CVPT thực hiện chỉnh sửa, bổ sung theo nội dung chỉ đạo, ký tắt, trình LĐ Phòng ký tắt để trình LĐ Cục xem xét, phê duyệt.
- Lãnh đạo Cục xem xét dự thảo quyết định:
+ Trường hợp đồng ý với dự thảo quyết định: Lãnh đạo Cục ký quyết định công bố.
+ Trường hợp Lãnh đạo Cục yêu cầu sửa, bổ sung nội dung của dự thảo quyết định, Lãnh đạo Cục ghi rõ ý kiến trong dự thảo, Lãnh đạo Phòng phải báo cáo và trình lại Lãnh đạo Cục nội dung tham mưu, đề xuất giải quyết.
7.2.10. Ban hành quyết định, đăng tải trên website:
Thời gian thực hiện: 01 ngày làm việc kể từ khi Lãnh đạo Cục ký Quyết định.
Người thực hiện: Văn thư Cục
Sau khi Lãnh đạo Cục ký Quyết định, Văn thư Cục cấp số Quyết định ban hành và cập nhật Quyết định lên Trang thông tin điện tử của Cục Quản lý Dược tối đa 01 ngày làm việc sau khi có Quyết định được ban hành.
8. HỒ SƠ:
- Văn bản đề nghị lựa chọn thuốc đối chứng.
- Biên bản lựa chọn thuốc đối chứng.
- Biên bản họp Hội đồng
9. BIỂU MẪU
- BM.ĐK.27.01/01: Mẫu Danh mục thuốc cần lựa chọn thuốc đối chứng
- BM.ĐK.27.01/02: Mẫu Biên bản lựa chọn thuốc đối chứng
- BM.ĐK.27.01/03: Danh mục thuốc đối chứng dùng trong thử tương đương sinh học trình Hội đồng xin ý kiến.
- BM.ĐK.27.01/04: Quyết định công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học.
BM.ĐK.27.01/01
DANH MỤC THUỐC CẦN LỰA CHỌN THUỐC ĐỐI CHỨNG DÙNG TRONG THỬ
TƯƠNG ĐƯƠNG SINH HỌC
| STT | Hoạt chất | Hàm lượng | Dạng bào chế |
| 1 |
|
|
|
| 2 |
|
|
|
| ... |
|
|
|
| Ngày.. .tháng... năm... | Ngày.. .tháng... năm... |
BM.ĐK.27.01/02
BIÊN BẢN LỰA CHỌN THUỐC ĐỐI CHỨNG DÙNG TRONG NGHIÊN CỨU TƯƠNG
ĐƯƠNG SINH HỌC
I. Thông tin thuốc thử cần lựa chọn thuốc đối chứng:
1. Thành phần hoạt chất và hàm lượng:
2. Dạng bào chế: (ghi rõ dạng bào chế kèm phân loại giải phóng ngay/giải phóng biến đổi)
II. Thông tin thuốc đối chứng(a):
| STT | Nội dung rà soát (b) | Có(c) | Không có/ không tra cứu được | Cơ sở dữ liệu rà soát | Căn cứ pháp lý |
| 1 | Thuốc thuộc danh mục thuốc biệt dược gốc đã được Bộ Y tế công bố |
|
| Danh mục thuốc được BYT (Cục QLD) công bố BDG, cụ thể:... | Điểm a khoản 1 Điều 6 Thông tư 07/2022/ TT-BYT |
| 2 | Thuốc được cấp GĐKLH có đầy đủ dữ liệu lâm sàng theo quy định |
|
| Danh mục thuốc được BYT cấp GĐKLH có HS lâm sàng (Tra cứu Danh mục do Phòng Đăng ký thuốc tổng hợp), cụ thể:... | Điểm a khoản 1 Điều 6 Thông tư 07/2022/TT-BYT |
| 3 | Thuốc phát minh được một trong các cơ quan quản lý dược chặt chẽ quy định tại khoản 9 Điều 2 Thông tư 08/2022/TT-BYT (SRA) phê duyệt và đang lưu hành tại thị trường quốc gia này |
|
| Tham khảo tra cứu tại website của các cơ quan quản lý SRA (nếu có) | Điểm b khoản 1 Điều 6 Thông tư 07/2022/TT-BYT |
| 4 | Thuốc được một trong các cơ quan quản lý dược chặt chẽ quy định tại khoản 9 Điều 2 Thông tư 08/2022/TT-BYT (SRA) phê duyệt và đang lưu hành tại thị trường quốc gia này (Ưu tiên lựa chọn thuốc có GĐKLH còn hiệu lực tại VN) |
|
| - Tham khảo tra cứu tại website của các cơ quan quản lý SRA (nếu có) - Tra cứu dịch vụ công dữ liệu cấp GĐKLH tại Việt Nam | Điểm c khoản 1 Điều 6 Thông tư 07/2022/TT-BYT |
| 5 | Thuốc đã được tiền thẩm định (prequalified) bởi Tổ chức Y tế thế giới (Ưu tiên lựa chọn thuốc thuốc có GĐKLH còn hiệu lực tại VN) |
|
| https://extranet.who. int/pqweb/medicines /finished- pharmaceutical- products/prequalified | Điểm c khoản 1 Điều 6 Thông tư 07/2022/TT-BYT |
Ghi chú:
(a) : Căn cứ thành phần hoạt chất, dạng bào chế của thuốc thử, lựa chọn thuốc đối chứng theo quy định tại khoản 2 Điều 6 Thông tư 07.
(b) : Thứ tự ưu tiên sẽ áp dụng từ tiêu chí 1 đến tiêu chí 5. Nếu có 1 tiêu chí đáp ứng sẽ không cần rà soát các tiêu chí còn lại.
(c) Nếu có ghi rõ thông tin thuốc tra cứu được bao gồm (tên thuốc, hoạt chất, hàm lượng, dạng bào chế, cơ sở sản xuất, nước sản xuất, nước cấp phép lưu hành)
Kết luận: Thuốc:........................ (SĐK:........................ ), hoạt chất:........................ hàm lượng:............... , dạng bào chế: ………………, cơ sở sản xuất: ......................nước sản xuất: ...................., nước cấp phép lưu hành: .................. đáp ứng tiêu chí số thứ tự được lựa chọn làm thuốc đối chứng trong nghiên cứu tương đương sinh học của thuốc generic chứa hoạt chất: ……………. , hàm lượng: …….. , dạng bào chế: .................
| Ngày rà soát | Chuyên viên đầu mối/Chuyên gia thẩm định | Chữ ký |
|
|
|
|
|
|
|
|
|
|
|
|
III. Xử lý của Phòng Đăng ký thuốc:
1. Chuyên viên phụ trách (trường hợp thuốc đối chứng đã được cấp GĐKLH tại Việt Nam):
- Hiệu lực GĐKLH thuốc đối chứng được lựa chọn: ....................................................
- Thông tin thuốc đối chứng đúng với thông tin đã được phê duyệt trong hồ sơ đăng ký thuốc □
- Ý kiến khác □
Ghi rõ ý kiến khác: .........................................................................................................
Ngày rà soát: Chữ ký:
2. Lãnh đạo Phòng kết luận:
Trình Hội đồng công bố thuốc đối chứng □ Ý kiến khác □
Ghi rõ ý kiến khác: ..........................................................................................................
Ngày rà soát: Chữ ký:
BM.ĐK.27.01/03
DANH MỤC THUỐC ĐỐI CHỨNG DÙNG TRONG THỬ TƯƠNG ĐƯƠNG SINH HỌC
TRÌNH HỘI ĐỒNG XIN Ý KIẾN (ĐỢT...)
| STT | Hoạt chất | Hàm lượng | Dạng bào chế | Tên thuốc | Số đăng ký | Cơ sở sản xuất | Nước sản xuất/Nước cấp phép lưu hành | Nội dung xin ý kiến (Nội dung báo cáo, đề xuất, ghi rõ căn cứ pháp lý đề xuất) |
| 1 |
|
|
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
|
|
| … |
|
|
|
|
|
|
|
|
| Ngày...tháng... năm... | Ngày.. .tháng... năm... | Ngày.. .tháng... năm... |
BM.ĐK.27.01/04
| BỘ Y TẾ | CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
| Số: /QĐ-QLD | Hà Nội, ngày tháng năm |
QUYẾT ĐỊNH
Về việc công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học -
Đợt…..
______________________________
CỤC TRƯỞNG CỤC QUẢN LÝ DƯỢC
Căn cứ Luật Dược số 105/2016/QH13 ngày 06/04/2016;
Căn cứ Nghị định 54/2017/NĐ-CP ngày 08/05/2017 của Chính phủ quy định chi tiết một số điều về biện pháp thi hành Luật Dược;
Căn cứ Nghị định số 155/2018/NĐ-CP ngày 12/11/2018 của Chính phủ sửa đổi một số quy định liên quan đến điều kiện đầu tư kinh doanh thuộc phạm vi quản lý nhà nước của Bộ Y tế;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20/6/2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Căn cứ Thông tư số 07/2022/TT-BYT ngày 05/9/2022 của Bộ trưởng Bộ Y tế quy định thuốc phải thử tương đương sinh học và các yêu cầu đối với hồ sơ báo cáo số liệu nghiên cứu tương đương sinh học trong đăng ký lưu hành thuốc tại Việt Nam;
Căn cứ Quyết định số 1969/QĐ-BYT ngày 26/4/2023 của Bộ trưởng Bộ Y tế quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Cục Quản lý Dược thuộc Bộ Y tế;
Căn cứ kết luận của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc... đợt... họp ngày...;
Theo đề nghị của Trưởng phòng Phòng Đăng ký thuốc - Cục Quản lý Dược.
QUYẾT ĐỊNH:
Điều 1. Công bố Danh mục thuốc đối chứng dùng trong thử tương đương sinh học - Đợt... gồm ...thuốc tại Phụ lục kèm theo Quyết định này.
Điều 2. Quyết định này có hiệu lực kể từ ngày ký ban hành.
Điều 3. Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Giám đốc cơ sở sản xuất và cơ sở đăng ký có thuốc nêu tại Điều 1 chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: | CỤC TRƯỞNG |
Phụ lục
DANH MỤC ...THUỐC ĐỐI CHỨNG DÙNG TRONG THỬ TƯƠNG ĐƯƠNG SINH HỌC
(ĐỢT...)
(Kèm theo Quyết định số .../QĐ-QLD ngày../../… của Cục Quản lý Dược)
______________________________________________
| STT | Tên thuốc | Hoạt chất, Hàm lượng/Nồng độ | Dạng bào chế | Số đăng ký | Cơ sở sản xuất | Nước sản xuất |
| 1 |
|
|
|
|
|
|
| 2 |
|
|
|
|
|
|
| … |
|
|
|
|
|
|
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Quyết định 344/QĐ-QLD PDF (Bản có dấu đỏ)
Quyết định 344/QĐ-QLD PDF (Bản có dấu đỏ) Quyết định 344/QĐ-QLD DOC (Bản Word)
Quyết định 344/QĐ-QLD DOC (Bản Word)

