Bản án số 44/2023/KDTM-PT ngày 24/05/2023 của TAND cấp cao tại TP.HCM về tranh chấp về quyền sở hữu trí tuệ
- Thuộc tính
- Nội dung
- VB gốc
- VB liên quan
- Lược đồ
- Đính chính
- Án lệ
- BA/QĐ cùng nội dung
- Tải về
Tải văn bản
-
Bản án số 44/2023/KDTM-PT
Quý khách vui lòng Đăng nhập tài khoản để tải file. Nếu chưa có tài khoản, Quý khách vui lòng đăng ký tại đây!
Báo lỗi
Thuộc tính Bản án 44/2023/KDTM-PT
| Tên Bản án: | Bản án số 44/2023/KDTM-PT ngày 24/05/2023 của TAND cấp cao tại TP.HCM về tranh chấp về quyền sở hữu trí tuệ |
|---|---|
| Quan hệ pháp luật: | Tranh chấp về quyền sở hữu trí tuệ |
| Cấp xét xử: | Phúc thẩm |
| Tòa án xét xử: | TAND cấp cao tại TP.HCM |
| Số hiệu: | 44/2023/KDTM-PT |
| Loại văn bản: | Bản án |
| Ngày ban hành: | 24/05/2023 |
| Lĩnh vực: | Kinh doanh thương mại |
| Áp dụng án lệ: |
Đã biết
Quý khách vui lòng Đăng nhập tài khoản để xem áp dụng án lệ. Nếu chưa có tài khoản, Quý khách vui lòng đăng ký tại đây! |
| Đính chính: |
Đã biết
Quý khách vui lòng Đăng nhập tài khoản để xem đính chính. Nếu chưa có tài khoản, Quý khách vui lòng đăng ký tại đây! |
| Thông tin về vụ/việc: | giữ nguyên bản án sơ thẩm |
Tóm tắt Bản án
Nội dung tóm tắt đang được cập nhật, Quý khách vui lòng quay lại sau!
Tải văn bản

TÒA ÁN NHÂN DÂN CẤP CAO
TẠI THÀNH PHỐ HỒ CHÍ MINH
—————————
Bản án số: 44/2023/KDTM-PT
Ngày: 24 - 5 - 2023
V/v: “Tranh chấp về quyền sở hữu trí
tuệ”.
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập – Tự do – Hạnh phúc
NHÂN DANH
NƯỚC CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
TÒA ÁN NHÂN DÂN CẤP CAO TẠI THÀNH PHỐ HỒ CHÍ MINH
- Thành phần Hội đồng xét xử phúc thẩm gồm có:
Thẩm phán - Chủ tọa phiên tòa: Bà Phạm Thị Duyên
Các Thẩm phán: Bà Huỳnh Thanh Duyên
Ông Hà Huy Cầu
- Thư ký phiên tòa: Bà Trần Thị Kim Yến – Thư ký Tòa án nhân dân cấp
cao tại Thành phố Hồ Chí Minh.
- Đại diện Viện kiểm sát nhân dân cấp cao tại Thành phố Hồ Chí Minh
tham gia phiên tòa: Ông Đặng Quốc Việt – Kiểm sát viên.
Ngày 24 tháng 5 năm 2023, tại trụ sở Tòa án nhân dân cấp cao tại Thành
phố Hồ Chí Minh mở phiên tòa xét xử phúc thẩm công khai vụ án kinh doanh
thương mại thụ lý số: 86/2022/TLPT-KDTM ngày 26 tháng 12 năm 2022 về
việc “Tranh chấp về quyền sở hữu trí tuệ”.
Do bản án kinh doanh thương mại sơ thẩm số: 13/2022/KDTM-ST ngày
07 tháng 9 năm 2022 của Tòa án nhân dân tỉnh Bình Dương bị kháng cáo.
Theo Quyết định đưa vụ án ra xét xử phúc thẩm số: 651/2023/QĐ-PT
ngày 27 tháng 3 năm 2023 giữa các đương sự:
- Nguyên đơn: L;
Địa chỉ: Cộng hòa Pháp.
Người đại diện theo ủy quyền: Ông Mai Duy L1, sinh năm 1985 (có mặt)
Địa chỉ : Phòng số 5, Tầng 15, Tòa nhà H, số 4A L, phường T, quận B,
thành phố Hà Nội.
Người đại diện ủy quyền lại:
1/Ông Bạch Hoàng G, sinh năm 1990 (có mặt);
Địa chỉ: Tầng 9, Tòa nhà Văn phòng Tổng Công ty 789, số 147 đường H,
phường N, quận C, thành phố Hà Nội.
2
2/Bà Nguyễn Thị Anh T1, sinh năm 1984 (vắng mặt);
Địa chỉ: Tầng 9, Tòa nhà Văn phòng Tổng Công ty 789, số 147 đường H,
phường N, quận C, thành phố Hà Nội.
- Bị đơn: Công ty Cổ phần Dược phẩm Đ;
Địa chỉ: Lô M7A, đường D17, Khu công nghiệp M, phường T, thị xã B,
tỉnh Bình Dương.
Người đại diện theo ủy quyền của bị đơn:
1/Ông Vũ Tuấn L2 (có mặt);
Địa chỉ liên lạc: Công ty Cổ phần Dược phẩm Đ; địa chỉ: Lô M7A, đường
D17, Khu công nghiệp M, phường T, thị xã B, tỉnh Bình Dương.
2/Bà Từ Thị Hồng H3 (vắng mặt);
Địa chỉ: Tầng 5M Tòa nhà H, số 1 N, phường N, quận T, thành phố Hà
Nội.
Người bảo vệ quyền và lợi ích hợp pháp của bị đơn:
1/Luật sư Phan Thị Lam H3 – Đoàn luật sư thành phố Hà Nội (vắng mặt).
2/Luật sư Nhâm Mạnh H4 – Đoàn luật sư thành phố Hà Nội (có mặt).
- Người kháng cáo: Bị đơn Công ty Cổ phần Dược phẩm Đ.
NỘI DUNG VỤ ÁN:
* Theo đơn khởi kiện, quá trình tố tụng và tại phiên tòa sơ thẩm, người
đại diện hợp pháp của nguyên đơn L trình bày:
Nguyên đơn L (sau đây viết tắt là S) yêu cầu Tòa án nhân dân tỉnh Bình
Dương giải quyết các vấn đề sau:
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ chấm dứt hành vi xâm
phạm quyền sáng chế được bảo hộ theo Điểm 1 của Yêu cầu bảo hộ, bao gồm
nhưng không giới hạn ở hành vi sản xuất, nhập khẩu, khai thác công dụng, lưu
thông, buôn bán, vận chuyển, quảng cáo, chào hàng và tàng trữ để lưu thông sản
phẩm xâm phạm Bằng độc quyền sáng chế số 7181 của nguyên đơn, bao gồm
nhưng không giới hạn bởi các sản phẩm thuốc Nisten (Ivabradine 5mg) và
Nisten - F (Ivabradine 7.5mg).
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ thu hồi toàn bộ các sản
phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) đã phân
phối trên thị trường; đồng thời tiêu hủy toàn bộ sản phẩm thuốc Nisten
(Ivabradine 5mg), Nisten - F (Ivabradine 7.5mg) đã thu hồi cũng như còn tồn
kho và các nguyên, vật liệu được sử dụng để sản xuất hoặc kinh doanh các sản
phẩm xâm phạm Bằng độc quyền sáng chế số 7181.
3
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ tiến hành thủ tục rút số
đăng ký VD-20362-13 đối với sản phẩm thuốc Nisten (Ivabradine 5mg) và số
đăng ký VD-21061-14 đối với sản phẩm thuốc Nisten - F (Ivabradine 7.5mg) tại
Cục quản lý Dược - Bộ Y tế.
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ bồi thường thiệt hại cho
nguyên đơn số tiền 500.000.000 đồng theo điểm c khoản 1 Điều 205 Luật Sở
hữu trí tuệ.
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ thanh toán chi phí hợp lý
trị giá 300.000.000 đồng mà nguyên đơn bỏ ra để thuê Luật sư bảo vệ quyền và
lợi ích hợp pháp cho nguyên đơn nhằm chống lại hành vi xâm phạm.
- Buộc bị đơn Công ty Cổ phần Dược phẩm Đ phải xin lỗi nguyên đơn và
cải chính công khai trên tạp chí Dược và Mỹ phẩm; tạp chí Khoa học và Đời
sống và Báo Thanh niên trong 03 kỳ liên tiếp về các hành vi xâm phạm quyền
đối với sáng chế.
Lý do:
- Thứ nhất: Bằng độc quyền sáng chế số 7181 của nguyên đơn đã và đang
có hiệu lực:
Nguyên đơn là chủ sở hữu Bằng độc quyền sáng chế số 7181, là một trong
những tập đoàn dược phẩm hàng đầu thế giới. Với vị trí như vậy, S luôn chú
trọng đến công tác nghiên cứu phát triển và hiện đang sở hữu rất nhiều bằng độc
quyền sáng chế trên toàn cầu.
Ivabradin Hydroclorua (tên quốc tế (INN) là Ivabradine Hydrochloride)
và các đối tượng liên quan đã được bảo hộ độc quyền sáng chế là một trong số
những sáng chế quan trọng nhất của S. Ivabradin là chất làm giảm chuyên biệt
nhịp tim. Tác dụng trên tim của thuốc là đặc hiệu với nút xoang mà không ảnh
hưởng tới thời gian dẫn truyền trong nhĩ, trong nhĩ-thất, sự tái cực thất hoặc co
cơ tim.
Tại Việt Nam, S là chủ sở hữu của nhiều quyền sở hữu trí tuệ liên quan
đến hợp chất Ivabradin Hydroclorua, bao gồm nhưng không giới hạn bởi Bằng
độc quyền sáng chế số 7181. Bằng độc quyền sáng chế số 7181 có thời hạn bảo
hộ đến hết ngày 15 tháng 02 năm 2026, bảo hộ bao gồm nhưng không giới hạn
cho các đối tượng sau đây: Hợp chất Ivabradin Hydroclorua dạng tinh thể
gamma, quy trình điều chế và dược phẩm chứa nó.
Phạm vi bảo hộ của sáng chế được xác định theo 6 điểm yêu cầu bảo hộ,
trong đó có 5 điểm độc lập (Điểm 1, 2, 4, 5, 6) và 1 điểm phụ thuộc (Điểm 3).
Đối tượng được bảo hộ theo Bằng độc quyền sáng chế số 7181 bao gồm nhưng
không giới hạn ở hợp chất Ivabradin Hydroclorua dạng tinh thể gamma, quy
trình điều chế và dược phẩm chứa nó.
Theo quy định của pháp luật, S có độc quyền sử dụng và ngăn cấm người
khác sử dụng các sáng chế đang được bảo hộ (Khoản 1 Điều 125 Luật Sở hữu trí
4
tuệ). Phạm vi quyền ngăn cấm người khác sử dụng sáng chế được quy định rõ
tại khoản 1 Điều 124 Luật Sở hữu trí tuệ, theo đó sử dụng sáng chế bao gồm
nhưng không giới hạn bởi việc sản xuất, nhập khẩu, khai thác công dụng, lưu
thông, bán, vận chuyển, quảng cáo, chào hàng, tàng trữ để lưu thông sản phẩm
được bảo hộ hoặc sản phẩm được sản xuất theo quy trình được bảo hộ.
Chiếu theo các quy định pháp luật nêu trên, mọi hành vi sử dụng sáng chế
đang được bảo hộ của S mà không được phép của S với tư cách là chủ sở hữu
được coi là hành vi xâm phạm quyền đối với các sáng chế đang được bảo hộ
(khoản 1 Điều 126 Luật Sở hữu trí tuệ).
- Thứ 2: Bị đơn phải chấm dứt hành vi xâm phạm quyền đối với Bằng độc
quyền sáng chế số 7181 (yêu cầu khởi kiện số 1):
+ Hành vi xâm phạm quyền đối với sáng chế:
Nguyên đơn là chủ sở hữu của Bằng độc quyền sáng chế số 7181. Do đó,
nguyên đơn được độc quyền sử dụng sáng chế, ngăn cấm người khác sử dụng
sáng chế và định đoạt đối với sáng chế.
Trong vụ việc này, trong khi chưa được sự cho phép của nguyên đơn, bị
đơn đã tiến hành sản xuất, lưu thông, buôn bán, vận chuyển, quảng cáo, chào
hàng, và tàng trữ để lưu thông sản phẩm thuốc Nisten (Ivabradine 5mg) và
Nisten - F (Ivabradine 7.5mg) có chứa hoạt chất Ivabradin Hydroclorua dạng
tinh thể gamma được bảo hộ theo Bằng độc quyền sáng chế số 7181. Theo quy
định tại khoản 1 Điều 124 Luật Sở hữu trí tuệ, các hành vi nêu trên của bị đơn là
hành vi sử dụng sáng chế.
Sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) có chứa hoạt chất Ivabradine cùng tên gọi, trùng công thức cấu tạo với
hoạt chất Ivabradin Hydroclorua dạng tinh thể gamma được bảo hộ của Bằng
độc quyền sáng chế số 7181. Thông qua phân tích bột nhiễu xạ tia X và ý kiến
chuyên môn của GS.TS Gerard Coquerel tại Đại học Rouen, Pháp thì sản phẩm
thuốc Nisten (Ivabradine 5mg) chứa hoạt chất Ivabradine có cấu tạo hóa học
trùng với cấu tạo hóa học của hợp chất được bảo hộ theo Điểm 1 của Bằng độc
quyền sáng chế số 7181. Ngoài ra, hoạt chất trong sản phẩm thuốc Nisten
(Ivabradine 5mg) cũng là dạng tinh thể gamma trùng với dạng tinh thế của hoạt
chất Ivabradine được bảo hộ theo Điểm 1 của Bằng độc quyền sáng chế số 7181.
Bên cạnh đó, theo ghi nhận trong phần Chỉ định của Tờ hướng dẫn sử
dụng thuốc thì sản phẩm thuốc Nisten được dùng để điều trị chứng đau thắt ngực
ổn định mãn tính. Như vậy, sản phẩm thuốc Nisten có chung mục đích sử dụng
với sáng chế đang được bảo hộ tại Bằng độc quyền sáng chế số 7181 vì đều là
sản phẩm được dùng để điều trị/phòng ngừa các triệu chứng của bệnh tim mạch.
Trong vụ việc này, bị đơn cho rằng sản phẩm thuốc Nisten có chứa hoạt
chất Ivabradin Hydroclorua dưới dạng bột vô định hình là không chính xác. Trên
thực tế, hoạt chất Ivabradin Hydroclorua trong thuốc Nisten là dạng tinh thể
gamma, trùng với sáng chế đang được bảo hộ tại điểm 1 Yêu cầu bảo hộ của
5
Bằng độc quyền sáng chế số 7181. Phòng thí nghiệm của Đại học Rouen, một
trong những phòng thí nghiệm thuốc hàng đầu thế giới, đạt tiêu chuẩn chứng
nhận Châu Âu và được phê chuẩn mã số EA 3233 bởi Bộ Nghiên cứu của Pháp,
đã thực hiện kiểm nghiệm thuốc Nisten do bị đơn sản xuất. Phòng thí nghiệm đã
sử dụng phương pháp nhiễu xạ tia X, một phương pháp hiện đại bậc nhất hiện
nay, để xác định rằng hoạt chất Ivabradin Hydroclorua trong thuốc Nisten là ở
dạng tinh thể gamma chứ không phải là dạng vô định hình. Do đó, sản phẩm
thuốc Nisten là yếu tố xâm phạm quyền đối với Bằng độc quyền sáng chế số
7181. Ngoài ra, S xin lưu ý bị đơn đưa ra nhận định rằng sản phẩm thuốc Nisten
có chứa hoạt chất Ivabradin Hydroclorua dưới dạng bột vô định hình mà không
hề đưa ra bất cứ bằng chứng xác đáng nào chứng minh cho vấn đề này. Do đó,
nhận định của bị đơn là hoàn toàn vô căn cứ.
Ngày 26/9/2016, Viện Khoa học Sở hữu trí tuệ Việt Nam đã ra Kết luận
giám định số SC015-16YC/KLGĐ với nội dung khẳng định sản phẩm thuốc
Nisten là yếu tố xâm phạm quyền đối với sáng chế đang được bảo hộ tại Yêu
cầu bảo hộ số 1 của Bằng độc quyền sáng chế số 7181.
Theo quy định tại điểm a khoản 1 Điều 8 Nghị định số 105/2006/NĐ-CP
của Chính phủ, khoản 1 Điều 16 Nghị định số 103/2006/NĐ-CP ngày 22/9/2006
của Chính phủ, Điều 11 Thông tư số 11/2015/TT-BKHCN ngày 26/6/2015 thì
sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) bị
coi là yếu tố xâm phạm quyền đối với Bằng độc quyền sáng chế số 7181 của
nguyên đơn.
Do đó, hành vi sản xuất, lưu thông, bán, quảng cáo, tàng trữ để lưu thông
sản phẩm thuốc nêu trên của bị đơn là hành vi xâm phạm quyền đối với sáng chế
đang được bảo hộ của nguyên đơn theo quy định tại khoản 1 Điều 126 Luật Sở
hữu trí tuệ. Căn cứ theo khoản 1 Điều 202 Luật Sở hữu trí tuệ, bị đơn phải chấm
dứt các hành vi xâm phạm quyền đối với sáng chế, bao gồm nhưng không giới
hạn bởi hành vi sản xuất và phân phối sản phẩm thuốc Nisten - F và Nisten.
+ Việc được cấp số đăng ký lưu hành không có nghĩa sản phẩm Nisten
không xâm phạm quyền sở hữu trí tuệ đối với Bằng độc quyền sang chế số
7181:
Quy định của pháp luật về vấn đề đã nêu rất rõ ràng, theo đó cơ sở đăng
ký thuốc chịu trách nhiệm về các vấn đề liên quan đến sở hữu trí tuệ của thuốc
đăng ký lưu hành. Cục Quản lý Dược không chịu trách nhiệm về vấn đề sở hữu
trí tuệ khi thực hiện việc đăng ký lưu hành thuốc.
Cụ thể, Điều 14 Thông tư số 22/2009/TT-BYT (“Thông tư 22”), là thông
tư có hiệu lực tại thời điểm đăng ký lưu hành thuốc Nisten, quy định rằng:
“Điều 14. Nguyên tắc chung
1. Cơ sở đăng ký thuốc chịu trách nhiệm về các vấn đề liên quan đến sở
hữu trí tuệ của thuốc đăng ký lưu hành.
6
2. Bộ Y tế khuyến khích các cơ sở đăng ký thuốc xác lập các quyền về sở
hữu trí tuệ hoặc tiến hành tra cứu các đối tượng sở hữu trí tuệ có liên quan
trước khi đăng ký lưu hành thuốc tại Việt Nam.
3. Trường hợp có tranh chấp về sở hữu trí tuệ trong khi xem xét cấp số
đăng ký, bên phản đối việc cấp số đăng ký cho thuốc có tranh chấp về sở hữu trí
tuệ phải cung cấp kết luận của cơ quan quản lý nhà nước về sở hữu trí tuệ hoặc
cơ quan có chức năng thực thi quyền sở hữu trí tuệ về hành vi xâm phạm. Bộ Y
tế sẽ từ chối cấp số đăng ký lưu hành cho thuốc đó nếu có đủ cơ sở để khẳng
định thuốc khi được cấp số đăng ký lưu hành sẽ xâm phạm quyền sở hữu trí tuệ
của cá nhân, cơ sở khác đang được bảo hộ.
4. Trường hợp có tranh chấp về sở hữu trí tuệ sau khi đã cấp số đăng ký
lưu hành, trên cơ sở xem xét đề nghị của chủ thể quyền sở hữu trí tuệ hoặc bên
thứ ba có lợi ích liên quan và căn cứ vào phán quyết của Tòa án hoặc kết luận
cuối cùng của cơ quan quản lý nhà nước về sở hữu trí tuệ hoặc cơ quan chức
năng thực thi quyền sở hữu trí tuệ về hành vi xâm phạm, Bộ Y tế sẽ quyết định
đình chỉ hoặc rút số đăng ký lưu hành đối với thuốc bị kết luận là xâm phạm
quyền sở hữu trí tuệ.”.
Điều 13 Thông tư số 44/2014/TT-BYT, là thông tư thay thế Thông tư 22,
cũng có quy định tương tự như quy định nêu trên của Thông tư 22.
Như vậy, khi nộp hồ sơ xin đăng ký lưu hành thuốc, chủ thể đăng ký phải
tự chịu trách nhiệm về các vấn đề liên quan đến sở hữu trí tuệ cả trong quá trình
đăng ký lẫn sau khi sản phẩm thuốc đã được cấp số đăng ký lưu hành. Cục Quản
lý Dược chỉ giải quyết hậu quả của vụ việc xâm phạm sở hữu trí tuệ đối với sản
phẩm thuốc tùy theo từng tình huống cụ thể khi có quyết định, kết luận của cơ
quan có thẩm quyền về sở hữu trí tuệ (Tòa án hoặc Thanh tra Khoa học và Công
nghệ). Trong những trường hợp này, hồ sơ xin đăng ký thuốc có thể bị từ chối
cấp số lưu hành hoặc giấy phép lưu hành thuốc đang tồn tại có thể bị đình chỉ
hoặc rút số đăng ký.
Pháp luật sở hữu trí tuệ là pháp luật chuyên ngành nên về nguyên tắc phải
áp dụng các quy định của pháp luật sở hữu trí tuệ để giải quyết các tranh chấp
liên quan đến sở hữu trí tuệ. Điều 5 Luật Sở hữu trí tuệ 2005, sửa đổi bổ sung
năm 2009 cũng quy định rằng: “trong trường hợp có sự khác nhau giữa quy
định về sở hữu trí tuệ của Luật này với quy định của luật khác thì áp dụng quy
định của Luật này”.
Theo Điều 2 Luật Sở hữu trí tuệ thì Luật Sở hữu trí tuệ áp dụng cho mọi
tổ chức, cá nhân Việt Nam cũng như tổ chức, cá nhân nước ngoài. Pháp luật sở
hữu trí tuệ, cụ thể là Điều 9 Luật Sở hữu trí tuệ, yêu cầu các cá nhân và tổ chức
có trách nhiệm tôn trọng quyền sở hữu trí tuệ của tổ chức, cá nhân khác. Như
vậy, mọi cá nhân, tổ chức, bao gồm cả bị đơn trong vụ án này là Công ty Đ phải
có nghĩa vụ tôn trọng quyền sở hữu trí tuệ nói chung và quyền đối với sáng chế
được bảo hộ tại Bằng độc quyền sáng chế số 7181 của S nói riêng.
7
Căn cứ theo Điều 14 Thông tư số 22, Công ty Đ phải tự chịu hoàn toàn
trách nhiệm về các vấn đề liên quan đến sở hữu trí tuệ. Cho đến hiện nay, Bằng
độc quyền sáng chế số 7181 vẫn đang có hiệu lực trên toàn lãnh thổ Việt Nam.
Do đó, việc được Cục Quản lý Dược cấp số đăng ký lưu hành thuốc chỉ liên
quan đến việc phê duyệt, cấp phép của cơ quan chức năng về tính an toàn, hiệu
quả của sản phẩm mà không, trong bất kỳ trường hợp nào, bao gồm cả các khía
cạnh về sở hữu trí tuệ của sản phẩm nói chung và của thuốc Nisten của Công ty
Đ nói riêng.
- Thứ ba: Bị đơn phải thu hồi và tiêu hủy toàn bộ các sản phẩm thuốc
Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) được thu hồi và còn
tồn; tiêu hủy các nguyên liệu, vật liệu cũng như các và các phương tiện chính
được sử dụng để sản xuất và/hoặc kinh doanh các sản phẩm xâm phạm Bằng
độc quyền sáng chế số 7181 (liên quan đến yêu cầu khởi kiện số 2):
Căn cứ theo khoản 5 Điều 202 của Luật Sở hữu trí tuệ và các khoản 1
Điều 29 và Điều 31 Nghị định số 105, toàn bộ sản phẩm thuốc toàn bộ sản phẩm
thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg), các nguyên
liệu, vật liệu và các phương tiện chính khác để sản xuất và kinh doanh sản phẩm
thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg), bao gồm
nhưng không giới hạn bởi nguyên liệu thuốc, màng nhôm, vỉ thuốc, hướng dẫn
sử dụng, hộp thuốc, tài liệu kinh doanh, đều phải được tiêu hủy dưới sự chứng
kiến của nguyên đơn cũng như các cơ quan chức năng có thẩm quyền.
- Thứ 4: Bị đơn phải rút số đăng ký các sản phẩm thuốc Nisten
(Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) tại Cục Quản lý Dược (liên
quan đến yêu cầu khởi kiện số 3):
Căn cứ theo Quyết định số 414/QĐ-QLD ngày 27/12/2013 và Quyết định
số 296/QĐ-QLD ngày 12/06/2014 của Cục trưởng Cục quản lý Dược thì bị đơn
đã đăng ký sản phẩm thuốc Nisten (Ivabradine 5mg) theo số đăng ký VD-
20362-13 và số đăng ký VD-21061-14 đối với sản phẩm thuốc Nisten - F
(Ivabradine 7.5mg) với Cục Quản lý Dược.
Căn cứ theo quy định tại các Điều 13.4, 32.6, 33.2 Thông tư số
44/2014/TT-BYT ngày 25/11/2014, để bảo vệ quyền và lợi ích hợp pháp của
nguyên đơn, nguyên đơn yêu cầu bị đơn rút hoặc hủy bỏ hai đăng ký thuốc nêu
trên do hai sản phẩm này là yếu tố xâm phạm quyền sở hữu trí tuệ. Bên cạnh đó,
nguyên đơn cũng yêu cầu bị đơn không được đăng ký bất kỳ loại thuốc nào xâm
phạm quyền đối với sáng chế đang được bảo hộ tại Bằng độc quyền sáng chế số
7181 trong thời hạn bảo hộ của sáng chế này.
- Thứ 5: Bị đơn phải bồi thường thiệt hại về vật chất cho nguyên đơn (liên
quan đến yêu cầu khởi kiện số 4):
Hành vi xâm phạm Bằng độc quyền sáng chế số 7181 của bị đơn đã, đang
và sẽ gây ra thiệt hại trong tương lai về vật chất cho nguyên đơn với tư cách là
chủ sở hữu Bằng độc quyền sáng chế số 7181. Các thiệt hại trên bao gồm các
8
tổn thất về tài sản, mức giảm sút về thu nhập và lợi nhuận, tổn thất về cơ hội
kinh doanh cũng như các chi phí khác mà nguyên đơn phải gánh chịu để ngăn
chặn và khắc phục thiệt hại.
Nhìn chung, các thiệt hại của nguyên đơn là không thể định lượng, không
thể khắc phục và không thể bù đắp được. Tuy nhiên, không ảnh hưởng đến yêu
cầu này và cho các mục đích của yêu cầu này, nguyên đơn yêu cầu bị đơn phải
bồi thường thiệt hại cho nguyên đơn, bao gồm các thiệt hại sau:
+ Thiệt hại vật chất gây ra bởi việc sản xuất và phân phối các sản phẩm
thuốc Nisten và Nisten-F ra thị trường;
+ Thiệt hại vật chất mà nguyên đơn đã phải bỏ ra để ngăn chặn các thiệt
hại gây ra bởi hành vi xâm phạm quyền trước khi khởi kiện, bao gồm chi phí để
xử lý vụ việc trước Tòa án nhân dân tỉnh Bình Dương;
+ Thiệt hại vật chất gây ra sẽ là việc giảm sút lợi nhuận và tổn thất về cơ
hội kinh doanh; và
+ Các thiệt hại phát sinh khác, ví dụ như nếu nguyên đơn buộc phải giảm
giá thành các sản phẩm của mình nếu Bị đơn lưu hành các sản phẩm vi phạm.
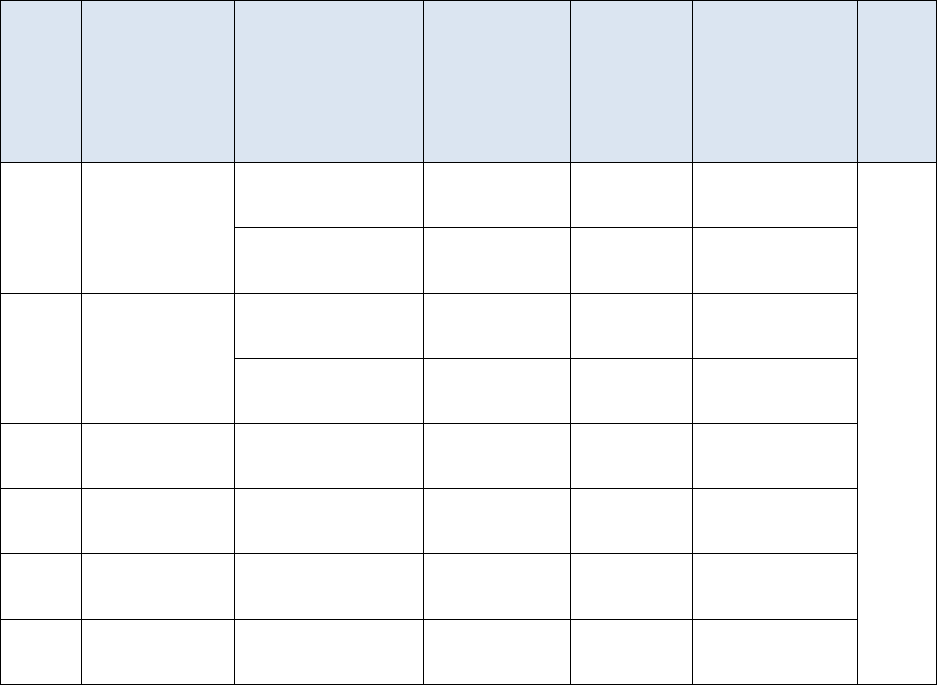
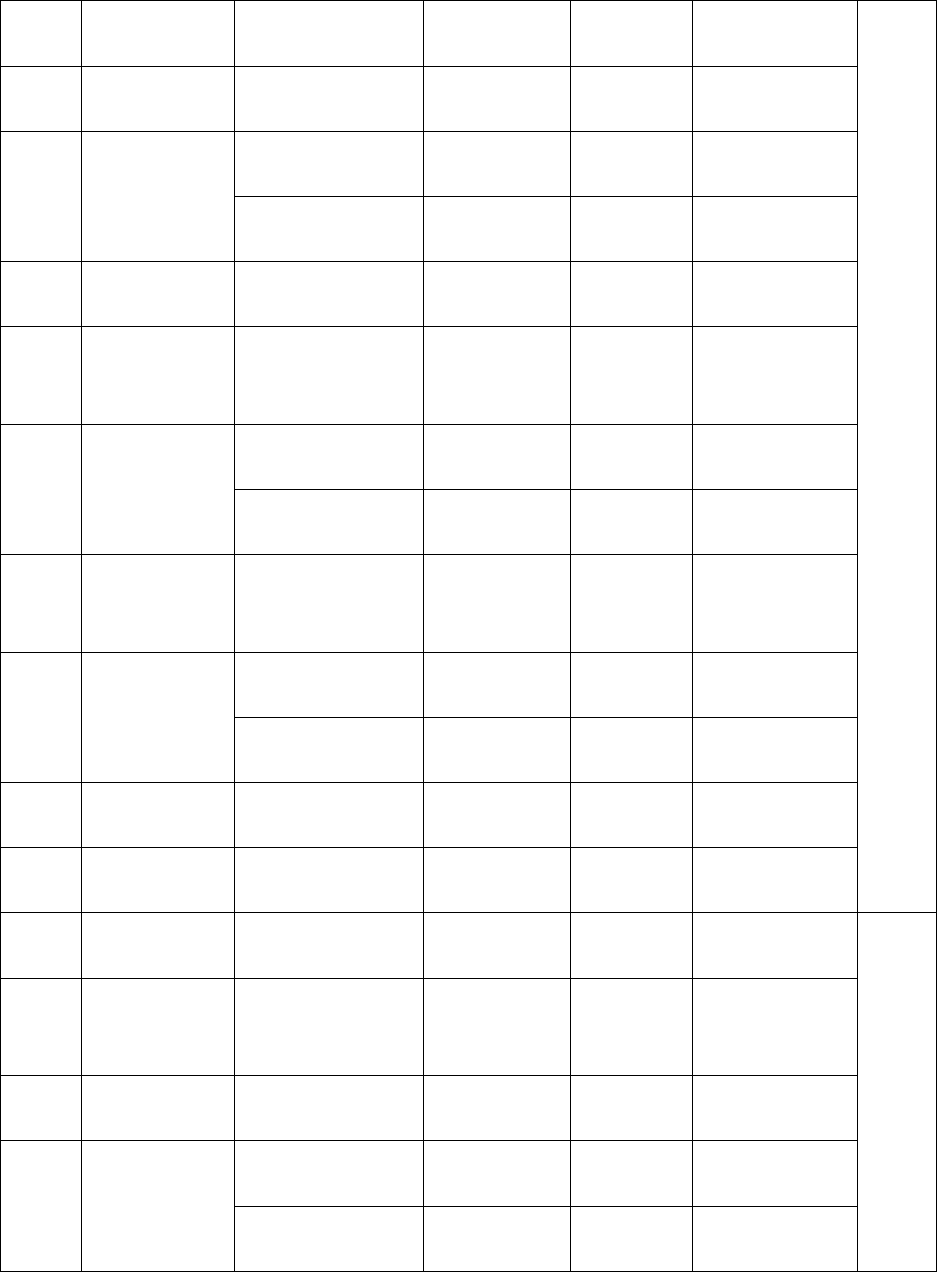
Từ những thông tin công khai trên các website của các Sở Y Tế, nguyên
đơn đã biết được bị đơn đã sản xuất và cung cấp số lượng thuốc Nisten như sau
cho một số Sở Y Tế:
STT
Sở Y Tế
Thuốc
Số lượng
thuốc
Nisten
(viên)
Đơn giá
(Đồng)
Tổng
(Đồng)
Năm
1
Bà Rịa
Vũng Tàu
NISTEN
22000
3149
69.278.000
Năm
2016
NISTEN-F
15000
6290
94.350.000
2
Bình
Phước
NISTEN
15500
3149
48.809.500
NISTEN-F
30500
6290
48.809.500
3
Bắc Ninh
NISTEN
5000
3880
19.400.000
4
Hà Nam
NISTEN
45000
3150
141.750.000
5
Long An
NISTEN
26500
3490
92.485.000
6
Đắc Nông
NISTEN
500
3200
1.600.000
9
NISTEN-F
500
6390
3.195.000
7
Thanh Hóa
NISTEN
7300
3180
23.214.000
8
Sóc Trăng
NISTEN
2000
3149
6.298.000
NISTEN-F
50000
6290
6.298.000
9
Hưng Yên
NISTEN
8000
3150
25.200.000
10
Bình
Dương
NISTEN
10000
3390
33.900.000
11
An Giang
NISTEN
24500
3149
77.150.500
NISTEN-F
3500
6290
22.015.000
12
Ninh
Thuận
NISTEN-F
50000
6290
314.500.000
13
Tiền Giang
NISTEN
55200
3149
173.824.800
NISTEN-F
12000
6290
75.480.000
14
Sơn La
NISTEN-F
21500
7000
150.500.000
15
Đồng Tháp
NISTEN
12000
3149
37.788.000
16
Đắc Lắc
NISTEN
150
3290
493.500
Năm
2017
17
Ninh
Thuận
NISTEN-F
50000
6290
314.500.000
18
Đồng Tháp
NISTEN
12000
3149
37.788.000
19
Hồ Chí
Minh
NISTEN
40950
3145
128.787.750
NISTEN-F
45500
6290
286.195.000
Như vậy, bị đơn đã sản xuất thuốc Nisten vi phạm để cung cấp cho các cơ
sở y tế trong 19 tỉnh thành nêu trên với tổng giá trị là 2.233.609.550 đồng (bằng
chữ: Hai tỷ hai trăm ba mươi ba triệu sáu trăm không chín nghìn năm trăm năm
mươi đồng). Trên đây là những thông tin mà nguyên đơn biết được từ năm 2016
đến năm 2017. Rất có thể, bị đơn còn cung cấp ra thị trường cũng như cho các
10
Sở Y tế các tỉnh, thành phố khác một số lượng lớn thuốc Nisten vi phạm. Nếu
không có sản phẩm thuốc của bị đơn thì nguyên đơn đã có thể cung cấp sản
phẩm của mình cho các Sở Y tế và các bệnh viện trên cả nước bởi vì nguyên
đơn là người duy nhất nắm giữ Bằng độc quyền sáng chế số 7181 bảo hộ cho,
cùng với những đối tượng khác, Ivabradin Hydroclorua dạng tinh thể gamma.
Như vậy, tính sơ bộ, thiệt hại vật chất của nguyên đơn trong việc cung cấp sản
phẩm ra thị trường có thể lên đến hàng tỷ đồng.
Hiện nay, nguyên đơn đang tiếp tục thu thập bằng chứng về các thiệt hại
nêu trên và cũng giám sát liên tục các hành vi vi phạm đang và sẽ xảy ra trong
tương lai của bị đơn. Nguyên đơn sẽ tiếp tục nỗ lực thu thập thông tin và tài liệu
cần thiết để chứng minh các thiệt hại phát sinh từ việc xâm phạm quyền đối với
sáng chế. Với tình hình như vậy, tại thời điểm này, căn cứ vào điểm c khoản 1
Điều 205 Luật Sở hữu trí tuệ, nguyên đơn yêu cầu bị đơn phải bồi thường thiệt
hại cho nguyên đơn với số tiền là 500.000.000 đồng (bằng chữ: năm trăm triệu
đồng chẵn).
Nguyên đơn sẽ yêu cầu tăng mức bồi thường thiệt hại trên cơ sở các
chứng cứ mới được thu thập và/hoặc hành vi xâm phạm tiếp tục hoặc sẽ diễn ra
trong tương lai của bị đơn.
- Thứ 6: Bị đơn phải bồi thường chi phí hợp lý mà nguyên đơn đã bỏ ra
để thuê luật sư (liên quan đến yêu cầu khởi kiện số 5):
Bên cạnh các thiệt hại vật chất mà nguyên đơn như đã nêu, do hành vi
xâm phạm quyền của bị đơn, nguyên đơn đã phải bỏ ra ít nhất là 300.000.000
đồng để thuê Luật sư bảo vệ quyền và lợi ích hợp pháp của mình trong vụ án
này.Theo quy định tại khoản 3 Điều 205 Luật Sở hữu trí tuệ, nguyên đơn yêu
cầu bị đơn phải thanh toán khoản chi phí hợp lý là 300.000.000 đồng chẵn mà
nguyên đơn đã phải bỏ ra để thuê Luật sư.
- Thứ 7: Bị đơn phải xin lỗi công khai nguyên đơn vì hành vi xâm phạm
quyền (liên quan đến yêu cầu khởi kiện số 6):
Hành vi xâm phạm quyền đối với sáng chế thực hiện bởi bị đơn không
những trực tiếp gây thiệt hại lớn về vật chất cho nguyên đơn mà còn ảnh hưởng
đến uy tín và danh tiếng của nguyên đơn với tư cách là chủ sở hữu hợp pháp của
Bằng độc quyền sáng chế số 7181. Do đó, theo quy định tại khoản 2 Điều 202
Luật Sở hữu trí tuệ, nguyên đơn yêu cầu bị đơn phải xin lỗi công khai nguyên
đơn trên các phương tiện thông tin đại chúng, cụ thể là đăng lời xin lỗi công khai
trên Tạp chí Dược và Mỹ phẩm, Tạp chí Sức khỏe và Đời sống và báo Thanh
niên trên ba số báo liên tiếp về hành vi xâm phạm quyền.
* Tại bản tự khai, quá trình tố tụng và tại phiên tòa, người đại diện hợp
pháp của bị đơn Công ty Cổ phần Dược phẩm Đ trình bày:
Công ty Cổ phần Dược phẩm Đ (sau đây gọi tắt là Công ty Đ) cho rằng
các yêu cầu khởi kiện của nguyên đơn là hoàn toàn không có căn cứ, không
đúng quy định pháp luật, bởi các lý do sau:
11
Thứ nhất: Sản phẩm Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) của Công ty Đ đã được đăng ký, sản xuất, lưu hành theo đúng quy định
pháp luật và đã được Cục quản lý Dược - Bộ Y tế cấp phép lưu hành thuốc.
Công ty Đ được thành lập và hoạt động từ năm 2004, trong suốt quá trình
hoạt động, sản xuất kinh doanh, Công ty luôn tuân thủ, chấp hành các quy định
pháp luật và thực hiện đầy đủ nghĩa vụ với Nhà nước. Không những tạo nguồn
công việc ổn định cho người dân, góp phần thúc đẩy kinh kế của tỉnh Bình
Dương nói riêng và đất nước nói chung, Công ty còn có những đóng góp trong
việc giảm nhẹ nỗi lo về bệnh tật và gánh nặng tài chính cho người bệnh với
những sản phẩm thuốc có chất lượng và hiệu quả điều trị cao.
Để được lưu hành sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F
(Ivabradine 7.5mg), Công ty Đ đã tiến hành đăng ký theo quy định pháp luật và
được Cục quản lý Dược - Bộ Y tế cấp Giấy phép lưu hành số đăng ký VD-
20362-13 đối với sản phẩm thuốc Nisten (Ivabradine 5mg) và số đăng ký VD-
21061-14 đối với sản phẩm thuốc Nisten - F (Ivabradine 7.5mg).
Như vậy, trong suốt quá trình nghiên cứu, đăng ký, sản xuất và lưu hành
sản phẩm thuốc, Công ty Đ đã thực hiện đầy đủ thủ tục pháp lý theo quy định
pháp luật, các sản phẩm thuốc mang tên Nisten đã được cơ quan nhà nước có
thẩm quyền cấp Giấy phép lưu hành.
Thứ hai: Sản phẩm Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) của Công ty Đ không vi phạm bằng độc quyền sáng chế 7181 của Công ty
L:
- Một là, hoạt chất Ivabradin hydroclorua trong sản phẩm Nisten (Ivabradine
5mg) và Nisten - F (Ivabradine 7.5mg) Công ty Đ sử dụng là dạng bột vô định hình
(amorphous poweder form) chứ không phải là dạng tinh thể gama.
Căn cứ theo quy định tại khoản 1 Điều 8 Nghị định số 105/2006/NĐ-CP
ngày 22/9/2006 quy định chi tiết và hướng dẫn thi hành một số điều của Luật Sở
hữu trí tuệ về bảo vệ quyền sở hữu trí tuệ và quản lý nhà nước về sở hữu trí tuệ thì
yếu tố xâm phạm quyền đối với sáng chế thuộc một trong các dạng sau đây:
“- Sản phẩm hoặc bộ phận (phần) sản phẩm trùng hoặc tương đương với
sản phẩm hoặc bộ phận (phần) của sản phẩm thuộc phạm vi bảo hộ sáng chế;
- Quy trình trùng hoặc tương đương với quy trình thuộc phạm vi bảo hộ
sáng chế;
- Sản phẩm hoặc bộ phận (phần) của sản phẩm được sản xuất theo quy trình
trùng hoặc tương đương với quy trình thuộc phạm vi bảo hộ sáng chế”.
Như vậy, để khẳng định một sản phẩm có yếu tố xâm phạm quyền đối với
sáng chế hay không thì phải xem xét sản phẩm, bộ phận của sản phẩm, quy trình
sản xuất có trùng hay tương đương với sản phẩm hoặc bộ phận, quy trình thuộc
phạm vi bảo hộ sáng chế hay không.

12
Theo nội dung Bằng độc quyền sáng chế 7181 thì phạm vi bảo hộ của sáng
chế là “Hợp chất Ivabradin Hydroclorua dạng tinh thể gama, quy trình điều chế và
dược phẩm chứa nó”. Trên thực tế, Ivabradin hydroclorua có rất nhiều dạng kết
tinh như α, β, βd, γ, γd, δ, δd, hoặc dạng vô định hình tùy thuộc vào quy trình tổng
hợp và tinh chế hoạt chất này và cũng được bảo hộ bằng nhiều patent EP. Qua việc
tra cứu thông tin trên trang web http://iplib.noip.gov.vn/WebUI/Wlogin.php cho
thấy hoạt chất Ivabradin hydroclorua đã được đăng ký bảo hộ rất nhiều như
Ivabradin hydroclorua dạng tinh thể β, Ivabradin hydroclorua dạng tinh thể βd...
Như vậy, cùng là dạng tinh thể nhưng hoạt chất Ivabradin hydroclorua được xem
xét bảo hộ tùy thuộc vào dạng kết tinh của nó.
Đối chiếu với sản phẩm Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) do Công ty Đ sản xuất, theo kết quả thử nghiệm hoạt chất Ivabradin
hydroclorua do Trung tâm Dịch vụ phân tích thí nghiệm Thành phố Hồ Chí Minh -
Sở Khoa học và Công nghệ Thành phố Hồ Chí Minh cung cấp thì hoạt chất chất
Ivabradin hydroclorua Công ty Đ sử dụng là dạng bột vô định hình (amorphous
poweder form) chứ không phải là dạng tinh thể gama. Ngoài ra, quy trình tổng hợp
và tinh chế Ivabradin hydroclorua amorphous form hoàn toàn không trùng hoặc
tương đương với Bằng độc quyền sáng chế 7181. Do đó, sản phẩm Nisten
(Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) do Công ty Đ sản xuất không
xâm phạm Bằng độc quyền sáng chế 7181 của nguyên đơn.
- Hai là, Kết luận giám định về sở hữu công nghiệp số SC015-16YC/KLGĐ
ngày 26/9/2016 của Viện Khoa học Sở hữu trí tuệ - Bộ Khoa học và Công nghệ kết
luận sản phẩm Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) của Công
ty Đ xâm phạm Bằng độc quyền sáng chế 7181 là không có giá trị pháp lý.
Quá trình giám định, Giám định viên Viện Khoa học sở hữu trí tuệ đã
không tiến hành thực hiện các thí nghiệm, phân tích nhiễu xạ bột tia X hoạt chất
Ivabradin hydroclorua có trong sản phẩm Nisten (Ivabradine 5mg) và Nisten - F
(Ivabradine 7.5mg) do Công ty Đ sản xuất.
Hơn nữa, cũng không có bất cứ tài liệu nào chứng minh rằng mẫu vật
giám định đúng là sản phẩm thuốc Nisten do Công ty Đ sản xuất, lưu hành bởi
căn cứ hồ sơ vụ án thì Kết luận giám định số SC015-16YC/KLGĐ được Viện
Khoa học Sở hữu trí tuệ thực hiện ngày 26/9/2016 trong khi Vi bằng về việc thu
thập mẫu vật giám định là sản phẩm thuốc Nisten được lập ngày 12/10/2016, sau
thời điểm thực hiện giám định.
Theo Kết luận giám định về sở hữu công nghiệp số SC015-16YC/KLGĐ
ngày 26/9/2016 của Viện Khoa học sở hữu trí tuệ - Bộ Khoa học và Công nghệ, cơ
quan này đã sử dụng tài liệu giám định là tài liệu số 2 Báo cáo phân tích nhiễu xạ
bột tia X sản phẩm thuốc Nisten do GS. TS. Gerard Coquerel - Đại học Rouen,
Pháp thực hiện và ý kiến đánh giá của giáo sư này về các vấn đề liên quan đến sáng
chế và đối tượng giám định (bằng tiếng Anh) và bản dịch tiếng Việt của tài liệu này
được chứng nhận bởi Văn phòng công chứng Vũ Đào, thành phố Hà Nội, là tài liệu
cơ bản và quan trọng nhất để so sánh bản chất kỹ thuật của sáng chế được bảo hộ
13
(Bắng độc quyền sáng chế số 7181) và đối tượng giám định (thuốc Nisten). Chúng
tôi cho rằng việc Giám định viên Viện Khoa học sở hữu trí tuệ sử dụng kết quả
Báo cáo phân tích nhiễu xạ bột tia X sản phẩm thuốc Nisten do GS. TS. Gerard
Coquerel - Đại học Rouen, Pháp thực hiện để ban hành Kết luận giám định số
SC015-16YC/KLGĐ ngày 26/9/2016 là không khách quan, không đúng quy
định pháp luật, xâm phạm nghiêm trọng quyền lợi hợp pháp của Công ty Đ bởi:
+ Nội dung Báo cáo Kết quả xét nghiệm không thể hiện đầy đủ các thông
tin về phương pháp, đối tượng nghiên cứu cũng như thể hiện được năng lực
chuyên môn, thẩm quyền của GS. TS. Gerard Coquerel.
+ Quá trình xét nghiệm của GS. TS. Gerard Coquerel không được bất cứ
cá nhân, tổ chức nào kiểm chứng, giám sát. Mẫu vật mà GS. TS. Gerard
Coquerel tiến hành thí nghiệm là do phía nguyên đơn cung cấp. Vậy căn cứ nào
để xác định mẫu vật thí nghiệm mà GS. TS. Gerard Coquerel thực hiện đúng là
sản phẩm thuốc Nisten do Công ty Đ sản xuất?
+ Theo quy định tại khoản 2 Điều 4 Nghị định số 111/2011/NĐ-CP: “Để
được công nhận và sử dụng tại Việt Nam, các giấy tờ, tài liệu của nước ngoài
phải được hợp pháp hóa lãnh sự, trừ trường hợp quy định tại Điều 9 Nghị định
này” thì để tài liệu bằng tiếng Anh về Báo cáo phân tích nhiễu xạ bột tia X sản
phẩm thuốc Nisten được công nhận và sử dụng tại Việt Nam thì tài liệu này phải
được hợp pháp hóa lãnh sự tại cơ quan nhà nước có thẩm quyền Việt Nam. Tuy
nhiên, trên thực tế tài liệu này đã không được hợp pháp hóa lãnh sự để được
công nhận và sử dụng tại Việt Nam. Hơn nữa, Công ty Đ không thấy bất kỳ
bằng chứng nào chứng minh rằng tài liệu bằng tiếng Anh về Báo cáo phân tích
nhiễu xạ bột tia X sản phẩm thuốc Nisten là của GS. TS. Gerard Coquerel - Đại
học Rouen, Pháp (không tìm thấy bất kỳ chữ ký nào của người này hoặc được
xác thực của bất kỳ tổ chức nào khác). Do vậy, Công ty Đ cho rằng ai cũng có
thể chuẩn bị được tài liệu này và tự công bố rằng nó là do GS. TS. Gerard
Coquerel - Đại học Rouen thực hiện. Việc dịch tài liệu này từ tiếng Anh sang
tiếng Việt và được chứng nhận tại Văn phòng công chứng Vũ Đào, thành phố
Hà Nội chỉ đơn giản là xác nhận chữ ký của người dịch của một tài liệu bất kỳ
bằng tiếng Anh sang tiếng Việt và theo quy định của pháp luật hiện hành, Văn
phòng công chứng này chỉ xác nhận bản dịch chính xác, không vi phạm pháp
luật, không trái với đạo đức xã hội chứ không chịu trách nhiệm về tính hợp pháp
của tài liệu tiếng Anh tại Việt Nam.
Trên thực tế, Bộ Y tế là cơ quan của Chính phủ thực hiện chức năng quản
lý nhà nước về y tế, bao gồm các lĩnh vực: khám bệnh, chữa bệnh, dược, an toàn
thực phẩm, v.v... nên bất kỳ ý kiến chuyên môn nào trong lĩnh vực (ví dụ như
dược phẩm) từ bất kỳ tổ chức, cá nhân nước ngoài nào, để có giá trị pháp lý và
được sử dụng tại Việt Nam thì trước tiên phải được công nhận bởi Bộ Y tế. Như
vậy, đối với tài liệu Báo cáo phân tích nhiễu xạ bột tia X sản phẩm thuốc Nisten,
muốn có giá trị pháp lý và được sử dụng tại Việt Nam thì phải được Bộ Y tế
công nhận, phải được hợp pháp hóa lãnh sự theo quy định. Trong khi đó, Công
ty Đ không thấy bất kỳ sự công nhận nào của Bộ Y tế đối với Báo cáo phân tích
14
nhiễu xạ bột tia X sản phẩm thuốc Nisten. Vì vậy, tài liệu giám định là tài liệu số
2 Báo cáo phân tích nhiễu xạ bột tia X sản phẩm thuốc Nisten do GS. TS.
Gerard Coquerel - Đại học Rouen, Pháp thực hiện và ý kiến đánh giá của giáo sư
này về các vấn đề liên quan đến sáng chế và đối tượng giám định (bằng tiếng
Anh) là không có giá trị pháp lý, không được công nhận và sử dụng tại Việt
Nam.
Với những lý do đã nêu ở trên, Công ty Đ khẳng định rằng Kết luận giám
định về sở hữu công nghiệp số SC015-16YC/KLGĐ ngày 24/9/2016 của Viện
Khoa học Sở hữu trí tuệ - Bộ Khoa học và Công nghệ là không có giá trị pháp lý do
sử dụng tài liệu giám định (tài liệu số 2) không có giá trị pháp lý, không được công
nhận và sử dụng tại Việt Nam.
Từ những căn cứ và phân tích nêu trên, Công ty Đ cho rằng yêu cầu khởi
kiện của nguyên đơn là không có căn cứ. Do vậy, Công ty Đ kính đề nghị Tòa án
bác toàn bộ yêu cầu khởi kiện của nguyên đơn.
* Tại Bản án kinh doanh thương mại sơ thẩm số: 04/2019/KDTM-ST
ngày 17/7/2019 của Tòa án nhân dân tỉnh Bình Dương đã quyết định: Chấp nhận
toàn bộ yêu cầu khởi kiện của nguyên đơn.
* Tại Bản án kinh doanh thương mại phúc thẩm số 17/2020/KDTM-PT
ngày 08/6/2020 của Tòa án nhân dân cấp cao tại Thành phố Hồ Chí Minh đã hủy
bản án sơ thẩm số 04/2019/KDTM-ST ngày 17/7/2019, chuyển hồ sơ vụ án về
cho Tòa án cấp sơ thẩm giải quyết lại vụ án với lý do: Tòa án cấp sơ thẩm đã
căn cứ vào các Tài liệu không được hợp pháp lãnh sự, mà theo quy định tại Điều
26 Hiệp định tương trợ tư pháp về các vấn đề dân sự giữa Cộng hòa xã hội chủ
nghĩa Việt Nam và Cộng hòa Pháp phải được hợp pháp hóa lãnh sự.
*Tại Bản án kinh doanh thương mại sơ thẩm số: 13/2022/KDTM-ST ngày
07 tháng 9 năm 2022 của Tòa án nhân dân tỉnh Bình Dương đã quyết định như
sau:
1. Chấp nhận một phần yêu cầu khởi kiện của nguyên đơn L đối với bị
đơn Công ty Cổ phần Dược phẩm Đ về việc “tranh chấp về quyền sở hữu trí
tuệ”.
1.1. Buộc Công ty Cổ phần Dược phẩm Đ phải chấm dứt hành vi xâm
phạm quyền sáng chế được bảo hộ theo Điểm 1 của Yêu cầu bảo hộ Bằng độc
quyền sáng chế số 7181.
1.2. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ bồi thường thiệt hại cho
nguyên đơn L số tiền 500.000.000 đồng (năm trăm triệu đồng) theo điểm c
khoản 1 Điều 205 Luật Sở hữu trí tuệ.
1.3. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ thanh toán cho nguyên
đơn L chi phí hợp lý số tiền 300.000.000 đồng (ba trăm triệu đồng).
Kể từ khi bản án có hiệu lực pháp luật, người được thi hành án có đơn yêu
cầu thi hành án, nếu người phải thi hành án chậm thanh toán số tiền trên thì còn
15
phải trả lãi theo mức lãi suất quy định tại khoản 2 Điều 468 Bộ luật Dân sự
tương ứng với số tiền và thời gian chậm thi hành án.
1.4. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ phải xin lỗi nguyên đơn
L và cải chính công khai trên tạp chí Dược và Mỹ phẩm; tạp chí Khoa học và
Đời sống và Báo Thanh niên trong 03 kỳ liên tiếp về các hành vi xâm phạm
quyền đối với sáng chế.
1.5. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ phải tiến hành các thủ
tục rút số đăng ký VD-20362-13 đối với sản phẩm thuốc Nisten (Ivabradine
5mg) và số đăng ký VD-21061-14 đối với sản phẩm thuốc Nisten - F
(Ivabradine 7.5mg) tại Cục Quản lý Dược - Bộ Y tế.
2. Không chấp nhận yêu cầu khởi kiện của nguyên đơn về việc buộc bị
đơn Công ty Cổ phần Dược phẩm Đ thu hồi toàn bộ các sản phẩm thuốc Nisten
(Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) đã phân phối trên thị trường;
đồng thời tiêu hủy toàn bộ sản phẩm thuốc Nisten (Ivabradine 5mg), Nisten - F
(Ivabradine 7.5mg) đã thu hồi cũng như còn tồn kho và các nguyên, vật liệu
được sử dụng để sản xuất hoặc kinh doanh các sản phẩm xâm phạm Bằng độc
quyền sáng chế số 7181.
Ngoài ra, bản án sơ thẩm còn quyết định về án phí, chi phí tố tụng và
quyền kháng cáo theo quy định của pháp luật.
Sau khi xét xử sơ thẩm, ngày 13/9/2022 bị đơn Công ty cổ phần Dược
phẩm Đ kháng cáo đề nghị hủy bản án sơ thẩm.
Tại phiên tòa phúc thẩm, bị đơn Công ty cổ phần Dược phẩm Đ (có ông
Vũ Tuấn L2 là đại diện theo ủy quyền) giữ nguyên yêu cầu kháng cáo, với các lý
do: Do bản án sơ thẩm có vi phạm tố tụng khi chưa xem xét tư cách tham gia tố
tụng của nguyên đơn. Vì đại diện theo ủy quyền của nguyên đơn không có quyền
ủy quyền lại, Tòa án cấp sơ thẩm không tiến hành thu thập chứng cứ và tạm đình
chỉ giải quyết vụ án để chờ kết quả khiếu nại bằng sáng chế là không đủ căn cứ để
giải quyết vụ án. Vì theo khoản 3 Điều 96 Luật sở hữu trí tuệ thì trong trường hợp
khiếu nại của bị đơn được Cục Sở hữu trí tuệ chấp nhận thì bằng sáng chế của
nguyên đơn không có hiệu lực, nên nguyên đơn không có quyền khởi kiện đối với
bị đơn và không có căn cứ xác định bị đơn vi phạm quyền sở hữu trí tuệ. Nguyên
đơn L (có ông Mai Duy L1 là đại diện theo ủy quyền) không đồng ý yêu cầu
kháng cáo, đề nghị Hội đồng xét xử giữ nguyên bản án sơ thẩm.
Trong phần tranh luận:
Người bảo vệ quyền lợi ích hợp pháp cho bị đơn phát biểu:
- Về phạm vi ủy quyền của nguyên đơn: Theo giấy ủy quyền của nguyên
đơn thì không có ủy quyền cho ông Mai Duy L1 làm việc với bị đơn, vì chỉ ủy
quyền làm việc với Tòa án và người có quyền lợi, nghĩa vụ liên quan. Vì vậy, ông
L1 không được tham gia hòa giải, tranh tụng nên vi phạm quy định của Bộ luật tố
tụng về hòa giải, thỏa thuận, tranh tụng trong xét xử. Do không thể hòa giải,
16
không tham gia hỏi, không tranh luận, nên đề nghị Hội đồng xét xử tạm dừng
phiên tòa để triệu tập nguyên đơn hoặc yêu cầu nguyên đơn bổ sung phạm vi ủy
quyền của ông L1. Do vậy, ông L1 không có quyền tranh luận với bị đơn.
- Trường hợp Tòa án không chấp nhận yêu cầu của người bảo vệ quyền lợi
ích hợp pháp của bị đơn, thì người bảo vệ quyền lợi ích hợp pháp của bị đơn tiếp
tục tranh luận về nội dung giải quyết vụ án: Tại bản tuyên bố của công ty có nội
dung chỉ định các cá nhân đại diện theo ủy quyền của công ty. Việc ủy quyền của
nguyên đơn cho ông L1 là không hợp pháp theo quy định pháp luật Việt Nam, vì
pháp luật Việt Nam không có quy định việc chỉ định ủy quyền, nên không có hiệu
lực pháp luật.
Từ những phân tích trên thì, Tòa án cấp sơ thẩm vi phạm tố tụng vì tại cấp
sơ thẩm không có người đại diện theo ủy quyền của nguyên đơn, nhưng Tòa án
cấp sơ thẩm vẫn công nhận tư cách người đại diện theo ủy quyền của nguyên đơn
là không đúng quy định pháp luật, nên đề nghị hủy bản án sơ thẩm. Về nội dung
khác thì người đại diện theo ủy quyền của bị đơn đã trình bày đầy đủ, nên người
bảo vệ quyền lợi ích hợp pháp của bị đơn không bổ sung.
Người đại diện theo ủy quyền của bị đơn trình bày: Tại phiên tòa sơ thẩm,
thì ông G bà T1 có mặt, ông L1 vắng mặt, nhưng theo giấy ủy quyền của nguyên
đơn thì ông L1 là người đại diện ủy quyền và không có quyền ủy lại, nên đề nghị
xem xét lại tư cách ông G, bà T1 tại phiên tòa sơ thẩm. Về nội dung thì quá trình
giải quyết vụ án thì bị đơn khẳng định bị đơn không vi phạm quyền sáng chế,
không vi phạm Luật Sở hữu trí tuệ.
Người đại diện theo ủy quyền của nguyên đơn (ông Mai Duy L1) trình bày:
Ông L1 có toàn quyền thay mặt nguyên đơn tham gia tố tụng tại Tòa án thể hiện
tại giấy ủy quyền, ông L1 có quyền khởi kiện, quyết định toàn bộ nội dung vụ
việc và liên hệ tổ chức, cá nhân. Ông L1 có tham gia hòa giải tại Tòa án cấp sơ
thẩm, có trình bày đã ủy quyền lại cho ông G, bà T1. Hồ sơ vụ án có nhiều chứng
cứ chứng minh sản phẩm của bị đơn là thuộc bảo hộ sáng chế của nguyên đơn
theo kết luận giám định, và các phiên tòa sơ thẩm. Do đó, đề nghị Hội đồng xét
xử bác kháng cáo của bị đơn, giữ nguyên bản án sơ thẩm.
Đại diện Viện kiểm sát nhân dân cấp cao tại Thành phố Hồ Chí Minh nêu
quan điểm giải quyết vụ án:
- Về tố tụng: Vụ án từ khi Tòa án cấp phúc thẩm thụ lý đến khi xét xử đã
thực hiện đầy đủ các quy định của Bộ luật tố tụng dân sự.
- Về nội dung: Ngày 10/6/2019 bị đơn có đơn đề nghị Tòa án tạm đình chỉ
giải quyết vụ án. Nguyên đơn là chủ sở hữu sáng chế đã được Cục Sở hữu trí tuệ
cấp bằng sáng chế tại Việt Nam. Trong quá trình giải quyết vụ án, bị đơn không
có ý kiến về văn bằng sáng chế, hiện tại văn bằng sáng chế của nguyên đơn vẫn
đang có hiệu lực pháp luật, nên yêu cầu tạm đình chỉ là không có căn cứ.
Theo kết luận giám định ngày 26/9/2019 sáng chế được bảo hộ hợp chất
(đối tượng giám định), thì sản phẩm của bị đơn có dùng công thức, biểu đồ
17
nhiễu xạ được bảo hộ của nguyên đơn. Theo quy định của Luật Sở hữu trí tuệ và
hướng dẫn Nghị định 99 thì sản phẩm của bị đơn có xâm phạm sáng chế của
nguyên đơn. Theo kết luận giám định sở hữu công nghiệp thì thuốc của bị đơn
có thành phần trùng với hợp chất sáng chế của nguyên đơn, là xâm phạm quyền
đối với sáng chế đang được bảo hộ. Vậy, bị đơn đã sản xuất thuốc và phân phối
tại thị trường Việt Nam có áp dụng sáng chế của nguyên đơn mà không xin phép
là vi phạm quyền sở hữu công nghiệp. Bản án sơ thẩm đã xét xử là có căn cứ.
Tại phiên tòa phúc thẩm, bị đơn cho rằng ủy quyền của nguyên đơn là không
hợp pháp, nhưng hồ sơ vụ án thể hiện tư cách người đại diện theo ủy quyền của
nguyên đơn là đúng quy định pháp luật, nên không có căn cứ chấp nhận lời trình
bày của người bảo vệ quyền lợi ích hợp pháp cho bị đơn. Từ đó, đề nghị Hội
đồng xét xử không chấp nhận kháng cáo của bị đơn, giữ nguyên bản án sơ thẩm.
NHẬN ĐỊNH CỦA TÒA ÁN:
Sau khi nghiên cứu các tài liệu có trong hồ sơ vụ án được thẩm tra tại
phiên tòa và căn cứ vào kết quả tranh tụng tại phiên tòa, ý kiến phát biểu của
Viện kiểm sát, Hội đồng xét xử nhận định:
[1] Theo Đơn khởi kiện 21/11/2016, nguyên đơn L khởi kiện yêu cầu bị
đơn Công ty cổ phần dược phẩm Đ phải chấm dứt hành vi xâm phạm quyền
sáng chế; Thu hồi toàn bộ các sản phẩm thuốc Nisten (Ivabradine 5mg), Nisten -
F (Ivabradine 7.5mg) đã phân phối trên thị trường và tiêu hủy toàn bộ sản phẩm
thuốc Nisten (Ivabradine 5mg), Nisten - F (Ivabradine 7.5mg) đã thu hồi cũng
như còn tồn kho và các nguyên, vật liệu được sử dụng để sản xuất hoặc kinh
doanh các sản phẩm xâm phạm Bằng độc quyền sáng chế số 7181; Tiến hành
thủ tục rút số đăng ký VD-20362-13 đối với sản phẩm thuốc Nisten (Ivabradine
5mg) và số đăng ký VD-21061-14 đối với sản phẩm thuốc Nisten - F
(Ivabradine 7.5mg) tại Cục quản lý Dược - Bộ Y tế; bồi thường thiệt hại cho
nguyên đơn số tiền 500.000.000 đồng theo điểm c khoản 1 Điều 205 Luật Sở
hữu trí tuệ; Thanh toán chi phí hợp lý trị giá 300.000.000 đồng; Phải xin lỗi
nguyên đơn và cải chính công khai trên tạp chí Dược và Mỹ phẩm, tạp chí Khoa
học và Đời sống và Báo Thanh niên trong 03 kỳ liên tiếp về các hành vi xâm
phạm quyền đối với sáng chế.
[2] Bản án sơ thẩm nhận định:
- L là chủ sở hữu Bằng độc quyền sáng chế số 7181 được Cục Sở hữu trí
tuệ cấp ngày 15/7/2008 theo Quyết định số 13701/QĐ-SHTT, có hiệu lực 20
năm (kể từ ngày 15/02/2006), bảo hộ đối với sáng chế: Hợp chất Ivabradin
Hydroclorua dạng tinh thể gama, quy trình điều chế và dược phẩm chứa nó.
Ivabradin là chất làm giảm chuyên biệt nhịp tim. Tác dụng trên tim của thuốc là
đặc hiệu với nút xoang mà không làm ảnh hưởng tới thời gian dẫn truyền trong
nhĩ, trong nhĩ - thất, sự tái cực thất hoặc co cơ tim.
- Nguyên đơn có tranh chấp với bị đơn vì bị đơn đã sản xuất, lưu hành,
tàng trữ trên thị trường sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten-F
18
(Ivabradine 7.5mg) có chứa hoạt chất Ivabradin Hydroclorua dạng tinh thể
gamma đã được bảo hộ bởi Bằng độc quyền sáng chế số 7181.
Bị đơn cho rằng, hoạt chất Ivabradin Hydroclorua trong sản phẩm thuốc
Nisten (Ivabradine 5mg) và Nisten-F (Ivabradine 7.5mg) của bị đơn sử dụng là
dạng bột vô định hình (amorphous poweder form) chứ không phải là dạng tinh
thể gamma và sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten- F (Ivabradine
7.5mg) đã được đăng ký sản xuất, lưu hành theo đúng quy định của pháp luật,
được Cục quản lý Dược - Bộ Y tế cấp Giấy phép lưu hành số đăng ký VD-
20362-13 đối với sản phẩm Nisten (Ivabradine 5mg) và số đăng ký VD-21061-
14 đối với sản phẩm Nisten - F (Ivabradine 7.5mg), nên không vi phạm Bằng
độc quyền sáng chế số 7181 của nguyên đơn.
- Xét, tại Kết luận Giám định về sở hữu công nghiệp ngày 03/5/2019 do
Giám định viên độc lập ông Phạm Phi Anh đối với 02 mẫu thuốc Nisten
(Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) do bị đơn cung cấp, xác
định:“Sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) do Công ty Cổ phần Dược phẩm Đ sản xuất chứa hoạt chất Ivabradine
trùng với hợp chất thuộc phạm vi bảo hộ của các điểm Yêu cầu bảo hộ của Bằng
độc quyền sáng chế số 7181 và do đó, sản phẩm thuốc Nisten (Ivabradine 5mg)
và Nisten - F (Ivabradine 7.5mg) bị coi là yếu tố xâm phạm quyền đối với sáng
chế đang được bảo hộ theo Bằng độc quyền sáng chế số 7181”. Đồng thời, tại
Văn bản số 11611/QLD-TTra ngày 21/6/2018 của Cục Quản lý Dược - Bộ Y tế
đã xác định: “việc sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F
(Ivabradine 7.5mg) được Bộ Y tế cấp Giấy phép lưu hành không phải là căn cứ
để khẳng định thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg)
có hay không vi phạm các bằng độc quyền sáng chế có liên quan”. Vì vậy, có đủ
căn cứ xác định bị đơn đã vi phạm Bằng độc quyền sáng chế số 7181 của
nguyên đơn.
- Theo quy định tại khoản 1 Điều 124, khoản 1 Điều 126 Luật Sở hữu trí
tuệ, việc bị đơn tiến hành tàng trữ, sản xuất, lưu thông, buôn bán, vận chuyển,
quảng cáo, chào hàng trên thị trường sản phẩm thuốc Nisten (Ivabradine 5mg)
và Nisten - F (Ivabradine 7.5mg) có chứa hoạt chất Ivabradin Hydroclorua dạng
tinh thể gama đang được bảo hộ tại Bằng độc quyền sáng chế số 7181, khi chưa
được sự cho phép của nguyên đơn là hành vi sử dụng đối tượng sở hữu công
nghiệp, xâm phạm quyền đối với sáng chế của S.
Do đó, theo quy định tại khoản 1 Điều 125 Luật Sở hữu trí tuệ thì nguyên
đơn có quyền yêu cầu cơ quan Nhà nước có thẩm quyền buộc bị đơn phải chấm
dứt hành vi xâm phạm quyền sáng chế được bảo hộ theo Điểm 1 của Bằng độc
quyền sáng chế số 7181 của nguyên đơn; phải xin lỗi nguyên đơn và cải chính
công khai trên tạp chí Dược và Mỹ phẩm; tạp chí Khoa học và Đời sống và Báo
Thanh niên trong 03 kỳ liên tiếp về các hành vi xâm phạm quyền đối với sáng
chế của nguyên đơn theo quy định tại khoản 2 Điều 202 Luật Sở hữu trí tuệ;
phải bồi thường thiệt hại số tiền 500.000.000 đồng theo quy định tại điểm c
khoản 1 Điều 205 Luật Sở hữu trí tuệ và thanh toán số tiền 300.000.000 đồng
19
chi phí hợp lý mà nguyên đơn đã bỏ ra để thuê Luật sư theo quy định tại khoản 3
Điều 205 Luật Sở hữu trí tuệ.
- Đối với yêu cầu buộc bị đơn Công ty Cổ phần Dược phẩm Đ thu hồi
toàn bộ các sản phẩm thuốc Nisten (Ivabradine 5mg) và Nisten - F (Ivabradine
7.5mg) đã phân phối trên thị trường; đồng thời tiêu hủy toàn bộ sản phẩm thuốc
Nisten (Ivabradine 5mg), Nisten - F (Ivabradine 7.5mg) đã thu hồi cũng như còn
tồn kho và các nguyên, vật liệu được sử dụng để sản xuất hoặc kinh doanh các
sản phẩm xâm phạm Bằng độc quyền sáng chế số 7181: Xét thấy, nguyên đơn
không xác định được số lượng cụ thể sản phẩm thuốc Nisten (Ivabradine 5mg)
và Nisten - F (Ivabradine 7.5mg) đã phân phối trên thị trường, đồng thời không
định danh, định lượng được chính xác nguyên liệu thô, vật liệu và máy móc
cũng như nơi bảo quản và người đang quản lý, sử dụng các nguyên, vật liệu
được sử dụng để sản xuất hoặc kinh doanh các sản phẩm xâm phạm Bằng độc
quyền sáng chế số 7181 nên không có tính khả thi khi thi hành án. Do đó, yêu
cầu này của nguyên đơn là không có căn cứ chấp nhận.
Từ những phân tích trên, Tòa án cấp sơ thẩm chấp nhận một phần yêu cầu
khởi kiện của nguyên đơn.
[3] Hội đồng xét xử phúc thẩm nhận định:
Tòa án cấp sơ thẩm đã nhận định, đánh giá đầy đủ tài liệu chứng cứ trong
hồ sơ và xét xử là có căn cứ, đảm bảo quyền lợi ích hợp pháp của các đương sự.
Ngoài ra, Hội đồng xét xử nhận định thêm:
- Bị đơn kháng cáo cho rằng Bản án sơ thẩm đã có vi phạm tố tụng khi
công nhận tư cách người đại diện theo ủy quyền của nguyên đơn tại cấp sơ
thẩm, và đề nghị tạm đình chỉ giải quyết vụ án để chờ kết quả giải quyết của Cục
Sở hữu trí tuệ đối với Bằng độc quyền sáng chế số 7181 của nguyên đơn.
Xét, theo Giấy chỉ định đại diện ngày 21/11/2016, L đã chỉ định ông Mai
Duy L1 là người đại diện, với nội dung: “Ông Mai Duy L1 là người đại diện
theo ủy quyền của chúng tôi có toàn quyền được ủy quyền lại, hủy bỏ việc ủy
quyền lại, để thực hiện các công việc sau nhân danh cho L...” là phù hợp Điều
138 Bộ luật Dân sự năm 2015. Căn cứ Giấy chỉ định đại diện ngày 21/11/2016,
ông Mai Duy L1 đã ủy quyền lại cho ông Bạch Hoàng G và bà Nguyễn Thị Anh
T1 tham gia tố tụng (theo Văn bản ngày 22/7/2022) là không trái pháp luật. Tại
cấp phúc thẩm, người đại diện theo ủy quyền của nguyên đơn ông Mai Duy L1
có mặt, xác định người được ủy quyền của nguyên đơn tại cấp sơ thẩm đã thực
hiện đúng quy định pháp luật, không ảnh hưởng đến quyền lợi ích hợp của
nguyên đơn. Do vậy, Hội đồng xét xử xác định Tòa án cấp sơ thẩm không vi
phạm tố tụng trong trường hợp này.
Đối với yêu cầu tạm đình chỉ giải quyết vụ án của phía bị đơn đã được
Tòa án cấp sơ thẩm nhận định không chấp nhận là đúng. Do vậy, yêu cầu kháng
cáo của bị đơn đề nghị Tòa án cấp phúc thẩm tạm đình chỉ giải quyết vụ án là
không có căn cứ chấp nhận. Hơn nữa, theo quy định của pháp luật thì từ khi biết
20
được hành vi hoặc văn bản hành chính của cơ quan Nhà nước có thẩm quyền
xâm phạm quyền, lợi ích hợp pháp của mình mà không được giải quyết theo quy
định pháp luật, thì đương sự có quyền khởi kiện vụ án hành chính. Theo bị đơn
trình bày từ năm 2019 bị đơn đã có văn bản đề nghị Cục Sở hữu trí tuệ xem xét
hủy bỏ hiệu lực Bằng độc quyền sáng chế số 0007181, đến nay chưa có kết quả
giải quyết nhưng bị đơn không yêu cầu khởi kiện vụ án hành chính là đã hết thời
hiệu khởi kiện theo quy định tại Điều 116 Luật tố tụng hành chính năm 2015.
[4] Từ những phân tích trên, Hội đồng xét xử xét thấy Tòa án cấp sơ thẩm
đã xét xử là có căn cứ. Bị đơn có kháng cáo nhưng không có tài liệu, chứng cứ
chứng minh. Do vậy, Hội đồng xét xử chấp nhận quan điểm của đại diện Viện
kiểm sát tham gia phiên tòa; Không chấp nhận yêu cầu kháng cáo của bị đơn;
Giữ nguyên bản án sơ thẩm.
[5] Các quyết định khác của bản án sơ thẩm không có kháng cáo, kháng
nghị đã có hiệu lực pháp luật kể từ ngày hết thời hạn kháng cáo, kháng nghị.
[6] Án phí kinh doanh thương mại phúc thẩm:
Do yêu cầu kháng cáo không được chấp nhận nên người có kháng cáo
phải chịu.
Vì các lẽ trên,
QUYẾT ĐỊNH:
Căn cứ khoản 1 Điều 308 Bộ luật Tố tụng dân sự,
I. Không chấp nhận yêu cầu kháng cáo của bị đơn Công ty cổ phần dược
phẩm Đ.
Giữ nguyên bản án kinh doanh thương mại sơ thẩm số 13/2022/KDTM-
ST ngày 07/9/2022 của Tòa án nhân dân tỉnh Bình Dương.
Áp dụng khoản 1 Điều 123, khoản 1 Điều 124, khoản 1 Điều 125, khoản
1 Điều 126, Điều 201, Điều 202, Điều 204, Điều 205 Luật Sở hữu trí tuệ năm
2005, được sửa đổi, bổ sung năm 2009; Các Điều 16, 20 Nghị định số
105/2006/NĐ-CP ngày 22/9/2006 của Chính phủ quy định chi tiết và hướng dẫn
thi hành một số điều của Luật Sở hữu trí tuệ về bảo vệ quyền sở hữu trí tuệ và
quản lý nhà nước về sở hữu trí tuệ; Nghị định số 119/2010/NĐ-CP ngày
30/12/2010 của Chính phủ sửa đổi, bổ sung một số điều của Nghị định số
105/2006/NĐ-CP ngày 22/9/2006 của Chính phủ quy định chi tiết và hướng dẫn
thi hành một số điều của Luật Sở hữu trí tuệ về bảo vệ quyền sở hữu trí tuệ và
quản lý nhà nước về sở hữu trí tuệ; Nghị quyết số 326/2016/UBTVQH14 ngày
30/12/2016 của Ủy ban Thường vụ Quốc hội quy định về mức thu, miễn, giảm,
thu, nộp, quản lý sử dụng án phí và lệ phí Tòa án;
Tuyên xử:
21
1. Chấp nhận một phần yêu cầu khởi kiện của nguyên đơn L đối với bị
đơn Công ty Cổ phần Dược phẩm Đ về việc “tranh chấp về quyền sở hữu trí
tuệ”.
1.1. Buộc Công ty Cổ phần Dược phẩm Đ phải chấm dứt hành vi xâm
phạm quyền sáng chế được bảo hộ theo Điểm 1 của Yêu cầu bảo hộ Bằng độc
quyền sáng chế số 7181.
1.2. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ bồi thường thiệt hại cho
nguyên đơn L số tiền 500.000.000 đồng (năm trăm triệu đồng) theo điểm c
khoản 1 Điều 205 Luật Sở hữu trí tuệ.
1.3. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ thanh toán cho nguyên
đơn L chi phí hợp lý số tiền 300.000.000 đồng (ba trăm triệu đồng).
Kể từ khi bản án có hiệu lực pháp luật, người được thi hành án có đơn yêu
cầu thi hành án, nếu người phải thi hành án chậm thanh toán số tiền trên thì còn
phải trả lãi theo mức lãi suất quy định tại khoản 2 Điều 468 Bộ luật Dân sự
tương ứng với số tiền và thời gian chậm thi hành án.
1.4. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ phải xin lỗi nguyên đơn
L và cải chính công khai trên tạp chí Dược và Mỹ phẩm; tạp chí Khoa học và
Đời sống và Báo Thanh niên trong 03 kỳ liên tiếp về các hành vi xâm phạm
quyền đối với sáng chế.
1.5. Buộc bị đơn Công ty Cổ phần Dược phẩm Đ phải tiến hành các thủ
tục rút số đăng ký VD-20362-13 đối với sản phẩm thuốc Nisten (Ivabradine
5mg) và số đăng ký VD-21061-14 đối với sản phẩm thuốc Nisten - F
(Ivabradine 7.5mg) tại Cục Quản lý Dược - Bộ Y tế.
2. Không chấp nhận yêu cầu khởi kiện của nguyên đơn về việc buộc bị
đơn Công ty Cổ phần Dược phẩm Đ thu hồi toàn bộ các sản phẩm thuốc Nisten
(Ivabradine 5mg) và Nisten - F (Ivabradine 7.5mg) đã phân phối trên thị trường;
đồng thời tiêu hủy toàn bộ sản phẩm thuốc Nisten (Ivabradine 5mg), Nisten - F
(Ivabradine 7.5mg) đã thu hồi cũng như còn tồn kho và các nguyên, vật liệu
được sử dụng để sản xuất hoặc kinh doanh các sản phẩm xâm phạm Bằng độc
quyền sáng chế số 7181.
3. Các quyết định khác của bản án sơ thẩm không có kháng cáo, kháng
nghị đã có hiệu lực pháp luật kể từ ngày hết thời hạn kháng cáo, kháng nghị.
II. Án phí kinh doanh thương mại phúc thẩm:
Công ty cổ phần dược phẩm Đ phải chịu 2.000.000 đồng (Hai triệu đồng),
được trừ vào 2.000.000 đồng (Hai triệu đồng) tạm ứng án phí đã nộp theo biên
lai thu số 0000247 ngày 28/9/2022 của Cục thi hành án dân sự tỉnh Bình Dương.
Trường hợp bản án được thi hành theo Điều 2 Luật thi hành án dân sự thì
người được thi hành án, người phải thi hành án có quyền thỏa thuận thi hành án,
quyền yêu cầu thi hành án, tự nguyện thi hành án, hoặc bị cưỡng chế thi hành án
22
theo qui định tại các Điều 6, 7, 7a, 9 Luật thi hành án dân sự; thời hiệu thi hành
án được thực hiện theo qui định tại Điều 30 Luật thi hành án dân sự.
Bản án phúc thẩm có hiệu lực pháp luật kể từ ngày tuyên án./.
Nơi nhận:
- Tòa án nhân dân tối cao;
- VKSND cấp cao tại TP.HCM
- TAND tỉnh Bình Dương;
- VKSND tỉnh Bình Dương;
- Cục THADS tỉnh Bình Dương;
- NĐ (1);
- BĐ (1);
- Lưu (10) 17b (Án TTKY).
TM. HỘI ĐỒNG XÉT XỬ PHÚC THẨM
THẨM PHÁN – CHỦ TỌA PHIÊN TÒA
Phạm Thị Duyên
Tải về
Quý khách vui lòng Đăng nhập tài khoản để tải file. Nếu chưa có tài khoản, Quý khách vui lòng đăng ký tại đây!
Bản án/ Quyết định cùng đối tượng
