- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 5164:2018 Xác định vitamin B1 bằng sắc ký lỏng hiệu năng cao
| Số hiệu: | TCVN 5164:2018 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Y tế-Sức khỏe , Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
2018 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 5164:2018
Nội dung tóm tắt đang được cập nhật, Quý khách vui lòng quay lại sau!
Tải tiêu chuẩn Việt Nam TCVN 5164:2018
TIÊU CHUẨN QUỐC GIA
TCVN 5164:2018
EN 14122:2014
THỰC PHẨM - XÁC ĐỊNH VITAMIN B1 BẰNG SẮC KÝ LỎNG HIỆU NĂNG CAO
Foodstuffs - Determination of vitamin B1 by high performance liquid chromatography
Lời nói đầu
TCVN 5164:2018 thay thế TCVN 5164:2008;
TCVN 5164:2018 hoàn loàn tương đương với EN 14122:2014;
TCVN 5164:2018 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F13 Phương pháp phân tích và lấy mẫu biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
THỰC PHẨM - XÁC ĐỊNH VITAMIN B1 BẰNG SẮC KÝ LỎNG HIỆU NĂNG CAO
Foodstuffs - Determination of vitamin B1 by high performance liquid chromatography
CẢNH BÁO - Khi áp dụng tiêu chuẩn này có thể cần phải sử dụng các vật liệu, thiết bị và các thao tác nguy hiểm. Tiêu chuẩn này không đề cập đến các vấn đề an toàn khi sử dụng chúng. Người sử dụng tiêu chuẩn này phải tự thiết lập các thao tác an toàn thích hợp và xác định khả năng áp dụng các giới hạn quy định trước khi sử dụng tiêu chuẩn.
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp xác định vitamin B1 trong thực phẩm bằng sắc ký lỏng hiệu năng cao (HPLC) xử lý bằng enzym và dẫn xuất hóa trước cột hoặc sau cột. Phương pháp này được đánh giá xác nhận trong hai nghiên cứu liên phòng. Nghiên cứu thứ nhất phân tích mẫu bột mì nguyên cám, sữa bột/sữa bột khô sấy phun, rau hỗn hợp đông khô và gan lợn đông lạnh, từ 0,295 mg/100 g đến 0,807 mg/100 g. Nghiên cứu thứ hai phân tích các mẫu thức ăn dùng bằng đường xông, thức ăn trẻ em bổ sung rau, sữa bột, thức ăn bổ sung hoa quả, nấm men, ngũ cốc, bột sô cô la và thực phẩm bổ sung từ 0,11 mg/100 g đến 486 mg/100 g. Vitamin B1 là tổng các phần khối lượng của thiamin bao gồm các dẫn xuất phosphoryl hóa.
Thông tin thêm về đánh giá xác nhận, xem Điều 8 và Phụ lục B.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau là rất cần thiết cho việc áp dụng tiêu chuẩn. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi.
TCVN 4851 (ISO 3696), Nước dùng để phân tích trong phòng thí nghiệm. Yêu cầu kỹ thuật và phương pháp thử.
3 Nguyên tắc
Thiamin được chiết từ thực phẩm bằng cách thủy phân axit, sau đó dephosphoryl hóa bằng enzym và định lượng bằng HPLC có dẫn xuất hóa trước cột hoặc sau cột với thiochrom. Sử dụng chất ngoại chuẩn để định lượng. Để biết thêm thông tin xem [1] đến [7]
4 Thuốc thử
Chỉ sử dụng thuốc thử loại tinh khiết phân tích và nước ít nhất đạt loại 1 của TCVN 4851 (ISO 3696) hoặc nước cất hai lần, trừ khi có quy định khác.
4.1 Metanol, khối lượng w(CH3OH) ≥ 99,8 %, loại dùng cho HPLC.
4.2 Dung dịch axit axetic, nồng độ chất c(CH3COOH) = 0,02 mol/l.
4.3 Isobutanol, w(C4H10O) ≥ 98 %.
4.4 Natri dihydro phosphat, w(NaH2PO4) ≥ 99,8 %.
4.5 Dung dịch axit clohydric, w(HCl) = 36 %.
4.6 Dung dịch axit clohydric, c(HCl) = 0,1 mol/l.
4.7 Dung dịch axit sulfuric, c(H2SO4) = 0,05 mol/l.
4.8 Natrl hydroxit, w(NaOH) ≥ 99 %.
4.9 Dung dịch natri hydroxit, nồng độ khối lượng ρ(NaOH) = 150 g/l.
4.10 Dung dịch natri hydroxit, ρ(NaOH) = 200 g/l.
4.11 Kali hexaxyanoferat III, wíK3[Fe(CN)6]ý ≥ 99 %.
4.12 Dung dịch kali hexaxyanoferat III, ρíK3[Fe(CN)6]ý = 10 g/l.
4.13 Dung dịch kali hexaxyanoferat III kiềm (dẫn xuất trước cột), ρíK3[Fe(CN)6]ý = 0,4 g/l.
Pha loãng 2,0 ml dung dịch kali hexaxyanoferat III (4.12) bằng dung dịch natri hydroxit (4.9) đến 50 ml. Dung dịch nên được chuẩn bị trong ngày sử dụng.
4.14 Dung dịch kali hexaxyanoferat III kiềm (dẫn xuất sau cột), ρíK3[Fe(CN)6]ý = 0,5 g/l.
Pha loãng 2,5 ml dung dịch kali hexaxyanoferat III (4.12) bằng dung dịch natri hydroxit (4.10) đến 50 ml.
4.15 Enzym hoặc hỗn hợp enzym, có khả năng giải phóng vitamin B1 từ thực phẩm không chứa thiamin tự do.
CHÚ THÍCH 1 Dữ liệu về độ chụm nêu trong Bảng B.1, sử dụng Taka-Diatase từ Pfaltz và Bauer1. Đối với độ chụm nêu trong Bảng B.2 và Bảng B.3, sử dụng kết hợp enzym β-amytase từ lúa mạch và Taka-Diataza1 từ Serva.
CHÚ THÍCH 2 Nếu xảy ra hiện tượng dephosphoryl hóa không đầy đủ, thì có thể tiến hành định lượng riêng TMP (Thiamin Mono Phosphat), xem [7].
____________________
1) Taka-Diastase Nr. T00040 là tên thương mại của sản phẩm được cung cấp bởi Pfaltz & Bauer, Waterbury, CT 06708, Mỹ. Thông tin này đưa ra tạo thuận lợi cho người sử dụng tiêu chuẩn này và CEN không ấn định phải sử dụng chúng. Có thể sử dụng các sản phẩm tương tự nếu cho các kết quả tương đương.
4.16 Dung dịch natri axetat, c(CH3COONa.3H2O) = 2,5 mol/l.
4.17 Dung dịch natri axetat, c(CH3COONa.3H2O) = 0,5 mol/l.
4.18 Pha động HPLC
Các ví dụ về các hỗn hợp thích hợp với các phần thể tích ví dụ từ 10 % đến 50 % metanol (4.1) trong nước hoặc sử dụng dung dịch đệm phosphat hoặc dung dịch đệm axetat được nêu trong Phụ lục A và Phụ lục C. Khả năng sử dụng các tác nhân tạo cặp ion cũng được đưa ra.
4.19 Đệm phosphat (pH = 3,5), c(KH2PO4) = 9,0 mmol/l.
4.20 Tetraetylamoniclorua, w(C8H20NCl) ≥ 98 %.
4.21 Natri heptansulfonat, w(C7H15NaO3S) ≥ 98 %.
4.22 Đệm axêtat (pH = 4,0), c(CH3COOH) = 50 mmol/l.
4.23 Chất chuẩn
4.23.1 Thiamin clorua hydroclorua, w(C12H17ClN4OS.HCl) ≥ 99 %.
Để hiệu chuẩn ngoài, xem 6.3.
4.23.2 Thiamin monophosphat clorua, w(C12H17ClN4O4PS) ≥ 98 %.
Để kiểm tra enzym, xem 6.2.2.
4.23.3 Thiamin pyrophosphat clorua (cocarboxylase), w(C12H19ClN4O7P2S) ≥ 98 %.
Để kiểm tra enzym, xem 6.2.2.
4.24 Dung dịch gốc
4.24.1 Dung dịch gốc thiamin clorua hydroclorua, ρ(C12H17ClN4OS.HCl) ≈ 0,1 mg/ml
Hòa tan một lượng chính xác chất chuẩn thiamin cloroa hydroclorua (4.23.1) trong một thể tích dung môi thích hợp đã xác định, ví dụ 10 mg chất chuẩn vitamin B1 trong 100 ml dung dịch axit clohydric (4.6). Dung dịch này có thể bảo quản được bốn tuần ở nhiệt độ + 4 °C.
4.24.2 Dung dịch gốc thiamin monophosphat, ρ(C12H17ClN4O4PS) ≈ 0,1 mg/ml
Hòa tan một lượng chính xác thiamin monophosphat clorua (4.23.2) trong một thể tích dung môi thích hợp đã xác định, ví dụ 10 mg thiamin monophosphat clorua trong 100 ml dung dịch axit clohydric (4.6). Dung dịch này có thể bảo quản được bốn tuần ở nhiệt độ - 20 °C.
4.24.3 Dung dịch gốc thiamin pyrophosphat, ρ(C12H19ClN4O7P2S) ≈ 0,1 mg/ml
Hòa tan một lượng chính xác thiamin pyrophosphat clorua (4.23.3) trong một thể tích dung môi thích hợp đã xác định, ví dụ 10 mg thiamin pyrophosphat clorua trong 100 ml dung dịch axit clohydric (4.6).
4.24.4 Kiểm tra nồng độ thiamin clorua hydroclorua
Pha loãng 10 ml dung dịch thiamin clorua hydrodorua (4.24.1) bằng dung dịch axit clohydric (4.6) trong bình định mức 100 ml đến vạch. Đo độ hấp thụ của dung dịch này ở bước sóng tối đa 247 nm (A247) trong cuvet 1 cm dựa vào dung dịch axit clohydric (4.6) trong cuvet chuẩn, sử dụng máy đo phổ UV (5.1). Tính nồng độ khối lượng, ρ, bằng microgram trên mililit dung dịch thiamin clorua hydroclorua (4.24.1), sử dụng Công thức (1):
![]()
Trong đó
| e | là hệ số hấp thụ phân tử của thiamin clorua hydroclorua ở bước sóng tối đa khoảng 247 nm. Giá trị là 14 200 l.mol-1.cm-1. Giá trị tính được từ hệ số tắt, |
| M | là khối lượng phân tử, tính bằng gam trên mol (g/mol). Giá trị là 337,21. |
| A247 | là giá trị hấp thụ của dung dịch thiamin clorua hydroclorua. |
4.25 Dung dịch chuẩn
4.25.1 Dung dịch chuẩn thiamin clorua hydroclorua, ρ(C12H17ClN4OS.HCl) ≈ 1 µg/ml đến 10 µg/ml
Dùng pipet lấy từ 1 ml đến 10 ml dung dịch thiamin clorua hydroclorua (4.24.1) cho vào bình định mức 100 ml và pha loãng đến vạch bằng dung môi thích hợp, ví dụ dung dịch axit clohydric (4.6). Dung dịch này có thể bảo quản được 1 tháng ở nhiệt độ 4 °C, ở nơi tối.
4.25.2 Dung dịch chuẩn thiamin monophosphat, ρ(C12H19ClN4O4PS) ≈ 1 µg/ml đến 10 µg/ml
Dùng pipet lấy từ 1 ml đến 10 ml dung dịch thiamin monophosphat (4.24.2) cho vào bình định mức 100 ml và pha loãng đến vạch bằng dung môi thích hợp, ví dụ dung dịch axit clohydric (4.6). Dung dịch này có thể bảo quản được 1 tháng ở nhiệt độ 4 °C, ở nơi tối.
4.25.3 Dung dịch chuẩn thiamin pyrophosphat, ρ(C12H19ClN4O7P2S) ≈ 1 µg/ml đến 10 µg/ml
Dùng pipet lấy từ 1 ml đến 10 ml dung dịch thiamin pyrophosphat (4.24.3) cho vào bình định mức 100 ml và pha loãng đến vạch bằng dung môi thích hợp, ví dụ dung dịch axit clohydric (4.6). Dung dịch này có thể bảo quản được 1 tháng ở nhiệt độ 4 °C, ở nơi tối.
5 Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ phòng thử nghiệm thông thường và cụ thể như sau:
5.1 Máy đo phổ UV, có thể đo độ hấp thụ ở các bước sóng xác định (247 nm), với cuvet thích hợp, ví dụ chiều dài đường quang 1 cm.
5.2 Thiết bị hấp áp lực hoặc gia nhiệt
Dùng thiết bị hấp áp lực cho mục đích chiết, ví dụ như kiểu nồi hấp áp lực, có bộ phận ghi nhiệt độ và áp suất, bộ phận đốt nóng bằng điện hoặc nồi cách thủy.
5.3 Hệ thống HPLC
Hệ thống HPLC gồm có bơm, bộ phận bơm mẫu, detector huỳnh quang có các bước sóng phát xạ 366 nm và kích thích 435 nm đã cài đặt, (xem Phụ lục C) và hệ thống đánh giá như bộ tích phân.
5.4 Cột HPLC
5.4.1 Yêu cầu chung
Có thể sử dụng các cột hoặc cỡ hạt có kích cỡ khác với quy định trong tiêu chuẩn này. Các thông số tách phải phù hợp với vật liệu sử dụng để đảm bảo các kết quả tương đương. Tiêu chí vận hành đối với các cột phân tích thích hợp là độ phân giải đường nền của thiamin từ các chất gây nhiễu2)
________________
2) Cột nhồi silica phủ vật liệu thích hợp có bán sẵn là Lichrosorb® Si 60, Spherisorb® SI, Hypersil® SI và Lichrospher® 100 DIOL. Các cột RP bao gói vật liệu thích hợp như Spherisorb® ODS, m-Bondapak® radial C18, Supelco® LC-18-DB và Hypersil® ODS. Thông tin này đưa ra tạo thuận tiện cho người sử dụng tiêu chuẩn này và CEN không ấn định phải sử dụng chúng.
.
5.4.2 Trường hợp ôxy hóa trước cột
Cột phân tích, ví dụ như Lichropher® 60 RP Select B 2), cỡ hạt 5 µm, đường kính từ 4,0 mm đến 4,6 mm, dài từ 100 mm đến 250 mm.
5.4.3 Trường hợp ôxy hóa sau cột
Cột phân tích, ví dụ như Supelco® LC-18-DB 2), cỡ hạt 5 µm, đường kính từ 4,0 mm đến 4,6 mm, dài từ 100 mm đến 250 mm.
5.5 Bộ lọc
Lọc pha động cũng như lọc dung dịch mẫu thử qua màng lọc, ví dụ cỡ lỗ 0,45 µm trước khi sử dụng hoặc bơm sẽ kéo dài tuổi thọ của cột.
5.6 Bơm phản ứng sau cột và ống dẫn xuất, hệ thống phân phối thuốc thử thích hợp là ống nối kiểu chữ T và ống dẫn xuất (ví dụ 10 m x 0,33 mm).
6 Cách tiến hành
6.1 Chuẩn bị mẫu thử
Đồng hóa mẫu thử. Nghiền nguyên liệu thô trong máy nghiền thích hợp và trộn lại. Cần thực hiện các biện pháp như làm nguội sơ bộ để tránh tiếp xúc với nhiệt độ cao trong thời gian dài.
6.2 Chuẩn bị dung dịch mẫu thử
6.2.1 Tách chiết
Cân một lượng mẫu thử thích hợp ví dụ từ 2 g đến 10 g, chính xác đến mg, cho vào bình nón. Thêm một thể tích xác định từ 60 ml đến 200 ml dung dịch axit clohydric (4.6) hoặc dung dịch axit sulfuric (4.7). pH của dung dịch này không được lớn hơn pH = 2,0. Đậy nắp bình bằng mặt kính đồng hồ và hấp áp lực phần mẫu thử ở 121 °C trong 30 min hoặc làm nóng ở 100°C trong 60 min.
Dữ liệu từ nghiên cứu BCR cho thấy rằng có thể áp dụng một dải rộng các điều kiện đối với việc thủy phân bằng axit (nhiệt độ từ 95 °C đến 130 °C, thời gian từ 15 min đến 60 min). Nhiệt độ cao hơn thì thời gian chiết ngắn hơn.
6.2.2 Xử lý bằng enzym
Sau khi làm nguội đến nhiệt độ phòng, chỉnh pH của dịch chiết tối ưu cho hoạt động của enzym bằng dung dịch natri axetat (4.16) hoặc (4.17) và thêm một lượng thích hợp enzym hoặc hỗn hợp enzym (4.15) vào mẫu. Ủ hỗn hợp trong một khoảng thời gian và nhiệt độ tối ưu đối với enzym sử dụng. Sau khi làm nguội đến nhiệt độ phòng, dùng nước cất hoặc dung môi thích hợp khác để chuyển dung dịch vào bình định mức và pha loãng đến thể tích xác định (Vts).
Đối với mỗi enzym sử dụng, cần kiểm tra pH tối ưu, nhiệt độ ủ và thời gian ủ.
Để đảm bảo khử phosphoryl hóa tối ưu, bước xử lý bằng enzym cần được kiểm tra bằng cách phân tích các mẫu đã thêm thiamin monophosphat clorua (4.23.2) hoặc thiamin pyrophosphat clorua (4.23.3) và vật liệu tương tự với mẫu thử. Vật liệu này phải là mẫu chuẩn đã được chứng nhận.
Lượng thiamin có khả năng thêm vào từ enzym (4.15) cần được tính đến trong phần tính kết quả.
CHÚ THÍCH Để xác định dữ liệu về độ chụm trong Bảng B.1, Bảng B.2 và Bảng B.3, Taka-Diastase và Taka-Diastase kết hợp1) với β-amylase từ lúa mạch đã được sử dụng đã khử phosphoryl dưới các điều kiện sau đây. Dịch chiết đã được điều chỉnh đến pH = 4,0 và pH = 4,5 tương ứng, với dung dịch natri axetat (4.16) hoặc (4.17) và đã bổ sung 100 mg Taka-Diastase và 10 mg β-amylase trên gam mẫu. Hỗn hợp này được ủ ở 37 °C đến 45 °C trong 4 h đến 24 h, xem [5], [10] và [16].
6.2.3 Dung dịch mẫu thử
Lọc dung dịch mẫu (6.2.2) qua giấy lọc hoặc bộ lọc màng cỡ lỗ 0,45 µm, nếu cần. Cũng có thể sử dụng ly tâm. Đây là dung dịch mẫu thử dùng cho quá trình oxy hóa (6.3.2 hoặc 6.3.3).
6.3 Oxy hóa thiamin thành thiocrom
6.3.1 Yêu cầu chung
Oxy hóa có thể được thực hiện trước cột (6.3.2) hoặc sau cột (6.3.3).
6.3.2 Oxy hóa trước cột
6.3.2.1 Quy trình oxi hóa
Dùng pipet lấy 1 ml mẫu thử đã xử lý bằng enzym (6.2.3), dung dịch chuẩn (4.25.1) hoặc dung dịch trắng ví dụ dung dịch axit clohydric (4.6) hoặc dung dịch axit sulfuric (4.7) tùy thuộc vào việc sử dụng trong 6.2.1 cho vào bình cầu hoặc lọ thích hợp, thêm 1 ml dung dịch hexaxyanoferat kiềm (4.13). Lắc dung dịch mẫu thử trong thời gian quy định (ví dụ: 10 s), để yên trong khoảng thời gian quy định (ví dụ: 1 min).
Để loại bỏ các hợp chất gây nhiễu và bảo vệ cột HPLC thì nên trung hòa dung dịch mẫu thử (ví dụ bằng H3PO4) hoặc tiến hành làm sạch bằng chiết pha rắn (xem thêm thông tin trong [5]).
Lọc dung dịch qua màng lọc 0,45 µm. Dung dịch mẫu thử được bơm vào hệ thống HPLC pha đảo (6.3.2.2).
Cách khác, dung dịch đã oxy hóa có thể được chiết vào 1,5 ml isobutanol (4.2.3) và có thể bơm dịch chiết.
CHÚ THÍCH Việc chuyển hóa thiamin thành thiocrom có thể bị ức chế trong một số loại thực phẩm. Hiện tượng này thường gặp trong các thực phẩm chứa cacao, cũng có thể thấy trong một số thực phẩm khác. Nếu nghi ngờ có hiện tượng này thì nên kiểm tra độ thu hồi của phương pháp bằng cách xử lý dịch chiết mẫu bằng một thể tích thích hợp dung dịch chuẩn thiamin trước phản ứng oxy hóa.
6.3.2.2 Nhận dạng bằng HPLC sau khi oxy hóa trước cột
Bơm các thể tích thích hợp giống nhau các dung dịch chuẩn (6.3.2.1), mẫu và mẫu trắng vào hệ thống HPLC. Nhận dạng thiocrom bằng so sánh thời gian lưu của các pic riêng lẻ trong sắc ký đồ thu được từ dung dịch mẫu thử và dung dịch thử chuẩn. Việc thêm các chất chuẩn vào dung dịch mẫu thử cũng có thể nhận dạng được pic.
Việc tách và định lượng cho thấy thỏa đáng nếu thực hiện theo các điều kiện thực nghiệm sau đây (xem thêm Hình A.1 và Phụ lục C về các điều kiện HPLC thay thế và ví dụ về sắc kí đồ).
| Pha tĩnh: | Lichrospher® RP Select B, 5 µm, 250 mm x 4,0 mm |
| Pha động: | 40 phần thể tích metanol (4.1) và 60 phần thể tích đệm axetat (4.22) |
| Tốc độ dòng: | 0,7ml/min |
| Thể tích bơm: | 20 µl |
| Dertector: | Huỳnh quang; bước sóng kích thích là 366 nm; bước sóng phát xạ là 435 nm. |
6.3.3 Trường hợp ôxy hóa sau cột
6.3.3.1 Quy trình oxi hóa
Oxy hóa thiamin thành thiocrom sử dụng phản ứng sau cột với dung dịch kali hexaxyanoferat kiềm III (4.14). Thêm liên tục (ví dụ: 0,3 ml/min) thuốc thử dẫn xuất qua ống nối kiểu chữ T cho vào dịch rửa giải HPLC để tạo thành thiocrom.
CHÚ THÍCH Việc oxy hóa sau cột bị ảnh hưởng ví dụ bởi nồng độ natri hydroxit. Các nồng độ cao hơn trong dung dịch dẫn xuất có thể được bù bởi tốc độ bơm thấp hơn và ngược lại.
6.3.3.2 Nhận dạng bằng HPLC sau oxy hóa sau cột
Bơm các thể tích thích hợp giống nhau của các chuẩn thiamin chlorua hydrochlorua (4.23.1) cũng như các dung dịch mẫu (6.2.3) vào hệ thống HPLC. Xác định thiamin bằng cách so sánh thời gian lưu của các pic riêng trong sắc ký đồ thu được với dung dịch mẫu thử và với chuẩn (4.23.1). Thêm thiamin chlorua hydrochlorua vào dung dịch mẫu thử cũng có thể nhận diện pic.
Việc tách và định lượng được cho thấy là thỏa đáng nếu tuân theo các điều kiện thí nghiệm sau (xem Phụ lục C và Hình A.2 đối với các hệ thống HPLC thay thế và các ví dụ về sắc ký đồ).
| Pha tĩnh: | Supelco® LC-18-DB, 5 µm, 250 mm x 4,6 mm |
| Pha động: | Metanol (4.2.1): đệm phosphat (4.2.19), chứa 1 g/l tetraetylamoni-clorua (4.2.20) và 5 mmol/l natri heptanesulfonat (4.2.21), (35:65) |
| Tốc độ dòng: | 1,0 ml/min |
| Thể tích bơm: | 20 µl |
| Thuốc thử sau cột: | dung dịch kali hexaxyanoferat III kiềm (4.2.14) |
| Tốc độ dòng thuốc thử: | 0,3 ml/min |
| Detector: | huỳnh quang; bước sóng kích thích là 368 nm; bước sóng phát xạ là 440 nm. |
CHÚ THÍCH Việc phân tích một số mẫu, ví dụ như thịt lợn nguyên liệu có thể có thêm pic của 2(1-hydroxyetyl) thiamin trong sắc ký đồ xem Phụ lục D.
6.4 Phép xác định
Tiến hành xác định bằng ngoại chuẩn sử dụng tích phân diện tích pic (nếu có thể) hoặc xác định chiều cao pic (tùy chọn) của mẫu và so sánh các kết quả với các giá trị tương ứng đối với thiocrom bằng cách sử dụng đường chuẩn. Kiểm tra độ tuyến tính của việc hiệu chuẩn.
7 Tính kết quả
Sử dụng đường chuẩn hoặc sử dụng chương trình thích hợp của bộ tích phân hoặc sử dụng quy trình đã đơn giản hóa dưới đây. Tính khối lượng vitamin B1, w, biểu thị theo thiamin clorua hydroclorua, bằng mg/100 g mẫu, sử dụng Công thức (2):
![]()
Trong đó
| Ats | là diện tích pic hoặc chiều cao pic của thiocrom thu được với dung dịch mẫu thử, tính bằng đơn vị chiều cao hoặc diện tích; |
| Ast | là diện tích pic hoặc chiều cao pic của thiocrom thu được với dung dịch thử chuẩn, tính bằng đơn vị chiều cao hoặc diện tích; |
| Vts | là thể tích dung dịch mẫu thử (6.2.2), tính bằng mililit (ml); |
| ρ | là nồng độ khối lượng của thiamin clorua hydroclorua trong dung dịch chuẩn (4.25.1), tính bằng microgam trên mililit (µg/ml); |
| ms | là khối lượng mẫu, tính bằng gam (g) (6.2.1); |
| 100 | là hộ số để tính hàm lượng trên 100 g; |
| 1000 | là hệ số chuyển đổi µg/100 g thành mg/100 g. |
Báo cáo kết quả vitamin B1 bằng mg/100 g được biểu thị theo thiamin clorua hydroclorua (M = 337,28). Nếu cần phải biểu thị kết quả theo thiamin (C12H17N4OS, M = 265,37) thì nhân kết quả với hệ số 0,787, theo thiamin clorua (C12H17ClN4OS, M = 300,82) thì nhân kết quả với hệ số 0,892.
8 Độ chụm
8.1 Yêu cầu chung
Dữ liệu về độ chụm của phương pháp này dựa trên các phương pháp HPLC khác nhau áp dụng để xác định thiamin trong nghiên cứu so sánh quốc tế được tổ chức bởi Chương trình của Ủy ban Châu Âu về Thử nghiệm và Đo chuẩn thực hiện trên mẫu bột mì (CRM 121)/ sữa bột/sữa bột sấy phun (CRM 421), rau hỗn hợp đông khô (CRM 485) và gan lợn đông lạnh (CRM 487). Nghiên cứu cung cấp thông tin thống kê nêu trong Phụ lục B, Bảng B.1. Hơn nữa, dữ liệu về độ chụm bao gồm các kết quả nghiên cứu cộng tác của Pháp đối với mẫu thức ăn dùng bằng đường xông, thức ăn trẻ em bổ sung rau, sữa bột, thức ăn bổ sung hoa quả, men, ngũ cốc, bột sô cô la và thực phẩm bổ sung. Kết quả của nghiên cứu này được nêu trong Phụ lục B, Bảng B.2 và Bảng B.3.
8.2 Độ lặp lại
Chênh lệch tuyệt đối giũa hai kết quả thử riêng rẽ, thu được khi tiến hành trên vật liệu thử giống hệt nhau, do một người thực hiện, sử dụng cùng thiết bị, trong một khoảng thời gian ngắn, không quá 5 % các trường hợp vượt quá giới hạn lặp lại r.
Các giá trị đối với thiamin clorua hydroclorua là:
| Bột mì nguyên cám |
| r = 0,043 mg/100 g |
| Sữa bột/sữa bột sấy phun |
| r = 0,071 mg/100 g |
| Rau hỗn hợp đông khô |
| r = 0,039 mg/100 g |
| Gan lợn đông lạnh |
| r = 0,088 mg/100 g |
| Thức ăn dùng bằng đường xông |
| r = 0,02 mg/100 g |
| Thức ăn cho trẻ có bổ sung rau |
| r = 0,05 mg/100 g |
| Sữa bột |
| r = 0,1 mg/100 g |
| Thức ăn có bổ sung hoa quả |
| r = 0,2 mg/100 g |
| Nấm |
| r = 0,34 mg/100 g |
| Ngũ cốc |
| r = 0,16 mg/100 g |
| Ngũ cốc |
| r = 0,49 mg/100 g |
| Bột socola |
| r = 0,36 mg/100 g |
| Thực phẩm bổ sung |
| r = 111 mg/100 g |
8.3 Độ tái lập
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ, thu được khi tiến hành trên vật liệu thử giống hệt nhau được phân tích bởi hai phòng thử nghiệm, không quá 5 % các trường hợp vượt quá giới hạn tái lập R.
Các giá trị đối với thiamin clorua hydroclorua là:
| Bột mì nguyên cám |
| R = 0,190 mg/100 g |
| Sữa bột sữa bột sấy phun |
| R = 0,243 mg/100 g |
| Rau hỗn hợp đông khô |
| R = 0,178 mg/100 g |
| Gan lợn đông lạnh |
| R = 0,623 mg/100 g |
| Thức ăn dùng bằng đường xông |
| R = 0,1 mg/100 g |
| Thức ăn cho trẻ có bổ sung rau |
| R = 0,12 mg/100 g |
| Sữa bột |
| R = 0,25 mg/100 g |
| Thức ăn có bổ sung hoa quả |
| R = 0,55mg/100 g |
| Nấm |
| R = 0,48 mg/100 g |
| Ngũ cốc |
| R = 0,75 mg/100 g |
| Ngũ cốc |
| R = 1,16 mg/100 g |
| Bột socola |
| R = 0,8 mg/100 g |
| Bột socola |
| R = 0,8 mg/100 g |
| Thực phẩm bổ sung |
| R = 212 mg/100 g |
9 Báo cáo thử nghiệm
Báo cáo thử nghiệm nên phù hợp với TCVN/ISO/IEC 17025 và ít nhất bao gồm các thông tin sau:
a) mọi thông tin cần thiết để nhận biết đầy đủ về mẫu;
b) phương pháp thử đã sử dụng hoặc viện dẫn tiêu chuẩn này;
c) ngày và thời gian lấy mẫu (nếu biết);
d) ngày nhận mẫu;
e) ngày thử nghiệm;
f) kết quả và các đơn vị kết quả biểu thị;
g) bất kỳ điểm đặc biệt nào quan sát được trong quá trình thử nghiệm;
h) mọi chi tiết thao tác không quy định trong tiêu chuẩn này, hoặc tùy ý lựa chọn cùng với các có thể ảnh hưởng tới kết quả.
Phụ lục A
(tham khảo)
Các ví dụ về sắc đồ HPLC
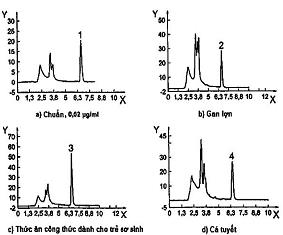
CHÚ DẪN
| Y | Huỳnh quang |
| X | Thời gian (min) |
| 1 | thiamin trong chuẩn, 0,02 µg/ml ở 6,620 min |
| 2 | thiamin trong gan lợn ở 6,616 min |
| 3 | thiamin trong thức ăn công thức dành cho trẻ sơ sinh ở 6,619 min |
| 4 | thiamin trong cá tuyết ở 6,614 min |
| Pha tĩnh: | Gemini C18, 5 µm, 250 mm x 4,6 mm (110 A) |
| Pha động: | Metanol (4.1): nước pH 9 (40:60) |
| Tốc độ dòng: | 0,8 ml/min |
| Thể tích bơm: | 20 µl |
| Detector: | Huỳnh quang: bước sáng kích thích là 366 nm; bước sóng phát xạ là 435 nm. |
Hình A1 - Ví dụ về tách thiamin bằng HPLC theo chuẩn thiocrom sử dụng dẫn xuất trước cột
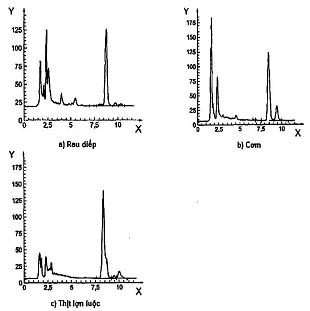
CHÚ DẪN
| Y | Huỳnh quang |
| X | thời gian (min) |
| Pha tĩnh: | Purospher® RP C18, được đậy nắp ở cuối, 5 µm, 250 mm x 4,6 mm |
| Pha động: | Metanol (4.1): đệm phosphat, pH 3,5, c(NH4H2PO4) = 10 mmol/l, chứa 1 g/l tetraetylamoniclorua (420) và 5 mmol/l natri heptanesulfonat (4.21), (35:70) |
| Tốc độ dòng: | 1,5 ml/min |
| Thể tích bơm: | 3 µl |
| Thuốc thử sau cột: | dung dịch kali hexaxyanoferat III kiềm (4.14) |
| Tốc độ dòng thuốc thử: | 0,3 ml/min |
| Detector: | Huỳnh quang: bước sóng kích thích là 365 nm; bước sóng phát xạ là 435 nm. |
CHÚ THÍCH Sắc ký đồ bổ sung đối với thịt/gan nêu trong Phụ lục D
Hình A.2 - Ví dụ về tách chuẩn thiamin bằng HPLC sử dụng dẫn xuất sau cột trong rau diếp (a), cơm (b) và thịt lợn luộc (c)
Phụ lục B
(tham khảo)
Dữ liệu về độ chụm
Theo những chỉ dẫn nghiên cứu chứng nhận EU SMT, các dữ liệu đưa ra trong Bảng B.1 đã được xác định trong một phép thử liên phòng thử nghiệm [10]. Viện nghiên cứu thực phẩm, Norwich, UK thay mặt cho Ủy ban EU tham gia nghiên cứu này. Các dữ liệu đưa ra trong Bảng B.2 và Bảng B.3 đã được xác định trong một phép thử liên phòng thử nghiệm của Pháp [5].
Bảng B.1 - Dữ liệu về độ chụm đối với bột mì thô, sữa bột/sữa bột sấy phun, rau hỗn hợp đông khô và gan lợn đông khô
| Mẫu | CRM 121 Bột mì thô | CRM 421 Sữa bột/sữa bột sấy phun | CRM 485 Rau hỗn hợp đông khôa | CRM 487 Gan lợn đông khô |
| Năm thử nghiệm liên phòng | 1996 | 1996 | 1996 | 1996 |
| Số phòng thử nghiệm | 13 | 14 | 12 | 15 |
| Số lượng mẫu | 2 | 2 | 2 | 2 |
| Số lượng phòng thử nghiệm còn lại sau khi trừ ngoại lệ | 13 | 14 | 12 | 15 |
| Số ngoại lệ | 0 | 0 | 0 | 0 |
| Số kết quả được chấp nhận | 65 | 70 | 58 | 72 |
| Giá trị trung bình | 0,452 | 0,645 | 0,295 | 0,807 |
| Độ lệch chuẩn lặp lại, sr, mg/100 g | 0,015 | 0,025 | 0,012 | 0,031 |
| Hệ số biến thiên lặp lại, % | 3,2 | 3,8 | 4,2 | 3,9 |
| Giá trị lặp lại r [r = 2,83 x sr], mg/100 g | 0,043 | 0,071 | 0,039 | 0,088 |
| Độ lệch chuẩn tái lập, sR, mg/100 g | 0,053 | 0,085 | 0,063 | 0,182 |
| Hệ số biến thiên tái lập, % | 11,8 | 13,2 | 13,3 | 22,6 |
| Giá trị tái lập R [R = 2,83 x sR], mg/100g | 0,190 | 0,243 | 0,178 | 0,623 |
| Giá trị HorRat, theo [13] | 0,9 | 1,1 | 1,0 | 1,9 |
| a Hỗn hợp của ngô ngọt, cà rốt và cà chua khô (10:1:1) | ||||
CHÚ THÍCH Dữ liệu thu được trong nghiên cứu so sánh quốc tế này đã được tạo ra bằng cách sử dụng các phương pháp đã được xác định giống với các quy trình kiểm định định kỳ tại nhà của các phòng thí nghiệm tham gia với các hệ thống HPLC được mô tả trong Phụ lục C.
Bảng B.2 - Dữ liệu về độ chụm đối với thức ăn dùng bằng đường xông, thức ăn cho trẻ em bổ sung rau, sữa bột, thức ăn bổ sung hoa quả và nấm
| Mẫu | Dung dịch thức ăn trong chai | Thức ăn cho trẻ em | Sữa bột | Bột trộn trái cây | Nấm |
| Năm nghiên cứu | 1995 | 1995 | 1995 | 1995 | 1995 |
| Số phòng thử nghiệm | 10 | 10 | 10 | 10 | 10 |
| Số lượng mẫu | 1 | 1 | 1 | 1 | 1 |
| Số lượng phòng thử nghiệm còn lại sau khi trừ ngoại lệ | 8 | 10 | 10 | 10 | 10 |
| Số ngoại lệ | 2 | 0 | 0 | 0 | 0 |
| Số kết quả được chấp nhận | 16 | 20 | 20 | 20 | 20 |
| Giá trị trung bình | 0,11 | 0,20 | 0,56 | 1,04 | 1,31 |
| Độ lệch chuẩn lặp lại, sr, | 0,01 | 0,02 | 0,04 | 0,07 | 0,12 |
| Hệ số biến thiên lặp lại, % | 7 % | 8 % | 7 % | 7 % | 9 % |
| Giá trị lặp lại r [r = 2,83 x sr], mg/100 g | 0,02 | 0,05 | 0,1 | 0,2 | 0,34 |
| Độ lệch chuẩn tái lập, sR, mg/100 g | 0,04 | 0,04 | 0,08 | 0,19 | 0,17 |
| Hệ số biến thiên tái lập | 32 % | 21 % | 16 % | 19 % | 13 % |
| Giá trị tái lập R [R = 2,83 x sR], mg/100 g | 0,1 | 0,12 | 0,25 | 0,55 | 0,48 |
| Giá trị HorRat, theo [13] | 1,0 | 1,5 | 1,3 | 1,7 | 1,2 |
Bảng B.3 - Dữ liệu về độ chụm đối với ngũ cốc, bột sôcôla và thức ăn bổ sung
| Mẫu | Ngũ cốc | Ngũ cốc | Bột sôcôla | Thức ăn bổ sung |
| Năm nghiên cứu | 1995 | 1995 | 1995 | 1995 |
| Số phòng thử nghiệm | 10 | 10 | 10 | 10 |
| Số lượng mẫu | 1 | 1 | 1 | 1 |
| Số lượng phòng thử nghiệm còn lại sau khi trừ ngoại lệ | 9 | 9 | 9 | 9 |
| Số ngoại lệ | 1 | 1 | 1 | 1 |
| Số kết quả được chấp nhận | 18 | 18 | 18 | 18 |
| Giá trị trung bình | 1,42 | 2,95 | 1,55 | 486 |
| Độ lệch chuẩn lặp lại, sr | 0,06 | 0,18 | 0,13 | 39 |
| Hệ số biến thiên lặp lại | 4 % | 6 % | 8 % | 8 % |
| Giá trị lặp lại r [r = 2,83 x sr], mg/100 g | 0,16 | 0,49 | 0,36 | 111 |
| Độ lệch chuẩn tái lập, sR, mg/100 g | 0,27 | 0,41 | 0,28 | 75 |
| Hệ số biến thiên tái lập | 19 % | 14 % | 19 % | 15 % |
| Giá trị tái lập R [R = 2,83 x sR], mg/100g | 0,75 | 1,16 | 0,8 | 212 |
| Giá trị HorRat, theo [13] | 1,8 | 1,5 | 1,8 | 3,4 a |
| a Năm 1980, Horwitz et al, xuất bản đánh giá của 1000 so sánh liên phòng. Từ những nghiên cứu này, kết luận rằng giá trị HorRat là 1, với giới hạn chấp nhận được trong khoảng 0,5 đến 2,0, cho thấy độ chính xác liên phòng là phù hợp. Sự tương ứng trong độ lệch chuẩn tương đối của phòng thí nghiệm cho thấy khoảng một nửa đến hai phần ba so với độ lệch chuẩn tương đối giữa các phòng thí nghiệm. Độ lệch liên tục từ tỷ lệ ở mặt dưới (giá trị < 0,3 hoặc 0,5) có thể cho thấy mức trung bình không được báo cáo hoặc được đào tạo tốt và có kinh nghiệm. | ||||
Phụ lục C
(tham khảo)
Hệ thống HPLC thay thế
Việc tách và định lượng được chứng minh là thích hợp nếu áp dụng các điều kiện về sắc ký như sau [10]:
Bảng C.1 - Điều kiện HPLC thay thế
| Pha tĩnh | Kích thước cột mm x mm | Pha động (V:V) | Sự tách sóng (Ex/Em) nm | Lưu lượng ml/min | Kiểu oxi hóa |
| Radial silica ® 10 µm | 250 x 4,6 | Etanol: dung dịch đệm phosphat pH = 7,4 c(K2HPO4) = 0,1 mol/l (50:50) | F: 365/435 | 3,0 | PCa |
| Supelco ® LC-18-DB 5 µm | 250 x 4,6 | Metanol: dung dịch đệm phosphat pH = 3,5 c(K2HPO4) = 9 mmol/l chứa tetraetylamoniumclorua, ρ(C8H20NCl) = 1 g/l và natri heptansulfonat, c(C7H15NaO3S) = 5 mmol/l (35:65) | F: 368/420 | 1,0 | PC |
| Lichrospher ® RP 18 5 µm | 250 x 4,6 | Metanol:natri haxansulfonat, c(C6H13NaO3S.H2O) = 1 mmol/l, pH = 3,0 (70:30) | F: 375/435 | 1,5 | PC |
| Eurospher ® 100 -C18 5 µm | 250 x 4,6 | Natri dihydrophosphat, c(NaH2PO4) = 10 mmol/l): natri perclorat, c(NaClO4) = 0,15 mol/l (50:50) | F: 375/435 | 1,0 | PC |
| Lichrospher ® RP Select B 5 µm | 250 x 4,6 | Metanol:dung dịch đệm axetat pH = 4,0, c(CH3COONa) = 50 mmol/l (40:60) | F: 366/435 | 0,7 | PRCb |
| µ-Bondapak ® radial C18 5 µm | 250 x 4,6 | Metanol:dung dịch đệm axetat pH= 4,5, c(CH3COONa) = 0,5 mml/l (40:60) | F: 366/435 | 0,8 | PRC |
| Spherisorb ® ODS2 5 µm | 250 x 4,6 | Metanol:dung dịch đệm phosphat pH = 4,0, c(KH2PO4) = 0,1 mol/l (70:30) | F: 375/435 | 1,0 | PRC |
| Lichrospher ® RP 18 10 µm | 250 x 4,6 | Kali dihydrophosphat, c(KH2PO4) = 10 mmol/l/dimetyl formamit (80:20) | F: 368:440 | 1,5 | PRC |
| Hamilton ® PRP-1 5 µm | 150 x 4,6 | Metanol:nước (40:60); pH được điều chỉnh tới 4,5 bằng axit axetic | F: 366/435 | 1,0 | PRC |
| Hamiton ® PRP-1 5 µm | 150 x 4,1 | Metanol:nước (35:65); pH = 9,0 được điều chỉnh bằng amoniac, w(NH3) = 25% | F: 366/435 | 1,0 | PRC |
| Hypersil ® NH2APS 2 5 µm | 250 x 4,6 | Diclometan/metanol (95:5) | F: 365/440 | 1,0 | PRC |
| a PC = Dẫn xuất sau cột. b PRC = Dẫn xuất trước cột. | |||||
Phụ lục D
(tham khảo)
Hợp chất vitamin B1: 2-(1-hydroxyetyl)thiamin (HET) thực hiện dẫn xuất sau cột
Thông thường, hàm lượng vitamin B1 được coi là thiamin và các dẫn xuất phosphat của nó. Tuy nhiên, việc sử dụng phương pháp dẫn xuất sau cột có thể cho thấy hai pic cho thiamin và xác nhận chất chuyển hóa phụ 2- (1-hydroxyetyl) thiamin (HET) đã được hiển thị, xem [11] và [12] và xem hình D.1. Nếu sử dụng kỹ thuật dẫn xuất trước cột, thì hai hợp chất thiamin và HET đồng rửa giải
Hàm lượng tương đối của HET được so sánh với thiamin phụ thuộc vào loại mẫu. Hàm lượng HET trong thịt và gan là 7% đến 23% hàm lượng thiamin. Trong nấm men, hàm lượng 3,8 %, trong khi ở bắp cải trắng, bông cải xanh, bột yến mạch, thức ăn công thức dành cho trẻ sơ sinh, sữa bột, bột sữa và bột mì, hàm lượng không dưới 2 %, xem [7].
Phép xác định định lượng vitamin B1 trong thực phẩm bằng dẫn xuất sau cột được khuyến nghị bao gồm việc xác định định lượng riêng thiamin và HET khi phân tích các mẫu thịt và để kiểm tra các mẫu khác cho sự xuất hiện của HET trên sắc ký đồ.
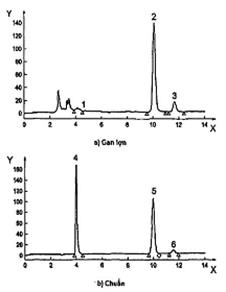
CHÚ DẪN
Y huỳnh quang
X thời gian (min)
1 thiamin mono phosphat(TMP) trong gan lợn ở 4,034 min
2 thiamin trong gan lợn ở 10,138 min
3 2-(1-Hydroxy Etyl) Thiamin (HET) trong gan lợn ở 11,741 min
4 TMP trong chuẩn 4,034 min
5 thiamin trong chuẩn ở 10,044 min
6 HET trong chuẩn ở 11,613 min
CHÚ THÍCH Thông tin về HPLC nêu trong [7].
Hình D.1 - Sắc ký đồ của chất chiết CRM 487 gan lợn (a) và chuẩn 0,1 µg/ml TMP (thiamin mono phosphat), 0,1 µg/ml thiamin và 0,01 µg/ml HET (2-(1-hydroxyetyl)thiamin) (b)
Thư mục tài liệu tham khảo
[1] BOGNAR A. Bestimmung von Riboflavin und Thiamine in Lebensmitteln mit Hilfe der Hochleistungsflussigkeitschromatographie (HPLC). Dtsch. Lebensmitt. Rundsch. 1981, 77 pp. 431-436
[2] HASSELMANN C., FRANCK D., GRIMM P., DIOP P.A., SOULES C. High-performance liquid chromatographic analysis of thiamine and riboflavin in dietetic foods. J. Micronutr. Anal. 1989, 5 pp. 269-279
[3] BOGNAR A. Determination of vitamin B1 in food by High-Performance-Liquid-Chromatography and postcolumn derivatization. FreseniusJ. Anal. Chem. 1992, 343 pp. 155-156
[4] HAGG M., KUMPULAINEN J. Thiamine and riboflavin contents in domestic and imported cereal products in Finland. J. Food Compos. Anal. 1993, 6 pp. 299-306
[5] ARELLA F., LAH£LY S., BOURGUIGNON J.B., HASSELMANN C. Liquid chromatographic determination of vitamin B1 and B2 in foods. A collaborative study. Food Chem. 1996, 56 pp. 81-86
[6] EITENMILLER R.R., LANDEN W.O. Vitamin Analysis for the Health and Food Sciences. CRC Press, Boca Raton, London, New York, Washington, D.C., 1999, pp. 271-97.
[7] JAKOBSEN J. Optimisation of the determination of thiamin, 2-(1-hydroxyethyl)thiamine, riboflavin in food samples by use of HPLC. Food Chem. 2008, 106 pp. 1209-1217
[8] DAWSON R.M.C., ELLIOTT D.C., ELLIOT W.H., JONES K. Data for Biochemical Research. Oxford Science Publication 3rd. ISBN 0 19 855299 8,1989
[9] HAGG M. Effect of various commercially available enzymes in the liquid chromatographic determination with external standardization of thiamine and riboflavin in foods. J. AOAC Int. 1994, 77 pp. 681-686
[10] FINGLAS P.M., SCOTT K.J., WTTTHOFT C.M., VAN DEN BERG H., DE FROIDMONT-GORTZ I. The certification of the mass fractions of vitamins in four reference materials: Wholemeal flour (CRM 121), milk powder (CRM 421), lyophilised mixed vegetables (CRM 485) and lyophilised pig’s liver (CRM 487). EUR-report 18320. Office for Official Publications of the European Communities, Luxembourg, 1999
[11] TAKASHI U., YUKIKO T., KOHEI M., MARI T., KANAME K. Simultaneous determination of 2(1-hydroxyethyl)thiamine and thiamine in foods by high performance liquid chromatography with post-column derivatisation. Vitamins (Japan). 1990, 64 pp. 379-385
[12] TAKASHI U., YUKIKO T., KOHEI M., MASAKO M., KANAME K. Distribution and stability of 2(1-hydroxyethyl)thiamine and thiamine in foods. Vitamins (Japan). 1991,65 pp. 249-256
[13] HORWITZ W., ALBERT R. The Horwitz Ratio (HorRat): A useful Index of Method Performance with Respect to Precision. J. AOAC Int. 2006, 89 pp. 1095-1109
[14] THOMPSON M. Recent trends in inter-laboratory precision at ppb and sub-ppb concentrations in relation to fitness for purpose criteria in proficiency testing. Analyst (Lond.). 2000,125 pp. 385-386
[15] HORWITZ W., KAMPS L.R., BOYER K.W. Quality assurance in the analysis of foods and trace constituents. J. AOAC Int. 1980, 63 pp. 1344-1354
[16] OLLILAINEN V., FINGLAS P.M., VAN DEN BERG H., DE FROIDMONT-GORTZ I. Certification of B-Group Vitamins (B1, B2, B6, and B12) in Four Food Reference Materials. J. Agric. Food Chem. 2001,49 pp. 315-321
[17] TCVN ISO/IEC 17025:2007 (ISO/IEC 17025:2005), Yêu cầu chung về năng lực của phòng thử nghiệm và hiệu chuẩn
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 5164:2018 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 5164:2018 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 5164:2018 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 5164:2018 DOC (Bản Word)