- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 13269:2021 Gạo, hạt hồ tiêu - Xác định dư lượng thuốc bảo vệ thực vật nereistoxin bằng kỹ thuật sắc ký lỏng ghép khối phổ LC-MS/MS
| Số hiệu: | TCVN 13269:2021 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
06/08/2021 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 13269:2021
Tiêu chuẩn Quốc gia TCVN 13269:2021 về Xác định Dư lượng Thuốc Bảo vệ Thực vật Nereistoxin
Ngày 06/08/2021, Cục Bảo vệ thực vật đã biên soạn Tiêu chuẩn Quốc gia TCVN 13269:2021 quy định phương pháp phân tích dư lượng thuốc bảo vệ thực vật nereistoxin trong gạo và hạt hồ tiêu bằng kỹ thuật sắc ký lỏng ghép khối phổ LC-MS/MS. Tiêu chuẩn này có hiệu lực ngay sau khi công bố.
Tiêu chuẩn này áp dụng cho việc xác định dư lượng thuốc bảo vệ thực vật nereistoxin và các dẫn xuất của nó như cartap, thiocyclam, và thiosultap trong gạo và hạt hồ tiêu. Giới hạn định lượng (LOQ) của phương pháp là 0,01 mg/kg.
Phương pháp và Nguyên tắc Phân tích
Mẫu được chiết xuất bằng dung dịch axit formic 2% và axetonitril với tỷ lệ 1:1, sau đó ly tâm để tách pha. Dịch chiết được phân tích bằng kỹ thuật LC-MS/MS để xác định nồng độ dư lượng thuốc bảo vệ thực vật.
Chuẩn bị Mẫu và Dung Dịch Chuẩn
Mẫu thu thập cần đảm bảo nguyên trạng và đại diện. Mẫu gạo và hồ tiêu được làm lạnh và nghiền trước khi phân tích. Dung dịch chuẩn được chuẩn bị từ các chất chuẩn thuốc bảo vệ thực vật với nồng độ 1.000 μg/ml và phân chia thành nhiều nồng độ khác nhau để thực hiện các phép thử.
Thiết bị và Dụng Cụ Sử Dụng
Thiết bị chính bao gồm máy LC-MS/MS, cột sắc ký và các dụng cụ hỗ trợ như máy nghiền mẫu, tủ lạnh, cân phân tích và bể siêu âm.
Đánh giá Kết quả và Độ thu hồi
Kết quả phân tích được đánh giá dựa trên độ lệch thời gian lưu và tỷ lệ các ion trong mẫu so với dung dịch chuẩn. Độ thu hồi trung bình của phương pháp dao động từ 79% đến 106% tùy thuộc vào từng hoạt chất. Báo cáo thử nghiệm cần ghi rõ thông tin về mẫu, phương pháp thử và kết quả tính bằng miligam trên kilôgam (mg/kg).
Phụ lục
Tiêu chuẩn bao gồm các phụ lục cung cấp thông tin về cấu trúc hóa học và trọng lượng mol của các hoạt chất thuốc bảo vệ thực vật như cartap, thiocyclam, nereistoxin và thiosultap, cùng với bảng số liệu về độ thu hồi theo từng nồng độ mẫu.
Tiêu chuẩn TCVN 13269:2021 là căn cứ quan trọng cho việc đảm bảo an toàn thực phẩm liên quan đến dư lượng thuốc bảo vệ thực vật trong nông sản và cung cấp phương pháp chuẩn hóa cho các phòng thí nghiệm phân tích trong nước.
Tải tiêu chuẩn Việt Nam TCVN 13269:2021
TIÊU CHUẨN QUỐC GIA
TCVN 13269:2021
GẠO, HẠT HỒ TIÊU - XÁC ĐỊNH DƯ LƯỢNG THUỐC BẢO VỆ THỰC VẬT NEREISTOXIN BẰNG KỸ THUẬT SẮC KÝ LỎNG GHÉP KHỐI PHỔ LC-MS/MS
Rice, peper - Determination nereistoxin residue by liquid chromatography mass spectrometry LC-MS/MS
Lời nói đầu
TCVN 13269:2021 do Cục Bảo vệ thực vật biên soạn, Bộ Nông nghiệp và Phát triển Nông thôn đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
GẠO, HẠT HỒ TIÊU - XÁC ĐỊNH DƯ LƯỢNG THUỐC BẢO VỆ THỰC VẬT NEREISTOXIN BẰNG KỸ THUẬT SẮC KÝ LỎNG GHÉP KHỐI PHỔ LC-MS/MS
Rice, peper - Determination nereistoxin residue by liquid chromatography mass spectrometry LC-MS/MS
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp phân tích dư lượng thuốc bảo vệ thực vật nereistoxin và các dẫn xuất: cartap, nereistoxin, thiocyciam và thiosultap trong gạo, hạt hồ tiêu bằng kỹ thuật sắc ký lỏng ghép khối phổ LC-MS/MS (xem Phụ lục A).
Giới hạn định lượng (LOQ) của phương pháp là 0,01 mg/kg.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau đây là cần thiết để áp dụng tiêu chuẩn này. Đối với tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851:1989 (ISO 3696-1987) Nước dùng để phân tích trong phòng thí nghiệm - Yêu cầu kỹ thuật và phương pháp thử.
3 Nguyên tắc
Mẫu đã đồng nhất được chiết bằng dung dịch axit formic 2 % và axetonitril theo tỷ lệ thể tích là 1:1, sau đó tách pha bằng cách ly tâm. Dịch chiết sau cùng được xác định bằng kỹ thuật sắc ký lỏng ghép khối phổ hai lần (LC-MS/MS).
4 Thuốc thử
Trong quá trình phân tích chỉ sử dụng các hóa chất, thuốc thử thuộc loại tinh khiết phân tích, trừ khi có quy định khác.
4.1 Nước, H2O, khử ion.
4.2 Axetonitril, CH3CN, loại dùng cho LC-MS.
4.3 Axit formic, HCOOH, 98 %.
4.4 Axit axetic băng, CH3COOH, 99 %.
4.5 Amoni axetat, CH3COONH4.
4.6 Dung dịch axit formic 1 %
Dùng micropipet (5.11) lấy 1 ml axit formic (4.3) cho vào bình định mức 100 ml (5.15) chứa sẵn khoảng 50 ml nước (4.1), định mức đến vạch và lắc đều.
4.7 Dung dịch axit formic 2 %
Dùng micropipet (5.11) lấy 2 ml axit formic (4.3) cho vào bình định mức 100 ml (5.15) chứa sẵn khoảng 50 ml nước (4.1), định mức đến vạch và lắc đều.
4.8 Dung dịch amoni axetat 5 mmol/l và axit axetic 0,1 %
Cân 0,38 g amoni axetat (4.5) vào bình định mức 1 000 ml (5.15), thêm khoảng 200 ml nước (4.1), thêm 1 ml axit axetic băng (4.4), định mức tới vạch bằng nước (4.1), lắc kỹ, siêu âm 15 min.
4.9 Các chất chuẩn thuốc bảo vệ thực vật: cartap hydrochloride, nereistoxin oxalate, thiocyclam hydrogenoxalate và thiosultap monosodium, đã biết trước hàm lượng.
CHÚ THÍCH: Một số chất chuẩn được bán dưới dạng muối. Hệ số chuyển đổi giữa chất chuẩn được bán và hoạt chất phân tích xem Bảng 1.
Bảng 1 - Hệ số chuyển đổi giữa chất chuẩn được bán và hoạt chất phân tích
| Hoạt chất phân tích | Khối lượng mol phân tử g/mol | Chất chuẩn được bán | Khối lượng mol phân tử g/mol | Hệ số chuyển đổi |
| Cartap | 237,3 | Cartap hydrochloride | 273,8 | 0,87 |
| Nereistoxin | 149,3 | Nereistoxin oxalate | 239,0 | 0,62 |
| Thiocyclam | 181,4 | Thiocyclam hydrogenoxalate | 271,4 | 0,67 |
| Thiosultap | 311,4 | Thiosultap monosodium | 333,4 | 0,93 |
4.10 Các dung dịch chuẩn gốc thuốc bảo vệ thực vật, nồng độ 1 000 μg/ml
Cân chính xác từng chất chuẩn thuốc bảo vệ thực vật (4.9) bằng cân phân tích (5.4) vào các bình định mức dung tích 10 ml (5.15) sao cho lượng hoạt chất phân tích khoảng 0,01 g, hòa tan và định mức đến vạch bằng dung dịch axit formic 1 % (4.6) và lắc đều.
CHÚ THÍCH: Nồng độ dung dịch chuẩn gốc đã được hiệu chỉnh dựa vào độ tinh khiết, lượng cân thực tế, hệ số chuyển đổi giữa chất chuẩn được bán và hoạt chất phân tích.
Dung dịch chuẩn gốc sau khi chuẩn bị xong được bảo quản ở nhiệt độ (4 ± 2) °C và có thời hạn sử dụng không quá 1 tháng.
4.11 Dung dịch chuẩn trung gian, nồng độ 10 μg/ml
Dùng micropipet (5.11) lấy 100 μl từng dung dịch chuẩn gốc (4.10) cho vào bình định mức dung tích 10 ml (5.15), định mức đến vạch bằng dung dịch axit formic 1 % (4.6) và lắc đều.
Dung dịch chuẩn trung gian được chuẩn bị ngay trước khi sử dụng.
4.12 Dung dịch chuẩn làm việc, nồng độ 0,1 μg/ml và 1 μg/ml
Dùng micropipet (5.11) lấy lần lượt 100 μl và 1 000 μl dung dịch chuẩn trung gian (4.11) cho vào hai bình định mức dung tích 10 ml (5.15), định mức đến vạch bằng dung dịch axit formic 1 % (4.6) và lắc đều, thu được dung dịch chuẩn làm việc có nồng độ tương ứng là 0,1 μg/ml và 1 μg/ml.
Dung dịch chuẩn làm việc được chuẩn bị ngay trước khi sử dụng.
4.13 Dãy dung dịch chuẩn làm việc trong nền mẫu (dung dịch chuẩn phù hợp với nền mẫu)
Dãy dung dịch chuẩn làm việc trong nền mẫu có nồng độ là: 0,0025; 0,005; 0,02; 0,1; 0,5 μg/ml được chuẩn bị bằng cách hút các thể tích dung dịch chuẩn làm việc nồng độ 0,1 μg/ml và 1 μg/ml (4.12), dung dịch chuẩn trung gian nồng độ 10 μg/ml (4.11), dịch chiết mẫu trắng (7.2) vào các lọ đựng mẫu (5.12) tương ứng theo Bảng 2 dưới đây và lắc đều.
Bảng 2 - Cách pha dãy chuẩn làm việc trong nền mẫu
| Điểm chuẩn, μg/ml | 0,0025 | 0,005 | 0,02 | 0,1 | 0,5 |
| Dung dịch chuẩn trung gian 10 μg/ml, μl | - | - | - | 10 | 50 |
| Dung dịch chuẩn làm việc 1 μg/ml, μl | - | - | 20 | - | - |
| Dung dịch chuẩn làm việc 0,1 μg/ml, μl | 25 | 50 | - | - | - |
| Dịch chiết mẫu trắng, μl | 975 | 950 | 980 | 990 | 950 |
| Tổng thể tích, μl | 1 000 | 1 000 | 1 000 | 1 000 | 1 000 |
5 Thiết bị, dụng cụ
5.1 Thiết bị LC-MS/MS TripleQuad, được trang bị nguồn ion hóa tia điện (ESI).
5.2 Cột sắc ký lỏng, ví dụ: EC 125/2 NUCLEODUR HILIC[1] (3 pm, 125 mm x 2 mm) hoặc tương đương.
5.3 Máy ly tâm, dùng được với loại ống ly tâm (5.10) được sử dụng trong quy trình (7.2) và có khả năng đạt tốc độ tối thiểu 3 000 r/min.
5.4 Cân phân tích, cân chính xác đến 0,01 mg.
5.5 Cân kỹ thuật, cân chính xác đến 0,01 g.
5.6 Tủ lạnh đông, có thể hoạt động liên tục ở nhiệt độ thấp hơn âm 18 °C.
5.7 Tủ lạnh, có thể hoạt động liên tục ở nhiệt độ 4 °C.
5.8 Máy nghiền mẫu, công suất lớn hơn hoặc bằng 350 W.
5.9 Máy lắc tròn, tốc độ tối đa 2 500 r/min.
5.10 Ống ly tâm có nắp đậy, dung tích 50 ml, bằng nhựa PP.
5.11 Micropipet, dung tích từ 1 μl đến 10 μl, từ 10 μl đến 100 μl, từ 200 μl đến 1 000 μl và từ 1 ml đến 10 ml.
5.12 Lọ đựng mẫu, dung tích 1,5 ml, có nắp và đệm PTFE.
5.13 Màng lọc, nylon, 0,45 pm, 25 mm.
5.14 Xyranh 5 ml, dùng 1 lần.
5.15 Bình định mức, dung tích 10, 100 và 1 000 ml.
5.16 Bể siêu âm.
6 Lấy mẫu
Mẫu gửi đến phòng thử nghiệm phải là mẫu đại diện. Mẫu không được hư hỏng hoặc không bị thay đổi trong suốt quá trình bảo quản và vận chuyển.
7 Cách tiến hành
7.1 Chuẩn bị và bảo quản mẫu thử
7.1.1 Mẫu phòng thử nghiệm
Mẫu được chuẩn bị ngay khi phòng thử nghiệm nhận được, trước khi có sự thay đổi đáng kể về lý hóa. Nếu không thể chuẩn bị mẫu ngay thì phải bảo quản mẫu trong các điều kiện thích hợp để tránh suy giảm chất lượng của mẫu. Mẫu khô có thể được giữ ở nhiệt độ phòng nhưng nếu thời gian bảo quản dự kiến vượt quá 2 tuần thì nên có mẫu phụ (sub-sample) và được bảo quản trong tủ đông [5].
7.1.2 Phần mẫu thử
Mẫu gạo, hạt hồ tiêu được trộn đều và làm lạnh ở nhiệt độ âm 18 °C qua đêm, sau đó mẫu được nghiền bằng máy nghiền mẫu (5.8) ở trạng thái đông lạnh. Có thể sử dụng đá khô hoặc nitơ lỏng để đạt được độ đồng đều cao. Mẫu sau khi đồng nhất được chia làm 2 phần: một phần lưu ở nhiệt độ âm 18 °C, một phần dùng cho phân tích mẫu.
7.2 Chiết mẫu
Cân 5 g (± 0,05 g) mẫu thử đã đồng nhất (7.1.2) vào ống ly tâm có nắp đậy (5.10). Thêm 5 ml dung dịch axit formic 2 % (4.7), đóng chặt nắp, lắc bằng máy lắc tròn (5.9) trong 2 min. Thêm tiếp 5 ml axetonitril (4.2), đóng chặt nắp, lắc bằng máy lắc tròn (5.9) trong 2 min. Siêu âm trong 30 min bằng bể siêu âm (5.16) và ly tâm trong 4 min ở tốc độ vòng > 3 000 r/min bằng máy ly tâm (5.3). Lọc dịch chiết thu được bằng màng lọc nylon 0,45 μm (5.13).
7.3 Chuẩn bị dung dịch mẫu trắng
Mẫu trắng là mẫu không chứa hoặc có giá trị không quá 30 % LOQ hoạt chất phân tích [1], mẫu được chuẩn bị như phần 7.2.
7.4 Chuẩn bị dung dịch mẫu kiểm tra độ thu hồi
Cân lượng mẫu trắng như phần 7.2 vào ống ly tâm có nắp đậy (5.10). Dùng micropipet (5.11) thêm 10 μl dung dịch chuẩn trung gian (4.11), để yên trong nhiệt độ phòng tối thiểu 30 phút và sau đó tiến hành phân tích cùng với mẫu thử (7.2).
7.5 Điều kiện phân tích bằng LC-MS/MS
Bơm lần lượt dãy dung dịch chuẩn làm việc trong nền mẫu (4.13), mẫu trắng (7.3), dung dịch mẫu kiểm tra độ thu hồi (7.4) và dung dịch mẫu thử (7.2) vào thiết bị. Dùng đường chuẩn để xác định nồng độ của mẫu thử và mẫu kiểm tra độ thu hồi. Nếu nồng độ của mẫu thử nằm ngoài đường chuẩn thì điều chỉnh bằng cách pha loãng dung dịch mẫu thử (không phải pha loãng thể tích mẫu bơm). Sau khi bơm mỗi 10 dung dịch mẫu thử và sau mẫu thử cuối cùng của mỗi lần phân tích thì bơm lặp lại 1 điểm chuẩn ở mức nồng độ LOQ. Khoảng dao động kết quả của tất cả các điểm chuẩn bơm lặp lại là ± 30 % so với giá trị đúng [5].
Một số thông số tham khảo của thiết bị và cột như sau:
- Cột: EC 125/2 NUCLEODUR HILIC (3 μm, 125 mm x 2 mm).
- Nhiệt độ cột: 40 °C.
- Tốc độ dòng: 0,5 ml/min.
- Pha động A: axetonitril (4.2).
- Pha động B: dung dịch amoni axetat 5 mmol/l và axit axetic 0,1 % (4.8).
Bảng 3 - Chương trình gradient
| Thời gian min | Pha động A % | Pha động B % |
| 0 | 100 | 0 |
| 4 | 100 | 0 |
| 4,01 | 70 | 30 |
| 12 | 70 | 30 |
| 12,01 | 100 | 0 |
| 30 | 100 | 0 |
- Thể tích bơm: 2 μl.
- Nguồn ion: ESI/+,-.
- Thế ion hóa: 4 500 V.
- Tốc độ dòng khí: khí làm khô (drying gas): 15 l/min; khí phun sương (nebulizing gas): 3 l/min.
Bảng 4 - Điều kiện MRM
| Hoạt chất | lon mẹ m/z | lon định lượng m/z | Năng lượng va chạm V | lon định tính m/z | Năng lượng va chạm V | ESI +/- |
| Cartap | 238,00 | 150,10 | 14 | 73,00 | 28 | + |
| Nereistoxin | 150,00 | 104,90 | 17 | 61,10 | 27 | + |
| Thiocyclam | 181,90 | 136,90 | 15 | 73,00 | 26 | + |
| Thiosultap | 309,80 | 230,10 | 14 | 184,90 | 22 | - |
CHÚ THÍCH: Có thể tiến hành đo trên các thiết bị, các thông số của thiết bị, cột và chương trình gradient khác, tùy theo điều kiện thực tế của phòng thử nghiệm để đạt độ nhạy tốt nhất.
8 Đánh giá kết quả
8.1 Nhận biết
Việc nhận biết thông qua các thông số sau [3]:
- Độ lệch thời gian lưu của chất cần phân tích trong mẫu thử nghiệm so với trong dung dịch chuẩn hoặc các mẫu thêm chuẩn là 0,1 min.
- Đối với mẫu khi phân tích bằng thiết bị khối phổ (MS/MS), cần có thêm điều kiện:
+) có 2 product ion (ion con) (2 MRM transition).
+) khoảng dao động của tỉ lệ ion về diện tích giữa ion định tính và lon định lượng trong mẫu thử nghiệm so với trong dung dịch chuẩn hoặc các mẫu thêm chuẩn là ± 30 %, được tính như sau:
trong đó:
Fm là tỉ lệ ion định tính và ion định lượng trong mẫu thử nghiệm;
Fc là tỉ lệ ion định tính và ion định lượng trong dung dịch chuẩn hoặc các mẫu thêm chuẩn.
8.2 Tính kết quả
8.2.1 Sử dụng đường chuẩn phù hợp nền mẫu
Phương trình đường chuẩn:
y = ax + b (2)
Dư lượng thuốc bảo vệ thực vật tìm thấy trong mẫu:
![]()
trong đó:
X là nồng độ dư lượng thuốc bảo vệ thực vật tìm thấy trong mẫu, tính bằng miligam trên kilôgam (mg/kg);
xm là nồng độ các dư lượng thuốc bảo vệ thực vật trong dung dịch mẫu thử được xác định bằng đường chuẩn, tính bằng microgam trên mililit (μg/ml);
y là diện tích pic thu được;
b là giá trị hệ số chặn của đường chuẩn;
a là giá trị độ dốc của đường chuẩn;
m là khối lượng mẫu thử, tính bằng gam (g);
Ve là thể tích cuối của mẫu, tính bằng mililít (ml).
8.2.2 Sử dụng phương pháp thêm chuẩn
Khi nghi ngờ các dư lượng có thể vượt quá mức cho phép hoặc đối với các chất bị ảnh hưởng nhiều bởi nền mẫu hoặc có hiện tượng triệt tiêu tín hiệu, nên sử dụng phương pháp thêm chuẩn với điều kiện có sự tuyến tính giữa tín hiệu phân tích và các nồng độ trong dải nồng độ dự kiến. Quy trình này đòi hỏi phải biết trước khoảng xấp xỉ mức dư lượng X từ phép phân tích sơ bộ.
Giả sử với lượng mẫu sử dụng là 5 g có mức dư lượng dự đoán là 0,8 mg/kg, đường chuẩn có thể được thực hiện như trong Bảng 5.
Bảng 5 - Chuẩn bị đường chuẩn đối với phương pháp thêm chuẩn
| Thêm | Lọ đựng mẫu 1 | Lọ đựng mẫu 2 | Lọ đựng mẫu 3 | Lọ đựng mẫu 4 |
| Thể tích dịch chiết mẫu, μl | 500 | 500 | 500 | 500 |
| Thể tích dung dịch chuẩn 4 μg/ml, μl | - | 25 | 50 | 75 |
| Khối lượng tạo thành của chất phân tích đã thêm, μg | - | 0,1 | 0,2 | 0,3 |
| Thể tích dung môi, μl | 100 | 75 | 50 | 25 |
| Thể tích cuối, μl | 600 | 600 | 600 | 600 |
Lượng chất phân tích có trong dịch chiết mẫu trước khi thêm chuẩn x được tính bằng cách sử dụng đồ thị như trong Hình 1 theo phép hồi quy tuyến tính.

Hình 1 - Đường chuẩn sử dụng cho phương pháp thêm chuẩn
Phương trình đường chuẩn:
y = ax + b (4)
trong đó:
x là lượng chất phân tích có trong dịch chiết mẫu trước khi thêm chuẩn, tính bằng microgam (μg);
![]()
b là giá trị hệ số chặn của đường chuẩn;
a là giá trị độ dốc của đường chuẩn.
Dư lượng thuốc bảo vệ thực vật tìm thấy trong mẫu:
![]()
trong đó:
X là nồng độ dư lượng thuốc bảo vệ thực vật tìm thấy trong mẫu, tính bằng miligam trên kilôgam (mg/kg);
V là thể tích dịch chiết mẫu dùng thêm chuẩn, tính bằng mililít (ml);
m là khối lượng mẫu thử, tính bằng gam (g);
Ve là thể tích cuối của mẫu, tính bằng mililít (ml).
9 Độ thu hồi
Độ thu hồi trung bình của phương pháp từ 79 % đến 106 % (Phụ lục B).
10 Báo cáo thử nghiệm
Báo cáo thử nghiệm phải ghi rõ:
- mọi thông tin cần thiết để nhận biết về mẫu thử;
- phương pháp lấy mẫu đã sử dụng, nếu biết;
- phương pháp thử đã dùng, viện dẫn tiêu chuẩn này;
- tất cả các chi tiết không quy định trong tiêu chuẩn này hoặc những điều được coi là tùy chọn có thể ảnh hưởng đến kết quả;
- kết quả thử nghiệm được biểu thị bằng đơn vị mg/kg (ppm) và có 2 chữ số sau dấu phẩy.
Phụ lục A
(Tham khảo)
Giới thiệu hoạt chất thuốc bảo vệ thực vật
A.1 Cartap
Tên hóa học: S,S'-[2-(dimethylamino) trimethylene] bis(thiocarbamate)
Công thức hóa học:
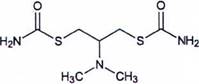
Công thức phân tử: C7H15N3O2S2
Khối lượng mol phân tử: 237,3 g/mol
A.2 Thiocyclam
Tên hóa học: N,N-dimethyl-1,2,3-trithian-5-ylamine
Công thức hóa học:

Công thức phân tử: C5H11NS3
Khối lượng mol phân tử: 181,4 g/mol
A.3 Nereistoxin
Tên hóa học: N,N-Dimethyl-1,2-dithiolan-4-amine
Công thức hóa học:

Công thức phân tử: C5H11NS2
Khối lượng mol phân tử: 149,3 g/mol
A.4 Thiosultap
Tên hóa học: dihydrogen S,S'-[2-(dimethylamino)trimethylene] di(thiosulfate)
Công thức hóa học:

Công thức phân tử: C5H13NO6S4
Khối lượng mol phân tử: 311,4 g/mol
Phụ lục B
(Tham khảo)
Kết quả nghiên cứu
Dùng mẫu trắng thêm chuẩn của các hoạt chất trên các nền mẫu gạo và tiêu ở các mức nồng độ: 0,02; 0,10 và 0,50 mg/kg để xác định độ thu hồi. Xác định độ thu hồi, độ lặp lại kết quả giữa các lần phân tích. Các kết quả thu được được thể hiện trong bảng B.1[2].
Bảng B.1 - Độ thu hồi (H), độ lặp lại (RSD) trên các nền mẫu
| Hoạt chất | Nồng độ mg/kg | Gạo | Tiêu | ||
| H | RSD | H | RSD | ||
| % | % | % | % | ||
| Cartap | 0,02 | 85 | 10 | 84 | 7 |
| 0,10 | 89 | 16 | 90 | 15 | |
| 0,50 | 90 | 13 | 92 | 14 | |
| Nereistoxin | 0,02 | 93 | 11 | 89 | 10 |
| 0,10 | 91 | 15 | 86 | 13 | |
| 0,50 | 91 | 14 | 90 | 10 | |
| Thiocyclam | 0,02 | 87 | 10 | 87 | 8 |
| 0,10 | 88 | 14 | 93 | 15 | |
| 0,50 | 79 | 7 | 106 | 6 | |
| Thiosultap | 0,02 | 90 | 11 | 92 | 11 |
| 0,10 | 88 | 14 | 91 | 15 | |
| 0,50 | 79 | 8 | 86 | 9 | |
Thư mục tài liệu tham khảo
[1] Á. Ambrus, A. Fajgelj (2000). Principles and practices of method validation. Royal Society of Chemistry, Cambridge.
[2] C. Ferrer & M. Mezcua & M. A. Martínez-Uroz & L. Pareja & A. Lozano & A. R. Fernández-Alba Method development and validation for determination of thiosultap sodium, thiocyclam, and nereistoxin in pepper matrix, Anal Bioanal Chem (2010) 398:2299-2306.
[3] Jinxia Dai, Hongping Chen, Guanwei Gao, Li Zhu, Yunfeng Chai, Xin Liu. Simultaneous determination of cartap and its metabolite in tea using hydrophilic interaction chromatography tandem mass spectrometry and the combination of dispersive solid phase extraction and solid phase extraction. Journal of Chromatography A (2019,) 16000: 148-157.
[4] Nghị định 86/2012/NĐ-CP Quy định chi tiết và hướng dẫn thi hành một số điều của luật đo lường.
[5] SANTE/12682/2019 Analytical quality control and method validation procedures for pesticides residues analysis in food and feed, 2020.
[1] EC 125/2 NUCLEODUR HILIC là sản phẩm được cung cấp bởi hãng MACHEREY-NAGE. Thông tin này được cung cấp để thuận tiện cho người sử dụng tiêu chuẩn này. Các sản phẩm tương đương có thể được sử dụng nếu chúng cho kết quả tương đương
[2] Dữ liệu về độ thu hồi, độ lặp lại thu được từ kết quả nghiên cứu của Trung tâm Kiểm định và Khảo nghiệm thuốc bảo vệ thực vật phía Nam.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 13269:2021 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 13269:2021 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 13269:2021 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 13269:2021 DOC (Bản Word)