- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 10993:2015 EN 15911:2010 Thực phẩm-Xác định đồng thời chín chất tạo ngọt bằng sắc ký lỏng hiệu năng cao sử dụng detector tán xạ bay hơi
| Số hiệu: | TCVN 10993:2015 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
31/12/2015 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 10993:2015
Tiêu chuẩn Quốc gia TCVN 10993:2015 EN 15911:2010: Phương pháp xác định chất tạo ngọt trong thực phẩm
Tiêu chuẩn Quốc gia TCVN 10993:2015 EN 15911:2010 được ban hành nhằm quy định phương pháp xác định đồng thời chín chất tạo ngọt trong đồ uống và nước trái cây bằng công nghệ sắc ký lỏng hiệu năng cao (HPLC) sử dụng detector tán xạ bay hơi (ELSD). Tiêu chuẩn này được ban hành bởi Bộ Khoa học và Công nghệ và có hiệu lực từ ngày công bố, thay thế các phương pháp cũ không phù hợp.
Tiêu chuẩn áp dụng cho việc phân tích các chất tạo ngọt như: acesulfame-K, alitame, aspartame, axit cyclamic, dulcin, neotame, neohesperidine-dihydrochalcone, saccharin, và sucralose. Mẫu thử cần được chuẩn bị và xử lý bằng cách chiết xuất và làm sạch trước khi tiến hành phân tích, từ đó đảm bảo độ chính xác trong xác định nồng độ của các chất này trong thực phẩm.
Trong tiêu chuẩn có chỉ rõ các yêu cầu về thuốc thử và dung môi, nhấn mạnh rằng cần sử dụng các loại thuốc thử loại tinh khiết phân tích cùng với nước cất, và cung cấp công thức chi tiết về các dung dịch cần thiết cho quá trình phân tích.
Công việc phân tích được thực hiện theo các bước cụ thể như chiết mẫu, phân tích bằng HPLC và diễn giải dữ liệu sắc ký. Đặc biệt, tiêu chuẩn quy định các chỉ tiêu liên quan đến độ chụm của phương pháp, nhằm đảm bảo tính lặp lại và tái lập trong các phòng thí nghiệm khác nhau.
Đáng chú ý là tiêu chuẩn này không chỉ quy định về phương pháp mà còn cung cấp thông tin chi tiết về thiết bị và dụng cụ cần thiết cho quá trình phân tích, từ máy nghiền trộn thực phẩm, ống ly tâm, tới hệ thống HPLC. Mỗi bước trong quy trình đều được mô tả một cách cụ thể để đảm bảo các thao tác được thực hiện chính xác, giúp thu được kết quả đáng tin cậy.
TCVN 10993:2015 cũng lưu ý rằng kết quả thu được từ phương pháp này cần được báo cáo đầy đủ, trong đó nêu rõ thông tin mẫu thử, phương pháp thử nghiệm được sử dụng cũng như các điều kiện xét nghiệm cụ thể.
Tiêu chuẩn này đánh dấu bước tiến mạnh mẽ trong việc quản lý chất lượng thực phẩm, đáp ứng nhu cầu kiểm soát an toàn và chất lượng sản phẩm tiêu dùng. Đồng thời, nó cũng góp phần hỗ trợ các nhà sản xuất thực phẩm thực hiện đúng các quy định và tiêu chuẩn an toàn thực phẩm hiện hành.
Tải tiêu chuẩn Việt Nam TCVN 10993:2015
TIÊU CHUẨN QUỐC GIA
TCVN 10993:2015
EN 15911:2010
THỰC PHẨM-XÁC ĐỊNH ĐỒNG THỜI CHÍN CHẤT TẠO NGỘT BẰNG SẮC KÝ LỎNG HIỆU NĂNG CAO SỬ DỤNG DETECTOR TÁN XẠ BAY HƠI
Foodstuffs-Simultaneous determination of nine sweeteners by high performance liquid chromatography and evaporative light scattering detection
Lời nói đầu
TCVN 10993:2015 hoàn toàn tương đương với EN 15911:2010;
TCVN 10993:2015 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F13 Phương pháp phân tích và lấy mẫu biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
THỰC PHẨM-XÁC ĐỊNH ĐỒNG THỜI CHÍN CHẤT TẠO NGỌT BẰNG SẮC KÝ LỎNG HIỆU NĂNG CAO SỬ DỤNG DETECTOR TÁN XẠ BAY HƠI
Foodstuffs-Simultaneous determination of nine sweeteners by high performance liquid chromatography and evaporative light scattering detection
1. Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp xác định đồng thời chín chất tạo ngọt trong đồ uống và nước trái cây đóng hộp hoặc đóng chai bằng sắc ký lỏng hiệu năng cao (HPLC) với detector tán xạ bay hơi (HPLC-ELSD).
Phương pháp này đã được đánh giá xác nhận trong nghiên cứu liên phòng phân tích các mẫu thêm chuẩn trên các nền mẫu sau đây:
- acesulfame-K (ACS-K) (từ 38,3 mg/l đến 383,5 mg/l) trong đồ uống và (từ 38,4 mg/kg đến 391,3 mg/kg) trong nước trái cây đóng hộp;
- alitame (ALI) (từ 31,1 mg/l đến 114,5 mg/l) trong đồ uống và (từ 36 mg/kg đến 175,2 mg/kg) trong nước trái cây đóng hộp;
- aspartame (ASP) (từ 38,1 mg/l đến 702 mg/l) trong đồ uống và (từ 37,2 mg/kg đến 1 120,2 mg/kg) trong nước trái cây đóng hộp;
- axit cyclamic (CYC) (từ 28,3 mg/l đến 307,2 mg/l) trong đồ uống và (từ 27,5 mg/kg đến 1 100,6 mg/kg) trong nước trái cây đóng hộp;
- dulcin (DUL) (từ 55,0 mg/l đến 115,1 mg/l) trong đồ uống và (từ 49,8 mg/kg đến 172,6 mg/kg) trong nước trái cây đóng hộp;
- neotame (NEO) (từ 37,6 mg/l đến 115,3 mg/l) trong đồ uống và (từ 37,3 mg/kg đến 173,7 mg/kg) trong nước trái cây đóng hộp;
- neohesperidine-dihydrochalcone (NHDC) (từ 31,4 mg/l đến 59,3 mg/l) trong đồ uống và (từ 35,3 mg/kg đến 59,3 mg/kg) trong nước trái cây đóng hộp;
- saccharin (SAC) (từ 36,2 mg/l đến 87,6 mg/l) trong đồ uống và (từ 44,3 mg/kg đến 235,3 mg/kg) trong nước trái cây đóng hộp;
- sucralose (SCL) (từ 36,8 mg/l đến 346,8 mg/l) trong đồ uống và (từ 35,3 mg/kg đến 462,4 mg/kg) trong nước trái cây đóng hộp.
Thông tin chi tiết về đánh giá xác nhận xem Điều 8 và Phụ lục C.
CHÚ THÍCH: Phương pháp này đã được đánh giá xác nhận đầy đủ [1] qua phép thử cộng tác theo quy trình của IUPAC [2], trên các hỗn hợp nền mẫu phân tích cho tất cả chín chất tạo ngọt có trong đồ uống và nước trái cây đóng hộp hoặc đóng chai.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau là rất cần thiết cho việc áp dụng tiêu chuẩn. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi (nếu có).
TCVN 4851:1989 (ISO 3696:1987), Nước dùng để phân tích trong phòng thí nghiệm-Yêu cầu kỹ thuật và phương pháp thử.
3. Nguyên tắc
Quy trình này bao gồm việc chiết chín chất tạo ngọt bằng dung dịch đệm, mẫu được làm sạch bằng cột chiết pha rắn sau đó phân tích bằng HPLC-ELSD.
4. Thuốc thử
Chỉ sử dụng thuốc thử loại tinh khiết phân tích và chỉ sử dụng nước cất hoặc nước ít nhất là loại 1 của TCVN 4851 (ISO 3696), trừ khi có quy định khác. Khi chuẩn bị các dung dịch, cần tính đến độ tinh khiết của các chất.
4.1. Acesulfame-K1 phần khối lượng w ít nhất là 99,0 %.
4.2. Alitame, w ≥ 99,0 %.
4.3. Aspartame, w ≥ 99,0 %.
4.4. Dulcin, loại dùng cho HPLC.
4.5. Neotame, w ≥ 99,0 %.
4.6. Neohesperidine-dihydrochalcone, w ≥ 95,0 %.
4.7. Saccharin, muối natri dihydrat, w ≥ 98,0 %.
4.8. Natri cyclamat, w ≥ 99,0 %.
4.9. Sucralose, w ≥ 99,0 %.
4.10. Axit formic, HCOOH loại dùng cho HPLC.
4.11. Triethyla mine, (C2H5)3N, w ≥ 99,5 %.
4.12. Metanol, loại dùng cho HPLC.
4.13. Axeton, loại dùng cho HPLC.
4.14. Dung dịch đệm (pH = 4,5).
Hòa tan 4 ml axit formic (4.10) trong 5 lít nước. Chỉnh đến pH 4,5 bằng khoảng 12,5 ml triethyla mine (4.11).
4.15. Pha động HPLC A, metanol/dung dịch đệm/axeton, với tỷ lệ 69:24:7 (thể tích).
Trộn 690 ml metanol (4.12) với 240 ml dung dịch đệm (4.14) và 70 ml axeton (4.13). Khử khí bằng siêu âm trong 10 min.
4.16. Pha động HPLC B, metanol/ dung dịch đệm/axeton, với tỷ lệ 11:82:7 (thể tích).
Trộn 110 ml metanol (4.12) với 820 ml dung dịch đệm (4.14) và 70 ml axeton (4.13). Khử khí bằng siêu âm trong 10 min.
4.17. Dung dịch gốc hỗn hợp, chứa ACS-K, ALI, ASP, CYC-Na, DUL, NEO, NHDC, SAC-Na và SCL; có nồng độ khối lượng ρ(chất tạo ngọt i) = 30 μg/ml đến 250 μg/ml.
Chuẩn bị dung dịch gốc hỗn hợp của tất cả chín chất tạo ngọt bằng cách cân các lượng quy định của từng chất chuẩn riêng rẽ (Bảng 1) đầu tiên cho vào cốc có mỏ 100 ml và hòa tan chúng trong 50 ml hỗn hợp metanol/nước (1:1) cho đến khi tan hoàn toàn. Sau đó chuyển định lượng dung dịch sang bình định mức 500 ml và thêm dung dịch đệm (4.14) đến vạch. Trộn kỹ bằng siêu âm cho đến khi tan hết.
Bảng 1-Lượng chất chuẩn riêng rẽ dùng để chuẩn bị dung dịch gốc hỗn hợp
| Chất chuẩn | Lượng chất chuẩn cho vào bình định mức 500 mlc mg | Nồng độ cuối cùng của chất tạo ngọt thứ i trong chất chuẩn gốc hỗn hợp μg/ml |
| Acesulfame-K (ACS-K) | 45 | 90 |
| Alitame (ALI) | 25 | 50 |
| Aspartame (ASP) | 125 | 250 |
| Natri cyclamat (CYC-Na) | 140a | - |
| Axit cyclamic (CYC) (axit tự do) | - | 249,42 |
| Dulcin (DUL) | 25 | 50 |
| Neotame (NEO) | 25 | 50 |
| Neohesperidine-dihydrochalcone (NHDC) | 15 | 30 |
| Saccharin, muối natri dihydrat (SAC- Na·2H2O) | 35b | - |
| Saccharin (SAC) (imit tự do) | - | 53,17 |
| Sucralose (SCL) | 50 | 100 |
| a tương đương với 124,71 mg axit cyclamic tự do; hệ số chuyển đổi để tính khối lượng axit cyclamic tự do = 0,890 8; mCYC = 0,890 8 x mCYC-Na b tương đương với 26,58 mg saccharin tự do; hệ số chuyển đổi để tính khối lượng saccharin tự do = 0,759 5; mSAC = 0,759 5 x mSAC-Na·2H2O c lượng đầu tiên cho vào cốc có mỏ 100 ml, hòa tan trong 50 ml hỗn hợp metanol/nước (tỷ lệ 1:1) và chuyển định lượng sang bình định mức 500 ml. | ||
CHÚ THÍCH: Trong trường hợp đối với axit cyclamic và saccharin, sử dụng các muối natri của chúng, vì không sẵn có ở dạng tự do và ít tan.
Nồng độ cuối cùng của các chất tạo ngọt riêng rẽ tính bằng microgam trên millilit trong dung dịch gốc hỗn hợp phải tính được bằng cách sử dụng các khối lượng thực tế chính xác.
4.18. Dung dịch chuẩn
Từ dung dịch gốc hỗn hợp (4.17), chuẩn bị các dãy dung dịch chuẩn của các chất tạo ngọt ở các mức giới hạn phù hợp, ví dụ: nồng độ cao nhất của dung dịch hiệu chuẩn phải ít nhất bằng 125 % giới hạn quy định hiện hành (theo Commission Directives [3], [4], [5] (xem Bảng D.1), có tính đến các bước pha loãng (xem Bảng 2). Đối với các chất tạo ngọt chưa có quy định hiện hành (ví dụ: ALI, DUL và NEO) thì liều dùng tối đa giả định là xấp xỉ 200 mg/l hoặc 200 mg/kg.
Người sử dụng tiêu chuẩn cần kiểm tra các giới hạn trong Bảng D.1 về hiệu lực của các giá trị giới hạn. Nếu không, nồng độ khối lượng của chất chuẩn trong dung dịch hiệu chuẩn phải được điều chỉnh phù hợp với mức liều dùng tối đa giả định.
CHÚ THÍCH: Quy trình này có thể đơn giản hóa bằng cách chuẩn bị một dãy dung dịch hiệu chuẩn đối với cả hai nền mẫu thực phẩm. Dãy hiệu chuẩn quy định là phù hợp với nước trái cây đóng hộp vì mức liều dùng tối đa giả định đối với nước trái cây đóng hộp trong một số trường hợp là cao hơn đối với các loại đồ uống giải khát khác. Trong trướng hợp chỉ phân tích nền mẫu nước trái cây, thì dãy dung dịch hiệu chuẩn có thể phù hợp cho cả mức liều dùng tối đa giả định của nước giải khát.
Dùng pipet lấy các thể tích (xem Bảng 2) dung dịch gốc hỗn hợp (4.17) cho vào các bình định mức thích hợp (10 ml đến 50 ml) và thêm dung dịch đệm (4.14) đến vạch và lắc kỹ.
Bảng 2-Chuẩn bị dãy dung dịch chuẩn
| Dung dịch hiệu chuẩn | Dung tích bình định mức, | Thể tích cần lấy từ dung dịch gốc hỗn hợp (4.17), | Thể tích cần lấy từ dung dịch đệm (4.14), |
| 1a | 10 | 10 | 0 |
| 2 | 10 | 8 | 2 |
| 3 | 10 | 6 | 4 |
| 4 | 10 | 4 | 6 |
| 5 | 10 | 2 | 8 |
| 6 | 25 | 3 | 22 |
| 7 | 50 | 3 | 47 |
| 8 | 50 | 1,5 | 48,5 |
| a là dung dịch gốc hỗn hợp không pha loãng (4.17). | |||
Bảng 3 nêu chi tiết nồng độ chất tạo ngọt thứ i trong mỗi chất chuẩn hiệu chuẩn được chuẩn bị theo Bảng 2.
Nếu không cần thiết phải phân tích tất cả các chất tạo ngọt nêu trong tiêu chuẩn này, thì sử dụng bộ mẫu cụ thể để giảm các mức của dung dịch hiệu chuẩn đối với các mẫu đó.
Bảng 3-Nồng độ chất tạo ngọt thứ i trong từng dung dịch chuẩn
| Chất tạo ngọt | Dung dịch hiệu chuẩn | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| ACS-K | 90,0 | 72,0 | 54,0 | 36,0 | 18,0 | 10,8 | 5,4 | 2,7a |
| ALI | 50,0 | 40,0 | 30,0 | 20,0 | 10,0 | 6,0 | 3,0a | 1,5a |
| ASP | 250,0 | 200,0 | 150,0 | 100,0 | 50,0 | 30,0 | 15,0 | 7,5 |
| CYC | 249,4 | 199,5 | 149,7 | 99,8 | 49,9 | 29,9 | 15,0 | 7,5 |
| DUL | 50,0 | 40,0 | 30,0 | 20,0 | 10,0 | 6,0a | 3,0a | 1,5a |
| NEO | 50,0 | 40,0 | 30,0 | 20,0 | 10,0 | 6,0 | 3,0a | 1,5a |
| NHDC | 30,0 | 24,0 | 18,0 | 12,0 | 6,0 | 3,6a | 1,8a | 0,9a |
| SAC | 53,2 | 42,5 | 31,9 | 21,3 | 10,6 | 6,4 | 3,2a | 1,6a |
| SCL | 100,0 | 80,0 | 60,0 | 40,0 | 20,0 | 12,0 | 6.0 | 3,0a |
| a Giới hạn nồng độ có thể thấp hơn giới hạn định lượng (LOQ). Nếu đúng thì kết quả thu được bằng phân tích HPLC có thể không được đưa vào để dựng đường chuẩn, ví dụ: đối với ACS-K thực hiện hiệu chuẩn bảy điểm, bỏ qua kết quả thu được với dung dịch hiệu chuẩn số 8. | ||||||||
5. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ thông thường của phòng thử nghiệm và cụ thể như sau:
5.1. Dụng cụ thủy tinh thông thường của phòng thử nghiệm, như ống đong chia vạch, pipet tính mức, cốc thủy tinh có mỏ.
5.2. Cân phân tích, có thể cân chính xác đến 0,01 mg.
5.3. Cân phòng thử nghiệm, có thể cân chính xác đến 0,01 g.
5.4. Pipet, có thể phân phối từ 1 ml đến 10 ml (dung tích khác nhau).
5.5. Bình định mức, có dung tích thích hợp, ví dụ: 10 ml, 25 ml, 50 ml, 100 ml và 500 ml.
5.6. Ống ly tâm bằng polypropylene, có dung tích thích hợp, ví dụ: 50 ml.
5.7. Ống nghiệm chia vạch, có dung tích thích hợp, ví dụ: 5 ml.
5.8. Máy nghiền trộn thực phẩm, thích hợp để đồng hóa mẫu thực phẩm.
5.9. Bể siêu âm.
5.10. Máy ly tâm, có thể duy trì tốc độ 4 000 min-1.
5.11. Hệ thống chân không SPE hoặc loại tương đương.
5.12. Dụng cụ làm bay hơi dung môi.
5.13. Máy đo pH.
5.14. Cột C18-SPE.
5.15. Cột phân tích pha đảo, có khóa đuôi, cho phép tách được tất cả chín chất tạo ngọt.
Ví dụ, cột có:
- pha tĩnh RP-C18 cỡ hạt 5 μm;
- chiều dài 250 mm;
- đường kính trong 3 mm.
5.16. Hệ thống HPLC, được trang bị bơm hai kênh có thể duy trì tốc độ dòng 0,5 ml/ min, tốt nhất là có hệ thống bơm mẫu tự động và có detector tán xạ bay hơi.
Có thể sử dụng các hệ thống detector khác như MS để thay thế ELSD hoặc UV và DAD khi các chất hấp thụ trong vùng UV với điều kiện là thu được các đặc tính tương tự.
5.17. Bộ thu thập dữ liệu và phần mềm phân tích.
6. Cách tiến hành
6.1. Yêu cầu chung
Sử dụng máy nghiền trộn (5.8) để nghiền toàn bộ mẫu thử để thu được huyền phù đồng nhất. Các mẫu dạng lỏng có thể thực hiện luôn quy trình chiết.
6.2. Chuẩn bị mẫu thử
6.2.1. Bước 1
Cân khoảng 5 g (M1, lấy đến hai chữ số thập phân) mẫu thử đồng nhất (6.1) cho vào bình định mức 50 ml (V1). Thêm dung dịch đệm (4.14) đến vạch, lắc trộn kỹ bằng tay để thu được huyền phù đồng nhất và cho siêu âm 15 min trong bể siêu âm (5.9).
6.2.2. Bước 2
Chuyển huyền phù thu được sang ống ly tâm 50 ml. Ly tâm 10 min ở tốc độ 4 000 min-1.
CHÚ THÍCH: Đối với trường hợp mẫu là dung dịch trong suốt (ví dụ: một vài loại nước giải khát), thì có thể bỏ qua bước này.
6.3. Chiết pha rắn
6.3.1. Bước 1
Ổn định cột (5.14) bằng cách cho 3 ml metanol (4.12) đi qua cột sử dụng chân không nhẹ để có tốc độ rửa giải từ 1 ml/ min đến 2 ml/ min. Đảm bảo một lượng nhỏ metanol còn lại trên đáy cột hấp phụ (1 mm).
6.3.2. Bước 2
Cân bằng cột (5.14) bằng cách cho 2 ml dung dịch đệm (4.14) đi qua cột sử dụng chân không nhẹ để có tốc độ rửa giải từ 1 ml/ min đến 2 ml/ min. Đảm bảo một lượng nhỏ metanol còn lại trên đáy cột hấp phụ (1 mm). Lặp lại quy trình này hai lần.
6.3.3. Bước 3
Cho 5 ml (V2) dịch chiết lên cột (5.14), nghĩa là cho phần nổi phía trên thu được trong 6.2.2, sử dụng chân không nhẹ để có tốc độ rửa giải từ 1 ml/ min đến 2 ml/ min. Đảm bảo rằng một lượng nhỏ còn lại trên đáy cột hấp phụ (1 mm). Lặp lại quy trình này hai lần (tổng V2 là 10 ml).
6.3.4. Bước 4
Rửa cột (5.14) bằng 3 ml dung dịch đệm (4.14), sử dụng chân không nhẹ để có tốc độ rửa giải từ 1 ml/ min đến 2 ml/ min. Đảm bảo rằng một lượng nhỏ còn lại trên đáy cột hấp phụ (1 mm).
6.3.5. Bước 5
Rửa giải các chất tạo ngọt ra khỏi cột (5.14) bằng cách sử dụng 2 ml metanol (4.12) và thu lấy dịch rửa giải vào ống chia vạch 5 ml. Sử dụng chân không nhẹ để có tốc độ rửa giải từ 1 ml/ min. Đảm bảo rằng một lượng nhỏ metanol còn lại trên đáy cột hấp phụ (1 mm). Đợi 10 min trước khi nạp phần thứ hai của 2 ml metanol và thu lấy dịch rửa giải này vào cùng ống nghiệm 5 ml, sử dụng cùng điều kiện chân không nhưng thời gian này để cho cột (5.14) chảy đến khô.
Không để cho các bước từ 6.2.1 đến 6.3.5 có chất hấp phụ chảy đến khô, trừ lần rửa giải thứ hai của bước cuối cùng 6.3.5.
6.3.6. Bước 6
Cho dung môi bay hơi ra khỏi dịch chiết SPE trong metanol đến khi còn 3 ml, dùng dòng khí nitơ ở nhiệt độ phòng.
Tránh để nhiệt độ vượt quá 40 °C, vì aspartame có thể bị phân hủy.
6.3.7. Bước 7
Cho dung dịch đệm (4.14) vào ống chia vạch có chứa dịch chiết SPE (6.3.6) đầy đến vạch 5 ml (V3). Trộn kỹ và chuyển lượng chứa sang lọ HPLC thích hợp và phân tích bằng HPLC.
6.4. Điều kiện của HPLC
Cài đặt các điều kiện của HPLC để đáp ứng được các tiêu chí thực hiện đã được định nghĩa trước trong 6.5. Việc tách và định lượng cho thấy tốt khi áp dụng các điều kiện thực nghiệm sau đây và các điều kiện gradient HPLC nêu trong Bảng 4.
- Cột: xem 5.15;
- Nhiệt độ cột: nhiệt độ môi trường;
- Thể tích bơm: 10 μl;
- Pha động: xem 4.15 và 4.16;
- Kiểu phân tách: gradient;
- Detector: detector tán xạ bay hơi (ELSD);
- Nhiệt độ ống kéo ELSD: 85 °C;
- Tốc độ dòng nitơ ELSD: 2,5 l/ min;
- Độ khuếch đại ELSD: 1
- Chế độ ELSD: tắt.
Bảng 4-Phân tích gradient HPLC, tốc độ dòng 0,5 ml/ min
| Thời gian, min | Pha động A, % | Pha động B, % |
| 0 | 0 | 100 |
| 4 | 0 | 100 |
| 11 | 53 | 47 |
| 23 | 100 | 0 |
| 24 | 100 | 0 |
| 26 | 0 | 100 |
| 36 | 0 | 100 |
CHÚ THÍCH: Các thông số detector có thể áp dụng cho hệ thống Alltech ELSD 2000ES1). Các hệ thống thay thế ELSD và các điều kiện thực nghiệm được sử dụng trong nghiên cứu liên phòng được nêu trong Phụ lục A. Các điều kiện vận hành HPLC và ELSD có thể được thay đổi để thu được việc tách tối ưu.
6.5. Phép thử sự phù hợp của hệ thống-Độ phân giải của hệ thống tách
Các chi tiết của quy trình sắc ký phụ thuộc vào nhiều yếu tố, thiết bị, kiểu, tuổi thọ, nhà cung cấp cột, kích cỡ mẫu và detector. Có thể sử dụng các cột khác nhau và các thể tích bơm khác, nếu đáp ứng được các phép thử sự phù hợp của hệ thống.
Hệ thống HPLC-ELSD có thể tách được tất cả chín chất tạo ngọt ra với sự phân tách các đường nên là rõ nhất. Yêu cầu này có thể được chứng minh bằng cách sử dụng dung dịch hiệu chuẩn 1 (4.18) nêu trong Hình B.1.
Ngoài ra hệ thống này có thể tách được tất cả chín chất tạo ngọt ra khỏi các thành phần khác của nền mẫu. Nhiều thành phần nền mẫu như natri benzoat, axit sorbic, axit xitric, axit phosphoric, axit malic, axit ascorbic, axit glutamic, sucrose, glucose, fructose, lactose, caffeine, taurine, D-glucurono-γ-lactone và sorbitol, v.v..., được tách bằng làm sạch trên cột SPE. Cặp tới hạn thường gặp nhất là alitame và quinine, không tách được bằng SPE [7].
Khi không tách được thì cần tối ưu các điều kiện sắc ký (ví dụ: thể tích mẫu bơm, tốc độ pha động, chương trình gradient, v.v...) hoặc các điều kiện ELSD (ví dụ: nhiệt độ ống trôi, tốc độ dòng khí nitơ/không khí).
6.6. Dựng đường chuẩn
Phân tích tất cả các dung dịch chuẩn (4.18, Bảng 2) sử dụng các điều kiện HPLC (6.4) giống hệt nhau như đã dùng cho các mẫu thử, nghĩa là bơm 10 μl mỗi dung dịch vào hệ thống HPLC. Dựng đường chuẩn cho mỗi chất tạo ngọt thứ i từ các kết quả thu được qua việc phân tích các dung dịch chuẩn.
Dựng đồ thị các diện tích pic thu được là Iog10 (diện tích pic thứ i) (trục y) với Iog10 (nồng độ chất thứ i) (trục x). Vẽ đường thẳng (y = a + bx) để thu được các kết quả, trong đó b là giá trị độ dốc của hàm tuyến tính và a là giá trị của điểm cắt của đường chuẩn với trục tung y. Nếu các kết quả phân tích các dung dịch chuẩn là đường thẳng thì các đường hiệu chuẩn có thể sử dụng để tính nồng độ chất tạo ngọt thứ i của dịch chiết mẫu.
Nếu sử dụng detector khác không phải là ELSD, thì có thể sử dụng các hàm hiệu chuẩn khác.
6.7. Phân tích dung dịch mẫu bằng HPLC
Phân tích 10 μl dung dịch mẫu thử thu được trong 6.3.7.
6.8. Diễn giải dữ liệu sắc ký
Nhận biết các chất tạo ngọt riêng rẽ trong mẫu thử bằng cách so sánh thời gian lưu của các chất tạo ngọt quan sát được trong quá trình phân tích dung dịch chuẩn được phân tích đồng thời với mẻ mẫu với thời gian lưu của các hợp chất rửa giải trong quá trình phân tích các mẫu thử. Thứ tự rửa giải của các chất tạo ngọt riêng rẽ cùng với thời gian lưu được nêu trong sắc ký đồ ở Hình B.1.
Đo diện tích pic đặc trưng (Ri) quan sát được của chất tạo ngọt thứ i trong từng dung dịch. Trong trường hợp diện tích của chất tạo ngọt thứ i trong sắc ký đồ của dung dịch mẫu thử vượt quá diện tích pic của chất tạo ngọt tương ứng thu được trong sắc ký đồ của dung dịch chuẩn có nồng độ cao nhất thì cần pha loãng dung dịch mẫu thử bằng dung dịch đệm (4.14) và phân tích lại dung dịch đã pha loãng.
7. Tính kết quả
Xác định hàm lượng chất tạo ngọt thử i bằng cách tích phân diện tích pic thứ i (Ri) thu được từ phép phân tích dịch chiết SPE được bơm vào. Sử dụng hàm hiệu chuẩn, nghĩa là y = a + bx (6.6) để tính nồng độ khối lượng chất tạo ngọt thứ i (ρ1i) trong dung dịch chất chiết mẫu đo được, sử dụng Công thức (1) và (2) sau đây:
![]() (1)
(1)
![]() (2)
(2)
Trong đó:
Ri là diện tích pic đặc trưng (6.8) đối với chất tạo ngọt thứ i;
ai là giao điểm của đường chuẩn (6.6) đối với chất tạo ngọt thứ i;
bi là độ dốc của đường chuẩn (6.6) đối với chất tạo ngọt thứ i;
ρ1i là nồng độ khối lượng của chất tạo ngọt thứ i có trong dịch chiết SPE tính bằng microgam trên mililit;
Tính tỷ lệ phần khối lượng trên nồng độ khối lượng wlρ2i của chất tạo ngọt thứ i có trong mẫu thử theo
Công thức (3) sau đây:
![]() (3)
(3)
Trong đó:
ρ1i là nồng độ khối lượng của chất tạo ngọt thứ i có trong dịch chiết SPE tính bằng microgam trên mililit (μg/ml) (xác định được theo Công thức 2);
M1 là khối lượng mẫu thử được lấy để chiết, tính bằng gam (g), trong trường hợp này là 5 g (6.2.1);
V1 là tổng thể tích dung dịch mẫu, tính bằng mililit, trong trường hợp này là 50 ml (6.2.1);
V2 là thể tích dung dịch mẫu đưa lên cột SPE, tính bằng mililit (ml), trong trường hợp này là 10 ml (6.3.3);
V2 là thể tích cuối cùng của dịch chiết SPE, tính bằng mililit (ml), trong trường hợp này là 5 ml (6.3.7).
8. Độ chụm
8.1. Yêu cầu chung
Chi tiết về các phương pháp được các phòng thử nghiệm riêng rẽ sử dụng trong phép thử liên phòng được nêu trong Bảng A.1. Các chi tiết của phép thử liên phòng về độ chụm được nêu trong Phụ lục C. Các dữ liệu thu được từ phép nghiên cứu cộng tác này có thể không áp dụng được cho các dài nồng độ chất phân tích và các nền mẫu khác với các dải nồng độ chất phân tích và nền mẫu nêu trong Phụ lục C.
8.2. Độ lặp lại và độ tái lập
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ, thu được khi tiến hành trên vật liệu thử giống hệt nhau, do một người thực hiện, sử dụng cùng thiết bị, trong một khoảng thời gian ngắn như nhau, không được quá 5 % các trường hợp vượt quá giới hạn lặp lại r.
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ, thu được bởi hai phòng thử nghiệm khi tiến hành trên vật liệu thử giống hệt nhau, không được quá 5 % các trường hợp vượt quá giới hạn tái lập R.
Các giá trị r và R được nêu trong Bảng 5 và Bảng 6, còn các dữ liệu về đánh giá xác nhận phương pháp được nêu trong Phụ lục C và tài liệu tham khảo [1].
Bảng 5-Các giá trị của chín chất tạo ngọt trong nước giải khát theo các Bảng C.1 đến C.9
|
| Mẫu 2 mg/l | Mẫu 3 mg/l | Mẫu 4 mg/l | Mẫu 5 mg/l | |
| acesulfame-K |
| 38,3 | 266,6 | 324,1 | 383,5 |
| r | 7,4 | 16,9 | 29,7 | 25,7 | |
| R | 11,6 | 43,8 | 56,2 | 54,0 | |
| alitame |
| 31,1 | 69,1 | 96,4 | 114,5 |
| r | 6,2 | 7,7 | 6,3 | 4,3 | |
| R | 8,3 | 21,1 | 7,2 | 11,0 | |
| aspartame |
| 38,1 | 485,1 | 584,8 | 702 |
| r | 5,2 | 26,5 | 14,1 | 16,2 | |
| R | 17,1 | 93,3 | 86,6 | 65,9 | |
| cyclamate |
| 28,3 | 248,9 | 256,8 | 307,2 |
| r | 3,5 | 18,4 | 10,2 | 16,5 | |
| R | 16,3 | 43,1 | 392 | 43,4 | |
| dulcin |
| 55,0 | 79,6 | 95,7 | 115,1 |
| r | 3,8 | 8,2 | 2,8 | 4,3 | |
| R | 9,4 | 10,9 | 14,7 | 14,7 | |
| neotame |
| 37,6 | 77,9 | 97,2 | 115,3 |
| r | 2,4 | 5,2 | 6,7 | 7,7 | |
| R | 6,8 | 12,9 | 13,5 | 14,4 | |
| neohesperidine- dihydrochalcone |
| 31,4 | 42,8 | 51,0 | 59,3 |
| r | 9,3 | 4,7 | 4,9 | 7,3 | |
| R | 25,1 | 18,7 | 12,4 | 14,5 | |
| saccharin |
| 36,2 | 60,1 | 74,1 | 87,6 |
| r | 3,9 | 4,7 | 8,3 | 2,7 | |
| R | 11,3 | 7,7 | 13,6 | 14,5 | |
| sucralose |
| 36,8 | 245,1 | 282,9 | 346,8 |
| r | 3,8 | 10,6 | 7,4 | 22,9 | |
| R | 14,7 | 28,2 | 45,3 | 374 | |
Bảng 6-Các giá trị của chín chất tạo ngọt trong nước trái cây theo các Bảng C.1 đến C.9
|
| Mẫu 7, mg/kg | Mẫu 8 mg/kg | Mẫu 9 mg/kg | Mẫu 10 mg/kg | |
| acesulfame-K |
| 38,4 | 259,2 | 323 | 391,3 |
| r | 7,4 | 25,6 | 11,5 | 32 | |
| R | 15,9 | 35,5 | 44,8 | 49,1 | |
| alitame |
| 36 | 113,7 | 142,5 | 175,2 |
| r | 9,7 | 6,9 | 8,8 | 18 | |
| R | 9,7 | 10,6 | 12,3 | 21,1 | |
| aspartame |
| 37,2 | 739,8 | 951,9 | 1 120,2 |
| r | 10,1 | 46,3 | 12,5 | 37,8 | |
| R | 10,1 | 82,0 | 77,1 | 88,8 | |
| cyclamate |
| 27,5 | 749,7 | 924,7 | 1 100,6 |
| r | 12,4 | 19,6 | 40,5 | 35,6 | |
| R | 13,7 | 86 5 | 124,2 | 104,3 | |
| dulcin |
| 49,8 | 111 | 141,7 | 172,6 |
| r | 10,3 | 8,4 | 10,1 | 8,6 | |
| R | 12,0 | 13,4 | 13,1 | 15,2 | |
| neotame |
| 37,3 | 116,2 | 140,6 | 173,7 |
| r | 3,6 | 10,1 | 6,2 | 13,5 | |
| R | 6,2 | 17,6 | 21,1 | 21,7 | |
| neohesperidine- dihydrochalcone |
| 35,3 | 40,5 | 49,8 | 59,3 |
| r | 6,1 | 2,8 | 5,6 | 6,5 | |
| R | 12,2 | 13,0 | 9,2 | 15,3 | |
| saccharin |
| 44,3 | 151,9 | 193,4 | 235,3 |
| r | 6,8 | 11,3 | 12,0 | 18,8 | |
| R | 23,6 | 29,6 | 37,7 | 42,0 | |
| sucralose |
| 35,3 | 306,1 | 380,2 | 462,4 |
| r | 6,3 | 20,6 | 23,8 | 27,1 | |
| R | 10,8 | 24,4 | 29,1 | 27,1 | |
9. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải nêu rõ các thông tin sau:
- mọi thông tin cần thiết để nhận biết đầy đủ về mẫu thử;
- viện dẫn tiêu chuẩn này và phương pháp đã sử dụng;
- ngày và phương pháp lấy mẫu đã sử dụng (nếu biết);
- ngày nhận mẫu;
- ngày thử nghiệm;
- kết quả thu được và đơn vị biểu thị;
- các điểm cụ thể quan sát được trong khi thử nghiệm;
- mọi chi tiết thao tác không quy định trong tiêu chuẩn này, hoặc được xem là tùy chọn, có thể ảnh hưởng đến kết quả.
Phụ lục A
(Tham khảo)
Các điều kiện thích hợp của phương pháp
Bảng A.1-Các điều kiện thích hợp của hệ thống
| Các đặc trưng của SPE | |||||||
| Tên hãng | Chromabond® | Chromabond® | Bakerbond spe® | Chromaband® | Chromabond® | Chromabond® | Chromabond® |
| - Pha tĩnh | C18ec | C18ec | C18 | C18ec | C18ec | C18ec | C18ec |
| - Dung lượng(ml/mg) | 6/1000 | 6/1000 | 3/500 | 6/1000 | 6/1000 | 6/1000 | 6/1000 |
| Đặc tính cột HPLC | |||||||
| - Tên hãng | Puropher® Star | Puropher® Star | Puropher® Star | Nucleodur® | Puropher® Star | Puropher® Star | Puropher® Star |
| - Pha tĩnh | RP-C18 endcapped | RP-C18 endcapped | RP-C18 endcapped | C-18ec Pyramid | RP-C18 endcapped | RP-C18 endcapped | RP-C18 endcapped |
| - Chiều dài | 250 | 250 | 250 | 250 | 250 | 250 | 250 |
| - Đường kính trong (mm) | 3 | 3 | 3 | 3 | 3 | 3 | 3 |
| - Cỡ hạt (μm) | 5 | 5 | 5 | 5 | 5 | 5 | 5 |
| Pha động HPLC | |||||||
| - Thành phần pha động A (thể tích) | Metanol: dung dịch đệm: axeton: 69:24:7 | Metanol: dung dịch đệm: axeton: 69:24:7 | Metanol: dung dịch đệm axeton: 69:24:7 | Metanol: dung dịch đệm: axeton: 69:24:7 | Metanol: dung dịch đệm: axeton: 69:24:7 | Metanol: dung dịch đệm: axeton: 69:24:7 | Metanol: dung dịch đệm: axeton: 69:24:7 |
| - Thành phần pha động B (thể tích) | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 | Metanol: dung dịch đệm: axeton: 11:82:7 |
| -Tốc độ dòng (ml/ min) | 0,5 | 0,5 | 0,5 | 0,5 | 0,6 | 0,55 | 0,5 |
| Phương thức tách bằng HPLC | |||||||
| - Chương trình gradient ( min-% pha động A) | 0 min-100%A; | 0 min-5%A; |
| 0 min-0%A | 0 min-0%A | 0 min-0%A; | 0 min-0%A; |
|
| 4 min-100%A; | 10 min-60%A; | 0 min-0%A; | 4 min-0%A; | 4 min-0%A; | 4 min-0%A; | 4 min-0%A; |
|
| 11 min-47%A; | 30 min-95%A; | 15 min-100%A; | 11 min-53%A; | 11 min-53%A; | 11 min-53%A; | 11 min-53%A; |
|
| 23 min-2%A; | 31 min-95%A; | 18 min-100%A; | 23 min-100%A; | 21 min-100%A; | 23 min-100%A; | 23 min-100%A; |
|
| 24 min-2 %A; | 32 min-5%A; | 20 min-0%A; | 24 min-100%A; | 23 min-100%A; | 24 min-100%A; | 24 min-100%A; |
|
| 26 min-100%A; | 45 min-5%A; | 35 min-0%A; | 26 min-0%A; | 25 min-0%A; | 26 min-0%A; | 26 min-0%A; |
|
|
|
|
| 36 min-0%A; | 31 min-0%A; | 36 min-0%A; | 36 min-0%A; |
| Phương thức bơm HPLC | |||||||
| - Thủ công-tự động | Tự động | Tự động | Tự động | Tự động | Tự động | Tự động | Tự động |
| Điều kiện ELSD | |||||||
| - Nhà sản xuất | Sedex 85, Sedere | Varex MKlll, Alltech | ELSD-LT II, Shimadzu | Sedex, Sedere | Sedex 75, Sedere | ELSD 2000ES, Altech | ELSD 2000ES, Atech |
| - Nhiệt độ ống kéo (oC) | 40 | 90 | 50 | 43 | 45 | 85 | 85 |
| - Nitơ/không khí (áp lực/tốc độ dòng) | Nitơ 3,2 bar | Nitơ 2,5 l/ min | Không khí 3 bar | Nitơ 3,5 bar | Không khí 2,5bar | Nitơ 2,5bar | Nitơ 2,5 l/ min |
| - độ khuếch đại | 7 | 1 | 9 | 10 | 2 | 1 | 1 |
Phụ lục B
(Tham khảo)
Ví dụ về sắc ký đồ
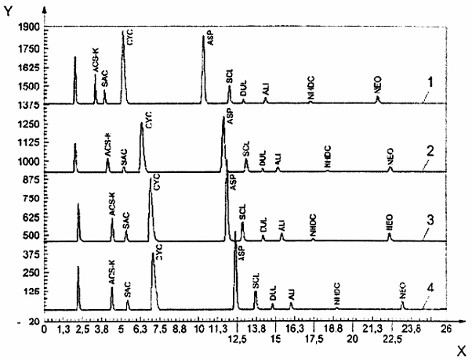
CHÚ DẪN
1 Zorbax Extend-C182)
2 Nucleodur® C18 Pyramid2)
3 Nucleodur® C18 Gravity2)
4 Purospher® Star RP-18, 5 μm3)
X Thời gian ( min)
Y Tín hiệu ELSD
Hình B.1-Sắc ký đồ của dung dịch chuẩn các chất tạo ngọt thu được sử dụng các cột HPLC khác nhau
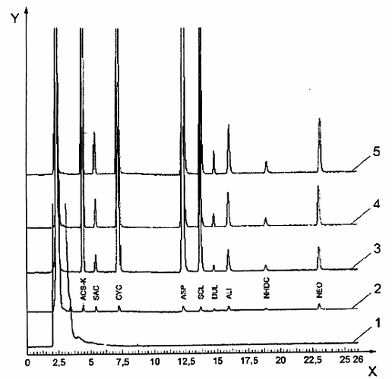
CHÚ DẪN:
1 Mẫu trắng đồ uống cung cấp năng lượng;
2 Đồ uống cung cấp năng lượng có bổ sung chất chuẩn ở mức xấp xỉ giới hạn định lượng;
3 Đồ uống không chứa cacbonat có bổ sung chất chuẩn ở mức xấp xỉ 80 % liều dùng tối đa;
4 Đồ uống chứa cacbonat có bổ sung chất chuẩn ở mức xấp xỉ 100 % liều dùng tối đa;
5 Đồ uống chứa cacbonat có bổ sung chất chuẩn ở mức xấp xỉ 120 % liều dùng tối đa.
X Thời gian ( min);
Y Tín hiệu ELSD.
Cột tách Purospher ® Star RP-18, 5 μm4)
Đường kính 3 mm;
Chiều dài cột 250 mm.
Các điều kiện để thí nghiệm được nêu trong tiêu chuẩn này.
Hình B.2-Sắc ký đồ của các loại đồ uống khác nhau bổ sung các chất tạo ngọt thu được sử dụng cột HPLC pha đảo
PHỤ LỤC C
(Tham khảo)
Dữ liệu về độ chụm
Có bảy phòng thử nghiệm đã tham gia phép thử liên phòng. Các đơn vị tham gia vào phép thử sơ bộ để đánh giá mọi trở ngại có thể xảy ra trước khi tham gia xác định chính thức. Trong suốt quá trình đánh giá sơ bộ, các đơn vị tham gia được giao hai mẫu thử với thành phần đã cho của tất cả chín chất tạo ngọt, nghĩa là một mẫu nước giải khát với nồng độ thấp và một mẫu với nồng độ cao của tất cả chín chất tạo ngọt. Hai mẫu thử đã được sử dụng cho mục đích tối ưu hóa và chứng minh tính chính xác hệ thống sắc ký.
Trong quá trình thử nghiệm liên phòng, các đơn vị tham gia được nhận hai mươi mẫu thử (mười mẫu kép mù) của nước giải khát, cụ thể như sau:
- Mẫu 1: Đồ uống cung cấp năng lượng mẫu trắng;
- Mẫu 2: Đồ uống cung cấp năng lượng có bổ sung chất chuẩn ở mức nồng độ xấp xỉ giới hạn định lượng (LOQ);
- Mẫu 3: Đồ uống không chứa cacbonat có bổ sung chất chuẩn ở mức nồng độ xấp xỉ 80 % liều dùng tối đa (MUDs);
- Mẫu 4: Đồ uống chứa cacbonat có bổ sung chất chuẩn ở mức nồng độ xấp xỉ 100 % liều dùng tối đa;
- Mẫu 5: Đồ uống chứa cacbonat có bổ sung chất chuẩn ở mức nồng độ xấp xỉ 120 % liều dùng tối đa
Và nước trái cây đóng hộp:
- Mẫu 6: Nước cocktail trái cây đóng hộp-mẫu trắng;
- Mẫu 7: Nước cocktail trái cây đóng hộp thêm chuẩn ở mức nồng độ xấp xỉ giới hạn định lượng (LOQ);
- Mẫu 8: Nước lê đóng hộp thêm chuẩn ở mức nồng độ xấp xỉ 75 % liều dùng tối đa (MUD);
- Mẫu 9: Nước lê đóng hộp thêm chuẩn ở mức nồng độ xấp xỉ 100 % liều dùng tối đa (MUD);
- Mẫu 10: Nước lê đóng hộp thêm chuẩn ở mức nồng độ xấp xỉ 115 % liều dùng tối đa (MUD).
với các lượng nồng độ thêm chuẩn khác nhau của chín chất tạo ngọt để phân tích.
Chi tiết của phương pháp được áp dụng tại các phòng thử nghiệm khác nhau nêu trong Bảng A.1.
Các dữ liệu sau đây thu được trong các phép thử liên phòng theo quy định của IUPAC Harmonised Protocol [2] do Viện Nghiên cứu vật liệu và phép đo chuẩn của Trung tâm nghiên cứu hỗn hợp Châu Âu (Institute for Reference Materials and Measurements of the European Commission’s Directorate General Joint Research Centre) tổ chức thực hiện.
Bảng C.1 - Acesulfame-K
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 38,3 | 266,6 | 324,1 | 383,5 |
| Giá trị đúng (mg/l) | 42,1 | 282,5 | 354,2 | 421,7 |
| Độ lệch chuẩn lặp lại sr, mg/l | 2,6 | 6,0 | 10,6 | 9,2 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 6,9 | 2,3 | 3,3 | 2,4 |
| Giới hạn lặp lại, r[mg/l] | 7,4 | 16,9 | 29,7 | 25,7 |
| Độ lệch chuẩn tái lập sR, mg/l | 4,2 | 15,6 | 20,1 | 19,3 |
| Độ lệch chuẩn tương đối tái lập, RSDr % | 10,9 | 5,9 | 6,2 | 5,0 |
| Giới hạn tái lập, R, mg/l | 11,6 | 43,8 | 56,2 | 54,0 |
| Giá trị Horrat | 1,2 | 0,9 | 0,9 | 0,8 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 38,4 | 259,2 | 323,0 | 391,3 |
| Giá trị đúng (mg/kg) | 36,5 | 265,6 | 338,8 | 410,0 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 2,7 | 9,1 | 4,1 | 11,4 |
| Độ lệch chuẩn tương đối lặp lại, RSDr % | 6,9 | 3,5 | 1,3 | 2,9 |
| Giới hạn lặp lại, r[mg/kg] | 7,4 | 25,6 | 11,5 | 32,0 |
| Độ lệch chuẩn tái lập sR [mg/kg] | 5,7 | 12,7 | 16,0 | 17,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR, [%] | 14,8 | 4,9 | 4,9 | 4,5 |
| Giới hạn tái lập, R, [mg/kg] | 15,9 | 35,5 | 44,8 | 49,1 |
| Giá trị Horrat | 1,6 | 0,7 | 0,7 | 0,7 |
Bảng C.2 - Alitame
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 31,1 | 69,1 | 96,4 | 114,5 |
| Giá trị đúng (mg/l) | 36,5 | 80,5 | 102,6 | 122,2 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 2,2 | 2,8 | 2,3 | 1,5 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 7,1 | 4,0 | 2,3 | 1,3 |
| Giới hạn lặp lại, r[mg/l] | 6,2 | 7,7 | 6,3 | 4,3 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 3,0 | 7,5 | 2,6 | 3,9 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 9,5 | 10,9 | 2,7 | 3,4 |
| Giới hạn tái lập, R, mg/l | 8,3 | 21,1 | 7,2 | 11,0 |
| Giá trị Horrat | 1,0 | 1,3 | 0,3 | 0,4 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 1 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 6 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 12 | 14 |
| Giá trị trung bình | 36,0 | 113,7 | 142,5 | 175,2 |
| Giá trị đúng [mg/kg] | 34,6 | 116,1 | 145,1 | 175,5 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 3,5 | 2,5 | 3,1 | 6,4 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 9,7 | 2,2 | 2,2 | 3,7 |
| Giới hạn lặp lại, r[mg/kg] | 9,7 | 6,9 | 8,8 | 18,0 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 3,5 | 3,8 | 4,4 | 7,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 9,7 | 3,3 | 3,1 | 4,3 |
| Giới hạn tái lập, R, [mg/kg] | 9,7 | 10,6 | 12,3 | 21,1 |
| Giá trị Horrat | 1,0 | 0,4 | 0,4 | 0,6 |
Bảng C.3 - Aspartame
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 1 | 0 | 0 | 1 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 6 | 7 | 7 | 6 |
| Số lượng kết quả được chấp nhận | 12 | 14 | 14 | 12 |
| Giá trị trung bình | 38,1 | 485,1 | 584,8 | 702,0 |
| Giá trị đúng [mg/l] | 42,0 | 485,0 | 605,0 | 720,3 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 1,9 | 9,5 | 5,0 | 5,8 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 4,9 | 1,9 | 0,9 | 0,8 |
| Giới hạn lặp lại, r[mg/l] | 5,2 | 26,5 | 14,1 | 16,2 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 6,1 | 33,3 | 30,9 | 23,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 16,0 | 6,9 | 5,3 | 3,4 |
| Giới hạn tái lập, R, mg/l | 17,1 | 93,3 | 86,6 | 65,9 |
| Giá trị Horrat | 1,7 | 1,1 | 0,9 | 0,6 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 1 | 0 | 2 | 1 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 6 | 7 | 5 | 6 |
| Số lượng kết quả được chấp nhận | 12 | 14 | 10 | 12 |
| Giá trị trung bình | 37,2 | 739,8 | 951,9 | 1 120,2 |
| Giá trị đúng [mg/l] | 37,3 | 752,1 | 967,8 | 1 171,1 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 3,6 | 16,5 | 4,5 | 13,5 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 9,7 | 2,2 | 0,5 | 1,2 |
| Giới hạn lặp lại, r[mg/kg] | 10,1 | 46,3 | 12,5 | 37,8 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 3,6 | 29,3 | 27,5 | 31,7 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 9,7 | 4,0 | 2,9 | 2,8 |
| Giới hạn tái lập, R, [mg/kg] | 10,1 | 82,0 | 77,1 | 88,8 |
| Giá trị Horrat | 1,0 | 0,7 | 0,5 | 0,5 |
Bảng C.4 - Cyclamate
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 28,3 | 248,9 | 256,8 | 307,2 |
| Giá trị đúng [mg/l] | 36,9 | 239,0 | 252,7 | 300,8 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 1,2 | 6,6 | 3,6 | 5,9 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 4,4 | 2,6 | 1,4 | 1,9 |
| Giới hạn lặp lại, r[mg/l] | 3,5 | 18,4 | 10,2 | 16,5 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 5,8 | 15,4 | 14,0 | 15,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 20,6 | 6,2 | 5,5 | 5,0 |
| Giới hạn tái lập, R, mg/l | 16,3 | 43,1 | 39,2 | 43,4 |
| Giá trị Horrat | 2,1 | 0,9 | 0,8 | 0,7 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 1 | 0 | 1 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 6 | 7 | 6 |
| Số lượng kết quả được chấp nhận | 14 | 12 | 14 | 12 |
| Giá trị trung bình | 27,5 | 749,7 | 924,7 | 1 100,6 |
| Giá trị đúng [mg/kg] | 32,2 | 752,6 | 968,8 | 1172,3 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 4,4 | 7,0 | 14,5 | 12,7 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 16,1 | 0,9 | 1,6 | 1,2 |
| Giới hạn lặp lại, r[mg/kg] | 12,4 | 19,6 | 40,5 | 35,6 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 4,9 | 30,9 | 44,4 | 37,2 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 17,9 | 4,1 | 4,8 | 3,4 |
| Giới hạn tái lập, R, [mg/kg] | 13,7 | 86,5 | 124,2 | 104,3 |
| Giá trị Horrat | 1,8 | 0,7 | 0,8 | 0,6 |
Bảng C.5 - Dulcin
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 55,0 | 79,6 | 95,7 | 115,1 |
| Giá trị đúng [mg/l] | 60,7 | 81,3 | 101,8 | 121,1 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 1,4 | 2,9 | 1,0 | 1,5 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 2,5 | 3,7 | 1,0 | 1,3 |
| Giới hạn lặp lại, r[mg/l] | 3,8 | 8,2 | 2,8 | 4,3 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 3,3 | 3,9 | 5,2 | 5,2 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 6,1 | 4,9 | 5,5 | 4,6 |
| Giới hạn tái lập, R, mg/l | 9,4 | 10,9 | 14,7 | 14,7 |
| Giá trị Horrat | 0,7 | 0,6 | 0,7 | 0,6 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 1 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 6 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 12 | 12 | 14 | 14 |
| Giá trị trung bình | 49,8 | 111,0 | 141,7 | 172,6 |
| Giá trị đúng [mg/kg] | 50,2 | 114,3 | 145,7 | 176,3 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 3,7 | 3,0 | 3,6 | 3,1 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 7,4 | 2,7 | 2,5 | 1,8 |
| Giới hạn lặp lại, r[mg/kg] | 10,3 | 8,4 | 10,1 | 8,6 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 4,3 | 4,8 | 4,7 | 5,4 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 8,6 | 4,3 | 3,3 | 3,1 |
| Giới hạn tái lập, R (R = 2,8 x sR), [mg/kg] | 12,0 | 13,4 | 13,1 | 15,2 |
| Giá trị Horrat | 1,0 | 0,5 | 0,4 | 0,4 |
Bảng C.6 - Neotame
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 37,6 | 77,9 | 97,2 | 115,3 |
| Giá trị đúng [mg/l] | 37,5 | 80,5 | 102,2 | 121,7 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 0,9 | 1,9 | 2,4 | 2,8 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 2,3 | 2,4 | 2,4 | 2,4 |
| Giới hạn lặp lại, r[mg/l] | 2,4 | 5,2 | 6,7 | 7,7 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 2,4 | 4,6 | 4,8 | 5,2 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 6,4 | 5,9 | 5,0 | 4,5 |
| Giới hạn tái lập, R, mg/l | 6,8 | 12,9 | 13,5 | 14,4 |
| Giá trị Horrat | 0,7 | 0,7 | 0,6 | 0,6 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 37,3 | 116,2 | 140,6 | 173,7 |
| Giá trị đúng [mg/kg] | 36,2 | 118,3 | 145,4 | 175,9 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 1,3 | 3,6 | 2,2 | 4,8 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 3,5 | 3,1 | 1,6 | 2,8 |
| Giới hạn lặp lại, r[mg/kg] | 3,6 | 10,1 | 6,2 | 13,5 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 2,2 | 6,3 | 7,5 | 7,7 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 5,9 | 5,4 | 5,3 | 4,5 |
| Giới hạn tái lập, R, [mg/kg] | 6,2 | 17,6 | 21,1 | 21,7 |
| Giá trị Horrat | 0,6 | 0,7 | 0,7 | 0,6 |
Bảng C.7 - Neohesperidine dihydrochalcone
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 31,4 | 42,8 | 51,0 | 59,3 |
| Giá trị đúng [mg/l] | 36,7 | 40,2 | 50,7 | 60,4 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 3,3 | 1,7 | 1,8 | 2,6 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 10,6 | 3,9 | 3,5 | 4,4 |
| Giới hạn lặp lại, r[mg/l] | 9,3 | 4,7 | 4,9 | 7,3 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 9,0 | 6,7 | 4,4 | 5,2 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 28,5 | 15,6 | 8,7 | 8,8 |
| Giới hạn tái lập, R, mg/l | 25,1 | 18,7 | 12,4 | 14,5 |
| Giá trị Horrat | 3,0 | 1,7 | 1,0 | 1,0 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 1 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 6 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 12 | 14 | 14 |
| Giá trị trung bình | 35,3 | 40,5 | 49,8 | 59,3 |
| Giá trị đúng [mg/l] | 33,4 | 37,5 | 48,9 | 59,1 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 105,6 | 108,0 | 102,0 | 100,4 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 6,1 | 2,5 | 4,0 | 3,9 |
| Giới hạn lặp lại, r[mg/kg] | 6,1 | 2,8 | 5,6 | 6,5 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 4,4 | 4,6 | 3,3 | 5,5 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 12,4 | 11,5 | 6,6 | 9,2 |
| Giới hạn tái lập, R(R = 2,8 x sR), [mg/kg] | 12,2 | 13,0 | 9,2 | 15,3 |
| Giá trị Horrat | 1,3 | 1,3 | 0,7 | 1,1 |
Bảng C.8 - Saccarin
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 1 | 0 | 1 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 6 | 7 | 6 |
| Số lượng kết quả được chấp nhận | 14 | 12 | 14 | 12 |
| Giá trị trung bình | 36,2 | 60,1 | 74,1 | 87,6 |
| Giá trị đúng [mg/l] | 40,3 | 65,2 | 80,9 | 96,3 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 1,4 | 1,7 | 3,0 | 1,0 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 3,8 | 2,8 | 4,0 | 1,1 |
| Giới hạn lặp lại, r[mg/l] | 3,9 | 4,7 | 8,3 | 2,7 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 4,0 | 2,8 | 4,9 | 5,2 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 11,1 | 4,6 | 6,6 | 5,9 |
| Giới hạn tái lập, R (R = 2,8 x sR), mg/l | 11,3 | 7,7 | 13,6 | 14,5 |
| Giá trị Horrat | 1,2 | 0,5 | 0,8 | 0,7 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 44,3 | 151,9 | 193,4 | 235,3 |
| Giá trị đúng [mg/kg] | 38,0 | 150,0 | 194,0 | 234,8 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 2,4 | 4,0 | 4,3 | 6,7 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 5,5 | 2,7 | 2,2 | 2,9 |
| Giới hạn lặp lại, r[mg/kg] | 6,8 | 11,3 | 12,0 | 18,8 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 8,4 | 10,6 | 13,5 | 15,0 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 19,0 | 7,0 | 7,0 | 6,4 |
| Giới hạn tái lập, R(R = 2,8 x sR), [mg/kg] | 23,6 | 29,6 | 37,7 | 42,0 |
| Giá trị Horrat | 2,1 | 0,9 | 1,0 | 0,9 |
Bảng C.9 - Sucralose
|
| Nước giải khát | |||
| Mẫu số | 2 | 3 | 4 | 5 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 36,8 | 245,1 | 282,9 | 346,8 |
| Giá trị đúng [mg/l] | 38,9 | 251,8 | 302,6 | 360,3 |
| Độ lệch chuẩn lặp lại sr, [mg/l] | 1,4 | 3,8 | 2,7 | 8,2 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 3,7 | 1,5 | 0,9 | 2,4 |
| Giới hạn lặp lại, r[mg/l] | 3,8 | 10,6 | 7,4 | 22,9 |
| Độ lệch chuẩn tái lập sR, [mg/l] | 5,2 | 10,1 | 16,2 | 13,3 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 14,2 | 4,1 | 5,7 | 3,8 |
| Giới hạn tái lập, R, [mg/l] | 14,7 | 28,2 | 45,3 | 37,4 |
| Giá trị Horrat | 1,5 | 0,6 | 0,8 | 0,6 |
|
| Nước trái cây đóng hộp | |||
| Mẫu số | 7 | 8 | 9 | 10 |
| Năm thử nghiệm | 2007 | 2007 | 2007 | 2007 |
| Số phòng thử nghiệm | 7 | 7 | 7 | 7 |
| Số lượng mẫu thử | 2 | 2 | 2 | 2 |
| Số phòng thử nghiệm ngoại lệ | 0 | 0 | 0 | 0 |
| Số phòng thử nghiệm còn lại sau khi loại trừ các ngoại lệ | 7 | 7 | 7 | 7 |
| Số lượng kết quả được chấp nhận | 14 | 14 | 14 | 14 |
| Giá trị trung bình | 35,3 | 306,1 | 350,2 | 462,4 |
| Giá trị đúng [mg/kg] | 34,6 | 313,1 | 388,2 | 469,7 |
| Độ lệch chuẩn lặp lại sr, [mg/kg] | 2,2 | 7,4 | 8,5 | 9,7 |
| Độ lệch chuẩn tương đối lặp lại, RSDr [%] | 6,3 | 2,4 | 2,2 | 2,1 |
| Giới hạn lặp lại, r[mg/kg] | 6,3 | 20,6 | 23,8 | 27,1 |
| Độ lệch chuẩn tái lập sR, [mg/kg] | 3,8 | 8,7 | 10,4 | 9,7 |
| Độ lệch chuẩn tương đối tái lập, RSDR [%] | 10,9 | 2,8 | 2,7 | 2,1 |
| Giới hạn tái lập, R, [mg/kg] | 10,8 | 24,4 | 29,1 | 27,1 |
| Giá trị Horrat | 1,2 | 0,4 | 0,4 | 0,3 |
PHỤ LỤC D
(Tham khảo)
Các giới hạn hiện hành của EU về chín chất tạo ngọt
Bảng D.1-Các giới hạn hiện hành của EU về chín chất tạo ngọt trong nước giải khát và nước trái cây đóng hộp
| Chất tạo ngọt | MUDa đối với nước giải khát, mg/l | MUDa đối với nước trái cây đóng hộp, mg/kg |
| ACS-K | 350 | 350 |
| ALIb | - | - |
| ASP | 600 | 1000 |
| CYC | 250 | 1000 |
| DULb | - | - |
| NEO | 20 | - |
| NHDC | 30 | 50 |
| SAC | 80 | 200 |
| SCL | 300 | 400 |
| a MUD = liều dùng tối đa theo giới hạn của EU [3] đến [6]. b Chất tạo ngọt chưa có quy định giới hạn của EU. | ||
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] Buchgraber M. and Wasik, A.: Validation of an analytical method for the simultaneous determination of nine intense sweeteners by HPLC-ELSD-Report on the collaborative trial. EUR 22726 EN, 2007
[2] IUPAC Harmonised Protocol for the Design, Conduct and Interpretaticn of method-Performance Studies. Pure & Appl Chem, 1995, 67, 331-343
[3] Directive 94/35/EC of European Parliament and of the Council of 30 June 1994 on sweeteners for use in foodstuffs. Official Journal of European Communities 1994, L237/13
[4] Directive 96/83/EC of the European Parliament and of the Council of 19 December 1996 amending Directive 94/35/EC on sweeteners for use in foodstuffs. Official Journal of European Union 1997, L048, 16-19
[5] Directive 2003/115/EC of the European Parliament and of the Council of 22 December 2003 amending Directive 94/35/EC on sweeteners for use in foodstuffs. Official Journal of European Union 2004, L024, 65-71
[6] Commission Directive 2009/163/EU of 22 December 2009 amending Directive 94/35/EC of the European Parliament and of the Council on sweeteners for use in foodstuffs with regard to neotame. Official Journal of European Union 2009, L344, 37-40
[7] Wasik, A., McCourt, J. and Buchgraber, M.: Simultaneous determination of nine sweeteners in foodstuffs by high performance liquid chromatography and evaporative light scattering detection-Single-laboratory validation. J Chromat A, 2007, 1157, 187-196
2) Đây là ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra để thuận tiện cho người sử dụng tiêu chuẩn mà không ấn định sử dụng sản phẩm này.
3) Purospher® Star RP-18, 5 μm là ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra để thuận tiện cho người sử dụng tiêu chuẩn mà không ấn định sử dụng sản phẩm này.
4) Purospher ® Star RP-18, 5 μm là ví dụ về sản phẩm thích hợp có bán sẵn. Thông tin này được đưa ra để thuận tiện cho người sử dụng tiêu chuẩn mà không ấn định sử dụng sản phẩm này.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 10993:2015 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 10993:2015 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 10993:2015 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 10993:2015 DOC (Bản Word)