- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 10626:2015 Phụ gia thực phẩm-Axit benzoic
| Số hiệu: | TCVN 10626:2015 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Thực phẩm-Dược phẩm |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
14/05/2015 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 10626:2015
Tiêu chuẩn Quốc gia TCVN 10626:2015: Phụ gia thực phẩm - Axit benzoic
Tiêu chuẩn Quốc gia TCVN 10626:2015 về axit benzoic được ban hành ngày 08/12/2015 và có hiệu lực từ ngày 01/01/2016. Tiêu chuẩn này được xây dựng dựa trên cơ sở nghiên cứu của JECFA (2004) và được soạn thảo bởi Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F4 về gia vị và phụ gia thực phẩm.
Tiêu chuẩn này áp dụng cho axit benzoic, hợp chất được sử dụng phổ biến như một loại phụ gia thực phẩm, với mã số INS là 210 và mã số C.A.S là 65-85-0. Công thức hóa học của axit benzoic là C7H6O2 với khối lượng phân tử 122,12. Trọng số ăn vào hàng ngày (ADI) được công nhận là từ 0 mg/kg đến 5 mg/kg thể trọng, với chức năng chính là chất bảo quản kháng vi sinh vật.
Các yêu cầu về nhận biết axit benzoic trong tiêu chuẩn gồm hình dáng tinh thể rắn màu trắng, có mùi đặc trưng nhẹ, độ hòa tan rất ít trong nước và dễ hòa tan trong etanol. Dải nhiệt độ nóng chảy của axit benzoic dao động từ 121°C đến 123°C. Các chỉ tiêu lý-hóa của axit benzoic cũng được quy định rõ ràng, bao gồm phép thử benzoat, trị số pH khoảng 4.0 và hàm lượng axit benzoic tối thiểu 99.5% khối lượng tính theo chất khô.
Tiêu chuẩn đưa ra các phương pháp thử nghiệm cụ thể để xác định các tính chất của axit benzoic, bao gồm phương pháp xác định độ hòa tan, nhiệt độ nóng chảy, hàm lượng tro sulfat, hàm lượng chì và hàm lượng các hợp chất hữu cơ clo hóa. Các chỉ tiêu này nhằm đảm bảo chất lượng và an toàn khi sử dụng axit benzoic trong thực phẩm.
Văn bản chỉ rõ rằng các tài liệu viện dẫn gồm nhiều tiêu chuẩn TCVN khác nhau như TCVN 6469:2010, TCVN 6534:2010, TCVN 8900-2:2012, TCVN 8900-6:2012, và TCVN 8900-8:2012. Những tài liệu này là cần thiết để đảm bảo tính chính xác và tính nhất quán trong việc kiểm tra và phân tích chất lượng axit benzoic.
Thông qua tiêu chuẩn này, các cơ quan quản lý thực phẩm, doanh nghiệp sản xuất và người tiêu dùng có thể nắm bắt được các thông tin và yêu cầu cần thiết liên quan đến axit benzoic. Việc áp dụng tiêu chuẩn sẽ giúp tăng cường sự an toàn thực phẩm và bảo vệ sức khỏe cộng đồng, đồng thời hỗ trợ các doanh nghiệp trong việc tuân thủ quy định về an toàn thực phẩm trong sản xuất và chế biến.
Tải tiêu chuẩn Việt Nam TCVN 10626:2015
TIÊU CHUẨN QUỐC GIA
TCVN 10626:2015
PHỤ GIA THỰC PHẨM - AXIT BENZOIC
Food additives - Benzoic acid
Lời nói đầu
TCVN 10626:2015 được xây dựng dựa trên cơ sở JECFA (2004), Benzoic acid;
TCVN 10626:2015 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F4 Gia vị và phụ gia thực phẩm biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
PHỤ GIA THỰC PHẨM - AXIT BENZOIC
Food additives - Ben zoic acid
1. Phạm vi áp dụng
Tiêu chuẩn này áp dụng cho hợp chất axit benzoic được sử dụng làm phụ gia thực phẩm.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 6469: 2010, Phụ gia thực phẩm - Phương pháp đánh giá ngoại quan và xác định các chỉ tiêu vật lý
TCVN 6534:2010, Phụ gia thực phẩm - Phép thử nhận biết
TCVN 8900-2:2012, Phụ gia thực phẩm - Xác định các thành phần vô cơ - Phần 2: Hao hụt khối lượng khi sấy, hàm lượng tro, chất không tan trong nước và chất không tan trong axit
TCVN 8900-6:2012, Phụ gia thực phẩm - Xác định các thành phần vô cơ - Phần 6: Định lượng antimon, bari, cadimi, crom, đồng, chì và kẽm bằng đo phổ hấp thụ nguyên tử ngọn lửa
TCVN 8900-8:2012, Phụ gia thực phẩm - Xác định các thành phần vô cơ - Phần 8: Định lượng chì và cadimi bằng đo phổ hấp thụ nguyên tử dùng lò graphit
TCVN 9052:2012, Phụ gia thực phẩm - Xác định các thành phần hữu cơ
3. Mô tả
3.1. Tên hóa học: axit benzoic, axit benzencacboxylic, axit phenylcacboxylic
3.2 Kí hiệu
INS (mã số quốc tế về phụ gia thực phẩm): 210
C.A.S (mã số hóa chất): 65-85-0
3.3. Công thức hoá học: C7H6O2
3.4. Công thức cấu tạo (xem Hình 1)
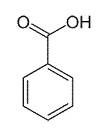
Hình 1 - Công thức cấu tạo của axit benzoic
3.5. Khối lượng phân tử: 122,12
3.6. Chức năng sử dụng: chất bảo quản kháng vi sinh vật.
CHÚ THÍCH: Lượng ăn vào hàng ngày chấp nhận được (ADI) của axit benzoic là từ 0 mg/kg thể trọng đến 5 mg/kg thể trọng.
4. Các yêu cầu
4.1. Nhận biết
4.1.1. Ngoại quan
Tinh thể rắn màu trắng, thường có dạng vảy hoặc hình kim.
4.1.2. Mùi
Có mùi đặc trưng nhẹ.
4.1.3. Độ hòa tan
Rất ít tan trong nước, dễ tan trong etanol.
CHÚ THÍCH: Theo TCVN 6469:2010, một chất được coi là “rất ít tan” nếu cần từ 100 đến dưới 1 000 phần dung môi để hòa tan 1 phần chất tan, một chất “dễ tan” nếu chỉ cần từ 1 đến dưới 10 phần dung môi để hòa tan 1 phần chất tan.
4.1.4. Dải nhiệt độ nóng chảy
Từ 121 oC đến 123 oC.
4.2. Các chỉ tiêu lí - hóa
Các chỉ tiêu lí - hóa của axit benzoic được quy định trong Bảng 1.
Bảng 1 - Chỉ tiêu lí - hóa của axit benzoic
| Tên chỉ tiêu | Mức |
| 1. Phép thử benzoat | Đạt phép thử tại 5.3 |
| 2. Trị số pH (dung dịch trong nước) | Khoảng 4,0 |
| 3. Hao hụt khối lượng sau khi làm khô bằng axit sulfuric trong 3 h, % khối lượng, không lớn hơn | 0,5 |
| 4. Phép thử thăng hoa | Đạt phép thử tại 5.6 |
| 5. Hàm lượng axit benzoic, % khối lượng tính theo chất khô, không nhỏ hơn | 99,5 |
| 6. Hàm lượng tro sulfat, % khối lượng, không lớn hơn | 0,05 |
| 7. Hàm lượng chì, mg/kg, không lớn hơn | 2,0 |
| 8. Các chất dễ bị cacbon hóa | Đạt phép thử tại 5.9 |
| 9. Các chất dễ bị oxy hóa | Đạt phép thử tại 5.10 |
| 10. Hàm lượng các hợp chất hữu cơ clo hóa, tính theo Cl2, % khối lượng, không lớn hơn | 0,07 |
5. Phương pháp thử
5.1. Xác định độ hòa tan, theo 3.7 của TCVN 6469:2010.
5.2. Xác định dải nhiệt độ nóng chảy, theo 3.2 của TCVN 6469:2010.
5.3. Phép thử benzoat, theo 4.2.4 của TCVN 6534:2010.
Sử dụng 0,1 g mẫu với 0,1 g canxi cacbonat và 5ml nước.
5.4. Xác định trị số pH, theo 3.8 của TCVN 6469:2010.
5.5. Xác định hao hụt khối lượng sau khi làm khô, theo 5.1 của TCVN 8900-2:2012.
5.6. Phép thử thăng hoa
Cho một lượng nhỏ mẫu thử vào trong một ống nghiệm khô. Bọc ống nghiệm bằng một giấy lọc ẩm cách đáy ống 4 cm. Đốt nóng ống nghiệm trên ngọn lửa yếu. Axit benzoic thăng hoa, các tinh thể ở phần lạnh hơn của ống nghiệm sẽ bay đi và không còn cặn ở đáy ống nghiệm.
5.7. Xác định hàm lượng tro sulfat, theo 5.3.3 của TCVN 8900-2:2012.
5.8. Xác định hàm lượng chì, theo TCVN 8900-6:2012 hoặc TCVN 8900-8:2012.
5.9. Xác định các chất dễ bị cacbon hóa
5.9.1. Thuốc thử
5.9.1.1. Axit sulfuric đặc, nồng độ từ 94,5 % đến 95,5 % (khối lượng/thể tích).
5.9.1.2. Dung dịch so màu
5.9.1.2.1. Dung dịch axit clohydric loãng
Pha loãng 25 ml axit clohydric đặc (nồng độ từ 36,5 % đến 38 % khối lượng/thể tích) trong 975 ml nước.
5.9.1.2.2. Dung dịch cobalt (II) clorua
Hòa tan khoảng 65 g cobalt (II) clorua ngậm sáu phân tử nước (CoCl2·6H2O) trong một lượng dung dịch axit clohydric loãng (5.9.1.2.1), thêm dung dịch axit clohydric loãng đến 1 000 ml.
Chuẩn hóa nồng độ dung dịch cobalt (II) clorua đã chuẩn bị như sau:
Dùng pipet lấy 5 ml dung dịch cobalt (II) clorua đã chuẩn bị, cho vào bình nón 250 ml có nút mài, thêm 5 ml dung dịch thử hydro peroxit (nồng độ từ 2,5 % đến 3,5 % khối lượng/thể tích) và 15 ml dung dịch natri hydroxit (nồng độ khoảng 20 % khối lượng/thể tích), đun sôi trong 10 min, để nguội rồi thêm 2 g kali iodua và 20 ml dung dịch axit sulfuric loãng (được chuẩn bị từ 1 phần thể tích axit sulfuric đặc và 4 phần thể tích nước). Sau khi kết tủa đã hòa tan hết, chuẩn độ lượng iodua giải phóng được bằng dung dịch natri thiosulfat 0,1 N, sử dụng 3 ml chất chỉ thị hồ tinh bột.
Tiến hành phép thử trắng với cùng lượng thuốc thử.
Mỗi mililit dung dịch natri thiosulfat 0,1 N đã sử dụng tương đương với 23,79 mg CoCl2·6H2O.
Chỉnh thể tích cuối cùng của dung dịch cobalt (II) clorua bằng cách thêm lượng vừa đủ dung dịch axit clohydric loãng (5.9.1.2.1) sao cho mỗi mililit dung dịch cobalt (II) clorua chứa 59,5 mg CoCl2·6H2O.
5.9.1.2.3. Dung dịch sắt (III) clorua
Hòa tan khoảng 55 g sắt (III) clorua ngậm sáu phân tử nước (FeCl3·6H2O) trong một lượng dung dịch axit clohydric loãng (5.9.1.2.1), thêm dung dịch axit clohydric loãng đến 1 000 ml.
Chuẩn hóa nồng độ dung dịch sắt (III) clorua đã chuẩn bị như sau:
Dùng pipet lấy 10 ml dung dịch sắt (III) clorua đã chuẩn bị, cho vào bình nón 250 ml có nút mài, thêm 15 ml nước, 3 g kali iodua và 5 ml axit clohydric đặc (nồng độ từ 36,5 % đến 38 % khối lượng/thể tích), để yên hỗn hợp trong 15 min. Pha loãng với 100 ml nước và chuẩn độ lượng iodua giải phóng được bằng dung dịch natri thiosulfat 0,1 N, sử dụng 3 ml chất chỉ thị hồ tinh bột.
Tiến hành phép thử trắng với cùng lượng thuốc thử.
Mỗi mililit dung dịch natri thiosulfat 0,1 N đã sử dụng tương đương với 27,03 mg FeCl3·6H2O.
Chỉnh thể tích cuối cùng của dung dịch sắt (III) clorua bằng cách thêm lượng vừa đủ dung dịch axit clohydric loãng (5.9.1.2.1) sao cho mỗi mililit dung dịch sắt (III) clorua chứa 45,0 mg FeCl3·6H2O.
5.9.1.2.4. Dung dịch đồng (II) sulfat
Hòa tan khoảng 65 g đồng (II) sulfat ngậm năm phân tử nước (CuSO4·5H2O) trong một lượng dung dịch axit clohydric loãng (5.9.1.2.1), thêm dung dịch axit clohydric loãng đến 1 000 ml.
Chuẩn hóa nồng độ dung dịch đồng (II) sulfat đã chuẩn bị như sau:
Dùng pipet lấy 10 ml dung dịch đồng (II) sulfat đã chuẩn bị, cho vào bình nón 250 ml có nút mài, thêm 40 ml nước, 4 ml axit axetic đặc (nồng độ không nhỏ hơn 99,7 % thể tích), 3 g kali iodua và 5 ml axit clohydric đặc (nồng độ từ 36,5 % đến 38 % khối lượng/thể tích). Chuẩn độ lượng iodua giải phóng được bằng dung dịch natri thiosulfat 0,1 N, sử dụng 3 ml chất chỉ thị hồ tinh bột.
Tiến hành phép thử trắng với cùng lượng thuốc thử.
Mỗi mililit dung dịch natri thiosulfat 0,1 N đã sử dụng tương đương với 24,97 mg CuSO4·5H2O.
Chỉnh thể tích cuối cùng của dung dịch đồng (II) sulfat bằng cách thêm lượng vừa đủ dung dịch axit clohydric loãng (5.9.1.2.1) sao cho mỗi mililit dung dịch đồng (II) sulfat chứa 62,4 mg CuSO4·5H2O.
5.9.1.2.5. Chuẩn bị dung dịch so màu
Chuẩn bị dung dịch so màu từ dung dịch cobalt (II) clorua (5.9.1.2.2), dung dịch sắt (III) clorua (5.9.1.2.3), dung dịch đồng (II) sulfat (5.9.1.2.4) và nước theo tỉ lệ 0,2 : 0,3 : 0,1 : 4,4 (phần thể tích).
5.9.2. Cách tiến hành
Cân 0,5 g mẫu thử, chính xác đến 1 mg, hòa tan trong 5 ml axit sulfuric đặc (5.9.1.1). Màu tạo thành trong dung dịch không được đậm hơn màu hồng nhạt của dung dịch so màu (5.9.1.2.5).
5.10. Xác định các chất dễ bị oxy hóa
5.10.1. Thuốc thử
5.10.1.1. Dung dịch kali permanganat, 0,1 N.
5.10.1.2. Thuốc thử oxy hóa
Thêm 1,5 ml axit sulfuric đặc (nồng độ từ 94,5 % đến 95,5 %) vào 100 ml nước, đun sôi hỗn hợp, nhỏ từng giọt dung dịch kali permanganat 0,1 N đến khi dung dịch có màu hồng bền trong 30 s.
5.10.2. Thiết bị, dụng cụ
5.10.2.1. Bếp điện.
5.10.2.2. Cân phân tích, có thể cân chính xác đến 1 mg.
5.10.2.3. Pipet.
5.10.2.4. Buret.
5.10.3. Cách tiến hành
Cân 1 g mẫu, chính xác đến 1 mg, cho vào dung dịch thuốc thử oxy hóa (5.10.1.2) còn nóng và chuẩn độ bằng dung dịch kali permanganat 0,1 N (5.10.1.1) cho đến khi dung dịch có màu hồng bền trong 15 s. Thể tích dung dịch kali permanganat sử dụng để chuẩn độ không lớn hơn 0,5 ml.
5.11. Xác định hàm lượng các hợp chất hữu cơ clo hóa, theo 2.2 của TCVN 9052:2012.
Sử dụng 0,25 g mẫu thử, hòa tan trong 10 ml dung dịch natri hydroxit 0,1 N thay vì 10 ml nước. Sử dụng 0,5 ml dung dịch axit clohydric 0,01 N khi chuẩn bị dung dịch so sánh.
5.12. Xác định hàm lượng axit benzoic
5.12.1. Thuốc thử
5.12.1.1. Etanol.
5.12.1.2. Dung dịch phenol đỏ (phenolsulfonphthalein)
Hòa tan 0,1 g phenolsulfonphthalein trong 100 ml etanol, lọc nếu cần.
5.12.1.3. Dung dịch natri hydroxit, 0,5 N.
5.12.1.4. Dung dịch phenolphthalein
Hòa tan 0,2 g phenolphthalein (C20H14O4) trong 60 ml etanol 90 % thể tích đựng trong bình định mức 100 ml, thêm nước đến vạch và trộn.
5.12.1.5. Nước cất hoặc nước có chất lượng tương đương.
5.12.2. Thiết bị, dụng cụ
5.12.2.1. Tủ sấy.
5.12.2.2. Cân phân tích, có thể cân chính xác đến 1 mg.
5.12.2.3. Pipet.
5.12.2.4. Buret.
5.12.3. Cách tiến hành
Cân 2,5 g mẫu thử đã được sấy khô, chính xác đến 1 mg. Hoà tan trong 15 ml etanol ấm, trước đó đã được trung hoà, sử dụng dung dịch phenol đỏ (5.12.1.2) làm chất chỉ thị. Thêm 20 ml nước và chuẩn độ bằng dung dịch natri hydroxit 0,5 N (5.12.1.3) với chỉ thị là phenolphthalein (5.12.1.4).
5.12.4. Tính kết quả
Hàm lượng axit benzoic có trong mẫu thử, X, biểu thị bằng phần trăm khối lượng tính theo chất khô, tính theo công thức sau:
![]()
Trong đó:
V là thể tích dung dịch natri hydroxit 0,5 N đã dùng để chuẩn độ, tính bằng mililit (ml);
61,06 là số miligam axit benzoic (C7H6O2) tương đương với 1 ml dung dịch natri hydroxit 0,5 N;
w là khối lượng mẫu thử tính theo chất khô, tính bằng gam (g);
1000 là hệ số chuyển đổi từ miligam sang gam.
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] U.S. Pharmacopeia (Dược điển Hoa Kì), Part 631 - Color and achromicity
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 10626:2015 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 10626:2015 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 10626:2015 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 10626:2015 DOC (Bản Word)