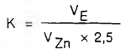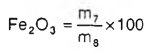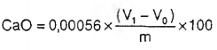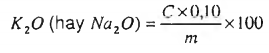- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 7131:2016 Đất sét - Phương pháp phân tích hóa học
| Số hiệu: | TCVN 7131:2016 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Tài nguyên-Môi trường |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
06/04/2016 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 7131:2016
Tiêu chuẩn Quốc gia TCVN 7131:2016 Đất sét - Phương pháp phân tích hóa học
Ngày 06/04/2016, Bộ Khoa học và Công nghệ đã công bố Tiêu chuẩn Quốc gia TCVN 7131:2016 về phương pháp phân tích hóa học đất sét, do Viện Vật liệu Xây dựng thuộc Bộ Xây dựng biên soạn và có hiệu lực ngay khi công bố. Tiêu chuẩn này thay thế cho TCVN 7131:2002.
Tiêu chuẩn này quy định những phương pháp để xác định các thành phần hóa học chủ yếu có trong đất sét. Nó áp dụng cho các loại vật liệu tự nhiên có thành phần tương tự như cao lanh, trường thạch và đất giàu sắt.
Phương pháp phân tích hóa học
TCVN 7131:2016 quy định chi tiết nhiều phương pháp phân tích hóa học. Trong đó, các bước phân tích bao gồm xác định hàm lượng mất khi nung, hàm lượng silic dioxide, hàm lượng sắt (III) oxide, và một số thành phần khác. Các mẫu phân tích phải được chuẩn bị kỹ lưỡng, bao gồm việc sấy nóng và nghiền mịn.
Chuẩn bị mẫu thử
Mẫu thử cần được lấy theo quy định kỹ thuật để đảm bảo tính đại diện. Khối lượng mẫu thử ít nhất phải là 500 g với kích thước hạt không lớn hơn 5 mm. Nghiền mịn mẫu thử cho đến khi lọt qua sàng 0,063 mm, sau đó sấy ở nhiệt độ quy định để đạt khối lượng không đổi.
Xác định hàm lượng các thành phần
Quy trình xác định hàm lượng các thành phần hóa học được thực hiện theo sơ đồ phân tích trong tiêu chuẩn. Ví dụ, để xác định hàm lượng silic dioxide (SiO2), mẫu thử phải được nung và xử lý với các hóa chất nhất định để tách và đo lường lượng SiO2 có trong mẫu. Tương tự, hàm lượng sắt (III) oxide (Fe2O3) có thể được xác định qua nhiều phương pháp như đo màu hoặc chuẩn độ phức chất.
Thông điệp từ tiêu chuẩn này là giúp các cơ sở nghiên cứu, kiểm định và sản xuất vật liệu xây dựng có một nền tảng vững chắc về các phương pháp phân tích hóa học đất sét, từ đó nâng cao chất lượng sản phẩm và bảo vệ sức khỏe cộng đồng.
Tải tiêu chuẩn Việt Nam TCVN 7131:2016
TIÊU CHUẨN QUỐC GIA
TCVN 7131:2016
ĐẤT SÉT - PHƯƠNG PHÁP PHÂN TÍCH HÓA HỌC
Clay - Methods for chemical analysis
Lời nói đầu
TCVN 7131:2016 thay thế TCVN 7131:2002.
TCVN 7131:2016 do Viện Vật liệu Xây dựng - Bộ Xây dựng biên soạn. Bộ Xây dựng đề nghị, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định. Bộ Khoa học và Công nghệ công bố.
ĐẤT SÉT - PHƯƠNG PHÁP PHÂN TÍCH HÓA HỌC
Clay - Methods for Chemical analysis
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp phân tích xác định các thành phần hóa học chủ yếu trong đất sét.
Tiêu chuẩn này có thể áp dụng phân tích các vật liệu tự nhiên có thành phần tương tự đất sét như: cao lanh, trường thạch, đất cao silic, đất giàu sắt.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau là cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851 (ISO 3696), Nước dùng để phân tích trong phòng thí nghiệm - Yêu cầu kỹ thuật và phương pháp thử.
3 Quy định chung
3.1 Nước dùng trong quá trình phân tích theo TCVN 4851 (ISO 3696) hoặc nước có độ tinh khiết tương đương (sau đây gọi là “nước”).
3.2 Hóa chất dùng trong phân tích có độ tinh khiết không thấp hơn “tinh khiết phân tích” (TKPT).
3.3 Hóa chất pha loãng được biểu thị theo tỷ lệ thể tích. Ví dụ HCl (1 + 1) là dung dịch gồm 1 thể tích HCl đậm đặc với 1 thể tích nước.
3.4 Nồng độ của dung dịch pha loãng tính phần trăm (%) được biểu thị bằng số gam chất tan trong 100 mL nước. Ví dụ bari chloride (BaCl2), dung dịch 5 % là dung dịch gồm 5 g bari chloride hòa tan trong 100 mL nước.
3.5 Khối lượng riêng (d) của thuốc thử đậm đặc được tính bằng gam trên mililít (g/mL).
3.6 Chỉ tiêu phân tích được tiến hành song song trên hai lượng cân của mẫu thử và một thí nghiệm trắng (bao gồm các lượng thuốc thử như đã nêu trong tiêu chuẩn, nhưng không có mẫu thử) để hiệu chỉnh kết quả.
Chênh lệch (tính theo gia trị tuyệt đối) giữa hai kết quả xác định song song không được vượt giới hạn cho phép, nếu vượt giới hạn cho phép phải tiến hành phân tích lại.
3.7 Việc xây dựng lại đường chuẩn (nếu có) được tiến hành định kỳ theo khuyến cáo của nhà sản xuất thiết bị và thực hiện theo quy trình trong tiêu chuẩn.
3.8 Xác định khối lượng không đổi
Xác định khối lượng không đổi bằng cách: nung hoặc sấy mẫu đến nhiệt độ quy định và giữ ở nhiệt độ này trong 15 min, để nguội mẫu trong bình hút ẩm đến nhiệt độ phòng và cân. Quá trình được lặp lại đến khi chênh lệch giữa hai lần cân liên tiếp không vượt quá 0,0005 g.
3.9 Biểu thị kết quả
Kết quả cuối cùng tính bằng phần trăm (%), là trung bình cộng của hai kết quả phân tích tiến hành song song, lấy đến 2 chữ số có nghĩa sau dấu phẩy.
4 Hóa chất, thuốc thử
4.1 Dinatri carbonat (Na2CO3) khan.
4.2 Dikali carbonat (K2CO3) khan.
4.3 Dikali disulfat (K2S2O7) khan.
4.4 Amoni chloride (NH4Cl) tinh thể.
4.5 Bạc nitrat (AgNO3).
4.6 Magnesi oxide (MgO) khan.
4.7 Hỗn hợp nung chảy carbonat
Trộn đều dinatri carbonat khan (4.1) với dikali carbonat khan (4.2) theo tỷ lệ 1:1 về khối lượng. Bảo quản trong bình polyethylen kín.
4.8 Hỗn hợp nung chảy eska
Trộn đều magnesi oxide khan (4.6) với dinatri carbonat khan (4.1) theo tỷ lệ 2:1 về khối lượng. Bảo quản trong bình polyethylen kín.
4.9 Hydro trioxonitrat (HNO3) đậm đặc, d = 1,12.
4.10 Hydro chloride (HCl) đậm đặc, d = 1,19.
4.11 Hydro chloride (HCl), pha loãng (1 + 1).
4.12 Hydro chloride (HCl), pha loãng (1 + 9).
4.13 Hydro chloride (HCl), pha loãng (5 + 95).
4.14 Hydro fluoride (HF) đậm đặc, d = 1,12 (38 % đến 40 %).
4.15 Dihydro sulfat (H2SO4), đậm đặc, d = 1,84.
4.16 Dihydro sulfat (H2SO4), pha loãng (1 + 1).
4.17 Dihydro sulfat (H2SO4), pha loãng (1 + 20).
4.18 Dihydro sulfat (H2SO4), pha loãng (9 + 1000).
4.19 Acid acetic (CH3COOH) đậm đặc, d = 1,05 đến 1,06.
4.20 Amoni hydroxide (NH4OH) đậm đặc, d = 0,88 (25 %).
4.21 Natri hydroxide (NaOH), dung dịch 10 %, bảo quản trong bình polyethylen.
4.22 Natri hydroxide (NaOH), dung dịch 30 %, bảo quản trong bình polyethylen.
4.23 Kali hydroxide (KOH), dung dịch 25 %, bảo quản trong bình polyethylen.
4.24 Kali cyanide (KCN), dung dịch 5 %, bảo quản trong bình polyethylen.
4.25 Bari chloride (BaCl2), dung dịch 10 %.
4.26 Acid sulfosalicylic (C6H4(OH)SO3H), dung dịch 10 %.
4.27 Bạc nitrat (AgNO3), dung dịch 0,5 %, bảo quản trong bình thủy tinh màu.
4.28 Natri flouride (NaF), dung dịch 3 %, bảo quản trong bình polyethylen.
4.29 Diantipyrin methane (C23H24N4O2), dung dịch 2 %: Khuấy đều 25 ml dihydro sulfat đậm đặc trong 300 mL nước, thêm 20 g thuốc thử diantipyrin methane, khuấy đều cho tan hết thuốc thử, pha loãng thành 1000 mL. Bảo quản trong chai thủy tinh màu.
4.30 Chỉ thị eriocrom T đen (ETOO) (C20H12N3NaO7S), dung dịch 0,1 %: Hòa tan 0,1 g chỉ thị ETOO trong 100 mL ethanol 90 %, thêm 3 g hydroxylamin hydrochloride (NH2OH.HCl), khuấy đều. Bảo quản trong chai thủy tinh tối màu.
4.31 Chất chỉ thị fluorexon (C30H26N2O13) 1 %: Dùng cối chày thủy tinh nghiền mịn 0,1 g chỉ thị màu fluorexon với 10 g kali chloride, bảo quản trong lọ thủy tinh màu.
4.33 Chỉ thị amoni sắt (III) sulfat (Fe(NH4)(SO4)2), dung dịch 1 %.
4.34 Thiourea (S(NH2)2), dung dịch 5 %: hòa tan 5 g thuốc thử trong 100 mL nước. Bảo quản trong chai thủy tinh tối màu.
4.35 Chỉ thị xylenol da cam (C31H28N2Na4O13S), dung dịch 0,1 %: Hòa tan 0,1 g thuốc thử xylenol da cam trong 100 mL nước. Dung dịch trong 30 ngày.
4.36 Chỉ thị phenolphtalein (C20H14O4), dung dịch 0,1 %: Hòa tan 0,1 g phenolphtalein trong 100 mL ethanol 90 %.
4.37 Chỉ thị Bari Diphenyiamine sulfonated (C24H20BaN2O6S2), dung dịch 0,1 %: Hòa tan 0,1 g Bari Diphenylamine sulfonated trong 100 mL nước. Dung dịch dùng trong 30 ngày.
4.38 Dung dịch đệm pH 5,5: Hòa tan 100 ml amoni hydroxide đậm đặc vào khoảng từ 300 mL đến 400 mL nước, thêm 100 mL acid acetic đậm đặc (4.19), thêm nước thành 1000 mL, khuấy đều. Dùng máy đo pH để kiểm tra lại giá trị pH của dung dịch đệm.
4.39 Dung dịch đệm pH 10,5: Hòa tan 54 g amoni chloride vào 500 mL nước, thêm 350 mL amoni hydroxide đậm đặc (4.20), thêm nước thành 1000 mL, khuấy đều. Dùng máy đo pH để kiểm tra lại giá trị pH của dung dịch đệm.
4.40 Hỗn hợp dung dịch khử: Hòa tan 15 g acid tartaric (H2C4H4O6) và 1 g acid ascorbic (C6H806) trong 100 mL nước. Dung dịch sử dụng được trong 2 đến 3 ngày, bảo quản trong bình thủy tinh tối màu.
4.41 Amoni heptamolybdat ((NH4)6Mo7O24.4H2O), dung dịch 5 %: Hòa tan 25 g amoni heptamolybdat ((NH4)6Mo7O24.4H2O) vào 200 mL nước đun ấm cho tan, (nếu dung dịch đục thì phải lọc), thêm nước đến thể tích 500 mL. Dung dịch sử dụng được trong bốn tuần, bảo quản trong bình polyethylen.
4.42 Dung dịch trihydro trioxoborat (H3BO3) bão hòa: hòa tan 50 g trihydro trioxoborat (H3BO3) vào 1000 mL nước nóng. Chỉ sử dụng dung dịch trong ngày.
4.43 Dung dịch acid citric (C6H8O7H2O), dung dịch 10 %: hòa tan 10 g acid citric (C6H8O7H2O) trong 100 mL nước. Nếu dung dịch đục thì phải lọc. Sử dụng dung dịch trong 2 đến 3 ngày, bảo quản trong bình thủy tinh.
4.44 Hỗn hợp dihydro sulfat - tetraoxophotsphat: Thêm từ từ 150 mL trihydro tetraoxophotsphat (H3PO4) vào 700 mL nước. Chờ cho đến khi dung dịch nguội đến nhiệt độ phòng, cẩn thận cho thêm từ từ 150 mL dihydro sulfat (H2SO4).
4.45 Dung dịch thủy ngân chloride (HgCl2) 5 %: Hòa tan 5 g HgCl2 vào 100 mL nước, đun nhẹ đến khi thu được dung dịch trong suốt.
4.46 Thiếc (II) chloride (SnCl2), dung dịch 5 %: hòa tan 5 g SnCl2.H2O vào 10 mL dung dịch HCl đậm đặc, thêm nước đến thể tích 100 mL rồi đun đến tan trong. Dung dịch sử dụng trong 30 ngày.
4.47 Dung dịch tiêu chuẩn EDTA (Na2H2C10H12O8N2.2H2O) 0,01 M: Pha chế từ ống chuẩn (fixanal) EDTA 0,01 M.
4.48 Dung dịch tiêu chuẩn bạc nitrat (AgNO3) 0,1 M: Pha từ ống chuẩn (fixanal) bạc nitrat (AgNO3) 0,1 M, bảo quản trong chai thủy tinh tối màu. Dung dịch sử dụng trong 30 ngày.
4.49 Dung dịch dikali dicromat (K2Cr2O7) 0,2 M: Pha từ ống chuẩn (fixanal) kali dicromat (K2Cr2O7) 0,2 M.
4.50 Dung dịch tiêu chuẩn amoni thiocyanat (NH4SCN) 0,1 M: Pha chế từ ống chuẩn (fixanal) amoni thiocyanat (NH4SCN) 0,1 M.
4.51 Dung dịch tiêu chuẩn kẽm acetat (Zn(CH3COO)2) 0,025 M
4.51.1 Pha chế dung dịch tiêu chuẩn kẽm acetat (Zn(CH3COO)2) 0,025 M
Hòa tan từ 5,5 g đến 5,7 g kẽm acetat (Zn(CH3COO)2.2H2O) vào 200 mL nước, thêm 2 mL acid acetic đậm đặc (4.2.10), đun đến tan trong, pha loãng thành 1000 mL.
4.51.2 Xác định tỷ số nồng độ K giữa dung dịch EDTA 0,01 M và dung dịch kẽm acetat 0,025 M
Dùng pipet lấy 25 ml dung dịch EDTA 0,01 M (4.47) vào cốc dung tích 250 mL, thêm 100 mL nước và 20 mL dung dịch đệm pH 5,5 (4.38), thêm 2 giọt đến 3 giọt chỉ thị xylenol da cam 0,1 % (4.35). Đun tới nhiệt độ đạt từ 70 °C đến 80 °C, chuẩn độ dung dịch khi còn nóng bằng dung dịch kẽm acetat pha được đến khi dung dịch trong cốc chuyển từ màu vàng sang hồng, ghi thể tích dung dịch kẽm acetat tiêu thụ (VZn).
Xác định tỷ số nồng độ (K) giữa hai dung dịch theo công thức (1) sau:
|
| (1) |
trong đó:
VE là thể tích dung dịch EDTA lấy để chuẩn độ, tính bằng mililít (mL);
VZn là thể tích dung dịch Zn(CH3COO)2 tiêu thụ khi chuẩn độ, tính bằng mililít (mL).
4.52 EDTA (Na2H2C10H12O8N2.2H2O), dung dịch 1 %, bảo quản trong bình polyethylen.
4.53 Dung dịch tiêu chuẩn gốc sắt (III) oxide (chứa 0,25 mg Fe2O3 trong 1 mL)
Sử dụng dung dịch tiêu chuẩn mua được hoặc:
Cân khoảng 0,25 g sắt oxide (Fe2O3) chính xác đến 0,0001 g đã sấy khô ở nhiệt độ 110 °C vào cốc thủy tinh dung tích 100 mL, thêm 50 mL dung dịch hydro chloride (1 + 1) (4.11) và đun sôi nhẹ đến tan trong. Để nguội, chuyển vào bình định mức 1000 mL, thêm nước tới vạch mức, lắc đều.
4.54 Dung dịch tiêu chuẩn sắt (III) oxide làm việc (chứa 0,05 mg Fe2O3 trong 1 mL)
Dùng pipet lấy 50 mL dung dịch tiêu chuẩn gốc sắt (III) oxide (4.53) vào bình định mức dung tích 250 ml, thêm nước tới vạch mức, lắc đều.
4.55 Dung dịch tiêu chuẩn gốc titani dioxide (chứa 0,1 mg TiO2 trong 1 mL).
Sử dụng dung dịch tiêu chuẩn mua được hoặc:
Cân khoảng 0,3005 g dikali titani hexaflouride (K2TiF6) chính xác đến 0,0001 g đã sấy khô ở nhiệt độ 110 °C vào chén bạch kim, thêm khoảng 10 ml đến 15 ml dung dịch (1 + 1) (4.16), làm bay hơi trên bếp điện đến khô. Thêm tiếp 5 mL dung dịch dihydro sulfat (1 + 1) (4.16) nữa, tiếp tục làm bay hơi đến khô kiệt (ngừng bốc khói trắng). Dùng dung dịch dihydro sulfat (1 + 20) (4.17) chuyển định dihydro sulfat lượng phần cặn còn lại trong chén vào cốc thủy tinh dung tích 250 mL. Thêm 5 mL dung dịch dihydro sulfat (1 + 1) (4.16) và đun tới sôi. Lấy ra để nguội, chuyển dung dịch vào bình định mức dung tích 1000 mL, dùng dung dịch dihydro sulfat (1 + 20) (4.17) định mức, lắc đều.
4.56 Dung dịch tiêu chuẩn titani dioxide làm việc (chứa 0,04 mg TiO2 trong 1 mL):
Dùng pipet lấy 100 mL dung dịch tiêu chuẩn gốc titani dioxide (4.55) vào bình định mức dung tích 250 mL, dùng dung dịch dihydro sulfat (1 + 20) (4.17) định mức, lắc đều.
4.57 Dung dịch tiêu chuẩn gốc silic dioxide (chứa 0,2 mg SiO2 trong 1 mL)
Sử dụng dung dịch tiêu chuẩn mua sẵn hoặc:
Nung chảy 0,10 g silic dioxide tinh khiết (đã được nung ở 1000 °C đến khối lượng không đổi) với 3 g - 4 g hỗn hợp nung chảy (4.6) trong chén bạch kim ở nhiệt độ (950 ± 50) °C trong thời gian từ 30 min đến 40 min. Lấy chén ra đặt nghiêng, để nguội. Chuyển định lượng khối nung chảy vào cốc đã có sẵn 200 mL nước và 10 g NaOH, rồi đun tới tan trong. Để nguội, thêm nước tới 500 mL, lắc đều. Bảo quản trong bình polyethylen.
4.58 Dung dịch tiêu chuẩn silic dioxide làm việc (chứa 0,02 mg SiO2 trong 1 mL)
Dùng pipet lấy 25 ml dung dịch tiêu chuẩn gốc silic dioxide (4.57) vào bình định mức dung tích 250 mL, thêm nước tới vạch mức, lắc đều. Bảo quản dung dịch trong bình polyethylen. Dung dịch sử dụng được trong 7 ngày.
4.59 Dung dịch tiêu chuẩn gốc dinatri oxide (chứa 0,3 mg Na2O trong 1 mL)
Sử dụng dung dịch tiêu chuẩn mua sẵn hoặc:
Hòa tan 0,5660 g NaCl đã sấy ở nhiệt độ 110 °C vào nước, chuyển vào bình định mức 1000 mL, thêm nước đến vạch mức, lắc đều. Bảo quản trong bình polyethylen.
4.60 Dung dịch tiêu chuẩn dinatri oxide làm việc (chứa 0,03 mg Na2O trong 1 mL)
Dùng pipet bầu lấy 10 mL dung dịch tiêu chuẩn gốc dinatri oxide (4.59) cho vào bình định mức làm bằng polyethylen dung tích 100 mL, thêm nước đến vạch mức, lắc đều. Chỉ sử dụng dung dịch trong ngày.
4.61 Dung dịch tiêu chuẩn gốc dikali oxide (chứa 0,3 mg K2O trong 1 mL)
Sử dụng dung dịch tiêu chuẩn mua sẵn hoặc:
Hòa tan 0,4750 g KCl đã sấy ở nhiệt độ 110 °C vào nước, chuyển vào bình định mức 1000 mL, thêm nước đến vạch mức, lắc đều. Bảo quản trong bình polyethylen.
4.62 Dung dịch tiêu chuẩn dikali oxide làm việc (chứa 0,03 mg K2O trong 1 mL)
Dùng pipet bầu lấy 10 mL dung dịch tiêu chuẩn gốc dikali oxide (4.61) cho vào bình định mức 100 mL, thêm nước đến vạch mức, lắc đều.
5 Thiết bị, dụng cụ
5.1 Cân phân tích, có độ chính xác 0,0001 g.
5.2 Cân kỹ thuật, có độ chính xác 0,001 g.
5.3 Tủ sấy, có bộ phận điều khiển và khống chế nhiệt độ đến (300 ± 5) °C.
5.4 Lò nung, có bộ phận điều khiển và khống chế nhiệt độ đến (950 ± 50) °C.
5.5 Máy đo màu UV-VIS (quang phổ hấp thụ phân tử), có bước sóng từ 380 nm đến 850 nm.
5.6 Thiết bị quang phổ hấp thụ nguyên tử (AAS), có trang bị thích hợp để đo kali và natri.
5.7 Bếp cách thủy hoặc cách cát, khống chế được nhiệt độ.
5.8 Chén bạch kim, dung tích 50 mL.
5.9 Chén sứ, dung tích 30 mL.
5.10 Sàng các loại, có kích thước lỗ 0,5 mm; 0,25 mm; 0,1 mm; 0,063 mm.
5.11 Chày, cối bằng mã não.
5.12 Chày, cối bằng đồng.
5.13 Bình hút ẩm, chứa hạt silicagel.
5.14 Bình định mức bằng thủy tinh, dung tích 100 mL; 250 mL; 500 ml; 1000 mL.
5.15 Bình định mức bằng polyethylen hoặc bằng thủy tinh borosilicat, dung tích 100 mL.
5.16 Pipet bầu, dung tích 2 ml; 5 mL; 10 ml; 20 ml; 25 mL; 50 mL; 100 mL.
5.17 Buret, dung tích 5 mL và 25 ml.
5.18 Cốc thủy tinh, dung tích 100 mL và 250 mL.
5.19 Bát cô mẫu, làm bằng thạch anh hoặc sứ, dung tích khoảng 500 mL.
5.20 Giấy lọc không tro
- Giấy lọc định lượng không tro chảy chậm (đường kính lỗ trung bình khoảng 2 μm).
- Giấy lọc định lượng không tro chảy trung bình (đường kính lỗ trung bình khoảng 7 μm).
- Giấy lọc loại chảy nhanh (đường kính lỗ trung bình khoảng 20 μm).
5.21 Các dụng cụ thủy tinh thông thường dùng trong phòng thí nghiệm.
6 Chuẩn bị mẫu thử
Mẫu thử dùng cho phân tích hóa học được lấy theo các quy định kỹ thuật về lấy mẫu thí nghiệm trong các cơ sở sản xuất và sử dụng nguyên liệu để đảm bảo mẫu thử là đại diện cho lô hàng được lấy.
Mẫu đưa tới phòng thí nghiệm có khối lượng không ít hơn 500 g, kích thước hạt không lớn hơn 5 mm.
Trộn đều mẫu, dùng phương pháp chia tư lấy khoảng 100 g, nghiền nhỏ đến lọt hết qua sàng 0,25 mm. Bằng phương pháp chia tư lấy khoảng 50 g mẫu nghiền mẫu đến lọt hết qua sàng 0,1 mm. Tiếp tục dùng phương pháp chia tư để lấy khoảng 12 g đến 15 g mẫu nghiền mịn trên cối mã não đến cỡ hạt lọt qua sàng 0,063 mm dùng làm mẫu phân tích hóa học. Lượng mẫu còn lại bảo quản trong lọ (túi) kín làm mẫu lưu.
Mẫu dùng để phân tích hóa học được sấy ở nhiệt độ (105 ± 5) °C đến khối lượng không đổi, làm nguội trong bình hút ẩm đến nhiệt độ phòng trước khi tiến hành cân để thử nghiệm.
7 Phương pháp thử
Quá trình phân tích hóa học được tiến hành theo sơ đồ trong Hình 1.
7.1 Xác định hàm lượng mất khi nung (MKN)
7.1.1 Nguyên tắc
Mẫu thử được nung ở nhiệt độ (950 ± 50) °C đến khối lượng không đổi. Từ sự giảm khối lượng của mẫu thử, tính ra lượng mất khi nung.
7.1.2 Cách tiến hành
Nung chén sứ ở nhiệt độ (950 ± 50) °C đến khối lượng không đổi, để nguội trong bình hút ẩm đến nhiệt độ phòng và cân để biết khối lượng chén.
Cân khoảng 1 g mẫu (Điều 6) chính xác đến 0,0001 g, cho vào chén sứ rồi nung chén có chứa mẫu ở nhiệt độ (950 ± 50) °C trong khoảng thời gian từ 1 h đến 1,5 h. Lấy chén ra, để nguội trong bình hút ẩm đến nhiệt độ phòng rồi cân. Lặp lại quá trình nung và cân chén có chứa mẫu đến khi thu được khối lượng không đổi.
7.1.3 Biểu thị kết quả
Lượng mất khi nung (MKN), tính bằng phần trăm (%), theo công thức (2):
|
| (2) |
trong đó:
m1 là khối lượng chén và mẫu trước khi nung, tính bằng gam (g);
m2 là khối lượng chén và mẫu sau khi nung, tính bằng gam (g);
m là lượng cân mẫu thử, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai thí nghiệm tiến hành song song không vượt quá 0,20 %.
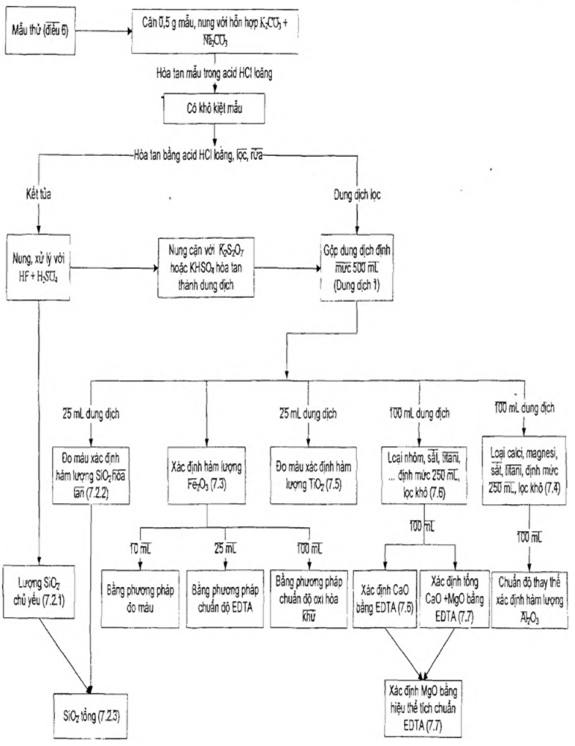
Hình 1: Sơ đồ phân tích hóa học mẫu đất sét.
7.2 Xác định hàm lượng silic dioxide (SiO2)
7.2.1 Xác định hàm lượng silic dioxide chủ yếu bằng phương pháp khối lượng
7.2.1.1 Nguyên tắc
Phân giải mẫu bằng hỗn hợp nung chảy, hòa tan khối chảy bằng hydro chloride (HCl) và cô cạn để tách nước của tetrahydro orthosilicat (H2SiO4). Lọc, tách và nung kết tủa ở nhiệt độ (950 ± 50) °C, xử lý kết tủa bằng dung dịch hydro fluoride để tách silic ở dạng silic tetraflouride (SiF4) dễ bay hơi. Từ sự giảm khối lượng của chén có chứa kết tủa sau khi xử lý bằng hydro fluoride xác định được lượng silic dioxide chủ yếu.
7.2.1.2 Cách tiến hành
Cân khoảng 0,5 g mẫu thử (Điều 6), chính xác đến 0,0001 g, cho vào chén bạch kim có lót sẵn 3 g đến 4 g hỗn hợp nung chảy (4.6) và phủ lên trên một lớp mỏng (khoảng 3 g) hỗn hợp nung chảy nữa.
Nung chảy hỗn hợp có trong chén ở nhiệt độ (950 ± 50) °C trong khoảng từ 40 min đến 45 min đến khi mẫu tan trong. Lấy chén ra khỏi lò nung, để nguội.
Chuyển toàn bộ khối nung chảy vào bát cô mẫu. Dùng dung dịch HCl (1 + 1) (4.11) và nước cất nóng rửa sạch chén bạch kim. Đậy bát sứ bằng mặt kính đồng hồ, thêm từ từ 30 mL HCl đậm đặc (4.10) để hòa tan khối chảy. Sau đó, dùng nước cất nóng tia rửa thành bát và mặt kính, khuấy đều dung dịch.
Cô cạn dung dịch trên bếp cách cát hoặc cách thủy (nhiệt độ khoảng từ 100 °C đến 110 °C) đến khi không còn giọt nước trên mặt kính đồng hồ. Trong quá trình cô mẫu, chú ý dùng đũa thủy tinh dằm nhỏ các hạt muối tạo thành.
Để nguội bát cô mẫu, thêm vào bát 15 mL HCl đậm đặc lặp lại quá trình cô mẫu lần 2 ở nhiệt độ trên để kết tủa triệt để silic dioxide (SiO2). Sau khi khô kiệt, tiếp tục cô mẫu ở nhiệt độ trên từ 1 h đến 2 h.
Lấy bát cô ra khỏi bếp, làm nguội rồi thêm vào bát 15 mL hydro chloride đặc, để yên 10 min, thêm tiếp vào bát 80 mL đến 100 mL nước sôi, khuấy đều, đun nhẹ để hòa tan các muối. Tráng mặt kính và thành bát bằng nước đun sôi. Lấy bát ra để nguội đến khoảng 50 °C.
Lọc dung dịch trong bát sứ khi còn nóng qua giấy lọc không tro chảy trung bình vào bình định mức dung tích 500 mL. Dùng giấy lọc không tro lau sạch đũa thủy tinh, thành bát và chuyển định lượng toàn bộ kết tủa lên phễu. Dùng dung dịch hydro chloride loãng (5 + 95) (4.13) đã đun nóng rửa kết tủa. Tiếp tục rửa sạch kết tủa đến hết ion Cl- bằng nước cất nóng (thử bằng dung dịch AgNO3 0,5 %) (4.27).
Chuyển giấy lọc có chứa kết tủa vào chén bạch kim, sấy và đốt giấy lọc trên bếp điện. Nung chén ở nhiệt độ (950 ± 50) °C trong 1 h 30 min, lấy chén ra để nguội trong bình hút ẩm đến nhiệt độ phòng rồi cân. Lặp lại quá trình nung chén ở nhiệt độ trên, làm nguội rồi cân đến khi thu được khối lượng không đổi (m3).
Tẩm ướt kết tủa trong chén bằng vài giọt nước cất, thêm vào chén từ 2 giọt đến 3 giọt dung dịch dihydro sulfat (1 + 1) (4.16) và 5 mL dung dịch hydro fluoride (HF) đậm đặc (4.14). Làm bay hơi chất chứa trong chén trên bếp điện đến khô. Thêm tiếp từ 3 mL đến 4mL hydro fluoride đậm đặc (4.14) và lặp lại quá trình làm bay hơi trên bếp, điện đến khi khô kiệt (không còn khói trắng bốc ra).
Cho chén vào lò nung ở nhiệt độ (950 ± 50) °C trong 30 min, lấy ra để nguội trong bình hút ẩm đến nhiệt độ phòng rồi cân. Lặp lại quá trình nung, làm nguội, cân đến khi thu được khối lượng không đổi (m4).
Nung cặn còn lại trong chén bạch kim với 3 g đến 4 g dikali disulfat (K2S2O7) (4.3) ở nhiệt độ (750 ± 50) °C trong 15 min. Lấy chén ra khỏi lò, để nguội và chuyển chén có chứa khối nung chảy vào cốc thủy tinh dung tích 250 mL có chứa sẵn khoảng 100 mL nước nóng để tách khối nung chảy khỏi chén bạch kim. Rửa sạch chén và thêm vào cốc thủy tinh khoảng 10 mL dung dịch hydro chloride (1+1) (4.11) rồi đun nóng dung dịch để hòa tan khối nung chảy. Để nguội dung dịch thu được rồi gộp dung dịch này với dung dịch trong bình định mức 500 mL, thêm nước đến vạch mức, lắc đều. Dung dịch này để xác định các thành phần SiO2 hòa tan, Fe2O3, Al2O3, CaO, MgO và TiO2 có trong mẫu thử (dung dịch 1).
7.2.1.3 Biểu thị kết quả
Hàm lượng silic dioxide (SiO2), tính bằng phần trăm (%), theo công thức (3):
|
| (3) |
trong đó:
m3 là khối lượng chén bạch kim và kết tủa trước khi xử lý bằng hydro fluoride (HF), tính bằng gam (g);
m4 là khối lượng chén bạch kim và kết tủa sau khi xử lý bằng hydro fluoride (HF), tính bằng gam (g);
m là khối lượng mẫu lấy để phân tích, tính bằng gam (g).
Chênh lệch cho phép giữa hai thí nghiệm tiến hành song song không vượt quá 0,25 %.
7.2.2 Xác định hàm lượng silic dioxide hòa tan trong dung dịch bằng phương pháp đo màu
7.2.2.1 Nguyên tắc
Trong môi trường dihydro sulfat (pH khoảng từ 1,0 đến 1,5), sau khi loại bỏ ảnh hưởng của phosphor, cho Si4+ tác dụng với amoni heptamolybdat tạo thành phức màu vàng, khử phức này bằng hỗn hợp khử (tartaric và ascorbic) sang dạng màu xanh có cực đại hấp thụ ở bước sóng λ = 815 nm, cường độ màu của phức tỷ lệ với lượng silic dioxide hòa tan trong dung dịch.
7.2.2.2 Cách tiến hành
7.2.2.2.1 Xây dựng đường chuẩn
Lấy 11 bình định mức làm bằng polyethylen dung tích 100 mL, sử dụng buret để lần lượt cho vào mỗi bình một thể tích dung dịch tiêu chuẩn silic dioxide làm việc (SiO2 = 0,02 mg/mL) (4.58) theo thứ tự: 0 mL; 1 mL; 2 mL; 4 mL; 6 mL; 8 mL; 10 mL; 12 mL; 16 mL; 20 mL; 25 mL, thêm vào mỗi bình dung dịch dihydro sulfat (9+1000) (4.18) đến thể tích khoảng 40 mL, tiếp tục thêm 2 mL dung dịch NaF 3 % (4.28) và lắc đều. Thêm tiếp lần lượt 5 mL dung dịch trihydro trioxoborat bão hòa (4.42), 5 mL dung dịch acid citric (4.43) và 10 mL dung dịch amoni heptamolybdat 5 % (4.41) (thời điểm t = 0 (min)). Sau 20 min [tính từ thời điểm t = 0 (min)], thêm tiếp 5 mL dung dịch khử (4.40), rồi dùng dung dịch dihydro sulfat (9 +1000) (4.18) để định mức tới vạch, lắc đều. Sau 50 min [tính từ thời điểm t = 0 (min)] đo độ hấp thụ quang của dung dịch mẫu ở bước sóng cực đại hấp thụ (815 nm). Dung dịch so sánh là dung dịch mẫu trắng (lấy từ thí nghiệm trắng).
Từ lượng silic dioxide có trong mỗi bình và giá trị độ hấp thụ quang tương ứng xây dựng đường chuẩn.
7.2.2.2.2 Phân tích mẫu
Dùng pipet lấy 25 mL “dung dịch 1” (7.2.1.2) vào bình định mức làm bằng polyethylen dung tích 100 mL, thêm dung dịch dihydro sulfat (9 + 1000) (4.18) đến thể tích khoảng 40 mL, tiếp tục thêm 2 mL dung dịch NaF 3 % (4.28) và lắc đều. Thêm tiếp lần lượt 5 ml dung dịch trihydro trioxoborat bão hòa (4.42), 5 mL dung dịch acid citric (4.43) và 10 mL dung dịch amoni heptamolybdat 5 % (4.41) [thời điểm t = 0 (min)]. Sau 20 min (tính từ thời điểm t = 0 (min)), thêm tiếp 5 mL dung dịch khử (4.40), rồi dùng dung dịch dihydro sulfat (9 + 1000) (4.18) để định mức tới vạch, lắc đều. Sau 50 min [tính từ thời điểm t = 0 (min)] đo độ hấp thụ quang của dung dịch mẫu ở bước sóng cực đại hấp thụ (815 nm). Dung dịch so sánh là dung dịch mẫu trắng (lấy từ thí nghiệm trắng).
Từ giá trị độ hấp thụ quang đo được, dựa vào đường chuẩn tìm được hàm lượng silic dioxide có trong bình.
7.2.2.3 Biểu thị kết quả
Hàm lượng silic dioxide hòa tan, tính bằng phần trăm (%), theo công thức (4):
|
| (4) |
trong đó:
m5 là lượng silic dioxide tìm được trên đường chuẩn, tính bằng gam (g);
m6 là khối lượng mẫu tương ứng với thể tích mẫu lấy để phân tích, tính bằng gam (g);
Chênh lệch giữa hai kết quả xác định song song không lớn hơn 0,10 %.
7.2.3 Xác định hàm lượng silic dioxide tổng số
Hàm lượng silic dioxide (SiO2) có trong mẫu là tổng hàm lượng silic dioxide xác định tại 7.2.1 và 7.2.2.
7.3 Xác định hàm lượng sắt (III) oxide (Fe2O3)
Tùy thuộc vào hàm lượng sắt (III) oxide có trong mẫu, tiến hành xác định hàm lượng theo một trong những phương pháp dưới đây.
7.3.1 Xác định hàm lượng sắt (III) oxide bằng phương pháp đo màu
Áp dụng đối với mẫu có hàm lượng Fe2O3 đến 2,00 %.
7.3.1.1 Nguyên tắc
Trong môi trường kiềm amoniac, ion sắt (III) tạo với thuốc thử acid sulfosalicylic một phức chất màu vàng, có cực đại hấp thụ ở bước sóng λ = 420 nm. Cường độ màu của phức tỷ lệ với nồng độ sắt có trong dung dịch.
7.3.1.2 Cách tiến hành
7.3.1.2.1 Xây dựng đường chuẩn
Lấy 6 bình định mức dung tích 100 mL, sử dụng buret để lần lượt cho vào mỗi bình một thể tích dung dịch tiêu chuẩn làm việc sắt (III) oxide (Fe2O3 = 0,05 mg/mL) (4.54) theo thứ tự: 0 mL; 1 mL; 2 mL; 4 mL; 8 mL; 10 mL. Thêm nước cất đến khoảng 50 mL, thêm tiếp 10 mL dung dịch acid sulfosalicylic 10 % (4.26). Vừa lắc đều bình vừa nhỏ từng giọt amoni hydroxide đậm đặc (4.20) cho đến khi dung dịch xuất hiện màu vàng. Cho dư 2 mL đến 3 mL amoni hydroxide nữa, thêm nước đến vạch mức, lắc đều. Sau 15 min, đo độ hấp thụ quang của dung dịch ở bước sóng cực đại hấp thụ (420 nm), dung dịch so sánh là dung dịch mẫu trắng.
Từ hàm lượng sắt (III) oxide (Fe2O3) có trong mỗi bình và trị số độ hấp thụ quang tương ứng xây dựng đường chuẩn.
7.3.1.2.2 Phân tích mẫu:
Dùng pipet lấy 10 mL dung dịch 1 (7.2.1.2) vào bình định mức dung tích 100 mL, pha loãng bằng nước đến thể tích khoảng 50 mL, thêm tiếp 10 mL dung dịch acid sulfosalicylic 10 % (4.26). Vừa lắc đều bình vừa nhỏ từng giọt amoni hydroxide đậm đặc (4.20) cho đến khi dung dịch xuất hiện màu vàng. Cho dư 2 mL đến 3 mL amoni hydroxide nữa, thêm nước đến vạch mức, lắc đều. Sau 15 min, đo độ hấp thụ quang của dung dịch ở bước sóng cực đại hấp thụ (420 nm), dung dịch so sánh là dung dịch mẫu trắng.
Từ giá trị độ hấp thụ quang đo được, dựa vào đường chuẩn tìm được hàm lượng sắt (III) oxide có trong bình.
7.3.1.3 Biểu thị kết quả
Hàm lượng sắt (III) oxide, tính bằng phần trăm (%), theo công thức (5):
|
| (5) |
trong đó:
m7 là lượng sắt (III) oxide tìm được trên đường chuẩn, tính bằng gam (g);
m8 là khối lượng mẫu tương ứng với thể tích mẫu lấy để xác định hàm lượng sắt (III) oxide, tính bằng gam (g);
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả tiến hành song song không lớn hơn 0,04 %.
7.3.2 Xác định hàm lượng sắt (III) oxide (Fe2O3) bằng phương pháp chuẩn độ phức chất
Áp dụng cho mẫu có hàm lượng Fe2O3 nằm trong khoảng từ lớn hơn 2,00 % đến 7,00 %.
7.3.2.1 Nguyên tắc
Chuẩn độ phức chất sắt (III) bằng dung dịch EDTA tiêu chuẩn ở môi trường pH từ 1,5 đến 2 với chỉ thị acid sulfosalicylic. Kết thúc chuẩn độ, dung dịch chuyển từ màu tím đỏ sang vàng rơm.
7.3.2.2 Cách tiến hành
Dùng pipet lấy 25 mL dung dịch 1 (7.2.1.2) vào cốc dung tích 250 mL. Thêm nước đến thể tích khoảng 100 mL, thêm tiếp 2 mL dung dịch acid sulfosalicylic (4.26). Dùng dung dịch hydro chloride (1+1) (4.11) và dung dịch natri hydroxide 10 % (4.21) nhỏ giọt để điều chỉnh pH của dung dịch đạt giá trị khoảng từ 1,5 đến 2 (sử dụng máy đo pH để kiểm tra). Đun nóng dung dịch trên bếp điện đến nhiệt độ khoảng từ 60 °C đến 70 °C. Chuẩn độ dung dịch khi còn nóng bằng dung dịch tiêu chuẩn EDTA 0,01 M đến khi màu của dung dịch chuyển từ tím đỏ sang vàng rơm. Ghi thể tích dung dịch EDTA tiêu thụ (V1).
Làm song song một thí nghiệm trắng gồm đầy đủ các dung dịch thuốc thử nhưng không có dung dịch mẫu. Ghi thể tích EDTA 0,01M tiêu thụ (V0).
7.3.2.3 Biểu thị kết quả
Hàm lượng sắt (III) oxide (Fe2O3), tính bằng phần trăm (%), theo công thức (6):
|
| (6) |
trong đó:
0,0007985 là số gam Fe2O3 tương ứng với 1 ml dung dịch EDTA 0,01 M, tính bằng gam (g);
V1 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ mẫu, tính bằng mililít (mL);
V0 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ mẫu trắng, tính bằng mililít (mL);
m là khối lượng mẫu tương ứng với thể tích dung dịch lấy để xác định hàm lượng sắt (III) oxide, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả tiến hành song song không lớn hơn 0,20 %.
7.3.3 Xác định hàm lượng sắt (III) oxide (Fe2O3) bằng phương pháp chuẩn độ oxi hóa khử
Áp dụng cho mẫu có hàm lượng Fe2O3 lớn hơn 7,00 %.
7.3.3.1 Nguyên tắc
Khử toàn bộ lượng sắt (III) có trong dung dịch phân tích thành Fe2+ bằng dung dịch SnCl2. Chuẩn độ ion Fe2+ thu được bằng dung dịch tiêu chuẩn K2Cr2O7 với chỉ thị bari diphenylamin sulfonat. Kết thúc chuẩn độ khi dung dịch chuyển từ không màu sang màu tím.
7.3.3.2 Cách tiến hành
Dùng pipet lấy 100 mL dung dịch 1 (7.2.1.2) vào cốc thủy tinh dung tích 250 mL và cô nhẹ trên bếp điện đến gần cạn (thể tích dung dịch trong cốc còn khoảng 25 mL). Lấy cốc ra khỏi bếp điện, vừa lắc đều cốc vừa thêm từ từ từng giọt dung dịch thiếc chloride thiếc (II) 5 % (4.46) cho đến khi dung dịch chuyển từ màu vàng sang không màu và cho dư thêm 1 giọt nữa.
Thêm nước đến thể tích khoảng 100 mL để làm nguội nhanh dung dịch thu được.
Thêm vào 10 mL hỗn hợp dihydro sulfat và tetraoxophosphat (4.44), thêm tiếp 5 mL dung dịch thủy ngân chloride 5 % (4.45) và vài giọt dung dịch chỉ thị Bari diphenylamine sulfonat (4.37).
Chuẩn độ bằng dung dịch tiêu chuẩn K2Cr2O7 0,2 M (4.49) cho đến khi màu dung dịch chuyển từ không màu sang màu tím, bền trong 30 s. Ghi thể tích dung dịch K2Cr2O7 tiêu thụ (V1).
Làm song song một thí nghiệm trắng gồm đầy đủ các dung dịch, thuốc thử nhưng không có dung dịch mẫu. Ghi lại thể tích K2Cr2O7 tiêu thụ (V0).
7.3.3.3 Biểu thị kết quả
Hàm lượng sắt (III) oxide (Fe2O3), tính bằng phần trăm (%) theo công thức (7):
|
| (7) |
trong đó:
0,002662 là số gam Fe2O3 tương ứng với 1 mL dung dịch K2Cr2O7 0,2 M;
V1 là thể tích dung dịch K2Cr2O7 0,2 M tiêu thụ khi chuẩn độ dung dịch mẫu phân tích, tính bằng mililít (mL);
V0 là thể tích dung dịch K2Cr2O7 0,2 M tiêu thụ khi chuẩn độ mẫu trắng, tính bằng mililít (mL);
m là khối lượng mẫu tương ứng với thể tích dung dịch mẫu lấy để xác định hàm lượng sắt (III) oxide, tính bằng gam (g).
Chênh lệch cho phép giữa hai kết quả xác định song song không lớn hơn 0,30 %.
7.4 Xác định hàm lượng nhôm oxide (Al2O3)
7.4.1 Nguyên tắc
Mẫu sau khi tách loại silic dioxide, tiếp tục tách loại nhôm ra khỏi các nguyên tố ảnh hưởng bằng kiềm mạnh. Tạo phức giữa nhôm và EDTA dư ở pH 5,5. Chuẩn độ lượng dư EDTA bằng dung dịch kẽm acetat với chỉ thị xylenon da cam. Dùng natri flouride để giải phóng EDTA khỏi phức nhôm complexonat, dùng dung dịch tiêu chuẩn kẽm acetat chuẩn độ lượng EDTA được giải phóng, từ đó tính ra hàm lượng nhôm.
7.4.2 Cách tiến hành
Dùng pipet lấy 100 mL dung dịch 1 (7.2.1.2) vào cốc thủy tinh dung tích 250 mL, thêm 30 mL dung dịch natri hydroxide 30 % (4.22). Khuấy đều và đun sôi dung dịch khoảng 2 min. Làm nguội và chuyển vào bình định mức dung tích 250 mL, thêm nước đến vạch mức, lắc đều. Lọc dung dịch qua giấy lọc chảy nhanh (khô), phễu (khô), vào bình côn (khô). Dung dịch lọc dùng để xác định nhôm (dung dịch 2).
Dùng pipet lấy 100 mL “dung dịch 2” vào cốc thủy tinh dung tích 250 mL, thêm 20 mL dung dịch EDTA 1 % (4.52), thêm tiếp 2 giọt chỉ thị phenolphtalein 0,1 % (4.36). Dùng dung dịch hydro chloride (1:1) (4.11) và dung dịch natri hydroxide 10 % (4.21) điều chỉnh dung dịch tới pH khoảng 7 (dung dịch không màu) rồi thêm 20 mL dung dịch đệm pH 5,5 (4.38).
Đun dung dịch trên bếp điện đến sôi. Lấy cốc ra khỏi bếp điện, để nguội đến nhiệt độ khoảng 70 °C. Thêm vào cốc vài giọt chỉ thị xylenol da cam 0,1 % (4.35) và dung dịch kẽm acetat 0,025 M (4.51) chuẩn độ đến khi xuất hiện màu hồng.
Thêm vào cốc 20 mL dung dịch natri flouride 3 % (4.28) và đun sôi dung dịch. Lúc này dung dịch có màu vàng, để nguội dung dịch đến nhiệt độ khoảng 70 °C rồi dùng dung dịch kẽm acetat 0,025 M chuẩn lượng EDTA vừa được giải phóng ra khỏi phức với nhôm cho đến khi dung dịch chuyển sang màu hồng. Ghi thể tích dung dịch kẽm acetat 0,025 M tiêu thụ (VZn).
Làm song song một thí nghiệm trắng gồm đầy đủ các dung dịch thuốc thử nhưng không có dung dịch mẫu. Ghi thể tích kẽm acetat 0,025 M tiêu thụ (V0).
7.4.3 Biểu thị kết quả
Hàm lượng nhôm oxide (Al2O3) tính bằng phần trăm (%), theo công thức (8)
|
| (8) |
trong đó:
0,0012745 là số gam nhôm oxide tương ứng với 1 mL dung dịch kẽm acetat 0,025 M;
k là tỷ số nồng độ giữa dung dịch kẽm acetat 0,025 M và dung dịch EDTA 0,01 M;
VZn là thể tích dung dịch kẽm acetat 0,025 M tiêu thụ khi chuẩn độ dung dịch mẫu phân tích, tính bằng mililít (mL);
V0 là thể tích dung dịch kẽm acetat 0,025 M tiêu thụ khi chuẩn độ dung dịch mẫu trắng, tính bằng mililít (mL);
m là khối lượng mẫu tương ứng với thể tích dung dịch mẫu lấy để xác định hàm lượng nhôm oxide, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả xác định song song không lớn hơn 0,35 %.
7.5 Xác định hàm lượng titani dioxide (TiO2)
7.5.1 Nguyên tắc
Diantipyrin methane tạo với ion titani (IV) trong môi trường acid mạnh một phức chất màu vàng, cường độ màu tỷ lệ với nồng độ titani trong dung dịch. Đo độ hấp thụ quang của dung dịch ở bước sóng 420 nm.
7.5.2 Cách tiến hành
7.5.2.1 Xây dựng đường chuẩn
Lấy 6 bình định mức dung tích 100 mL, sử dụng buret để lần lượt cho vào mỗi bình một thể tích dung dịch tiêu chuẩn titani làm việc (TiO2 = 0,04 mg/mL) (4.56) theo thứ tự: 0 mL; 2 mL; 4 mL; 6 mL; 8 mL; 12 mL. Thêm tiếp 15 mL dung dịch HCl (1+1) (4.11), 5 mL dung dịch thiourea 5 % (4.34), lắc đều. Để yên dung dịch cho đến khi dung dịch hết màu vàng của sắt (dung dịch chuyển sang không màu). Thêm tiếp vào bình 15 ml dung dịch diantipyrin methane 2 % (4.29), thêm nước cất tới vạch, lắc đều. Sau 1 h, đo giá trị độ hấp thụ quang của dung dịch ở bước sóng 420 nm, dung dịch so sánh là dung dịch mẫu trắng.
Từ lượng titani dioxide có trong mỗi bình và giá trị độ hấp thụ quang tương ứng xây dựng đường chuẩn.
7.5.2.2 Phân tích mẫu
Dùng pipet bầu lấy 25 mL dung dịch 1 (7.2.1.2) cho vào bình định mức dung tích 100 mL. Thêm 15 mL dung dịch hydro chloride (1 + 1) (4.11) và 5 mL dung dịch thiourea 5 % (4.34), lắc đều. Để yên dung dịch cho đến khi dung dịch hết màu vàng của sắt (dung dịch chuyển sang không màu). Thêm tiếp vào bình 15 ml dung dịch diantipyrin methane 2 % (4.29), thêm nước cất tới vạch, lắc đều. Sau 1 h, đo giá trị độ hấp thụ quang của dung dịch ở bước sóng 420 nm, dung dịch so sánh là dung dịch mẫu trắng.
Dựa vào đường chuẩn tìm được lượng titani dioxide có trong bình.
7.5.3 Biểu thị kết quả
Hàm lượng titani dioxide (TiO2), tính bằng phần trăm (%), theo công thức (9):
|
| (9) |
trong đó:
m9 là lượng titani dioxide tìm được từ đường chuẩn, tính bằng gam (g);
m là khối lượng mẫu tương ứng với thể tích dung dịch mẫu lấy để xác định hàm lượng titani doxide, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai thí nghiệm tiến hành song song không vượt quá 0,05 %.
7.6 Xác định hàm lượng calci oxide (CaO)
7.6.1 Nguyên tắc
Sau khi tách loại silic dioxide, tiếp tục tách sắt, nhôm, titani,... khỏi dung dịch chứa calci và magnesi bằng amoni hydroxide, chuẩn độ lượng calci bằng dung dịch EDTA tiêu chuẩn ở pH lớn hơn 12 với chỉ thị fluorexon, ở điểm tương đương dung dịch mất màu xanh huỳnh quang chuyển sang màu hồng.
7.6.2 Cách tiến hành
Dùng pipet bầu lấy 100 mL “dung dịch 1” vào cốc thủy tinh dung tích 250 mL. Thêm vào cốc khoảng 2 g amoni chloride (4.4), đun nóng dung dịch đến nhiệt độ khoảng từ 70 ⁰C đến 80 ⁰C , rồi vừa khuấy đều dung dịch vừa thêm từ từ dung dịch amoni hydroxide NH4OH đặc (4.20) đến khi xuất hiện kết tủa hydroxide của sắt, nhôm, titani,v.v... thêm dư khoảng 2 mL nữa.
Đun sôi nhẹ dung dịch và cô cạn trên bếp điện đến khi thể tích dung dịch còn khoảng 25 mL để đông tụ kết tủa và loại amoni hydroxide dư. Làm nguội dung dịch và chuyển vào bình định mức dung tích 250 mL, thêm nước đến vạch mức, lắc đều. Lọc dung dịch qua giấy lọc chảy nhanh (khô), phễu (khô), vào bình nón (khô). Dung dịch lọc dùng để xác định calci, magnesi (dung dịch 3).
Dùng pipet lấy 100 mL “dung dịch 3” cho vào cốc dung tích 250 mL, thêm 20 mL kali hydroxide 25 % (4.23), 2 mL kali cyanide 5 % (4.24) và một ít chỉ thị fluorexon 1 % (4.31).
Đặt cốc lên một nền đen, dùng dung dịch EDTA 0,01 M (4.47) chuẩn độ dung dịch trong cốc đến khi dung dịch mất màu xanh huỳnh quang chuyển sang màu hồng. Ghi thể tích dung dịch EDTA 0,01 M tiêu thụ (V1).
Làm song song một thí nghiệm trắng để hiệu chỉnh lượng calci oxide (CaO) có trong dung dịch và thuốc thử. Ghi thể tích EDTA 0,01 M tiêu thụ (V0).
7.6.3 Biểu thị kết quả
Hàm lượng calci oxide (CaO), tính bằng phần trăm (%), theo công thức (10):
|
| (10) |
trong đó:
V0 là thể tích EDTA 0,01 M tiêu thụ khi chuẩn độ mẫu trắng, tính bằng mililít (mL);
V1 là thể tích EDTA 0,01 M tiêu thụ khi chuẩn độ mẫu thử, tính bằng mililít (mL);
0,00056 là khối lượng calci oxide tương ứng với 1 mL dung dịch EDTA 0,01 M, tính bằng gam (g);
m là khối lượng mẫu tương ứng với thể tích dung dịch mẫu lấy để xác định hàm lượng calci oxide, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai thí nghiệm tiến hành song song không vượt quá 0,20 %.
7.7 Xác định hàm lượng magnesi oxide (MgO)
7.7.1 Nguyên tắc
Chuẩn độ tổng lượng calci và magnesi trong mẫu bằng dung dịch EDTA tiêu chuẩn theo chỉ thị eriocrom T đen ở pH 10,5. Xác định hàm lượng magnesi oxide (MgO) theo hiệu số thể tích EDTA tiêu thụ khi chuẩn độ tổng lượng calci và magnesi ở pH 10,5 và khi chuẩn độ riêng calci ở pH > 12.
7.7.2 Cách tiến hành
Dùng pipet bầu lấy 100 mL dung dịch 3 (7.6.2) cho vào cốc dung tích 250 mL, thêm tiếp vào cốc 20 mL dung dịch đệm pH 10,5 (4.39); 2 ml dung dịch kali cyanide 5 % (4.24) và từ 2 giọt đến 3 giọt chỉ thị eriocrom T đen 0,1 % (4.30). Chuẩn độ tổng lượng calci và magnesi bằng dung dịch EDTA 0,01 M (4.47), đến khi dung dịch chuyển từ màu đỏ tím sang màu xanh nước biển. Làm song song một thí nghiệm trắng để hiệu chỉnh tổng lượng calci và magnesi có trong các thuốc thử. Ghi thể tích EDTA 0,01 M tiêu thụ (V2).
Làm song song một thí nghiệm trắng gồm đầy đủ các dung dịch thuốc thử nhưng không có dung dịch mẫu. Ghi lại thể tích EDTA 0,01 M tiêu thụ (V02).
7.7.3 Biểu thị kết quả
Hàm lượng magnesi oxide (MgO), tính bằng phần trăm (%), theo công thức (11):
|
| (11) |
trong đó:
V01 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ riêng lượng calci trong mẫu trắng, tính bằng mililít (mL);
V1 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ riêng lượng calci trong dung dịch mẫu, tính bằng mililít (mL);
V02 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ tổng lượng calci và magnesi trong mẫu trắng, tính bằng mililít (mL);
V2 là thể tích dung dịch tiêu chuẩn EDTA 0,01 M tiêu thụ khi chuẩn độ tổng lượng calci và magnesi trong dung dịch mẫu, tính bằng mililít (mL);
0,000403 là khối lượng magnesi oxide tương ứng với 1 ml dung dịch EDTA 0,01 M, tính bằng gam (g);
m là khối lượng mẫu tương ứng với thể tích dung dịch mẫu lấy để xác định tổng hàm lượng calci oxide và magnesi oxide, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai thí nghiệm tiến hành song song không vượt quá 0,20 %.
7.8 Xác định hàm lượng tổng lưu huỳnh tính theo sulfur trioxide (SO3)
7.8.1 Nguyên tắc
Nung chảy mẫu thử bằng hỗn hợp eska (4.8) rồi hòa tan trong dung dịch hydro chloride loãng, toàn bộ lượng lưu huỳnh có trong mẫu thử sẽ tan trong vào dung dịch ở dạng ion sulfat. Sau khi tách loại các nguyên tố ảnh hưởng, tiến hành kết tủa sulfat ở dạng BaSO4 trong môi trường acid. Nung kết tủa BaSO4 ở nhiệt độ 950 °C và tính ra hàm lượng tổng lưu huỳnh tính theo sulfur trioxide (SO3) có trong mẫu.
7.8.2 Cách tiến hành
Cân khoảng 0,5 g mẫu (Điều 6) chính xác đến 0,0001 g vào chén sứ đã có sẵn khoảng 2 g hỗn hợp nung chảy eska, trộn đều và phủ lên trên đó một lớp mỏng hỗn hợp nung chảy (khoảng 2 g) nữa.
Nung chảy chất chứa trong chén ở nhiệt độ 800 °C đến 850 °C trong khoảng 2 h. Lấy chén ra khỏi lò, để nguội. Chuyển toàn bộ các chất có trong chén vào cốc thủy tinh dung tích 250 mL bằng nước sôi và dung dịch hydro chloride (1+1) (4.11). Đậy cốc bằng mặt kính đồng hồ và thêm vào cốc 15 mL hydro chloride đậm đặc (4.10). Sau khi mẫu đã tan hết, rửa sạch mặt kính và thành cốc.
Thêm vào dung dịch trong cốc từ 1 đến 2 giọt chỉ thị metyl đỏ và khoảng 1 g amoni chloride, khuấy cho tan và vừa khuấy vừa thêm từ từ từng giọt amoni hydroxide 25 % cho đến khi dung dịch chuyển sang màu vàng, cho dư thêm khoảng 1 đến 2 giọt nữa. Đun nóng dung dịch để đông tụ kết tủa. Lọc dung dịch còn nóng qua giấy lọc chảy trung bình, rửa cốc và kết tủa bằng nước nóng từ 5 đến 6 lần, thu nước lọc rửa vào cốc thủy tinh dung tích 250 mL. Nếu dung dịch thu được có thể tích lớn, cô cạn bớt đến thể tích còn khoảng 150 mL. Thêm vào cốc 1 giọt đến 2 giọt dung dịch chỉ thị metyl đỏ 0,1 % và trung hòa dung dịch bằng dung dịch hydrochloride (1+1) (4.11) cho đến khi dung dịch có màu đỏ, tiếp tục cho dư khoảng 1 mL đến 1,5 mL nữa. Đun nóng dung dịch trên bếp điện tới gần sôi rồi vừa khuấy, vừa thêm từ từ 10 mL dung dịch bari chloride 10 % (4.25) đã được đun nóng vào cốc và tiếp tục đun sôi nhẹ dung dịch trong 5 min. Để yên dung dịch nơi ấm trong khoảng từ 6 h đến 8 h (hoặc để qua đêm). Lọc dung dịch qua giấy lọc không tro chảy chậm, rửa sạch kết tủa và giấy lọc bằng nước đun sôi cho đến hết ion chloride (thử bằng dung dịch bạc nitrat 0,5 % (4.27)). Chuyển giấy lọc có chứa kết tủa vào chén sứ đã nung đến khối lượng không đổi (m10). Sấy và đốt cháy giấy lọc chứa kết tủa trên bếp điện rồi chuyển vào lò nung, nung ở nhiệt độ 950 ⁰C trong khoảng 1 h đến 1,5 h. Lấy chén ra để nguội trong bình hút ẩm đến nhiệt độ phòng rồi cân. Lặp lại quá trình nung, làm nguội, cân đến khi thu được khối lượng không đổi (m11).
7.8.3 Biểu thị kết quả
Hàm lượng tổng lưu huỳnh tính theo sulfur trioxide SO3 tính bằng phần trăm (%), theo công thức (12):
|
| (12) |
trong đó:
m10 là khối lượng chén không, tính bằng gam (g);
m11 là khối lượng chén có chứa kết tủa, tính bằng gam (g);
m là khối lượng mẫu lấy để phân tích, tính bằng gam (g);
0,343 là hệ số chuyển đổi từ BaSO4 sang SO3.
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả xác định song song không lớn hơn
- 0,02 % đối với mẫu có hàm lượng SO3 đến 0,20 %;
- 0,05 % đối với mẫu có hàm lượng SO3 lớn hơn 0,20 %.
7.9 Xác định hàm lượng dikali oxide (K2O) và dinatri oxide (Na2O)
7.9.1 Nguyên tắc
Mẫu, sau khi phân hủy thành dung dịch bằng hỗn hợp hydro fluoride - dihydro sulfat, được phun vào ngọn lửa axetylen - không khí. Lần lượt đo cường độ vạch phổ hấp thụ nguyên tử tự do của nguyên tử kali ở bước sóng 766,50 nm và natri ở bước sóng 589,00 nm để từ đó tính ra hàm lượng nguyên tố theo phương pháp đường chuẩn.
7.9.2 Cách tiến hành
7.9.2.1 Xác định đường chuẩn
Dùng buret lấy vào các bình định mức làm bằng polyethylen, dung tích 100 mL, lần lượt các thể tích 0,00 mL; 1,00 mL; 2,00 mL; 3,00 mL; 4,00 mL; 5,00 mL của dung dịch tiêu chuẩn dinatri oxide làm việc (4.60) (khi xác định hàm lượng dinatri oxide) hoặc dung dịch tiêu chuẩn dikali oxide làm việc (4.61) (khi xác định hàm lượng dikali oxide). Thêm nước đến vạch mức, lắc đều.
Đo độ hấp thụ quang của các dung dịch chuẩn vừa chuẩn bị được trên thiết bị hấp thụ nguyên tử với nguồn bức xạ đơn sắc tại bước sóng 589,00 nm (cho natri) hoặc 768,00 nm (cho kali) và lập đường chuẩn bậc 1 theo hướng dẫn của thiết bị.
7.9.2.2 Phân tích mẫu
Cân khoảng 0,25 g mẫu (Điều 6.2) chính xác đến 0,0001 g vào chén bạch kim, tẩm ướt bằng vài giọt nước, thêm tiếp vào chén 0,5 mL dihydro sulfat (1 + 1) (4.16) và 15 mL hydro fluoride (4.14), làm bay hơi từ từ trên bếp điện đến khô.
Thêm vào chén từ 8 mL đến 10 mL hydro fluoride (4.13) và làm bay hơi đến khô kiệt (không còn khói trắng thoát ra). Làm nguội chén, thêm vào khoảng 10 mL dung dịch hydro chloride (1 + 1) (4.11) và đun nóng. Dùng nước nóng chuyển định lượng toàn bộ dung dịch hỗn hợp có trong chén vào cốc thủy tinh dung tích 100 mL. Tiếp tục vừa thêm từ từ từng giọt dung dịch amoni hydroxide 25 % (4.20) vừa khuấy đều dung dịch cho đến khi xuất hiện kết tủa. Cho dư thêm khoảng 1 mL đến 2 mL dung dịch amoni hydroxide nữa. Đun dung dịch đến nhiệt độ khoảng 70 °C để đông tụ kết tủa. Làm nguội đến nhiệt độ phòng rồi chuyển toàn bộ dung dịch vào bình định mức dung tích 250 mL, thêm nước cất đến vạch mức, lắc đều.
Lọc khô dung dịch qua giấy lọc không tro chảy trung bình vào bình tam giác khô (sử dụng phễu khô), thu được dung dịch 4.
Tùy theo hàm lượng dikali oxide hoặc dinatri oxide có trong mẫu, dùng pipet lấy 2 mL hoặc 5 mL hoặc 10 mL dung dịch 4 vào bình định mức làm bằng polyethylen, dung tích 100 mL. Thêm nước cất đến vạch mức lắc đều (dung dịch E). Đo độ hấp thụ quang trên thiết bị hấp thụ nguyên tử với nguồn bức xạ đơn sắc tại bước sóng 768,00 nm (cho kali) và 589,00 nm (cho natri) dựa trên các đường chuẩn vừa được thiết lập.
7.9.3 Biểu thị kết quả
Hàm lượng dikali oxide (K2O) hay dinatri oxide (Na2O) trong mẫu, tính bằng phần trăm (%), theo công thức (13):
|
| (13) |
trong đó:
C là lượng dikali oxide hay dinatri oxide đo được trên thiết bị hấp thụ nguyên tử, tính bằng miligam trên mililit (mg/ mL);
m là khối lượng mẫu tương ứng với thể tích dung dịch lấy ra để phân tích, tính bằng miligam trên mililit (mg/ mL);
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả xác định song song không lớn hơn 0,04 %.
7.10 Xác định hàm lượng ion chloride (Cl-)
7.10.1 Nguyên tắc
Kết tủa ion chloride (Cl-) bằng lượng dư dung dịch tiêu chuẩn bạc nitrat, chuẩn độ lượng dư bạc nitrat bằng dung dịch tiêu chuẩn amoni sulfocyanide, từ đó tính ra lượng ion chloride (Cl-) có trong mẫu.
7.10.2 Cách tiến hành
Cân khoảng 1 g mẫu (điều 6) chính xác đến 0,0001 g vào cốc dung tích 250 mL, thêm vào cốc 50 mL nước, thêm tiếp 2 mL dung dịch bạc nitrat tiêu chuẩn 0,1 M (4.48) và 5 mL hydro trioxonitrat (HNO3) đậm đặc (4.9). Khuấy kỹ dung dịch rồi đun đến sôi trên bếp điện. Lấy cốc ra để nguội. Lọc dung dịch qua giấy lọc chảy trung bình. Dùng nước nóng rửa cốc và kết tủa đến hết acid (sử dụng giấy pH). Nước lọc rửa thu vào cốc thủy tinh dung tích 250 mL.
Thêm vào dung dịch 2 mL dung dịch amoni sắt (III) sulfat 0,2M (4.32). Dùng dung dịch tiêu chuẩn amoni thiocyanat (NH4SCN) 0,1M (4.50) chuẩn độ cho đến khi dung dịch xuất hiện màu nâu gạch. Ghi thể tích dung dịch amoni thiocyanat 0,1M tiêu thụ (V1).
Làm song song thí nghiệm trắng để hiệu chỉnh kết quả. Ghi thể tích dung dịch amoni thiocyanat 0,1 M tiêu thụ (V0).
7.10.3 Biểu thị kết quả
Hàm lượng ion chloride (Cl-), tính bằng phần trăm (%), theo công thức (14):
|
| (14) |
trong đó:
V0 là thể tích dung dịch tiêu chuẩn amoni thiocyanat 0,1 M đã tiêu tốn khi chuẩn độ mẫu trắng, tính bằng mililít (mL);
V1 là thể tích dung dịch tiêu chuẩn amoni thiocyanat NH4SCN 0,1 M đã tiêu tốn khi chuẩn mẫu thử, tính bằng mililít (mL);
m là khối lượng cân mẫu thử, tính bằng gam (g);
0,003546 là khối lượng ion chloride tương ứng với 1 mL dung dịch amoni thiocyanat NH4SCN 0,1 M, tính bằng gam (g).
Chênh lệch (tính theo giá trị tuyệt đối) giữa hai kết quả xác định song song không lớn hơn 0,05 %
8 Báo cáo thử nghiệm
Trong báo cáo thử nghiệm bao gồm ít nhất các thông tin sau:
a) viện dẫn tiêu chuẩn này;
b) các chi tiết cần thiết để nhận biết mẫu thử;
c) kết quả thử ở Điều 7;
d) các đặc điểm bất thường ghi nhận trong quá trình thử;
e) các thao tác bất kỳ được thực hiện không quy định trong tiêu chuẩn này.
MỤC LỤC
1 Phạm vi áp dụng
2 Tài liệu viện dẫn
3 Quy định chung
4 Hóa chất, thuốc thử
5 Thiết bị, dụng cụ
6 Chuẩn bị mẫu thử
7 Phương pháp thử
7.1 Xác định hàm lượng mất khi nung (MKN)
7.2 Xác định hàm lượng silic dioxide (SiO2)
7.3 Xác định hàm lượng sắt (III) oxide (Fe2O3)
7.4 Xác định hàm lượng nhôm oxide (Al2O3)
7.5 Xác định hàm lượng titani dioxide (TiO2)
7.6 Xác định hàm lượng calci oxide (CaO)
7.7 Xác định hàm lượng magnesi oxide (MgO)
7.8 Xác định hàm lượng tổng lưu huỳnh tính theo sulfur trioxide (SO3)
7.9 Xác định hàm lượng dikali oxide (K2O) và dinatri oxide (Na2O)
7.10 Xác định hàm lượng ion chloride (Cl-)
8 Báo cáo thử nghiệm
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 7131:2016 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 7131:2016 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 7131:2016 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 7131:2016 DOC (Bản Word)