- Tổng quan
- Nội dung
- Tiêu chuẩn liên quan
- Lược đồ
- Tải về
Tiêu chuẩn Quốc gia TCVN 12959:2020 ISO 11206:2011 Chất lượng nước - Xác định bromat hòa tan - Phương pháp sử dụng sắc ký ion(IC) và phản ứng sau cột (PCR)
| Số hiệu: | TCVN 12959:2020 | Loại văn bản: | Tiêu chuẩn Việt Nam |
| Cơ quan ban hành: | Bộ Khoa học và Công nghệ | Lĩnh vực: | Tài nguyên-Môi trường |
|
Ngày ban hành:
Ngày ban hành là ngày, tháng, năm văn bản được thông qua hoặc ký ban hành.
|
31/12/2020 |
Hiệu lực:
|
Đã biết
|
| Người ký: | Đang cập nhật |
Tình trạng hiệu lực:
Cho biết trạng thái hiệu lực của văn bản đang tra cứu: Chưa áp dụng, Còn hiệu lực, Hết hiệu lực, Hết hiệu lực 1 phần; Đã sửa đổi, Đính chính hay Không còn phù hợp,...
|
Đã biết
|
TÓM TẮT TIÊU CHUẨN VIỆT NAM TCVN 12959:2020
TCVN 12959:2020: Phương pháp xác định bromat hòa tan trong nước
Tiêu chuẩn Quốc gia TCVN 12959:2020 được ban hành bởi Bộ Khoa học và Công nghệ, tương đương với ISO 11206:2011 và có hiệu lực từ ngày ban hành. Tiêu chuẩn này quy định phương pháp xác định bromat hòa tan trong các loại nước khác nhau như nước uống và nước thô thông qua việc sử dụng sắc ký ion (IC) và phản ứng sau cột (PCR).
Tiêu chuẩn yêu cầu người sử dụng phải là những cá nhân đã được đào tạo phù hợp và có kỹ năng trong phòng thí nghiệm. Đặc biệt, tiêu chuẩn không đề cập đầy đủ tới các vấn đề an toàn nên các cá nhân cần tự đảm bảo các biện pháp an toàn phù hợp.
Bromat hòa tan trong mẫu nước có thể được phát hiện với nồng độ tối thiểu ≥ 0,5 µg/L. Cách thức xác định này liên quan đến việc xử lý sơ bộ mẫu nước để loại bỏ các chất gây ảnh hưởng như ozon và clorit. Kết quả sẽ được đo dựa trên độ hấp thụ UV ở bước sóng 352 nm.
Tiêu chuẩn đề cập rằng cường độ pic trong sắc ký đồ cần đạt được độ phân giải không nhỏ hơn 1,3 giữa bromat và pic gần nhất. Để thực hiện, các hệ thống sắc ký ion cần phải được lắp đặt theo yêu cầu kỹ thuật cụ thể, bao gồm thiết bị ghi dữ liệu và detector UV.
Các chất thử nghiệm chỉ sử dụng các hóa chất có cấp phân tích. Để chuẩn bị dung dịch rửa giải và các thuốc thử khác, cần đảm bảo không có sự thâm nhập của không khí trong quá trình thao tác.
Kết quả thử nghiệm phải được báo cáo với tối đa hai số có nghĩa, thể hiện nồng độ bromat trong mẫu nước. Đặc biệt, phải có đầy đủ thông tin về phương pháp thử, mẫu nước và kết quả thu được. Việc xác nhận hiệu quả của hàm hiệu chuẩn cũng được quy định rõ ràng trong tiêu chuẩn để đảm bảo tính chính xác trong các phép đo đòi hỏi.
Những yêu cầu về thiết bị và dụng cụ trong quy chuẩn này đều nhằm đảm bảo rằng các phép thử đo đúng và đủ chất lượng của nước, giúp quản lý và bảo vệ nguồn nước một cách hiệu quả. Việc áp dụng TCVN 12959:2020 đóng vai trò quan trọng trong công tác quản lý chất lượng nước ở Việt Nam.
Tải tiêu chuẩn Việt Nam TCVN 12959:2020
TIÊU CHUẨN QUỐC GIA
TCVN 12959:2020
CHẤT LƯỢNG NƯỚC - XÁC ĐỊNH BROMAT HÒA TAN PHƯƠNG PHÁP SỬ DỤNG SẮC KÝ ION (IC) VÀ PHẢN ỨNG SAU CỘT (PCR)
Water quality - Determination of dissolved bromate - Method using ion chromatography (IC) and post column reaction (PCR)
Lời nói đầu
TCVN 12959:2020 hoàn toàn tương đương với ISO 11206:2011;
TCVN 12959:2020 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC147 Chất lượng nước biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
CHẤT LƯỢNG NƯỚC - XÁC ĐỊNH BROMAT HÒA TAN PHƯƠNG PHÁP SỬ DỤNG SẮC KÝ ION (IC) VÀ PHẢN ỨNG SAU CỘT (PCR)
Water quality - Determination of dissolved bromate - Method using ion chromatography (IC) and post column reaction (PCR)
CẢNH BÁO - Người sử dụng tiêu chuẩn này cần phải thành thạo với các thực hành trong phòng thí nghiệm thông thường. Tiêu chuẩn này không đề cập tới mọi vấn đề an toàn đối với người sử dụng tiêu chuẩn, nếu có. Người sử dụng có trách nhiệm xây dựng biện pháp bảo đảm an toàn và sức khỏe phù hợp với các quy định.
QUAN TRỌNG - Chỉ những nhân viên đã được đào tạo phù hợp mới được tiến hành phép thử theo tiêu chuẩn này.
1 Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp để xác định bromat hòa tan trong nước (ví dụ nước uống, nước khoáng, nước thô, nước mặt, nước đã xử lý một phần hoặc nước bể bơi).
Xử lý sơ bộ mẫu thích hợp (ví dụ pha loãng) cho phép xác định bromat ở nồng độ ≥ 0,5 µg/L.
Khoảng làm việc bị giới hạn do khả năng trao đổi ion của cột tách. Mẫu cần được pha loãng trong khoảng làm việc của bromat.
2 Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851 (ISO 3696), Nước dùng để phân tích trong phòng thí nghiệm - Yêu cầu kỹ thuật và phương pháp thử;
TCVN 6661-1 (ISO 8466-1), Chất lượng nước - Hiệu chuẩn và đánh giá các phương pháp phân tích và ước lượng các đặc trưng thống kê - Phần 1: Đánh giá thống kê các hàm hiệu chuẩn tuyến tính;
TCVN 6661-2 (ISO 8466-2), Chất lượng nước - Hiệu chuẩn và đánh giá các phương pháp phân tích và ước lượng các đặc trưng thống kê - Phần 2: Nguyên tắc hiệu chuẩn đối với các hàm hiệu chuẩn bậc hai không tuyến tính.
3 Cản trở
Kim loại có trong mẫu và dung dịch rửa giải sẽ liên kết với vật liệu nhựa của cột tách, kết quả là làm giảm tính năng của cột. Các ion kim loại có thể được loại bỏ với sự hỗ trợ của các thiết bị trao đổi cation đặc biệt (xem 6.2 và Điều 8, Chú thích 1).
Các hạt rắn và các hợp chất hữu cơ (ví dụ dầu khoáng, chất tẩy rửa và axit humic) làm giảm thời gian sử dụng của tiền cột và cột tách (xem Điều 8, Chú thích 2 và 3).
Clorit có thể gây cản trở đến việc xác định bromat. Nếu cần, loại bỏ clorit theo quy trình đã quy định trong 9.4.
CHÚ THÍCH: Chất có thời gian lưu trùng với bromat và tạo ra tín hiệu phản hồi trên detector đều có thể gây cản trở. Nồng độ ion cao có thể có tác động đến độ phân giải và thời gian lưu của chất phân tích. Việc pha loãng mẫu và/hoặc rửa giải gradient sẽ khắc phục sự cản trở rất nhiều.
4 Nguyên tắc
Mẫu được xử lý sơ bộ để loại bỏ ôzôn, clo đioxit, clorit, kim loại và chất rắn, nếu cần (xem Điều 8). Bromat được tách bằng sắc ký ion (IC). Sử dụng nhựa trao đổi anion làm pha tĩnh và sử dụng hoặc axit (ví dụ axit sunfuric) hoặc các dung dịch nước muối của các axit yếu hóa trị một và axit hóa trị hai làm dung dịch rửa giải cho rửa giải đẳng dòng hoặc rửa giải gradient (ví dụ cacbonat, hydro cacbonat, dung dịch rửa giải hydroxit, ví dụ chuẩn bị thủ công, tự động hoặc điện hóa tại chỗ) (5.13).
Độ phát hiện của bromat [ρ(BrO-3) ≥ 0,5µg/L] đạt được bằng cách sử dụng dung dịch kali iotđua có tính axit có chứa một lượng xúc tác molypden (IV), tại đây bromat phản ứng với iotđua để tạo thành ion tri-iotđua trong giai đoạn phản ứng sau cột (PCR), trong đó bromat được đo bằng độ hấp thụ UV ở bước sóng 352 nm.
CHÚ THÍCH: Phương pháp này có thể kết hợp với TCVN 6491-1 (ISO 10304-1)[2], TCVN 6491-4 (ISO 10304-4)[3] và ISO 15061[4].
Nồng độ của bromat được xác định sau khi hiệu chuẩn theo TCVN 6661-1 (ISO 8466-1) hoặc TCVN 6661-2 (ISO 8466-2) của toàn bộ quy trình.
Cần kiểm soát các thực nghiệm để kiểm tra giá trị sử dụng của hàm hiệu chuẩn (9.5). Có thể cần lặp lại các phép xác định. Phương pháp thêm chuẩn có thể được sử dụng nếu dự kiến được các cản trở nền mẫu (9.3).
5 Thuốc thử
Chỉ sử dụng các thuốc thử đạt cấp phân tích được công nhận. Cân các thuốc thử chính xác đến ±1 % khối lượng danh định, trừ khi có quy định khác. Lần lượt chuẩn bị các dung dịch như đã nêu trong 5.13 đến 5.19, nếu cần.
5.1 Nước, TCVN 4851 (ISO 3696), Cấp 1.
5.2 Natri cacbonat, Na2CO3.
5.3 Axit sunfuric, c(H2SO4) = 1 mol/L.
5.4 Natri hydroxit, NaOH.
5.5 Kali hydroxit, KOH.
5.6 Natri hydrocacbonat, NaHCO3.
5.7 Amoni heptamolybdat ngậm bốn phân tử nước, (NH4)6Mo7O24.4H2O.
5.8 Kali iotđua, KI.
5.9 Axit nitric, ρ(HNO3) = 1,41 g/mL.
5.10 Sắt (II) sunfat ngậm bẩy phân tử nước, FeSO4.7H2O.
5.11 Kali bromat, KBrO3.
5.12 Etylendiamin, C2H8N2, 99 %.
5.13 Dung dịch rửa giải
Khử khí tất cả các dung dịch rửa giải được sử dụng. Thực hiện các bước để tránh mọi sự thâm nhập của không khí trong quá trình thao tác (ví dụ sục khí heli, bộ khử khí trực tiếp).
Việc lựa chọn dung dịch rửa giải phụ thuộc vào cách chọn cột và detector; tham khảo thông tin từ nhà cung cấp cột. Lựa chọn kết hợp cột tách và dung dịch rửa giải phải phù hợp với các yêu cầu về độ phân giải được nêu trong Điều 7. Sử dụng các dung dịch rửa giải phù hợp với các yêu cầu trong Điều 7 và trong 9.3.
Việc chọn thuốc thử cho dung dịch rửa giải thông thường được nêu trong 5.2 đến 5.6. Ví dụ về các dung dịch rửa giải thích hợp được nêu trong 5.13.2 và 5.13.3.
5.13.1 Natri cacbonat đặc, c(Na2CO3) = 0,09 mol/L.
Dung dịch rửa giải đặc phù hợp để chuẩn bị dung dịch rửa giải (5.13.2) được pha như sau.
Hòa tan 9,54 g natri cacbonat (5.2) với nước (5.1) trong bình định mức 1000 mL và pha loãng tới vạch bằng nước (5.1).
Dung dịch bền trong 6 tháng nếu bảo quản ở nhiệt độ từ 2 °C đến 8 °C.
5.13.2 Dung dịch rửa giải natri cacbonat, c(Na2CO3) = 0,009 mol/L.
Sử dụng dung dịch rửa giải sau đây để xác định bromat:
Cho 100 mL natri cacbonat đặc (5.13.1) và bình định mức 1000 mL và pha loãng tới vạch bằng nước (5.1).
5.13.3 Dung dịch rửa giải axit sunfuric, c(H2SO4) = 0,1 mol/L
Cho 100 mL axit sunfuric (5.3) vào bình định mức 1000 mL và pha loãng đến vạch bằng nước (5.1).
CHÚ THÍCH: Có thể thêm amoni heptamolybdat ngậm bốn phân tử nước (5.7) vào dung dịch rửa giải sao cho thành phần phù hợp với nồng độ cuối của thuốc thử PCR trong thiết bị PCR (5.15).
5.14 Dung dịch amoni heptamolybdat, c[(NH4)6Mo7O24] = 0,002 mol/L.
Hòa tan 0,25 g amoni heptamolybdat ngậm bốn phân tử nước (5.7) với 100 mL nước (5.1).
Dung dịch bền trong 1 tháng nếu bảo quản trong chai tối ở nhiệt độ phòng.
5.15 Thuốc thử phản ứng sau cột (PCR)
Khử khí tất cả nước được sử dụng để chuẩn bị thuốc thử PCR. Thực hiện các bước để tránh bất cứ việc nhận không khí mới trong quá trình thao tác (ví dụ sục khí heli).
Hòa tan 45 g kali iotđua (5.8) với khoảng 500 mL nước (5.1), thêm 25 mL dung dịch amoni heptamolybdat (5.14) trong bình định mức 1000 mL và pha loãng tới vạch bằng nước (5.1).
Sục dung dịch với khí heli khoảng 20 min để loại bỏ tất cả các lượng vết của oxy hòa tan, và đặt ngay vào trong mođun của PCR và tạo áp suất bằng khí heli.
Dung dịch chứa 0,27 mol/L kali iotđua và 0,05 mmol/L amoni heptamolybdat. Chuẩn bị dung dịch trong ngày sử dụng. Bảo quản dung dịch trong chai tối (ví dụ bọc bằng giấy nhôm) và bảo vệ dung dịch khỏi sự tiếp xúc với ánh sáng.
CHÚ THÍCH: Vì kali iotđua là nhạy sáng, dung dịch có thể tạo màu vàng nhạt theo thời gian, thậm chí khi bảo quản trong chứa khí heli. Có thể tránh hiện tượng này bằng cách thêm natri hydroxit (5.4) với nồng độ cuối là 0,001 mol/L.
5.16 Dung dịch sắt (III), ρ(Fe2+) = 1000 mg/L.
Cho 6 µL axit nitric (5.9) vào khoảng 15 mL nước (5.1) trong bình định mức 25 mL, hòa tan 0,124 g sắt (II) sunfat ngậm bẩy phân tử nước (5.10) và pha loãng đến vạch bằng nước (5.1).
Giá trị cuối cùng của pH là 2. Dung dịch bền trong 2 ngày.
5.17 Dung dịch chuẩn gốc bromat, ρ(BrO-3) = 1000 mg/L.
Sấy khô khoảng 1,5 g kali bromat (5.11) ít nhất 1 h ở nhiệt độ 105 °C ± 5°C. Bảo quản chất rắn đã sấy khô trong bình hút ẩm.
Hòa tan 1,306 g ± 0,001 g kali bromat đã sấy khô với khoảng 800 mL nước (5.1) trong bình định mức 1000 mL và pha loãng đến vạch bằng nước (5.1). Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C trong chai thủy tinh hoặc polyetylen và thay mới dung dịch sau 12 tháng.
Cách khác, sử dụng các dung dịch gốc có sẵn ngoài thị trường với nồng độ theo yêu cầu.
5.18 Dung dịch chuẩn bromat 3S
Tùy thuộc vào các nồng độ đã dự kiến, chuẩn bị các dung dịch chuẩn có các nồng độ bromat khác nhau từ các dung dịch chuẩn gốc (5.17). Chú ý đến khả năng rủi ro có thể làm thay đổi nồng độ do tương tác của bromat với vật liệu của bình, sự tương tác này tăng lên sẽ làm giảm nồng độ bromat. Bảo quản các dung dịch chuẩn trong chai thủy tinh hoặc polyetylen.
5.18.1 Dung dịch chuẩn bromat I, ρ(BrO-3) = 100 mg/L.
Dùng pipet lấy 10,0 mL dung dịch chuẩn gốc bromat I (5.17) vào bình định mức 100 mL và pha loãng tới vạch bằng nước (5.1).
Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C trong chai thủy tinh hoặc polyetylen. Dung dịch bền trong 6 tháng.
5.18.2 Dung dịch chuẩn bromat II ρ(BrO-3) = 1 mg/L
Dùng pipet lấy 1,0 mL dung dịch chuẩn I (5.18.1) vào trong bình định mức 100 mL và pha loãng tới vạch bằng nước (5.1).
Bảo quản dung dịch ở nhiệt độ từ 2 °C đến 8 °C trong chai thủy tinh hoặc polyetylen. Dung dịch bền trong 3 tháng.
5.19 Dung dịch hiệu chuẩn bromat
Phụ thuộc vào nồng độ bromat dự kiến có trong mẫu, sử dụng dung dịch chuẩn bromat I (5.18.1) hoặc II (5.18.2) để chuẩn bị từ năm đến mười dung dịch hiệu chuẩn, các dung dịch này có nồng độ phân bố càng đều trên toàn bộ khoảng làm việc dự kiến càng tốt.
Ví dụ, tiến hành như sau với khoảng làm việc của bromat từ 0,5 µg/L đến 5 µg/L.
Dùng pipet lấy các thể tích như sau: 50 µL, 100 µL, 150 µL, 200 µL, 250 µL, 300 µL, 350 µL, 400 µL, 450 µL và 500 µL dung dịch chuẩn bromat II (5.18.2) cho vào một dãy các bình định mức 100 mL và pha loãng tới vạch bằng nước (5.1).
Nồng độ bromat trong các dung dịch hiệu chuẩn này tương ứng là: 0,5 µL/L, 1,0 µL/L, 1,5 µL/L, 2,0 µL/L, 2,5 µL/L, 3,0 µL/L, 3,5 µL/L, 4,0 µL/L, 4,5 µL/L và 5,0 µL/L, tương ứng.
Chuẩn bị các dung dịch hiệu chuẩn trong ngày sử dụng.
5.20 Dung dịch trắng
Đổ đầy nước vào bình định mức (5.1), ví dụ 100 mL.
6 Thiết bị, dụng cụ
Sử dụng thiết bị phòng thử nghiệm thông thường và, cụ thể, như sau:
6.1 Hệ thống sắc ký IC, tuân thủ các yêu cầu về chất lượng quy định trong Điều 7, nghĩa là độ phân giải. Thông thường, hệ thống này phải bao gồm các thành phần sau (xem Hình 1).
6.1.1 Bình chứa dung dịch rửa giải, và bộ khử khí.
6.1.2 Bơm IC, phù hợp cho kỹ thuật đẳng dòng hoặc gradient.
6.1.3 Thiết bị phân chia mẫu, ví dụ bơm mẫu, bao gồm cả hệ thống bơm mẫu gắn với vòng lấy mẫu có dung tích thích hợp (ví dụ từ 0,1 mL đến 1 mL) hoặc bơm mẫu tự động.
6.1.4 Thiết bị ghi, ví dụ máy tính PC với phần mềm thu nhận và xử lý dữ liệu.
6.1.5 Thiết bị phản ứng sau cột (PCR), bao gồm các bộ phận sau:
6.1.5.1 Bình chứa thuốc thử PCR.
6.1.5.2 Thiết bị phân chia H+, ví dụ thiết bị chứa H2SO4, thiết bị triệt nhiễu nền.
6.1.5.3 Hệ thống phân chia thuốc thử, ví dụ bơm nhu động.
6.1.5.4 Cuộn phản ứng, ví dụ dung tích bên trong 500 µL.
6.1.5.5 Bộ gia nhiệt phản ứng, có khả năng duy trì nhiệt độ ở 80 °C.
6.1.6 Detector UV, ví dụ máy quang phổ, từ 190 nm đến 400 nm.
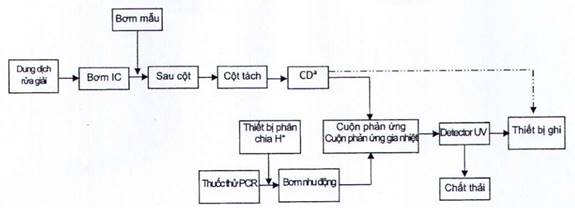
CHÚ DẪN:
CD Detector độ dẫn
a Tùy chọn
Hình 1 - Sơ đồ mô tả hệ thống sắc ký ion bao gồm cả hệ thống PCR nối tiếp
6.2 Cột trao đổi ion
6.2.1 Cột trao đổi cation ở dạng Na (cartridge).
6.2.2 Cột trao đổi cation, các pha không phân cực được sử dụng để chuẩn bị mẫu (ví dụ polyvinylpyrrolidone).
7 Yêu cầu chất lượng
7.1 Cột tách
Trong sắc ký đồ của các mẫu và các dung dịch chuẩn của bromat, độ phân giải pic, R, giữa bromat với pic gần nhất phải có giá trị không nhỏ hơn 1,3 [xem Công thức (1) và Hình 2]. Điều chỉnh các điều kiện tách phù hợp.
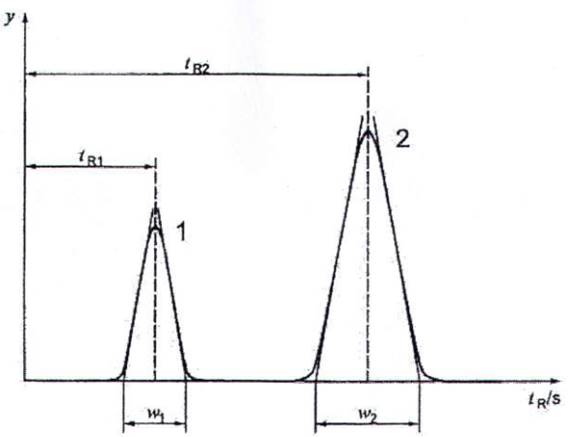
CHÚ DẪN:
w1 Chiều rộng pic 1
w2 Chiều rộng pic 2
tR Thời gian lưu
y Tín hiệu
1 Pic 1
2 Pic 2
Hình 2 - Mô tả hình học của các thông số để tính độ phân giải pic, R
CHÚ THÍCH 1: Trong phạm vi áp dụng của tiêu chuẩn này, việc tính độ phân giải, R, là thích hợp cho cả rửa giải đẳng dòng và rửa giải gradient.
Tính độ phân giải pic cho các pic 2,1, R2,1 sử dụng Công thức (1):
| R2,1 | = | 2(tR2 - tR1) |
| w2 - w1 |
(1)
Trong đó:
tR1 là thời gian lưu, tính theo giây, của pic đầu tiên;
tR2 là thời gian lưu, tính theo giây, của pic thứ hai;
w1 là chiều rộng của pic, tính theo giây, trên trục thời gian của pic đầu tiên;
w2 là chiều rộng của pic, tính theo giây, trên trục thời gian của pic thứ hai.
CHÚ THÍCH: Các giá trị w1 và w2 là chiều rộng đáy của tam giác cân được tạo thành qua từng pic Gaus.
7.2 Điều kiện PCR
Các điều kiện phân tích điển hình được mô tả trong 7.3 và 7.4.
Điều chỉnh nồng độ amoni hetamolybdat tới khoảng từ 11 µmol/L đến 15 µmol/L và nồng độ kali iôtđua khoảng từ 55 mmol/L đến 65 mmol/L.
Cho phép những thay đổi trong các thông số của quy trình (ví dụ lưu lượng, nồng độ kali iôtđua hoặc nồng độ amoni heptamolybdat trong dung dịch rửa giải hoặc thuốc thử PCR). Nếu áp dụng, tính bằng cách sử dụng Công thức (2):
| qV1·c1+qV2·c2 = (qV1+qV2)·c3 | (2) |
Trong đó:
qV1 là lưu lượng của dung dịch rửa giải, tính theo mililít trên phút;
c1 là nồng độ của dung dịch amoni heptamolybdat trong dung dịch rửa giải, tính theo mol trên lít;
qV2 là lưu lượng của bơm PCR, tính theo mililít trên phút;
c2 là nồng độ của dung dịch amoni heptamolybdat hoặc kali iotđua trong thuốc thử PCR, tính theo mol trên lít;
c3 là nồng độ của dung dịch amoni heptamolybdat hoặc kali iotđua sau khi tiến hành trộn trong thiết bị PCR, tính theo mol trên lít.
VÍ DỤ: Ví dụ về sự tính toán nồng độ amoni heptamolybdat trong bộ phản ứng PCR.
| Lưu lượng dung dịch rửa giải: | qV1 = 0,7 mL/min |
| Nồng độ amoni heptamolybdat trong dung dịch rửa giải: | c1 = 0 µmol/L |
| Lưu lượng PCR: | qV2 = 0,2 mL/min |
| Nồng độ amoni heptamolybdat trong thuốc thử PCR: | c2 = 50 pmol/L |
| 0,7 mL/min . 0 µmol/L + 0,2 mL/min . 50 pmol/L = (0,7 mL/min + 0,2 mL/min).c3 | |
| Nồng độ amoni heptamolybdat trong bộ phản ứng PCR: | c3 =11,1 µmol/L |
CHÚ THÍCH: Dung dịch có giá trị pH > 1 có thể cần gia nhiệt dung dịch phản ứng trong bộ phản ứng PCR.
7.3 Điều kiện sắc ký và PCR cho sắc ký đồ nêu trong Hình 3
| Cột: | Chất trao đổi ion |
| Dung dịch rửa giải: | Axit sunturic 100 mmol/L |
| Thể tích bơm mẫu: | 1000 µL |
| Lưu lượng rửa giải: | 0,7 mL/min |
| Thuốc thử PCR: | 0.27 mol/L kali iotđua + 50 µmol/L amoni heptamolybdat |
| Lưu lượng thuốc thử PCR: | 0,2 mL/min |
| Điều kiện tại cuộn phản ứng PCR: | Thể tích: 400 µL Nhiệt độ: nhiệt độ xung quanh 11,1 µmol/L amoni heptamolybdat 60 mmol/L kali iotđua |
| Detector: | UV, λ = 352 nm |

CHÚ DẪN:
D Độ hấp thụ
tR Thời gian lưu
| Pic | lon | Nồng độ |
| 1 | Bromat | 1,0 µg/L |
Hình 3 - Ví dụ sắc ký đồ của dung dịch chuẩn phù hợp với tiêu chuẩn này
7.4 Điều kiện sắc ký và PCR cho sắc ký đồ đã nêu trong Hình 4
| Tiền cột: | Chất trao đổi ion |
| Cột: | Chất trao đổi ion |
| Dung dịch rửa giải: | Na2CO3 100 mmol/L |
| Thể tích bơm mẫu: | 225 µL |
| Lưu lượng rửa giải: | 1,3 mL/min |
| Thuốc thử PCR: | 0,27 mol/L kali iôtđua + 50 µmol/L amoni heptamolybdat |
| Lưu lượng thuốc thử PCR: | 0,4 mL/min |
| Điều kiện tại cuộn phản ứng PCR: | Thể tích: 375 µL Nhiệt độ: 80 °C 12 µmol/L amoni heptamolybdat 64 mmol/L KI |
| Detector: | UV, λ = 352 nm |
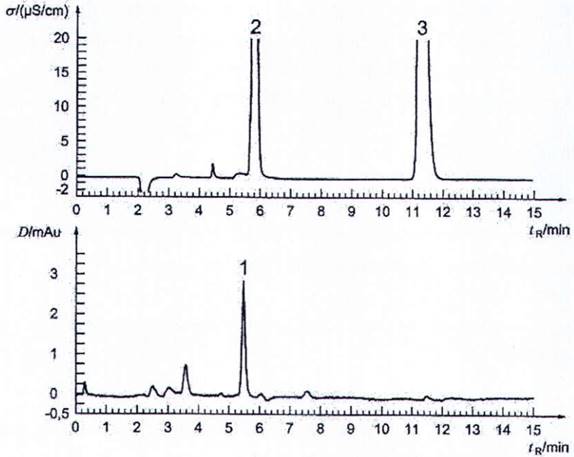
CHÚ DẪN:
σ Độ dẫn
D Độ hấp thụ
tR Thời gian lưu
| Pic | lon | Nồng độ |
| 1 | Bromat | 8,0 µg/L |
| 2 | Clorua | 14 mg/L |
| 3 | Sunfat | 19 mg/L |
Hình 4 - Ví dụ sắc ký đồ của mẫu nước uống phù hợp với tiêu chuẩn này
CHÚ THÍCH: Trình tự rửa giải và thời gian lưu, tR có thể thay đổi, tùy thuộc vào loại cột và thành phần của dung dịch rửa giải.
8 Lấy mẫu và xử lý sơ bộ mẫu
Sử dụng các bình polyetylen sạch để lấy mẫu.
Tránh mọi sự hình thành bromat sau khi lấy mẫu và loại bỏ ngay ozon có trong mẫu bằng cách thêm 50 mg etylendiamin (5.12) vào 1 L mẫu ngay sau khi lấy mẫu.
CHÚ THÍCH 1: Có thể loại bỏ kim loại xuất hiện trong mẫu với sự hỗ trợ của chất trao đổi cation (ví dụ cuộn/cột trao đổi cation dạng Na).
CHÚ THÍCH 2: Có thể loại bỏ chất rắn với sự hỗ trợ của màng lọc cỡ lỗ 0,45 µm.
CHÚ THÍCH 3: Có thể loại bỏ các hợp chất hữu cơ và chất rắn với sự hỗ trợ của chất hấp phụ không phân cực (ví dụ cuộn/cột trao đổi cation SPE, cột tách lắp trực tiếp trên cột, thẩm tách trực tiếp).
Xử lý các dung dịch hiệu chuẩn (5.19) và dung dịch trắng (5.20) theo cùng cách với dung dịch mẫu.
9 Cách tiến hành
9.1 Khái quát
Lắp đặt hệ thống sắc ký ion (6.1) bao gồm cả thiết bị PCR, theo hướng dẫn của nhà sản xuất thiết bị.
Chạy dung dịch rửa giải và hệ thống phân chia thuốc thử PCR. Khi đường nền ổn định, có thể bắt đầu phân tích.
Tiến hành hiệu chuẩn như quy định trong 9.2. Đo các mẫu và dung dịch trắng (5.20) theo quy trình quy định trong 9.3.
9.2 Hiệu chuẩn
Bơm các dung dịch hiệu chuẩn bromat đã xử lý sơ bộ (5.19 và Điều 8). Diện tích (hoặc chiều cao) của pic (tín hiệu) tỷ lệ với nồng độ của ion bromat.
Khi hệ thống phân tích được đánh giá lần đầu tiên, và ở các khoảng thời gian sau, thiết lập hàm hiệu chuẩn (theo TCVN 6661-1 (ISO 8466-1) hoặc TCVN 6661-2 (ISO 8466-2)) cho các phép đo như sau:
Chuẩn bị các dung dịch hiệu chuẩn bromat như đã quy định trong 5.19 và Điều 8.
Phân tích các dung dịch hiệu chuẩn bằng sắc ký.
Sử dụng dữ liệu đã thu được (diện tích pic hoặc chiều cao pic) để tính đường hồi quy theo quy định trong TCVN 6661-1 (ISO 8466-1) hoặc TCVN 6661-2 (ISO 8466-2).
Sau đó, kiểm tra xác nhận tính liên tục của hàm hiệu chuẩn đã thiết lập (9.5).
9.3 Đo bromat
Sau khi thiết lập hàm hiệu chuẩn, bơm mẫu đã xử lý sơ bộ (xem Điều 8) vào máy sắc ký và đo các pic như đã mô tả ở trên (xem Điều 9). Trước khi bơm vào máy phân tích, lọc mẫu qua màng lọc (cỡ lỗ 0,45 µm) để loại bỏ mọi chất lơ lửng, nếu cần. Ngăn ngừa khả năng nhiễm bẩn của mẫu từ màng lọc (ví dụ súc rửa màng với một lượng mẫu nhỏ và gạn bỏ phần đầu tiên của dịch lọc).
Nhận biết pic bromat bằng cách so sánh thời gian lưu của bromat đo được với thời gian lưu của bromat trong các dung dịch hiệu chuẩn (5.19). Độ lệch của thời gian lưu phải không quá ±10 % trong một dãy mẫu.
Nếu nồng độ bromat trong mẫu nằm ngoài khoảng hiệu chuẩn, pha loãng mẫu và phân tích lại mẫu.
Nếu nồng độ bromat trong mẫu giảm thấp hơn khoảng hiệu chuẩn, thiết lập hàm hiệu chuẩn riêng cho khoảng làm việc thấp hơn, nếu cần.
Nếu dự kiến có các cản trở nền mẫu, sử dụng phương pháp thêm chuẩn để xác nhận các kết quả (kiểm tra xác nhận các pic bằng cách so sánh thời gian lưu của mẫu thêm chuẩn với thời gian lưu của mẫu gốc).
Đo dung dịch mẫu trắng (5.20) theo đúng cách đo đối với mẫu.
CHÚ THÍCH: Do dung dịch kali iôtđua trong PCR dễ bị oxi hóa, dẫn đến dung dịch có màu vàng nhạt dung dịch này bị đẩy ra từ tất cả các phần của thiết bị (ví dụ cuộn phản ứng và ngăn detector) có nước sau khi hoàn thành phân tích cuối cùng và ngăn sự rò rỉ qua cuộn phản ứng bằng trọng lực kể cả khi hệ thống ngừng hoạt động.
9.4 Loại bỏ clorit
Nếu clorit có biểu hiện gây cản trở sắc ký đồ của bromat, loại bỏ clorit như sau:
Cho 10 mL dịch mẫu vào trong cốc có mỏ 20 mL, điều chỉnh pH từ 5 đến 6 bằng cách thêm axit sunfuric (5.3), thêm 40 µL dung dịch sắt (II) (5.16), trộn và để phản ứng khoảng 10 min. Lọc dung dịch qua màng lọc (cỡ lỗ 0,45 µm) để loại bỏ hydroxit sắt kết tủa. Sau đó đưa dịch lọc qua cuộn/cột trao đổi cation của thiết bị trao đổi cation dạng Na (6.2.1) đã ổn định ở lưu lượng khoảng 1 mL/min để loại bỏ sắt hòa tan còn lại. Gạn bỏ 3 mL đầu tiên, và lấy một thể tích thích hợp để phân tích. Mẫu đã xử lý bền trong 24 h.
Thêm chuẩn bromat vào 10 mL dịch mẫu thứ hai ở mức gần hai lần mức đã xác định trong mẫu ban đầu. Xử lý dịch mẫu đã thêm chuẩn này theo biện pháp xử lý đã mô tả ở trên. Độ thu hồi của bromat phải ở trong khoảng từ 80 % đến 120 %.
Xử lý các dung dịch hiệu chuẩn (5.19) và dung dịch trắng (5.20) theo cùng cách với dung dịch mẫu.
9.5 Xác nhận giá trị sử dụng của hàm hiệu chuẩn
Để xác nhận giá trị sử dụng liên tục của hàm hiệu chuẩn, đo các dung dịch chuẩn độc lập có các nồng độ khác nhau trong giới hạn dưới và một phần ba giới hạn trên của khoảng làm việc. Tiếp tục tiến hành sau khi thiết lập quy trình (xem 9.1) và sau ít nhất là mỗi dãy mẫu, nhưng sau 20 phép đo. Độ thu hồi phải nằm trong khoảng từ 90 % đến 110 % giá trị danh định. Hiệu chuẩn lại nếu cần.
10 Tính toán
Tính nồng độ khối lượng, ρ, tính theo microgam trên lít hoặc miligam trên lít, của bromat trong dung dịch sử dụng các diện tích pic hoặc chiều cao pic như đã mô tả trong TCVN 6661-1 (ISO 8466-1) hoặc TCVN 6661-2 (ISO 8466-2).
Đưa vào tính toán tất cả các bước pha loãng.
11 Biểu thị kết quả
Các kết quả phải được báo cáo tối đa hai số có nghĩa.
VÍ DỤ:
Bromat (BrO-3) 5,1 µg/L
Bromat (BrO-3) 0,62 µg/L
12 Báo cáo kết quả thử nghiệm
Báo cáo kết quả thử nghiệm phải bao gồm ít nhất thông tin sau:
a) Phương pháp thử được sử dụng, và viện dẫn tiêu chuẩn này;
b) Nhận biết mẫu nước;
c) Các kết quả thử nghiệm thu được, biểu thị theo Điều 11;
d) Mô tả quá trình xử lý sơ bộ mẫu, nếu có liên quan;
e) Bất cứ độ lệch nào từ phương pháp này và báo cáo các trường hợp có ảnh hưởng đến kết quả.
Phụ lục A
(Tham khảo)
Dữ liệu độ chụm
Thử nghiệm liên phòng do viện Đo lượng và Vật liệu chuẩn (RMM) của Trung tâm Nghiên cứu chung (JRC) của Ủy ban Châu Âu tổ chức năm 2009 với sự tham gia của các phòng thử nghiệm từ Bỉ, Pháp, Đức, Ấn Độ, Triều Tiên, Hà Lan, Thụy Điển, Anh và Mỹ. Sự đa dạng về thiết bị và các điều kiện phân tích khác được sử dụng phù hợp với các thông số chất lượng đã quy định trong phương pháp.
Dữ liệu thống kê của các kết quả được đánh giá theo TCVN 6910-2 (ISO 5725-2)[1] được trình bày trong Bảng A.1.
Để mô tả nền mẫu xem Bảng A.2.
Bảng A.3 liệt kê hệ số biến thiên, Vx0 của quy trình (thu được từ các hàm hiệu chuẩn được xác định như với các hàm hiệu chuẩn đã mô tả trong 9.2). Dữ liệu này đến từ các phòng thử nghiệm chuyên môn và được chuẩn bị kỹ lưỡng trong quá trình xác định giá trị sử dụng của phương pháp.
Bảng A.1 - Dữ liệu độ chụm
| Mẫu | Nền mẫu | l | n | o | X |
| η | sR | CV,R | sr | CV,r |
|
|
| % | µg/L | µg/L | % | µg/L | % | µg/L | % | ||
| 1 | Nước uống, mềm | 13 | 52 | 7,1 | 2,61 | 2,68 | 97,4 | 0,132 | 5,1 | 0,084 | 3,2 |
| 2 | Nước uống, cứng | 12 | 48 | 14,3 | 8,93 | 10,0 | 89,3 | 0,476 | 5,3 | 0,112 | 1,3 |
| 3 | Nước khoáng | 11 | 44 | 21,4 | 2,94 | 3,00 | 98,1 | 0,107 | 3,6 | 0,067 | 2,3 |
| 4 | Nước bể bơi | 12 | 48 | 14,3 | 7,66 | - | - | 0,171 | 2,2 | 0,095 | 1,2 |
| 5 | Nước thô | 14 | 55 | 1,8 | 7,86 | 7,95 | 98,9 | 0,243 | 3,1 | 0,125 | 1,6 |
| 6 | Mẫu trắnga | 14 | - | - | - | - | - | - | - | - | - |
| 7 | Tiêu chuẩn tổng hợp | 14 | 56 | 0 | 1,65 | 1,67 | 99,0 | 0,097 | 5,9 | 0,068 | 4,1 |
| l n o X
η sR CV,R sr CV,r | Số phòng thử nghiệm tham gia sau khi loại bỏ các phòng ngoại lai Số kết quả thử nghiệm đơn lẻ sau khi loại bỏ các giá trị ngoại lai Phần trăm các giá trị ngoại lai Giá trị chỉ định Giá trị trung bình toàn bổ của các kết quả (trừ các giá trị ngoại lai) Tỷ lệ thu hồi Độ lệch chuẩn tái lập Hệ số biến thiên của độ tái lập Độ lệch chuẩn lặp lại Hệ số biến thiên của độ lặp lại | ||||||||||
| CHÚ THÍCH: Tất cả các dữ liệu sử dụng trong hiệu chuẩn theo TCVN 6910-2 (ISO 5725-2)[2] được sử dụng dưới sự cho phép của Viện RMM. | |||||||||||
| a Không có phòng thử nghiệm nào trong số các phòng thử nghiệm tham gia báo cáo giá trị định lượng của mẫu trắng. | |||||||||||
Bảng A.2 - Mô tả các nền mẫu
(được phân tích trước khi thêm chuẩn với bromat và etylendiamin)
| Giá trị đo | Đơn vị | Mẫu | ||||
| 1 | 2 | 3 | 4 | 5 | ||
| Chất khử khuẩn | ||||||
| ClO2 | ClO2 | Không có tác nhân | ClO2 | Không biết tác nhân | ||
| Dung lượng axit (pH 4,3) | mmol/L | 1,1 | 5,1 | 3,7 | 2 | 3,6 |
| Dung lượng bazơ (pH 8,2) | mmol/L | ≤0,02 | 0,06 | 0,12 | 0,04 | 0,08 |
| Độ cứng ∑(Ca2++Mg2+) | mmol/L | 0,7 | 3,4 | 2,0 | 2,7 | 2,7 |
| Nitrơ tổng (TNb) | mg/L | 2,7 | 1,1 | 2,0 | 2,4 | 2,1 |
| Tổng cacbon vô cơ (TIC) | mg/L | 13 | 61 | 47 | 24 | 44 |
| Tổng cacbon hữu cơ (TOC) | mg/L | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Nhôm (Al) | mg/L | 0,01 | 0,02 | ≤0,01 | 0,06 | 0,05 |
| Antimon (Sb) | mg/L | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Asen (As) | mg/L | ≤0,0005 | ≤0,0005 | ≤0,0005 | 0,001 | 0,002 |
| Bari (Ba) | mg/L | 0,02 | 0,12 | ≤0,01 | 0,06 | 0,05 |
| Bo (B) | mg/L | 0,02 | 0,05 | 0,03 | 0,05 | 0,05 |
| Cadmi (Cd) | mg/L | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Canxi (Ca) | mg/L | 20 | 110 | 80 | 88 | 85 |
| Crom (Cr) | mg/L | ≤0,002 | ≤0,002 | ≤0,002 | 0,002 | ≤0,002 |
| Đồng (Cu) | mg/L | 0,004 | 0,17 | 0,002 | 0,004 | 0,003 |
| Sắt (Fe) | mg/L | 0,009 | 0,088 | ≤0,01 | 0,001 | 0,002 |
| Chì (Pb) | mg/L | ≤0,0005 | 0,003 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Magie (Mg) | mg/L | 4,8 | 17 | 0,74 | 13 | 13 |
| Mangan (Mn) | mg/L | 0,003 | 0,002 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Niken (Ni) | mg/L | 0,001 | 0,003 | ≤0,001 | 0,002 | 0,004 |
| Kali (K) | mg/L | 1,0 | 2,6 | 0,2 | 3,6 | 3,1 |
| Selen (Se) | mg/L | ≤0,005 | ≤0,005 | ≤0,005 | ≤0,005 | ≤0,005 |
| Silic (Si) | mg/L | 8,8 | 7,7 | 2,4 | 3,3 | 3,1 |
| Natri (Na) | mg/L | 7,4 | 17 | 1,8 | 77 | 28 |
| Thiếc (Sn) | mg/L | 0,0005 | 0,016 | ≤0,0005 | ≤0,0005 | ≤0,0005 |
| Kẽm (Zn) | mg/L | 0,01 | 0,05 | ≤0,01 | 0,008 | 0,003 |
| Amoni (NH4+-N) | mg/L | ≤0,07 | ≤0,07 | ≤0,07 | ≤0,07 | ≤0,07 |
| Bromua (Br-) | mg/L | 0,06 | 0,06 | ≤0,05 | 0,03 | 0,1 |
| Clorua (Cl-) | mg/L | 9,5 | 34 | 2,9 | 140 | 63 |
| Clorit (CIO2-) | mg/L | 0,06 | ≤0,01 | ≤0,01 | ≤0,01 | ≤0,01 |
| Florua (F-) | mg/L | 0,1 | 0,17 | 0,02 | 0,19 | 0,17 |
| Nitrat (NO3-N) | mg/L | 2,3 | 0,52 | 1,5 | 1,9 | 1,7 |
| Nitrit (NO2-N) | mg/L | ≤0,02 | ≤0,02 | ≤0,02 | ≤0,02 | ≤0,02 |
| o-Phosphat (PO43-P) | mg/L | 0,008 | 0,012 | ≤0,005 | 0,02 | 0,039 |
| Phospho tổng (P) | mg/L | 0,17 | 0,17 | 0,1 | 0,1 | 0,11 |
| Sunfat (SO42-) | mg/L | 19 | 67 | 18 | 140 | 48 |
Bảng A.3 - Sự ước tính các đặc tính tính năng như đã quy định trong TCVN 6661-1 (ISO 8466-1) và TCVN 6661-2 (ISO 8466-2) được chỉ thị bằng hệ số biến thiên của quy trình, Vx0
| Phương pháp theo | Khoảng làm việc | Tính hiệu sử dụng | Vx0 TCVN 6661-1 (ISO 8466-1) | Vx0 TCVN 6661-2 (ISO 8466-2) |
| µg/L |
| % | % | |
| 7.3 | 0,5 đến 5,0 | Diện tích pic | 1,15 | 1,18 |
| 7.4 | 0,5 đến 5,0 | Diện tích pic | 1,72 | 1,82 |
Thư mục tài liệu tham khảo
[1] TCVN 6910 (ISO 5725-2), Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo - Phần 2: Phương pháp cơ bản xác định độ lặp lại và độ tái lập của phương pháp đo tiêu chuẩn
[2] TCVN 6494-1 (ISO 10304-1), Chất lượng nước - Xác định các anion hòa tan bằng phương pháp sắc kí lỏng ion - Phần 1: Xác định bromua, dorua, florua, nitrat, nitrit, phosphat và sunphat hòa tan
[3] TCVN 6494-4 (ISO 10304-4), chất lượng nước - Xác định các anion hoà tan bằng sắc ký lỏng ion - Phần 4 - Xác định clorat, clorua và clorit trong nước nhiễm bẩn thấp
[4] ISO 15061, Water quality - Determination of dissolved bromate - Method by liquid chromatography of ions
[5] US EPA Method 326.0, Determination of inorganic oxyhalide disinfection by-products in drinking water using ion chromatography incorporating the addition of a suppressor acidified post column reagent for trace bromate analysis. EPA Document number: EPA 815R03007
[6] CORDEIRO RAPOSO, F.et al. IMEP-25a: Determination of bromate in drinking water - A collaborative trial report. EUR 24469 EN. Publications Office of the European Union, 2010
[7] CORDEIRO RAPOSO, F. et al. IMEP-25b: Determination of bromate in drinking water - Interlaboratory comparison report.EUR 24136 EN. Publications Office of the European Union, 2009
[8] HADDAD, P.R., JACKSON, P.E. Ion chromatography: Principles and applications. Amsterdam: Elsevier, 1990. 776 p. (Journal of Chromatography Library, Vol. 46)
[9] SALHI, E., VON GUNTEN, U. Simultaneous determination of bromide, bromate and nitrite in low µg·l-1 levels by ion chromatography without sample pretreatment. Water Res. 1999, 33, pp. 3239-3244
[10] WAGNER, H.P.et al. US Environmental Protection Agency Method 326.0, a new method for monitoring inorganic oxyhalides and optimization of the postcolumn derivatization for the selective determination of trace levels of bromate. J. Chromatogr. A 2002, 956, pp. 93-101
[11] WEISS, J. Handbook of ion chromatography, 3rd edition, 2 vols, WEISS, T., translator. Weinheim: Wiley-VCH, 2004. 894 p.
Bạn chưa Đăng nhập thành viên.
Đây là tiện ích dành cho tài khoản thành viên. Vui lòng Đăng nhập để xem chi tiết. Nếu chưa có tài khoản, vui lòng Đăng ký tại đây!
 Tiêu chuẩn Việt Nam TCVN 12959:2020 PDF (Bản có dấu đỏ)
Tiêu chuẩn Việt Nam TCVN 12959:2020 PDF (Bản có dấu đỏ) Tiêu chuẩn Việt Nam TCVN 12959:2020 DOC (Bản Word)
Tiêu chuẩn Việt Nam TCVN 12959:2020 DOC (Bản Word)